磁共振特征追踪技术定量左心室应变评估急性STEMI患者微血管阻塞
2020-03-03魏晓婷邹锦森胡根文徐坚民
魏晓婷,邹锦森,胡根文,徐坚民
(暨南大学第二临床医学院 深圳市人民医院放射科,广东 深圳 518000)
ST段抬高型心肌梗死(ST segment elevation myocardial infarction, STEMI)是冠状动脉次全堵塞造成相应心肌缺血、缺氧、坏死的严重心脏病,远期预后较差[1]。心肌梗死部位、范围及微血管阻塞(microvascular obstruction, MVO)与STEMI预后显著相关[2]。心脏共振(cardiovascular MR, CMR)可无创评估心肌梗死,其钆对比剂延迟强化成像(late gadolinium enhancement, LGE)可评估心肌活性及检测MVO[3]。磁共振组织特征追踪技术(CMR feature tracking, CMR-FT)可通过后处理软件量化心肌应变[4],客观评估心肌运动功能。本研究应用CMR-FT量化STEMI患者急性期左心室应变及心功能改变,探讨以之检测心肌梗死伴MVO的可行性。
1 资料与方法
1.1 一般资料 收集2017年10月—2018年12月于深圳市人民医院确诊的78例急性STEMI患者(梗死组)。纳入标准:①符合STEMI诊断标准[5];②首次发病且经冠状动脉造影明确诊断;③过去8 h内无新发梗死或再发胸痛,无明显心力衰竭失代偿征象,心肌损伤标志物无进一步升高。排除标准:既往心肌梗死史、完全性左束支阻塞及预激综合征;近期严重心功能不全、重度瓣膜疾病、急性心包炎或心肌炎。所有患者均于心肌梗死24 h内接受经皮冠状动脉介入术(percutaneous coronary intervention, PCI)并开通闭塞血管成功,术后2~6天内接受CMR。另外收集10名健康志愿者作为对照组。本研究经我院伦理委员会审核并批准,患者及家属均知情同意。
1.2 仪器与方法 采用Siemens Skyra 3.0T MR扫描仪,18通道心脏相控线圈,配备呼吸门控和心电向量门控。以稳态进动快速电影序列采集标准左心室短轴及左心室二腔、三腔、四腔心电影图像,参数:TR 3.8 ms,TE 1.4 ms,FA 80°,FOV 340 mm×340 mm,矩阵139×208,层厚8 mm,层间距1.6 mm,于呼气末分次屏气扫描,采集时间15~18 s。以0.1 mmol/kg体质量,流率4 ml/s经肘静脉团注对比剂钆喷酸葡胺后,采用反转恢复梯度回波序列延迟强化技术采集图像,TR 7.6 ms,TE 1.09 ms,FA 20°,FOV 340 mm×340 mm,矩阵128×128,层厚8 mm,层间距1.6 mm,采集时间1 min。通过梯度回波反转恢复序列实时确定心肌最黑层面的TI值(240~300 ms)。
1.3 图像分析 采用心血管后期处理软件 (CVI42, version 5.9.3, Calgary, Albert, Canada)分析图像。软件自动标记左心室短轴收缩末期及舒张末期的心内膜及心外膜边界后,由1名具有4年心脏影像学诊断经验的住院医师对标记线进行检查并调整,另外手动标记舒张末期左心室长轴二腔、三腔及四腔层面心内膜及心外膜轮廓(图1)。随机抽取10份资料,由2名分别具有2年和4年心脏影像学诊断经验的住院医师对标记线进行描记,由后者间隔1周后进行第2次描记,分析医师测量左心室应变结果的一致性。根据美国心脏病协会17节段划分法[6]划分左心室短轴心肌。心尖段(第17段)测量误差较大[7],本研究未将其纳入分析。MRI显示心肌信号强度大于同层面远侧正常心肌的5个标准差[8]时,判断为延迟强化区域(图2)。MVO定义为延迟强化图像显示强化心肌核心靠近内膜下斑片状或条带状低信号[9](图3)。经CVI42处理获得左心室应变[左心室整体峰值径向(global peak radial strain, GPRS)、整体峰值周向(global peak circumferential strain, GPCS)、整体峰值纵向应变值(global peak longitudinal strain, GPLS)和节段峰值径向(peak radial strain, PRS)、节段峰值周向(peak circumferential strain, PCS)、节段峰值纵向应变值(peak longitudinal strain, PLS)]以及心功能结果[左心室射血分数(left ventricular ejection fraction, LVEF)、左心室舒张末期容积、左心室收缩末期容积及左心室输出量],心功能指标除以体表面积(body surface area, BSA, BSA=0.0 061×身高(cm)+0.0 124×体质量(kg)-0.0099)为标准化心功能指标,包括左心室舒张末期容积指数(left ventricular end-diastolic volume index, LVEDVi)、左心室收缩末期容积指数(left ventricular end-systolic volume index, LVESVi)及心脏指数(cardiac index, CI)。
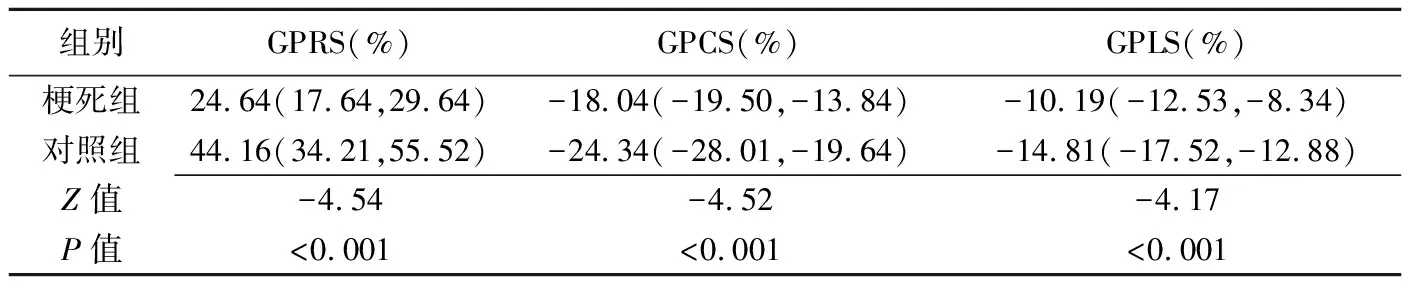
表1 梗死组与对照组的左心室整体应变比较[中位数(上下四分位数)]
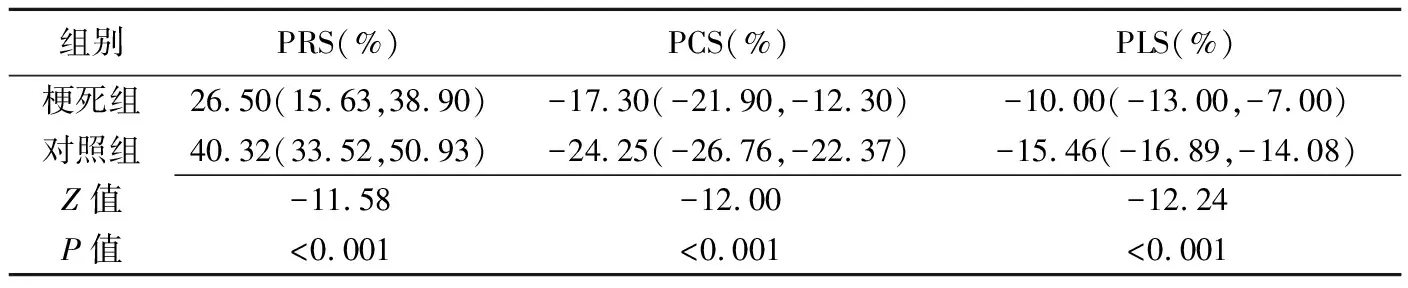
表2 梗死组与对照组的左心室心肌节段应变比较[中位数(上下四分位数)]

图1 患者男,51岁,急性下壁、后壁心肌梗死 A~C.左心室短轴层面收缩末期(A)、舒张末期(B)及左心室四腔心(C)MRI,绿线为心外膜,红线为心内膜

图2 患者男,45岁,急性下壁、间壁、后壁心肌梗死 MR LGE图像示左心室中间段下壁、间壁、后壁延迟强化(箭) 图3 患者男,70岁,急性前壁、前间壁、间壁心肌梗死 A.MRI LGE序列图像示左心室中间段前壁、前间壁、间壁延迟强化区域条带状低信号(箭),即MVO;B.伪彩图显示延迟强化及MVO
1.4 统计学分析 采用SPSS 22.0统计分析软件。计量资料符合正态分布以±s表示,不符合正态分布以中位数(上下四分位数)表示。以组内相关系数(intraclass correlation coefficient, ICC)检验2名医师测量结果的一致性,ICC>0.75为一致性佳,0.40≤ICC≤0.75为一致性良好,ICC<0.40为一致性差。采用Mann-WhitneyU检验分析梗死组与对照组、MVO组与无MVO组以及MVO节段组与无MVO节段组间左心室应变和心功能的差异。将组间差异有统计学意义的应变指标绘制成ROC曲线并计算AUC值。P<0.05为差异有统计学意义。
2 结果
2.1 急性STEMI患者一般临床特点 梗死组共纳入78例急性STEMI,男71例、女7例,平均年龄(51.1±10.6)岁,平均体质量指数(24.67±2.70)kg/m2;前降支闭塞46例,回旋支闭塞8例,右冠状动脉闭塞30例;根据是否存在MVO将其分为MVO组(n=50)和无MVO组(n=28),根据左心室短轴心肌各节段是否存在MVO,将其左心室1 248个心肌节段分为MVO节段组(n=173)和无MVO节段组(n=1 075)。
2.2 一致性分析 2名医师测量GPRS、PRS、GPCS、PCS、GPLS和PLS结果的一致性较好(ICC值分别为0.926、0.829、0.934、0.915、0.522和0.651,除GPLS的P=0.122外,余P均<0.05);同一医师2次测量结果一致性较好(ICC值分别为0.979、0.908、0.994、0.959、0.748和0.773,P均<0.05)。
2.3 梗死组与对照组左心室应变及心功能比较 梗死组整体峰值应变及节段峰值应变绝对值均低于对照组(P均<0.001,表1、2)。除CI外,2组间LVEF、LVEDVi、LVESVi差异有统计学意义(表3)。
2.4 MVO组与无MVO组左心室应变及心功能比较 MVO组左心室整体应变与无MVO组差异无统计学意义(表4);MVO节段组左心室节段应变绝对值均低于无MVO节段组(P均<0.05,表5)。MVO组与无MVO组CI差异有统计学意义,余标准化心功能指标差异均无统计学意义(表6)。
2.5 诊断效能 将MVO节段组与无MVO节段组间差异有统计学意义的应变指标绘制成ROC曲线并计算AUC值,发现PRS、PCS和PLS截断值分别为24.65%、-14.05%和-10.65%时,检出MVO梗死节段的敏感性、特异性及AUC分别为89.0%、60.6%及0.816(P<0.001),75.7%、75.9%及0.818(P<0.001)和71.1%、45.7%及0.577(P=0.001)(图4)。
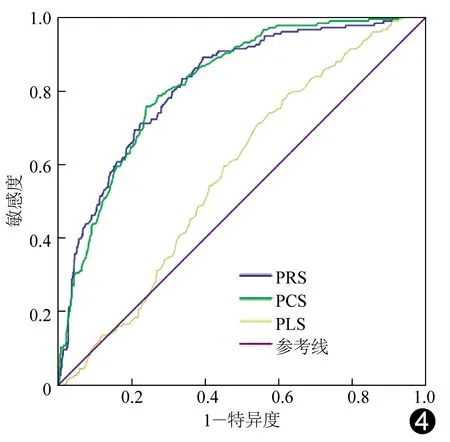
图4 左心室心肌节段应变诊断发生MVO的ROC曲线

表3 梗死组和对照组左心室心功能比较[中位数(上下四分位数)]
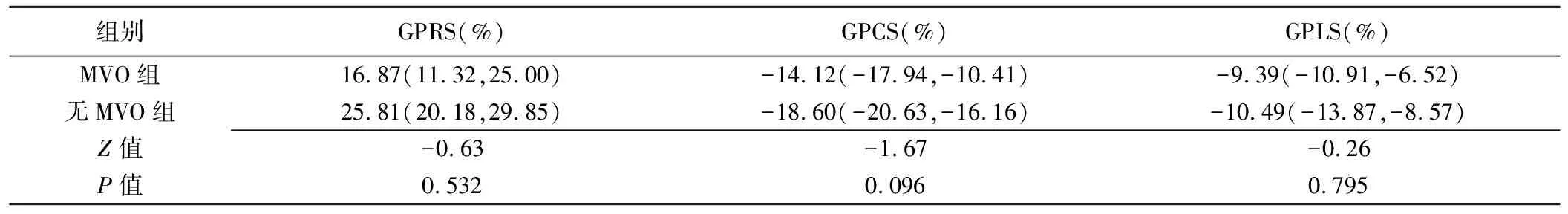
表4 MVO组与无MVO组左心室整体应变比较[中位数(上下四分位数)]
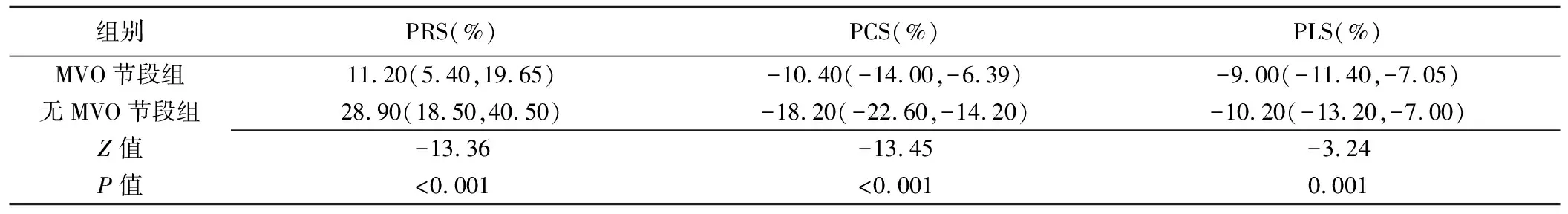
表5 MVO节段组与无MVO节段组节段应变比较[中位数(上下四分位数)]

表6 MVO组和无MVO组左心室心功能比较[中位数(上下四分位数)]
3 讨论
MVO是急性心肌梗死冠状动脉再灌注治疗后的并发症之一。研究[10]表明,超过50%的STEMI患者经PCI恢复相关动脉血流后发生MVO,且MVO是主要心血管不良事件和不良左心室重构的重要预测因子。准确识别MVO有助于完善对于STEMI患者的风险分层及评估预后。心肌应变指前后负荷作用下心肌组织从收缩到舒张的变形程度,能客观反映左心室结构及功能。CMR定量组织标记技术是评估心肌应变的“金标准”[11],但存在检查及后处理时间长、时间分辨率较差和心内膜标记线欠清等局限性,尚未在临床工作中广泛应用。
CMR-FT基于常规电影序列,可通过后处理软件较为简便地量化心肌应变,是能够无创、便捷地定量评估心肌梗死后结构及功能变化的新技术。既往研究[12]认为CMR-FT测量的心肌应变结果组内和组间重复性差。随着软件的发展,测量心肌节段应变结果的一致性逐步提高。近期研究[13]显示,CMR-FT测得的左心室整体及节段应变均有较好的重复性;本研究结果与之相符。
本研究中梗死组与对照组间左心室整体及节段应变值差异均有统计学意义,提示左心室整体及节段应变值有助于区分急性STEMI患者及健康人。MVO组左心室整体峰值应变绝对值均低于无MVO组,但差异无统计学意义,原因可能在于部分患者MVO面积较小或仅局限于某一节段心肌,所致节段心肌功能异常被代偿而未影响到整体应变。本研究中MVO节段组左心室节段峰值应变与无MVO节段组差异有统计学意义,与文献[7]报道相似;其中PRS、PCS诊断效能较高,可能与MVO的分布、心肌纤维走行及排列方式相关:心肌梗死时,最先累及远端心内膜下肌层;发生心肌缺血时,无论梗死程度及是否发生MVO,心内膜下肌束对应的纵向应变均不同程度受损[14],推测PLS可能是探测心内膜下肌层受损的最敏感预测因子,但其诊断MVO的特异性较低。
本研究的局限性:①样本量较小,且性别分布不均,男性明显多于女性;②未分析MVO严重程度和梗死透壁程度与心肌应变的相关性;③缺乏随访资料。
综上所述,通过CMR-FT测量左心室心肌节段峰值应变可检测心肌梗死患者是否发生MVO,为临床对急性STEMI患者进行早期风险分层管理提供了无创、便捷的新方法。
