海茸中L-岩藻糖及硫酸基的测定
2020-03-02颜丽刘秀河赵方铭李同乐
颜丽,刘秀河*,赵方铭,李同乐
(1.齐鲁工业大学(山东省科学院),济南 250353;2.济南褐藻生物工程有限公司,济南 250353)
海茸是海藻中一种淡黑巨海藻,是野生天然的深海植物,又因其生长环境特殊,采摘期短,因此非常珍贵稀有[1]。国内外对海茸保健功能的研究逐步深入,在我国海茸有着悠久的食用传统,在许多古代医学典籍中都有提及[2]。在食品行业,李建杰等[3]以木糖醇、甘露醇、山梨醇3种糖醇复配作为填充剂,以抹茶粉和食盐作为风味调节剂,成功研制了一款具有海洋特色的抹茶海盐口味南极海茸多糖咀嚼片。多糖是食品中的一类重要物质,可独立成胶替代传统增稠乳化稳定剂,常用于海产品中改良产品体系的质构和功能特性[4]。随着多糖成为研究热点,海洋多糖备受重视,多糖提取的方法有水提醇沉法、碱水提取法、酶解法等[5],海茸中L-岩藻糖含量对于岩藻多糖在食品与调味品领域的应用具有重要的指导意义。
本文主要对海茸中L-岩藻糖含量及硫酸基含量、褐藻胶含量等进行了测定,为后期实验的进行奠定一定的基础。
1 材料与方法
1.1 实验材料与仪器
1.1.1 主要仪器
TG16-WS高速台式离心机 湖南湘仪开发有限公司;数显恒温水浴锅 金坛市金南仪器厂;紫外分光光度计 上海美谱达仪器有限公司。
1.1.2 主要试剂
海茸:智利海域;L-岩藻糖标准溶液(20 mg):北京中科质检生物技术有限公司;硫酸钾:天津市大茂化学试剂厂;三氯乙酸、蒽酮:国药集团化学试剂有限公司;明胶:天津市富宇精细化工有限公司;氯化钡:天津市广成化学试剂有限公司。
1.2 溶液的配制
1 mg/mL L-岩藻糖标准样品:在购买的L-岩藻糖标准溶液中加入20 mL水。
0.12 mg/mL L-岩藻糖标准样品:吸取1200 μL 1 mg/mL L-岩藻糖标准样品,定容至10 mL。
0.1%蒽酮-硫酸溶液:称取0.1 g蒽酮,溶于100 mL浓硫酸中,于棕色瓶中保存,该溶液最多于冰箱中放置48 h。
0.5%明胶:精确称取1.25 g明胶于蒸馏水中,于60~70 ℃水浴中溶解完全,定容至250 mL容量瓶中。4 ℃下静置过夜,冷藏陈化。
明胶-氯化钡溶液:精确称取1.0 g氯化钡溶液于100 mL明胶溶液中,定容,于4 ℃静置2 h,冷藏保存。
硫酸钾标准溶液:精确称取105 ℃干燥至恒重的K2SO4固体 108.75 mg,用1 mol/L的盐酸定容至100 mL,即得0.6 mg/mL的硫酸钾标准溶液[6]。
1.3 海茸中L-岩藻糖含量的测定
1.3.1 L-岩藻糖标准溶液的制备
分别吸取0.12 mg/mL L-岩藻糖标准样品0.2,0.4,0.6,0.8,1.0,1.2 mL,置于10 mL具塞试管中,用蒸馏水定容至2.0 mL,之后迅速加入0.1%的蒽酮-硫酸溶液6 mL,摇匀后静置15 min,之后立即放入冰水浴中15 min,取出后在580 nm处测定吸光度,以浓度为横坐标,以吸光度为纵坐标,绘制标准曲线。
1.3.2 样品溶液中L-岩藻糖的测定
将海茸粉碎后过80目筛,用天平称取1.002 g粉末(精确到0.001 g),加入50 mL蒸馏水,静置1 h,加热回流4 h,静置冷却至室温,置于离心机中以9000 r/min 离心30 min,然后将上清液移入100 mL容量瓶中,沉淀用少量水分次洗涤,以9000 r/min离心后将上清液转入同一容量瓶中[7]。
量取上清液2 mL,置于50 mL离心管中,边搅拌边加入30 mL无水乙醇,摇匀,于4 ℃放置12 h,取出后以9000 r/min 离心30 min,弃去上清液,沉淀用沸水溶解,放冷,转移至100 mL容量瓶中定容。
吸取2 mL上清液,置于10 mL具塞试管中,迅速精密加入0.1%的蒽酮-硫酸溶液6 mL,摇匀静置15 min,之后立即放入冰水浴中15 min,测定样品吸光值。海茸中L-岩藻糖含量计算公式如下[8]:
L-岩藻糖含量=C×D×f/m×100%。
式中:C为L-岩藻糖的浓度,mg/mL;D为样品稀释倍数;f为换算因子;m为样品重量,mg。
1.3.3 换算因子测定
精密吸取L-岩藻糖标准液0.5 mL,按标准曲线的操作方法,测吸光度值,由回归方程求供试液中L-岩藻糖的含量,计算换算因子[9]:
f=w/cd。
式中:f为换算因子;w为所取L-岩藻糖浓度,mg/mL;c为L-岩藻糖测定浓度,mg/mL;d为稀释因子。
1.3.4 回收率实验
为了检验本方法的准确性和可靠性,要进行回收率实验,测定方法如下:
因标品配制浓度过高,经预实验后将L-岩藻糖标品浓度稀释20倍,配制成0.006 mg/mL的溶液,取L-岩藻糖标准溶液2 mL与L-岩藻糖样品液2 mL组成加样样品液,然后吸取此加样样品液2 mL,按标准曲线的制作方法,在580 nm处测定吸光度。
回收率=(加标L-岩藻糖含量-样品L-岩藻糖含量)/标品含量×100%。
1.3.5 重复性测定
精密量取6份海茸各1 g,按供试品溶液的配制方法制备成6份供试品溶液,各精密吸取2 mL,按上述方法测定L-岩藻糖的含量,检验该方法的重复性。
1.3.6 精密度实验
精密吸取同一个均匀供试品溶液6份各2 mL,按上述方法测定L-岩藻糖的含量,检验该方法的精密度。
1.4 L-岩藻糖中硫酸基的测定
1.4.1 K2SO4标准溶液配制
吸取标准 K2SO4溶液 0.00,0.04,0.08,0.12,0.16,0.20 mL,用1 mol/L盐酸溶液定容至0.20 mL,加入3%三氯乙酸3.8 mL 及氯化钡明胶溶液1.0 mL,摇匀,室温静置 15 min,于360 nm 波长处测定吸收度 A1;以1.0 mL明胶溶液代替氯化钡明胶溶液,测吸收度A2。以硫酸基浓度(mg/mL) 为横坐标,吸光度(A1-A2)为纵坐标绘制标准曲线。
1.4.2 L-岩藻糖样品溶液中硫酸基测定
取1.3.2所述的醇沉后的岩藻糖溶液,于烘箱中烘干,得约50 mg干制岩藻糖粉末,然后加入25 mL 1 mol/L盐酸溶液,于100 ℃下加热6 h,冷却后以8000 r/min离心20 min,过滤,用HCl定容至25 mL。吸取0.2 mL,加入3% TCA 3.8 mL 及BaCl2-明胶溶液1.0 mL,摇匀,室温静置 15 min,于360 nm 波长处测定吸收度 A1;以1.0 mL明胶溶液代替氯化钡明胶溶液,测吸收度A2,公式如下[10]:
SO42-含量=f×(C/0.2)×V/W×100%。
式中:f为换算因子;C为SO42-测定浓度,mg/mL;V为样品水解液总体积;W为初始样品质量。
1.4.3 换算因子的测定
精密吸取K2SO42-标准贮备液0.15 mL,按标准曲线的操作方法,测吸光度值,由回归方程求供试液中SO42-的含量,根据 f=w/cd 计算换算因子,其中 w 为所取硫酸根浓度,c为硫酸根测定浓度,d为稀释因子。
1.4.4 回收率实验
因标品配制浓度过高,经预实验后将SO42-标品浓度稀释10倍,配制成0.06 mg/mL的溶液,分别取0.2 mL标准溶液与0.2 mL样品溶液组成加样样品液,然后吸取此加样样品液0.2 mL,按标准曲线的制作方法,在360 nm处测定吸光度。
1.4.5 精密度的测定
精密吸取同一个均匀供试品溶液6份各0.2 mL,按上述方法测定SO42-的含量,检验该方法的精密度。
1.4.6 重复性的测定
精密量取 6 份干燥的L-岩藻糖样品各50 mg,按供试品溶液的配制方法制备成 6 份供试品溶液,各精密吸取0.2 mL,测定硫酸基含量。
1.5 褐藻胶含量的测定(质量法)[11]
将海茸粉碎过40目筛网,称取过筛后的海茸2 g于烧杯中,向其中加入0.5 g固体碳酸钠和50 mL水,在80~90 ℃下水浴加热2 h,期间不断搅拌,当烧杯内全部物质呈糊状时停止,加水稀释至100 mL,搅拌均匀,以4000 r/min离心10 min,收集上清液,向滤渣中加入少量的水,加温搅拌,离心,收集上清,合并2次上层液,其中加入1∶1的盐酸,调制pH为2.0,静置老化30 min后,经过100目筛网过滤,使大部分酸液流出,不断搅拌酸液并向其中不断加入2 mol/L氢氧化钠溶液至pH 6.0~7.0;加入海藻酸钠溶液1倍体积的95%乙醇,沉淀脱水,用尼绒筛绢过滤拧干,放入烘箱中,于103 ℃烘干至恒重,记录质量。测定结果按下式计算:
褐藻胶含量=m1/m2×100%。
式中:m1为烘干后褐藻胶的质量,g;m2为样品质量,g。
2 结果与分析
2.1 海茸中L-岩藻糖含量
2.1.1 L-岩藻糖标准曲线绘制
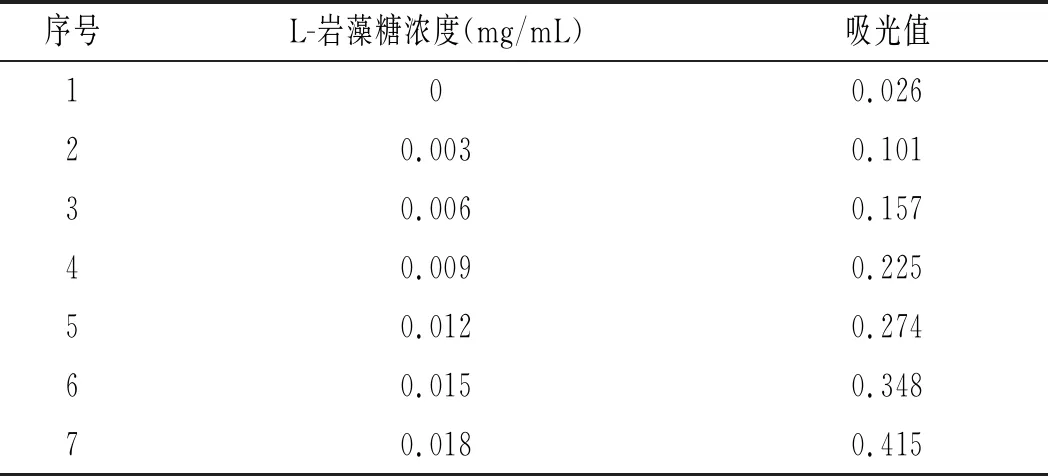
表1 L-岩藻糖标准曲线测定结果Table 1 Determination results of L-fucose standard curve
根据表1绘制的L-岩藻糖标准曲线见图1。
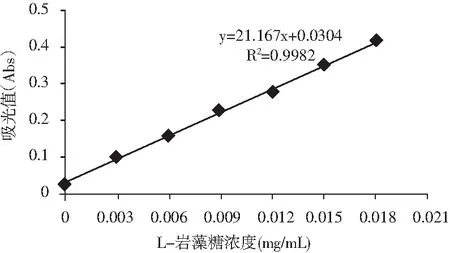
图1 L-岩藻糖标准曲线Fig.1 Standard curve of L-fucose
由图1可知,当L-岩藻糖浓度在0~18 μg/mL范围内线性关系良好,所得的回归方程为y=21.167x+0.0304,R2=0.9982。
2.1.2 换算因子测定结果
根据公式f=w/cd计算,w为所取岩藻糖的浓度,为0.12 mg/mL,c为岩藻糖测定浓度,测定吸光值为0.195,根据标准曲线所得,L-岩藻糖浓度为0.0077 mg/mL,因此得出换算因子f=0.965。
2.1.3 样品中L-岩藻糖含量
根据海茸中L-岩藻糖含量的测定公式:L-岩藻糖含量=C×D×f/m×100%,得出结果见表2。
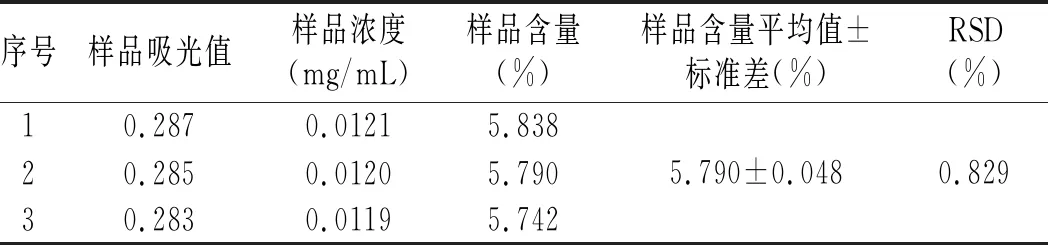
表2 样品中L-岩藻糖的含量测定Table 2 Determination of L-fucose content in samples
2.1.4 回收率实验结果
回收率实验结果见表3。
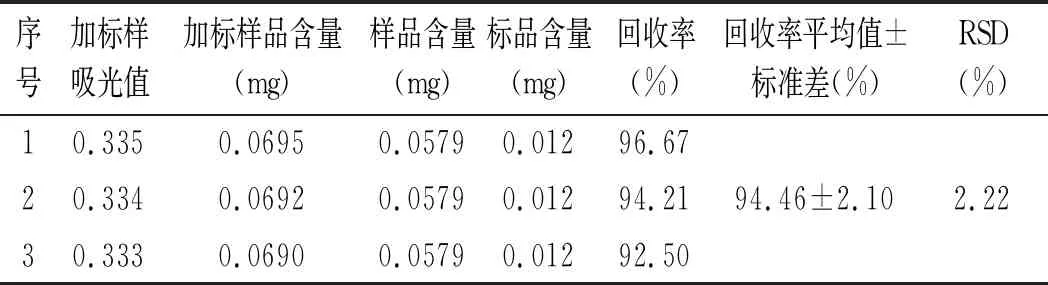
表3 样品回收率实验结果Table 3 Experimental results of recovery rates of samples
由公式回收率=(加标样品含量-样品含量)/标品含量×100%,可计算出回收率为94.46%,且RSD=2.22%<5%,证明该结果准确性良好。
2.1.5 精密度实验测定结果
取同一份样品测量6次,实验结果见表4。

表4 海茸中L-岩藻糖含量Table 4 The content of L-fucose in seaweed
经实验结果证明,RSD为1.46%<5%,证明该实验精密度良好。
2.1.6 重复性实验结果
按照2.1.5所述的6个海茸样品测得的L-岩藻糖含量见表5。

表5 L-岩藻糖含量测定结果Table 5 Determination results of L-fucose content
由表5可知,6组海茸样品的含量差不多,得出的RSD为1.06%<5%,因此该实验的重复性良好。
2.2 L-岩藻糖中SO42-含量测定
2.2.1 硫酸根标准曲线绘制
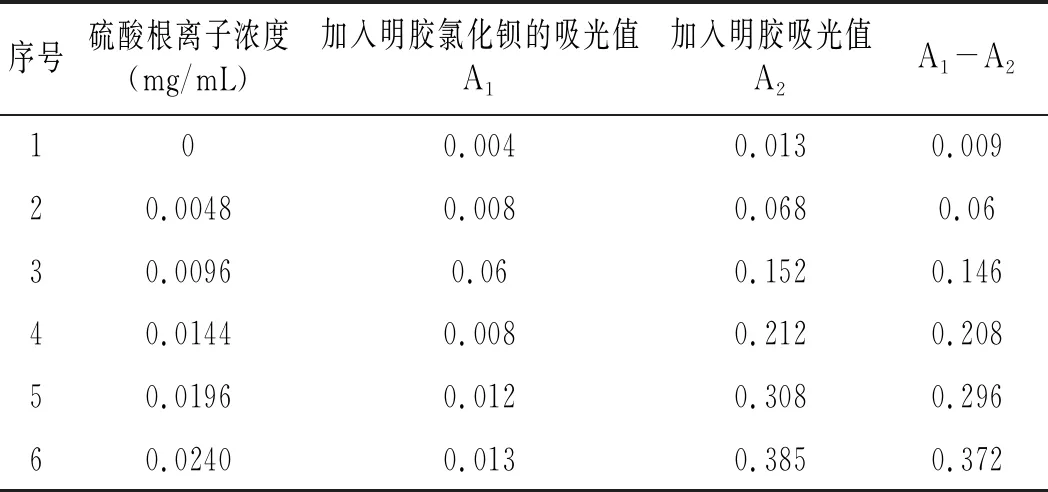
表6 SO42-标准曲线测定结果Table 6 Determination results of SO42- standard curve
根据表6绘制的SO42-标准曲线见图2。
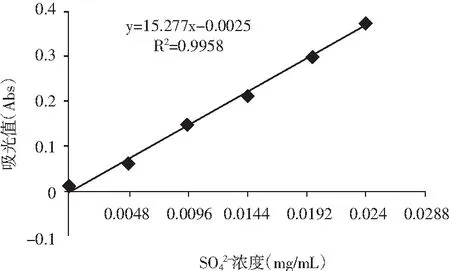
图2 SO42-标准曲线Fig.2 Standard curve of SO42-
由图2可知,SO42-浓度在0~24 μg/mL时呈现良好的线性关系,此时标准曲线回归方程为y=15.277x-0.0025,R2=0.9958。
2.2.2 换算因子测定
根据公式f=w/cd,w为所取SO42-的含量,为0.09 mg,c为SO42-测定含量,测定吸光值为0.293,根据标准曲线所得,SO42-浓度为0.0193 mg/mL,测得的SO42-含量为0.002895 mg,因此得出换算因子f=1.241。
2.2.3 L-岩藻糖中SO42-含量
SO42-含量测定结果见表7。
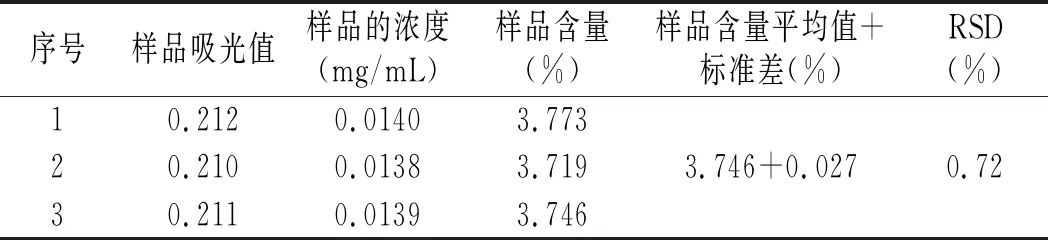
表7 SO42-的测定结果Table 7 Determination results of SO42-
由公式得SO42-含量=(C/0.2)×V×f/W=3.746%,且RSD为0.72%,说明该数据准确性良好。
2.2.4 回收率实验结果
SO42-的回收率结果见表8。
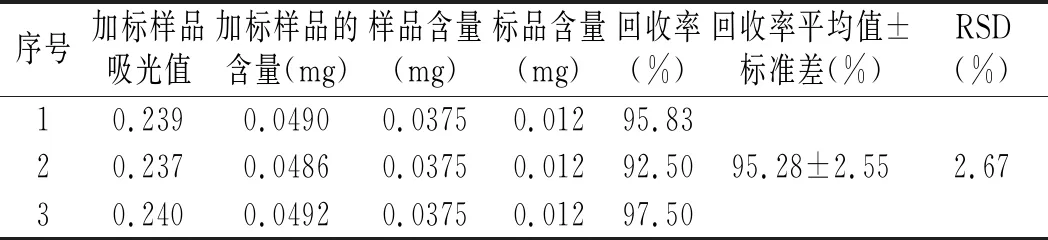
表8 SO42-回收率测定结果Table 8 Determination results of SO42- recovery rates
由公式回收率=(加标样品含量-样品含量)/标品含量×100%,可计算出回收率为95.28%,且RSD=2.67%<5%,证明该结果准确性良好。
2.2.5 精密度实验测定结果
取同一份样品测量6次,实验结果见表9。

表9 L-岩藻糖中SO42-含量Table 9 The content of SO42- in L-fucose
经实验结果证明,相对标准偏差RSD为1.41%<5%,证明该实验重复性良好。
2.2.6 重复性实验结果
按照2.2.5所述的称取的6组岩藻糖样品测得的SO42-含量的结果见表10。

表10 SO42-含量重复性测定结果Table 10 Repeatability testing results of SO42- content
2.3 褐藻胶含量测定
海茸的褐藻胶含量测定结果见表11。
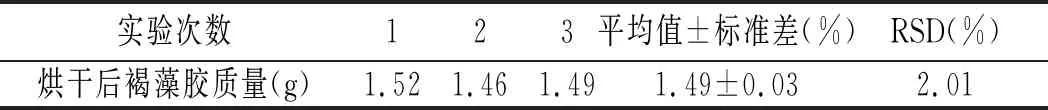
表11 褐藻胶含量测定结果Table 11 Determination results of sodium alginate content
根据公式褐藻胶含量=m1/m2×100%=74.5%,RSD值为2.01%<5%,证明该结果准确性良好。
3 结论
绘制了L-岩藻糖的标准曲线,L-岩藻糖在0~18 μg/mL呈良好的线性关系,R2=0.9982;采用热水浸提法提取海茸中L-岩藻糖,其含量为5.790%,回收率为94.46%,相对标准偏差为1.46%和1.06%,表明精密度和重复性良好,用比色法测定 L-岩藻糖简单、准确、快速、方便,适合在实验室中操作。用硫酸钡比浊法测定多糖中硫酸基含量,设备要求较低,操作简便,适用于普通实验室[12];硫酸根浓度的吸光值在0~24 μg/mL范围内线性关系良好,R2=0.9958;测定海茸中L-岩藻糖的SO42-为3.746%,回收率为95.28%,相对标准偏差为1.41%和3.22%,精密度和重复性良好。海茸中褐藻胶含量达到74.5%。
