复杂混合气体组分在低温活性炭表面的吸附特性
2020-02-25杜卫星龙兴贵
马 浚,杜卫星,龙兴贵
(中国工程物理研究院 核物理与化学研究所,四川 绵阳 621900)
反应堆事故或核爆核查气体,近区组分较复杂,不仅有空气的气体组分和裂变产生的放射性气体Kr、Xe[1],还有一些有机物不完全燃烧得到的特殊气体组分,如H2、CH4、CO和CO2等。对这些气体的全组分取样测量,可了解反应堆事故中的裂变发生状况以及其中相关材料的变化情况,或了解被核查方是否遵守核禁试条约[2]。但相对目标气体Kr、Xe,气体中含有大量的杂质,如大量的CH4和CO2等,这些组分对重要气体核素Kr、Xe的回收有很大的影响,不能使用目前处理Ar[3]、Xe[4-8]的方法,需要开拓新流程,对影响Kr、Xe回收的气体组分进行去除。
混合气体的吸附特性目前报道较多,尤其以二元或三元气体吸附研究居多,更多气体组分组成的混合气体研究较少。所使用的气体吸附剂虽在近几年针对不同的目标吸附物有一些改进,但在实际工作中,活性炭仍是使用最广泛的吸附剂。相对于碳分子筛[9]、碳纤维[10],活性炭表面吸附的气体更易实现解吸,在以Kr、Xe为目标气体的分离测量过程中,能缩短实验时间和减少吸附残余从而提高目标气体产率。
目前,出于对反应堆安全的担忧,需模拟反应堆事故环境,对事故后可能的混合气体进行分离,测量特征生成物,判断事故的严重程度和所需采取的措施。核事故中生成的放射性Kr、Xe气体较少,且易在环境中扩散,要达到测量要求,需对反应堆周围大体积的空气组分进行处理,提取出Kr、Xe组分,这方面的研究还很少见报道。当前,需加工一套处理100 L模拟气体样品的分离系统用于在突发核事故中处理来自于内部的气体样品。本文拟对4A分子筛吸附水和CO2的能力进行评估,并对混合气体中各组分在低温活性炭柱上的吸附特性进行研究,选择适宜的吸附、分离条件,为分离流程的建立提供依据。
1 实验
1.1 主要器材
GC-450气相色谱仪,Varian公司;质量流量计,Alberg公司;压力传感器,宝鸡传感器厂;真空计,四川成华有限责任公司;温度显示仪,成都科宝中计测试技术实业有限公司。
混合气体(主要组分为N2、10%的H2和CO、7%的CO2、3%的CH4、微量的Kr和Xe),西南化工研究设计院;高纯氦气,99.999 5%,西南化工研究设计院;4A分子筛,上海恒业分子筛厂;活性炭,北京市光华晶科活性炭有限公司;低温循环泵,常州诺基仪器有限公司。
1.2 方法
混合气体中各组分的吸附特性研究在图1所示实验装置上进行。
实验过程如下:1) 将4A分子筛的吸附床在673 K温度下抽真空活化至少10 h;2) 将活性炭柱(由直径6.35 mm铜管制备成螺旋状填充柱,装量为6 g,管长约120 mm)在573 K下抽真空活化至少8 h;3) 采用真空泵抽空和高纯氦气流洗的方法将系统中的空气排出,充入氦气使系统的压力为1.01×105Pa;4) 将混合气体减压后流出,并调节流量;5) 混合气体先经过4A分子筛除去其中的水分和CO2,再流经低温下的活性炭柱对混合气体进行分离,在尾气出口,用气相色谱仪间隔测定各气体组分的浓度。
1.3 气相色谱条件
采用气相色谱仪测量气体组分,载气为高纯氦气,其他分析条件列于表1。

图1 实验装置示意图Fig.1 Schematic diagram of experimental device
表1 气相色谱仪分析条件
Table 1 Analysis condition for gas chromatograph
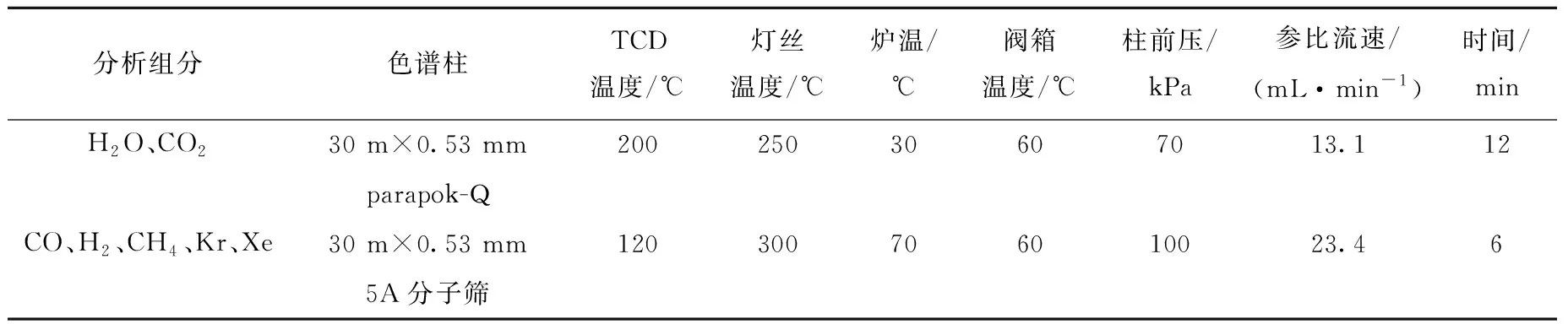
分析组分色谱柱TCD温度/℃灯丝温度/℃炉温/℃阀箱温度/℃柱前压/kPa参比流速/(mL·min-1)时间/minH2O、CO230 m×0.53 mm20025030607013.112parapok-QCO、H2、CH4、Kr、Xe30 m×0.53 mm120300706010023.465A分子筛
1.4 定量分析
以氦气为底气,使用压力法配制的双组分气体作为标准气体,采用标准曲线法进行定量分析。实验中使用的模拟混合气体各组分的含量列于表2。

表2 模拟混合气体中各组分的含量Table 2 Content of component in simulated mixture gas
取样分析采用气体直接进样的方式。选择进样压力以保证合适的进样量,使气体浓度不超出检测上限。
将第1次测量到某组分的浓度c和原料气浓度c0的比值,即穿透率c/c0=0.05所对应的时间作为穿透时间来计算穿透体积。饱和穿透时间则定义为穿透率c/c0=0.95时对应的穿透时间,进而计算饱和穿透体积。
2 结果及讨论
2.1 混合气体中水和CO2的去除
1) 4A分子筛对水分的去除
采用4A分子筛实现对水分的去除。使用4根不同的4A分子筛柱,考查动态吸附下,4A分子筛对水分的吸附容量。4根4A分子筛柱分别为:直径12.7 mm铜管制备的4 g分子筛柱(柱1);直径6.35 mm铜管制备的8 g分子筛柱(柱2);直径12.7 mm铜管制备的8 g分子筛柱(柱3);直径12.7 mm铜管制备的33 g分子筛柱(柱4)。使用气相色谱仪检测尾气中水分的流出时间,作为4A分子筛吸水达到饱和的时间,计算其动态吸水量。为更好地模拟4A分子筛对水分的吸附作用,实验中使气体穿过200 mL蒸馏水形成常温含水分饱和的混合气体,实验时的环境温度为25 ℃,1.01×105Pa气压下饱和水蒸气含水量为20.356 g/kg,气体流速为0.4 L/min。计算的动态吸水量列于表3。由表3可见,动态吸水量为118~123 mg/g,这与理论吸水量200 mg/g有较大差距,但与一般估算的动态吸水量较接近。4根径高比不同的4A分子筛柱的动态吸水量相近,且在实验中均随气体的快速通过而达到动态吸附饱和,说明4A分子筛对水分的吸附速率较快。根据动态吸水量的数据,以气体通过水达到饱和来计算,100 L样品气包含的水分为2.4 g,被充分吸附所需要的4A分子筛的量约为20 g,如果考虑气体流速、气体与吸附剂的接触、柱的径高比引起的效率问题,至少需要2~3倍以上余量,4A分子筛柱才能较完全除去混合气体中的水。

表3 4A分子筛的动态吸水量Table 3 Dynamic water absorption of 4A molecular sieve
2) 4A分子筛对CO2的去除
CO2的吸附剂较多,4A分子筛是其中之一。研究中为减少步骤,在同一根4A分子筛柱上实现水和CO2的同时分离。开始也使用了以上的4根4A分子筛吸附柱,柱1、3在第1次测量时已达到饱和穿透点,柱2、4在进样量为10 L和25 L时达到饱和穿透点。另采用2根φ60 mm×750 m的4A分子筛柱串联1根容量较大的柱(柱5)进行实验。柱5填装的分子筛约为2.9 kg。柱2、4、5的CO2吸附穿透曲线示于图2。由图2可见,柱5在进样225 L时达到CO2穿透时间,在进样约235 L时达到饱和穿透时间。

图2 常温下CO2在4A分子筛上的吸附穿透曲线Fig.2 Adsorption breakthrough curve of CO2 on 4A molecular sieve at room temperature
与4A分子筛对水的吸附相比,其对CO2的吸附量不大。柱5中4A分子筛的容量达到2.9 kg,流速为0.5 L/min,以达到穿透点为处理样品的最大体积,则能处理的样品气约为220 L,在此流速下处理100 L样品需要的分子筛容量应不低于1.4 kg。考虑后续气路中低温活性炭柱气阻作用导致的流速变化、水和CO2存在的竞争吸附、被吸附CO2在气流作用下的迁移等因素,采用2~3倍容量(约3 kg)的4A分子筛柱是适宜的。
混合气体中的水和CO2对目标气体组分Kr、Xe的吸附影响较大[9,11],文献[12]认为使用13X分子筛去除CO2效果较好,但常温下13X分子筛能吸附目标气体Xe,使Xe回收率偏低。本实验选择4A分子筛作为水和CO2的吸附剂,更重要的原因是4A分子筛对目标气体Kr、Xe不吸附。
3) CO2和水的竞争吸附关系
根据4A分子筛的动态吸水量,100 L样品所需的4A分子筛的容量只需约50 g。但混合气体中同时含有水和CO2时,二者存在竞争吸附,水的极性很大,吸附能力较强,会阻碍CO2的吸附,因此4A分子筛的用量会显著增加。CO2和水在活性炭表面的吸附行为完全不同[13],在活性炭表面CO2的吸附速率较水大得多,而在4A分子筛上,其对水的吸附量远大于对CO2的。究其原因,一方面与水和CO2分子及2种吸附剂的极性有关,CO2是非极性分子,易吸附在非极性吸附剂表面,活性炭偏非极性,但其表面也有许多极性基团,故也能吸附少量的极性分子,如水等;而水是极性很强的极性分子,4A分子筛表面有很多极性基团,因此水很容易吸附在这种极性吸附剂表面,而吸附剂表面还存在非极性基团,故也能吸附非极性分子。另一方面,也与这2种吸附剂中的孔径有很大关系,活性炭中存在中空和微孔结构,在活性炭吸附CO2时,CO2首先被吸附在活性炭的微孔中,水不一定局限在微孔中,而是更多地吸附在活性炭表面的亲水基团上,因此可将CO2和水在活性炭上的吸附看作是两个相对独立的过程[13]。而CO2和水在4A分子筛上的吸附则正好相反,水首先吸附在微孔中,而CO2则选择性吸附在4A分子筛表面的非极性基团上。CO2和水在活性炭上的吸附,首先是CO2吸附,然后才是水的吸附,水的吸附会产生较多的热量促使CO2解吸,并推动CO2向柱出口迁移;CO2和水在4A分子筛上的吸附首先是水的吸附产生较大的热量,随后CO2的吸附产生较少的热量,与在活性炭上的吸附相比,其对水在柱中的向前推动作用小得多。因此,水更多地吸附在4A分子筛的前部,相比之下,CO2在柱中移动较快,较易穿透流出。
2.2 低温下混合气体中各组分在活性炭表面的吸附特性
1) H2的吸附
在273、264、255、246、238 K下进行各组分在活性炭上的穿透实验,除Xe外,其他组分的吸附实验采用的气体流速均为10 mL/min。
H2在5个温度下都极易穿透。H2的穿透在246 K和238 K下稍有延迟,但流洗100 mL样品,出口尾气中H2的浓度已达到平衡。因此H2在活性炭表面的吸附与其他组分存在显著差异,属不易吸附组分。在较低温度下进行分离时,可利用H2在活性炭上不易吸附的性质,使H2随尾气流出而去除。
2) N2的吸附
模拟混合气体中N2是作为混入环境空气组分加入的。N2一般在H2后随即流出,因为含量较高,也可看作是一种载气,在活性炭柱上达到饱和吸附,且吸附系数低较,较强吸附能力的气体很容易将活性炭表面的N2置换,置换出的N2又会在活性炭柱靠后的空隙中吸附,这样不断地吸附解吸使N2向出口迁移,最终随尾气流出而去除。
3) CO的吸附
在273、264、255 K下,CO很容易穿透,基本在进行第1次测量时就已达到饱和穿透点。246 K和238 K下的CO在活性炭上的吸附穿透曲线示于图3。由图3可见,246 K时,CO穿透时间稍延后,但达到平衡的时间约为25 min;238 K时,达到平衡的时间约为100 min。温度逐渐降低时,CO在活性炭表面的吸附明显增强。温度降低时,CO在活性炭表面的吸附可能从大孔表面吸附逐渐过渡到微孔吸附,238 K下的吸附穿透曲线符合微孔吸附的特征。

图3 低温下混合气体组分CO在活性炭柱上的吸附穿透曲线Fig.3 Adsorption breakthrough curve of CO in mixture gas on activated carboncolumn at low temperature
4) CH4的吸附
CH4在273、264、255、246、238 K下的吸附穿透曲线示于图4。由图4可知,CH4在5个温度下的穿透时间分别为15、35、50、60、100 min。观察5条吸附穿透曲线上穿透率上升最快过程的直线斜率,均是在初次穿透后约20 min达到饱和穿透时间。
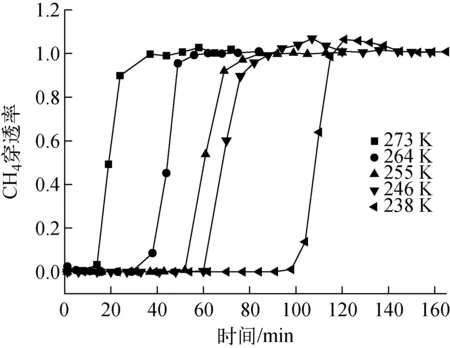
图4 低温下混合气体组分CH4在活性炭柱上的吸附穿透曲线Fig.4 Adsorption breakthrough curve of CH4 in mixture gas on activated carbon column at low temperature

图5 低温下混合气体组分Kr在活性炭柱上的吸附穿透曲线Fig.5 Adsorption breakthrough curve of Kr in mixture gas on activated carboncolumn at low temperature
5) Kr的吸附
Kr在273、264、255、246、238 K下的吸附穿透曲线示于图5,分别在24、49、69、74、104 min到达穿透时间。对Kr的穿透影响最大的温度是238 K,此温度下Kr的穿透时间明显后移。
与图4相比可见,在低温下,Kr在活性炭表面的吸附性能与CH4相似。尤其在238 K时,CH4和Kr的穿透时间已非常接近。因此,如果要在活性炭上利用吸附特性实现CH4和Kr的分离,温度须在238 K以上,根据穿透时间的比较可知,255~246 K温度范围适于实现CH4和Kr的吸附分离,此时,所需要的活性炭的容量和活性炭柱的长度都将大幅增加,且需要有很大的设计余量,所以对于百升级的总混合气体量,要实现这2种气体的吸附分离所需要的活性炭的容量将很大。因此,对CH4的去除主要采用氧化法。
CH4和Kr在低温下的吸附性能相近,在活性炭上主要吸附在微孔中,且存在竞争吸附。但由于混合气体中2种气体组分浓度相差较大,浓度大的CH4在活性炭上吸附占据了大量的微孔阻碍了目标物Kr的吸附,因此CH4的去除是Kr回收的关键步骤。
6) Xe的吸附
Xe在273、264、255、246、238 K下的吸附穿透曲线示于图6。由于Xe在低温下的穿透较困难,实验中采用的气体流速为80 mL/min。由图6可知,Xe相对于其他气体组分有最大的穿透体积,因此Xe在活性炭上的吸附能力较强,分离相对容易。
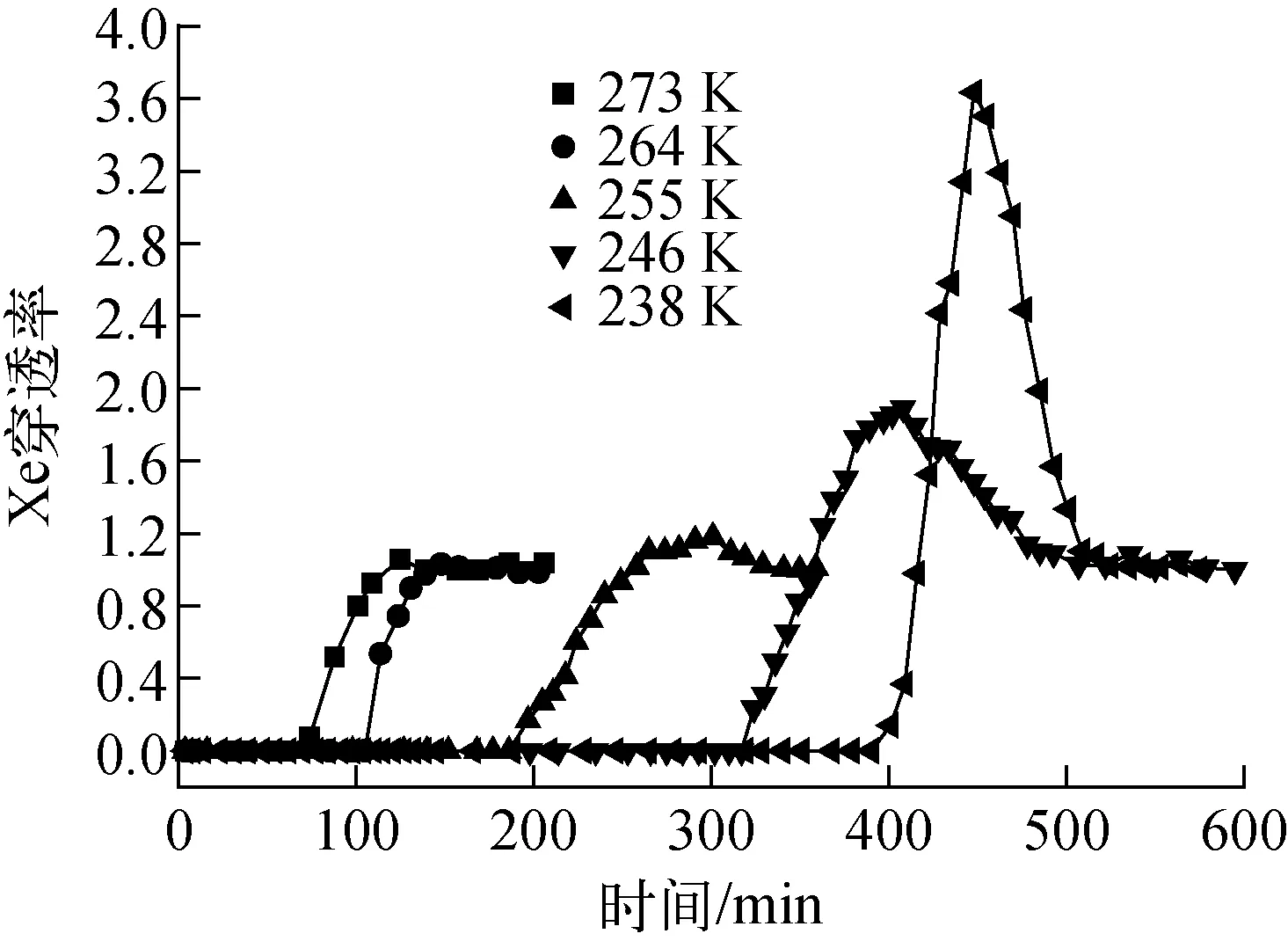
图6 低温下混合气体组分Xe在活性炭柱上的吸附穿透曲线Fig.6 Adsorption breakthrough curve of Xe in mixture gas on activated carboncolumn at low temperature
实验中还发现,随着温度的逐渐降低,Xe和CO2在活性炭表面还发生了竞争吸附。低温时,CO2和Xe的竞争吸附不仅与两者浓度有关,更重要的是与吸附时的温度有关,温度越低,CO2对Xe的吸附影响越明显,183 K下,1%含量的CO2使Xe的吸附量减少81.8%[14]。245 K下,CO2浓度不同对Xe吸附的影响也不同,CO2浓度小于4.5×10-5mol/L时,对Xe动态吸附基本无影响;CO2浓度在4.5×10-5~2.2×10-3mol/L时,对Xe的吸附有较小的影响;CO2浓度大于2.2×10-3mol/L时,对Xe动态吸附影响显著[12]。实验中CO2的来源主要是4A分子筛对CO2吸附不彻底造成的。虽然按照前文的穿透实验,CO2没有穿透,但仍有极微量的CO2没有被4A分子筛床吸附,且由于CO2的吸附能力很强,从而在活性炭床逐渐聚集,并随温度的降低这种竞争吸附就更加明显。CO2和Xe在活性炭表面发生的竞争吸附主要在相同孔径区域,一般认为是发生在炭的过渡孔[14]。这与在高温下活性炭对CO2的吸附发生在微孔的情况截然不同,可认为,CO2在较高温度时由于在过渡孔吸附后易解吸迁移,吸附主要发生在吸附能较大的微孔区域[14],273 K下,CO2的吸附量还与活性炭中微孔孔容呈正相关关系[15],随着温度降低到273 K以下,CO2的吸附不仅在微孔区,更多的吸附在过渡孔区。这种现象在研究CO2和Xe在不同材料制备的活性炭纤维表面吸附时也得到了印证[16],在259~291 K温度范围,2种气体吸附在吸附材料相同的孔径中,具有相似的吸附规律。由图6可知,在238 K时,尾气流出的Xe的浓度最大时达到进口浓度的4倍;246 K时,尾气流出的Xe的最大浓度是进口浓度的2倍;255 K时,尾气流出的Xe的最大浓度仅稍有增加;而在273、264 K时尾气流出Xe的最大浓度和进口浓度基本一致。这说明,在273~238 K温度范围内,使用4A分子筛吸附后剩余的CO2流入活性炭床,随着温度的降低,竞争吸附逐渐变强,CO2的吸附能大于Xe的吸附能,从而使易吸附组分在流出口的浓度大幅增加。
本文采用SUNNA系统的方法,去除CO2采用三级:首先是4A分子筛对CO2和H2O进行去除;随后对吸附柱进行解吸,对CO2和H2O进行进一步去除;对吸附柱进行二次解吸,CO2采用3A分子筛完全去除。
由图3~6可见,对H2的分离去除几种温度下都较易实现。对CO的分离去除,238 K时,活性炭的吸附力显著增大,穿透时间大幅延长,达到平衡后,CH4和Kr相继穿透,严重影响目标气体Kr的回收率。因此,分离CO时温度应适当增加,根据实验结果,选择246 K较适宜。考虑到在238 K以下,CH4和Kr在活性炭表面的吸附性能非常相近,为对CH4进行部分分离,也应采取238 K以上的温度,因此选择246 K的低温分离较适宜。
2.3 CH4的氧化
在实际的气体流程中,CH4的分离去除较困难。因此,对CH4的去除采用2种方法:1) 对于CH4含量在1%以上的混合气体,处理量大于百升级时,先用MnO2氧化,剩余少量的CH4再用锆钒铁吸气剂进一步氧化;2) 对于CH4含量在1%以下的气体,处理量小于百升级时,直接用锆钒铁吸气剂进行去除,此外,在制备锆钒铁柱时应控制温度和径高比。一般在使用锆钒铁吸气剂时,首先应在约773 K温度下通高纯氦气对吸附柱进行活化,在对混合气体活性组分的去除中,锆钒铁中的有效组分逐渐损耗,温度须渐次升高,在873 K以上逐渐失去氧化吸气性能后,需更换锆钒铁柱。
3 结论
为实现较复杂混合气体的分离,测定了组分中的水和CO2在4A分子筛上的吸附穿透曲线及H2、N2、CO、CH4、Kr、Xe在低温活性炭上的吸附穿透曲线。得到以下主要结论。
1) 4A分子筛对H2O的吸附速率较对CO2的快,吸附量也较大。采用加大容量的4A分子筛也能较好地去除CO2,但微量的CO2仍会进入活性炭柱,在低温下对活性炭吸附Xe产生影响。
2) H2、N2、CO、CH4、Kr和Xe在低温活性炭上的吸附特性研究表明:N2是混合气体的底气,基本在活性炭柱上达到饱和吸附;H2很容易穿透随尾气流出而去除;Xe最易在低温活性炭上吸附,作为目标气体最后可通过解吸而回收;CO在活性炭上的吸附随温度的变化较显著,可选择适宜的温度和活性炭柱合适的径高比使CO随尾气流出而去除;在低温下,CH4和Kr在活性炭表面的吸附性质非常相似,很难用吸附法进行分离,采用氧化法对CH4进行氧化去除,可较好地实现对目标气体Kr的回收。
