TACE联合围术期连续服用索拉菲尼治疗中晚期肝细胞癌的安全性探讨
2020-02-21杜帅邓毅磊赵龙栓
杜帅 邓毅磊 赵龙栓
郑州大学第一附属医院肝胆胰外科 郑州 450052
原发性肝癌是全球范围内最普遍的恶性肿瘤之一,也是我国第4位常见的恶性肿瘤及第3位肿瘤致死病因,严重威胁我国人民的生命和健康[1]。而肝细胞癌(Hepatocellular Carcinoma,HCC)占原发性肝癌的85%~90%,早期诊断率低,确诊时多已至中晚期[2]。对于中晚期已失去根治性手术机会的HCC患者,经导管肝动脉化疗栓塞术(transcatheter arterial chemoembolization,TACE)联合索拉菲尼治疗已被证实为最佳治疗方案,但二者联合治疗的时机尚无定论。国内外推荐的治疗方案有三种。(1)序贯治疗:TACE治疗后待肝功能或疾病恶化再服用索拉菲尼。(2)间断治疗:两次TACE治疗间歇期间服用索拉菲尼。(3)连续治疗:TACE联合索拉菲尼服用,无间歇期[3]。日本最新TACTICS研究选用的方案为每次TACE治疗前2 d和治疗后3 d中断索拉菲尼,目的是维持器官功能,以免发生严重不良反应。但其忽略了TACE后24 h内VEGF便可显著升高,从而诱导肿瘤新生血管生成,促进残余肿瘤细胞增殖,导致复发转移。而索拉菲尼的清除半衰期为25~48 h,给药7 d后血药浓度才能达到稳态,从而最大程度抑制VEGF的升高。如围术期停用索拉菲尼,会导致一段时间内VEGF逐渐升高而增加术后肝癌复发转移的可能性。因此,理论上TACE联合围术期连续服用索拉菲尼可带来最佳疗效,但是否会引起不良反应的叠加而导致严重不良反应,需临床进行探讨。选取2017-01—2019-01间我院收治的220例中晚期HCC患者,对其临床资料进行回顾性分析,以探讨TACE联合围术期连续服用索拉菲尼的安全性。
1 资料与方法
1.1一般资料本组220例患者均依据2017版原发性肝癌诊疗规范确诊。BCLC分期B期~C期,中国肝癌分期Ⅱ期~Ⅲ期。肝功能Child-Pugh分级A级~B级。美国东部肿瘤协作组 (Eastern Cooperative Oncology Group,ECOG)体力状况评分≤2分。未合并其他恶性肿瘤、血液系统疾病、严重肾功能及凝血功能障碍。均由同一组医生行TACE及相关治疗。患者均签署知情同意书。根据围术期是否连续服用索拉菲尼分为对照组(162例)和观察组(58例),2组患者的基线资料比较,差异无统计学意义(P>0.05),有可比性,见表1。
1.2治疗方法对照组实施TACE:采用Seldinger法经股动脉插管引入导管,选择性腹腔动脉及超选择性肝动脉造影,确定肿瘤供应血管后经微导管推注奥沙利铂100 mg、雷替曲塞2 mg水溶液行局部灌注化疗。后使用超液态碘化油10 mL与雷替曲塞2 mg水溶液行化疗栓塞术,并使用150~350 μmPVA颗粒巩固栓塞。观察组:于TACE治疗前至少1周至TACE治疗后至少3 d,早晚各口服索拉菲尼400 mg。TACE术后2组均常规使用相同厂家及相同剂量的抗生素、保肝、护胃、止吐药物。
1.3观察指标TACE术前2 d及术后第3天的实验室指标及发热、腹痛、上消化道出血和术后3~4级胃肠道反应发生率。实验室指标包括淋巴细胞(Lymph)、中性粒细胞(Neut)、血小板(PLT)、谷丙转氨酶(ALT)、谷草转氨酶(AST)、总胆红素(TBIL)、直接胆红素(DBIL)、白蛋白(ALB)、凝血酶原时间(PT)、肌酐(SCr)、尿素氮(BUN)。
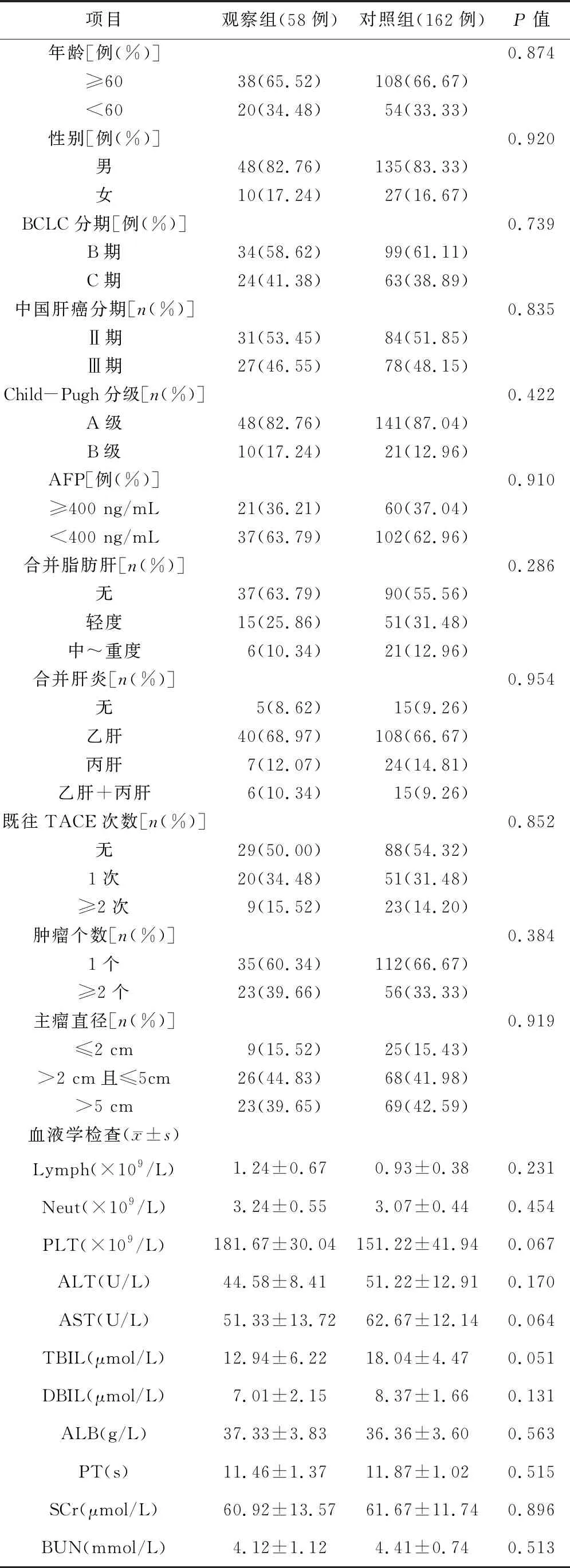
表1 2组患者的基线资料比较
注:血液学检查标本来源于TACE术前2天。中国肝癌分期参考《原发性肝癌诊疗规范(2017年版)》中的肝癌临床分期,并将Ⅱa期及Ⅱb期统计为Ⅱ期,将Ⅲa期及Ⅲb期统计为Ⅲ期
2 结果
220例患者均完成相关治疗并顺利出院。2组患者TACE术后Lymph、Neut、PLT等各指标水平,以及发热、腹痛、上消化道出血和3~4级胃肠道反应发生率比较,差异均无统计学意义(P>0.05),见表2。
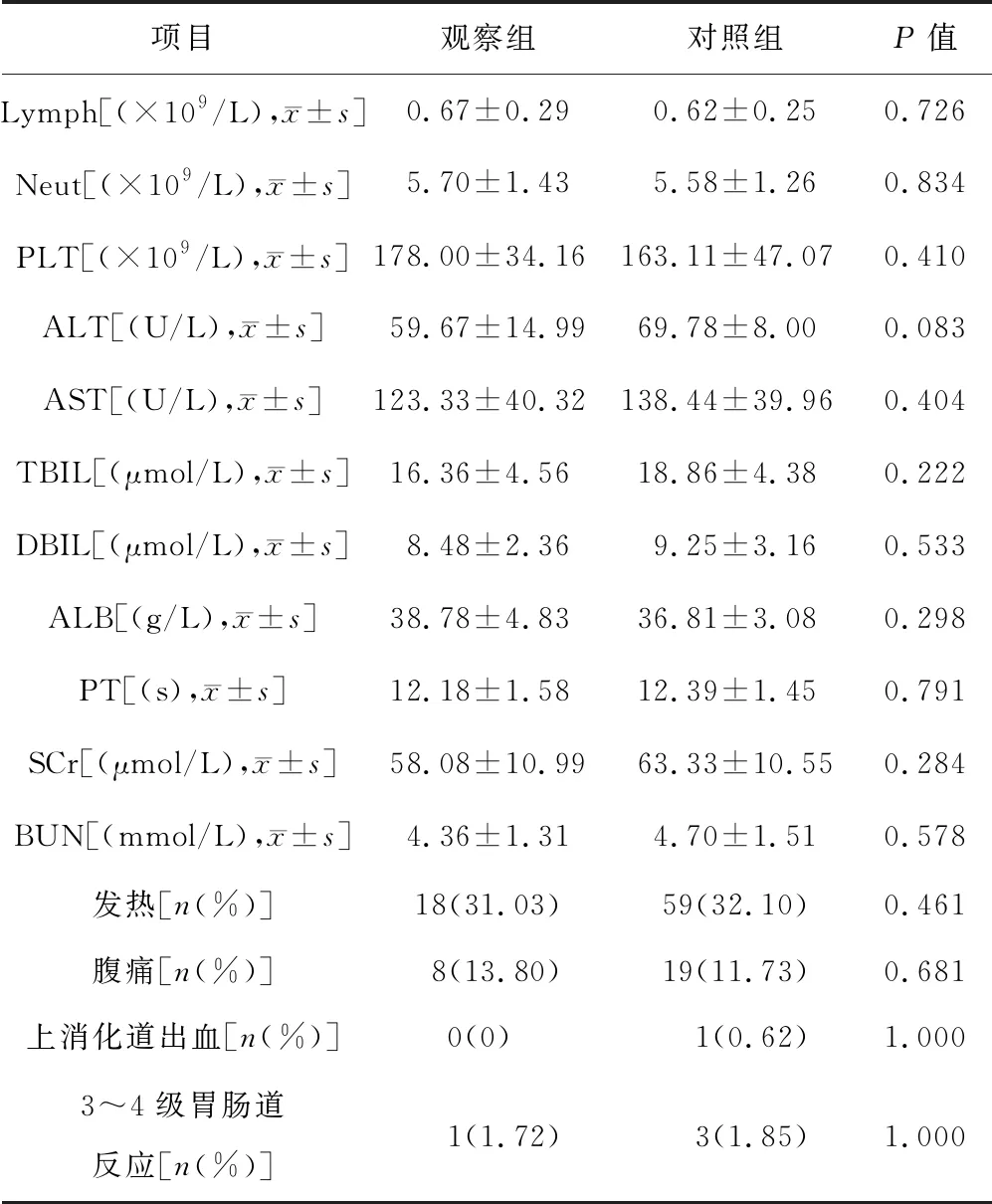
表2 2组患者TACE治疗后各指标水平比较
注:血液学检查标本来源于TACE术后第3天
3 讨论
HCC是常见的、恶性程度极高、预后较差的恶性肿瘤,其发病受环境和饮食双重因素影响,是多因素、多步骤的复杂过程。流行病学及实验研究资料表明,乙型肝炎病毒(HBV)感染、丙型肝炎病毒(HCV)感染、吸烟、饮酒、肥胖、糖尿病、黄曲霉毒素(Aflatoxins,AFs)、蓝藻毒素等都与肝癌发病相关[4]。由于HCC起病隐匿、早期诊断率低,临床确诊的患者多已至中晚期,大多丧失行根治性手术的机会[5],国内外多项研究证实TACE联合索拉菲尼治疗是最佳的治疗方案。
HCC是起源于肝细胞的富血供恶性肿瘤,90%血供来自肝动脉,TACE便是经皮将导管超选择插管至肝癌的供血动脉内,将带有化疗药物的碘化油乳剂对肝癌供血动脉末梢进行栓塞,以期达到“饿死”肿瘤的目的[6]。目前已广泛应用于无法手术切除的肝癌、肝癌术后的预防性治疗、肝癌手术切除后复发、肝癌手术前的减瘤治疗等,有效延长了患者的总生存时间。但基于其治疗原理,可能会引起术后感染(如肝脓肿、胆汁瘤等)、肝肾功能受损乃至衰竭、骨髓抑制、胃肠道反应等不良反应。同时,TACE治疗会不可避免导致肿瘤组织缺氧,诱导VEGF等促血管因子分泌增加、肿瘤新生血管生成,促进残余肿瘤细胞增殖,导致复发转移,因此其远期疗效不甚理想[7]。
索拉菲尼是一种新型多靶点抗肿瘤药物,由德国拜耳制药公司研制,可同时作用于肿瘤细胞和肿瘤血管。既可通过阻断由RAF/MEK/ERK介导的细胞信号传导通路而直接抑制肿瘤细胞的增殖,还可通过抑制血管内皮生长因子受体(VEGFR)和血小板衍生生长因子受体(PDGFR)而阻断肿瘤新生血管的形成,间接抑制肿瘤细胞的生长[8]。2009年8月正式用于我国失去手术机会的晚期肝癌患者。多项研究证实对术后病理提示MVI阳性的患者也有减少早期复发及延长总生存期的效果,但同样可能会带来肝肾功能损害、骨髓抑制、胃肠道反应、高血压、手足部皮肤反应等不良反应。
索拉菲尼能够对抗TACE导致VEGF浓度升高带来的新生血管生成,发挥协同抑制肿瘤的作用,理论上能够完美配合,但有可能发生不良反应的累积,从而导致比较严重的后果。关于TACE与索拉菲尼联合治疗的时机尚未达成共识。Kudo等[9]认为由于TACE后血清中VEGF水平明显升高,所以TACE术前或术后应尽快服用索拉菲尼,并建议连续使用,无间歇期。而Chao等[10]认为TACE治疗前后应暂停索拉菲尼的服用以减少药物不良反应,从而获得更高疗效。有研究证实TACE后24 h内VEGF便可显著升高[11],而索拉菲尼的清除半衰期为25~48 h,给药7 d血药浓度达到稳态,因此理论上在TACE术前至少1周开始服药并一直维持至TACE术后可使血药浓度达到最为稳定,可以最大限度抑制VEGF的升高,达到最好的治疗效果。本研究发现,TACE联合围术期连续服用索拉菲尼较单纯行TACE并不会增加肝肾功能的损害、骨髓抑制及严重胃肠道反应,具有较高的安全性,可能与TACE术后使用抗生素、保肝、护胃、止吐等药物有关。说明TACE联合围术期连续服用索拉菲尼治疗所带来的不良反应可以使用药物进行预防和治疗。因此,针对中晚期HCC需行TACE联合索拉菲尼治疗的患者,最佳联合治疗方案应为TACE术前至少1周开始服用索拉菲尼且持续至术后,中间无间歇期。
由于本研究属于回顾性分析,纳入患者数量有限,因此还有待于进一步开展多中心、大样本量随机对照试验进行深入分析。
