老年慢性阻塞性肺疾病并肺诺卡菌感染9例临床分析
2020-02-19熊洁任小平任亚娟魏声泓李艳徐灵彬
熊洁 任小平 任亚娟 魏声泓 李艳 徐灵彬
慢性阻塞性肺疾病(chronic obstructive pulmonary diseases, COPD)发病率与年龄密切相关,伴随全球人口老龄化加剧,老年COPD患者逐年增加。由于在COPD发展过程中容易因感染诱发疾病反复急性加重,将导致患者疾病加速进展,从而增加疾病死亡率。诺卡菌是一组需氧的革兰染色阳性细菌,可导致严重的化脓性或肉芽肿性疾病,主要累及皮肤、肺和脑组织。COPD等慢性结构性肺病是肺诺卡菌感染的重要危险因素[1-4]。由于肺诺卡菌感染主要表现为亚急性或慢性病程,临床症状常不典型,且病原体分离培养时间长,极易漏诊或误诊,死亡率高。在此,我们分析了我院近5年来收治的9例老年COPD合并肺诺卡菌感染的患者,并复习相关文献,以帮助临床医生提高对该病的诊治水平。
资料与方法
一、研究对象
收集我院2014.1-2018.12确诊的慢性阻塞性肺疾病并肺诺卡菌感染老年患者9例,其中男性6例,女性3例,年龄65~83岁,平均年龄73.78±6.14岁。
二、研究方法
回顾性分析患者的临床资料,包括人口统计学、临床表现、影像及实验室检查、治疗方法及预后。所有病例均系临床标本(肺泡灌洗液、痰及肺组织)培养出诺卡菌而确诊。
结 果
一、一般情况
9例患者均存在基础疾病,其中7例长期吸入糖皮质激素; 2型糖尿病4例,胰岛素或口服降糖药治疗;慢性肺源性心脏病4例;高血压病2例;慢性肾功能不全l例;陈旧性肺结核2例(见表1)。
二、临床表现
9例患者中2例为急性起病,6例为亚急性起病,1例为慢性起病(见表1)。所有患者均有发热症状,其中2例为高热,4例低热,3例中度发热;所有患者均出现咳嗽、咳痰症状,7例为中等量黄脓痰,2例为大量黄脓痰,易或不易咳出。所有患者均出现气短,咯血2例,为鲜红色血丝痰(见表1)。
三、影像学表现实验室检查
9例患者均行高分辨率胸部CT检查,最常见的影像学表现为团块影(7/9)和空洞(5/9),其次为实变(4/9),亦可见结节(3/9)、支气管扩张(2/9),1例呈现出磨玻璃影(1/9),(见表2,图1)。血气分析提示Ⅰ型呼吸衰竭3例,Ⅱ型呼吸衰竭4例,低氧血症2例(见表2)。9例患者中5例为肺泡灌洗液培养出诺卡菌;3例痰标本培养出诺卡菌,1例经皮肺穿刺活检组织标本培养出诺卡菌(见表2)。

表1 9例老年COPD并肺诺卡菌感染患者的一般资料和临床表现
四、确诊方式及病原学
9例患者中5例经肺泡灌洗液培养出诺卡菌确诊;3例痰培养标本,培养出诺卡菌确诊,1例进行肺穿刺活检,组织标本培养出诺卡菌;9例中豚鼠诺卡菌3例,皮疽诺卡菌和星形诺卡菌各1例,盖尔森基辛诺卡菌1例,其他3例未归类(见表2)。此外,9例患者中2例痰培养出铜绿假单胞菌,1例肺炎克雷伯菌,1例屎肠球菌,2例念珠菌,1例烟曲霉菌。
五、治疗及转归
9例患者中应用无创机械通气者5例,经口气管插管有创机械通气患者2例;抗感染治疗为美罗培南(0.5g 1次/8h)、头孢哌酮/舒巴坦(1.5g 1次/8h)、莫西沙星(400mg 1次/d)、利奈唑胺(600mg 1次/12h)、依替米星(300mg 1/d)及伏立康唑(200mg 1次/12h),确诊诺卡菌感染后8例患者接受磺胺甲噁唑/甲氧苄啶(3~6g/d)联合治疗,1例因磺胺过敏给予米诺环素(200mg 2/d)联合治疗。6例患者好转出院,2例患者院内死亡,1例患者自动出院后死亡(见表2)。
讨 论
随着全球老龄化进程加快、大气污染加剧,COPD患病率呈逐年上升趋势,目前已成为位列全球死亡原因的第三大疾病。老年 COPD 患者极易并发肺部感染,从而导致疾病加速进展甚至死亡。诺卡菌属放线菌属,为需氧革兰阳性菌,呈分枝状或丝状结构,有弱抗酸性,主要通过呼吸道吸入或皮肤接触致病,肺部是最常见的感染部位,临床表现为局限性或播散性化脓性疾病[5-6]。COPD是诺卡菌感染的主要宿主因素之一,主要原因除了使用类固醇激素外,可能由于支气管结构改变,黏膜纤毛功能障碍,上皮损伤,频繁住院或抗生素治疗以及合并症等多种原因而对病原微生物感染的易感性增加[7-8]。然而由于COPD合并肺诺卡菌感染的临床表现多无特异性,缺乏特异的血清学标志物,且分离鉴定和培养的经验较少,常常出现诊断延迟或误诊,从而导致死亡率升高[6,9-11]。
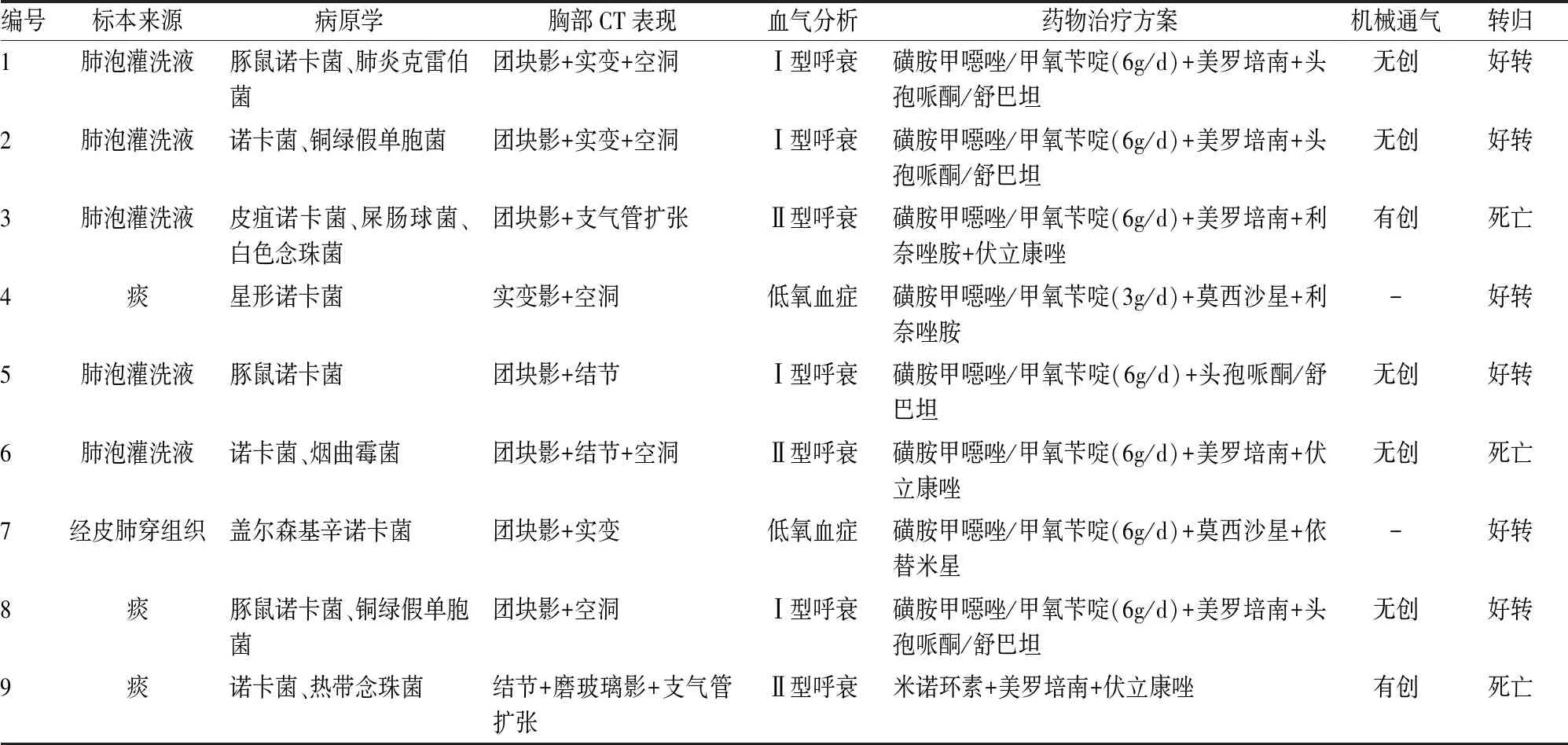
表2 9例老年COPD并肺诺卡菌感染患者的检查、治疗及转归

图1 COPD并肺诺卡菌感染患者胸部CT
a.入院1周胸部CT示双肺团片状高密度影;b.入院2周胸部CT示双肺团块影及空洞形成,伴支气管扩张(病例3); c.入院胸部CT示右肺上叶团片影、结节影伴多发空洞形成;d.治疗2周胸部CT示右肺上叶病变有所吸收(病例5); e.入院胸部CT示双肺磨玻璃影及结节影,伴支气管扩张影(病例9)
肺诺卡菌感染多为慢性或亚急性起病,男性多见,主要症状为发热及咳痰,也可有气短、咯血等,症状可持续数周或数月,常难以早期诊断[4]。本研究纳入的9例老年COPD并肺诺卡菌感染患者,2例表现为急性起病(22.22%),6例为亚急性起病(66.67%),1例为慢性起病(11.11%); 7例为低~中度发热(77.78%),2例为高热(22.22%);所有患者均有咳痰、气短症状(100%),2例伴咯血(22.22%); 7例患者由于不同程度的呼吸衰竭需要机械通气治疗,以上症状与COPD急性加重期临床表现相比,并无显著特异差别,因此诊断需依赖于影像学检查。文献报道肺诺卡菌病常见的胸部CT表现主要为实变、结节、空洞及肿块影[12-14],宿主因素也会影响肺诺卡菌感染的影像学表现,如肿瘤或激素治疗史等免疫抑制患者常表现为散在结节影[15],而免疫功能正常宿主常出现支气管扩张及磨玻璃样改变[7]。本研究中9例患者胸部CT多表现为多发团块影(77.78%)伴空洞形成(55.56%),其次可见实变影(44.44%)及支气管扩张(22.22%),1例表现为结节影及磨玻璃影(11.11%)。但由于这些影像特点并无特异性,在结核、肿瘤、侵袭性肺曲霉菌病及肺脓肿等疾病也可出现,因此需要加以鉴别[16]。肺诺卡菌感染的CT影像常有实变范围大、空洞出现早且多为胸膜下多发非偏心空洞、磨玻璃影多为小片散在分布等特点,且大多为双肺受累[17],因此对于老年COPD患者在短期内肺部影像学出现团块影、结节影伴空洞形成或支气管扩张及磨玻璃影像时需警惕肺诺卡菌感染可能。诺卡菌属中对人致病的主要包括皮疽诺卡菌、星形诺卡菌和豚鼠诺卡菌等[18-19],确诊主要依靠微生物培养和鉴定,痰涂片及痰培养是主要的无创诊断方法。此外,经支气管肺泡灌洗液培养、胸水及脓肿穿刺培养也能显著提高细菌分离及培养的阳性率[4,6]。本研究中5例(55.56%)经肺泡灌洗液培养出诺卡菌确诊;3例(33.33%)为痰标本培养出诺卡菌,1例(11.11%)经皮肺穿刺活检组织标本培养出诺卡菌,显示出支气管镜检在肺诺卡菌感染诊断中的重要地位。由于诺卡菌生长缓慢,因此早期行痰涂片检查对诊断肺诺卡菌感染也有很强的提示作用。
尽管体外药敏结果提示诺卡菌对磺胺的耐药率增加,目前仍将磺胺类药物作为肺诺卡菌感染的一线用药。此外,氨基糖苷类、碳青霉烯类、喹诺酮类及部分头孢类对诺卡菌均敏感,可单用或联合使用。利奈唑胺对多重耐药诺卡菌有效,对耐药菌株可应用利奈唑胺治疗[18]。肺诺卡菌病的治疗疗程长,一般不少于6个月,且疾病预后较差,因此早期诊断及合理的联合用药极为关键。目前推荐初始治疗应为包含至少2种以上抗生素联合治疗方案,主要的药物包括磺胺甲噁唑、阿米卡星、碳青霉烯类、米诺环素、头孢曲松及利奈唑胺。本研究中确诊肺诺卡菌感染的COPD患者还分别合并G-杆菌、G+球菌及真菌混合感染,其中8例患者接受了以磺胺甲噁唑/甲氧苄啶为基础的联合治疗,1例患者应用米诺环素为基础的联合治疗方案,此外还依据GOLD指南给予抗炎、扩张气道、祛痰、机械通气/吸氧治疗。文献报道肺诺卡菌感染将显著影响COPD的预期寿命:第一个月内死亡率为17%,第一年死亡率为33%[20]。相比之下,COPD急性加重的死亡率在住院期间为8%,在随访1年后为23%[11]。因此,COPD合并肺诺卡菌感染的治疗非常具有挑战性。Garcia-Bellmunt等的研究提示活动性肿瘤及全身应用糖皮质激素与诺卡菌病诊断后1年死亡率相关[20]。本研究中COPD并肺诺卡菌感染的死亡率为33.33%,其中2例患者有可导致免疫功能低下的2型糖尿病,2例长期吸入糖皮质激素。3例死亡患者均合并真菌感染,且合并严重Ⅱ型呼吸衰竭。
综上所述,老年COPD患者合并肺诺卡菌感染时常为多重混合感染,常见的症状为发热及咳痰,容易合并严重呼吸衰竭,病死率高。由于确诊时间长,早期诊断及治疗非常重要。临床医生了解肺诺卡菌感染与COPD之间的关系将有助于减少误诊并降低疾病的死亡率。综合本研究及既往文献研究结果,对于老年COPD患者在短期内肺部影像学出现团块影、实变影伴空洞、支气管扩张影像或结节及磨玻璃影像,且常规抗感染治疗无效时,应警惕肺诺卡菌感染的可能,反复多次的病原学检查尤其是支气管肺泡灌洗液培养,有助于早期确诊。除COPD常规治疗方案外,以足剂量的磺胺甲噁唑/甲氧苄啶等为一线方案的联合抗感染治疗及机械通气治疗是改善疾病预后的关键。
