分散液-液微萃取与高效液相色谱联用快速测定水样中的增塑剂
2020-02-18薛林科
薛 林 科
(甘肃医学院 公共课教学部, 甘肃 平凉 744000)
增塑剂,又称塑化剂,是一种高分子材料助剂,普遍应用于塑料、橡胶、粘合剂、纤维素、树脂、医疗器械、电缆等材料以增强其柔韧性和可塑性[1].邻苯二甲酸酯类化合物(phthalates, PAEs)是目前应用最广的一种增塑剂,被添加在玩具、医用血袋和胶管、壁纸、乙烯地板、清洁剂、润滑油、个人护理用品、食品包装材料等多种产品中[2-3].由于PAEs与基体之间没有共价键作用,随着使用时间的推移,易受到外在环境因素如温度、pH值等的影响而释放到环境中[4-5],经食物链浓缩最终到达生物体.虽然PAEs物质的急性毒性很低, 但其具有生物累积性,PAEs增塑剂具有影响生物体内分泌和导致癌细胞增殖的作用,属于致癌、致畸、致突变的环境激素.早在20世纪80年代,美国环境保护部门通过研究发现PAEs可以引发肝组织癌变,扰乱内分泌系统,从而影响生殖、发育和行为.其中邻苯二甲酸二(2-乙基)己酯(DEHP)等已被欧盟等政府机构限用或禁用[6],中国也将常用的6种PAEs列为优先污染物.如今,由于被大量而广泛地使用,PAEs被认为是无处不在的环境污染物.PAEs及它们的代谢物和降解产物会对人体健康产生不良影响,尤其是对肝、肾和睾丸[7-8].因此,有必要建立一种可靠、灵敏的分析方法来监测这类化合物.
目前,各种各样的预处理技术被用来从不同的样品中萃取PAEs,如液-液萃取(LLE)[9]、固相萃取(SPE)[10],这类方法一般来说操作复杂繁琐、成本较高,而且费时,劳动强度大,会使用大量对人体有害的有机溶剂,易造成交叉污染,而且对人类健康和环境造成危害.近来的研究趋向开发高效、经济和小型化的样品制备方法.固相微萃取(SPME)[11]、液相微萃取(LPME)[12]、搅拌棒吸附萃取(SBSE)[13]和中空纤维液相微萃取(HF-LPME)[14]已经被用来测定环境中的PAEs.然而,这些方法一般需要很长的萃取时间才能获得较好的萃取效率.
分散液-液微萃取(DLLME) 是2006年由Rezaee等[15]提出的一种基于萃取剂、分散剂和水样组成的三元液相微萃取技术.操作步骤主要有2步,首先将微升级有机萃取剂和数毫升水溶性的分散剂混合均匀,然后用注射器将混合溶液快速注入到含有目标物的样品溶液中.在分散剂的辅助作用下,萃取剂形成极小的液滴广泛而均匀地分布于整个样品溶液中,由于萃取剂和样品溶液之间有着无限大的接触面积,所以目标分析物在水溶液和萃取剂之间的分配平衡能在瞬间完成,萃取时间短是分散液-液微萃取最主要的优势;最后经过离心后密度大于水的萃取剂沉积在离心管底部,取出萃取剂进行适当的处理之后进行相应的仪器分析检测.DLLME是一种集采样、萃取和浓缩于一体的样品前处理技术,它具有快速、操作简单、成本低、有机溶剂使用量少、对目标物萃取效率和富集倍数高,以及易与大部分分析仪器联用等特点.DLLME不仅适用于痕量有机物的分离富集,也可用于痕量无机金属离子的检测,已被广泛应用于坏境、医疗、工业、食品、生物等样品中痕量组分的分析测定.
本文建立了一种超声辅助分散液-液微萃取与高效液相色谱联用测定环境水样中常见PAEs的方法.采用超声可以加速萃取平衡,极大地缩短了萃取时间,提高了萃取效率.利用高效液相色谱成功地测定了河水、雨水和废水中的PAEs.
1 实验部分
1.1 仪器与试剂
日本岛津Prominence-i LC-2030型液相色谱一体机(包括LC-2030泵、LC-2030脱气机、LC-2030自动进样器、SPD-M20A二级管阵列检测器、LC-2030柱温箱);岛津LabSolutions色谱工作站; Shim-pack VP-ODS-C18柱(150 mm×4.6 mm,粒径5 μm);KQ-250B型超声波清洗器(昆山市超声仪器有限公司);AXTD6M型高速离心机(金坛市精达仪器制造有限公司),UPH-I-20T型优普系列超纯水器(四川优普超纯科技有限公司),UH5300型紫外扫描仪(日本日立科技有限公司);PHS-3C酸度计(上海雷磁仪器有限公司).
邻苯二甲酸二甲酯(DMP)、邻苯二甲酸二乙酯(DEP)、邻苯二甲酸二正丁酯(DBP)、邻苯二甲酸二正辛酯(DOP)和邻苯二甲酸二(2-乙基己基)酯(DEHP) 标准品购自美国AccuStandard公司(由百灵威科技有限公司代理),它们的性质见表1;CH2Cl2、CHCl3(分析纯,国药集团化学试剂有限公司),CCl4(分析纯,百灵威科技有限公司),CS2(分析纯,阿拉丁试剂有限公司),C6H5Cl(分析纯,上海中秦化学试剂有限公司);甲醇、乙腈(色谱纯,山东禹王实业有限公司),丙酮和乙醇(分析纯,国药集团化学试剂有限公司).实验用水为超纯水.
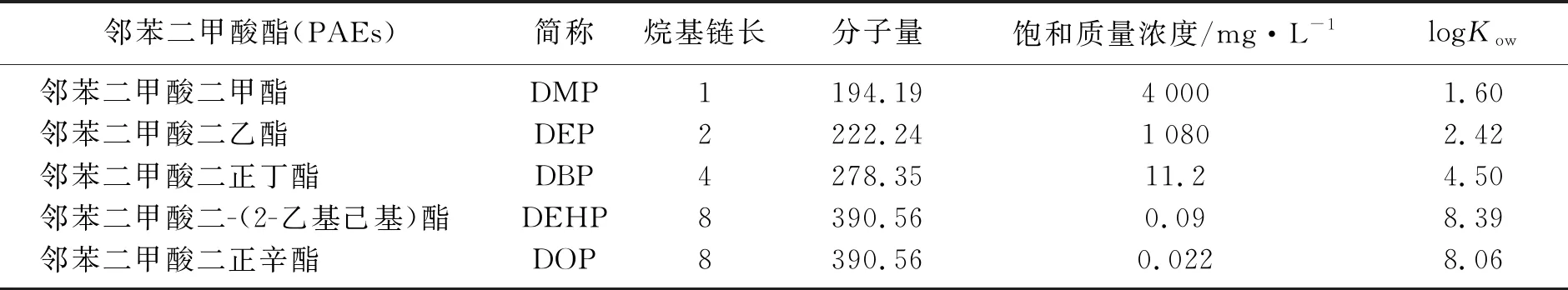
表1 实验用邻苯二甲酸酯的性质[16]Table 1 Physical properties of PAEs
本实验中,环境水样包括泾河水样,雨水样和废水样.所有水样收集在棕色的玻璃容器内,先用布氏漏斗粗滤,再用0.45 μm滤膜过滤后4 ℃避光保存.
1.2 标准溶液的配制
分别准确称取5种邻苯二甲酸酯标准品各25 mg(精确至0.1 mg)至50 mL容量瓶中,用甲醇溶解并定容至刻度,配制成质量浓度为500 mg·L-1的储备液,4 ℃避光保存,分别量取4 mL标准储备溶液至100 mL容量瓶中,用甲醇定容至刻度,配制成质量浓度为20 mg·L-1的混合标准储备液,准确移取混合标准储备液2.5 mL用超纯水稀释至100 mL得到质量浓度为50 μg·L-1的混合标准溶液.
1.3 实验方法
取10.00 mL样品溶液置于15 mL带塞刻度玻璃离心管中,然后向其中迅速注入一定量的含有萃取剂和分散剂的混合液,超声萃取2 min,使萃取剂均匀分散在样品溶液中,形成乳浊液,然后将其放入离心机中,以3 500 r·min-1离心分离5 min后,含有PAEs的微量萃取剂沉积于离心试管底部,用微量进样器移取于样品瓶中用甲醇稀释至300 μL,置于样品瓶架进行分离检测,同时做对应萃取剂和分散剂的空白试验.
2 结果与讨论
2.1 色谱条件的优化
利用UH5300在200~500 nm对PAEs进行紫外扫描,发现5种PAEs在254 nm有最大吸收,故选择检测波长为254 nm,经优化其他色谱条件,甲醇与水体积比为90∶10,进样体积20 μL,流速为1.0 mL·min-1.
2.2 萃取条件的优化
为了获得最佳的萃取条件, 实验中采用富集因子(EF)来衡量分散液液微萃取的性能和效率, 考察不同萃取条件下对PAEs的富集和分离效果. 在常规DLLME中一般使用密度比水高的溶剂作萃取剂, EF被定义为目标物在沉积相中的浓度(csed)和在样品溶液中的初始浓度(c0)的比值,
式中,csed由一系列不同浓度的标准溶液的线性方程计算得到.
2.2.1 萃取剂的优化
萃取剂一般需要满足以下几点要求:①萃取剂密度大于水;②萃取剂在水中的溶解度要尽可能小;③萃取剂对分析物有一定的萃取行为;④萃取剂能与分散剂混溶;⑤溶剂峰与目标峰在适合的色谱条件下可以完全分离[17].依据这些原则,实验选取CH2Cl2、CHCl3、CCl4、CS2、C6H5Cl分别作为萃取剂(40 μL)与4种分散剂(1 000 μL)甲醇、乙醇、乙腈、丙酮对EF的影响.实验发现,CH2Cl2、CS2和CHCl3萃取效果不理想,离心后没有沉积相无法进行HPLC分析,CCl4和C6H5Cl作为萃取剂时,能有效地萃取5种PAEs,富集倍数相差不大,由于C6H5Cl和 DMP的色谱峰部分重叠,选择CCl4作萃取剂.
2.2.2 分散剂的优化
DLLME要求分散剂对萃取剂有良好的溶解性,能与水互溶,分散剂的加入有效降低两相之间的界面张力,而且还可使萃取剂在水相中均匀分散成微小的液滴,形成水/分散剂/萃取剂的乳浊液体系,增大萃取剂与水相的接触面积,从而快速高效萃取目标物[18].因此,分散剂的选择是影响EF的另一个关键因素.基于此,对4种常用分散剂甲醇、乙醇、乙腈和丙酮进行了实验研究.如图1a所示,4种分散剂和CCl4对PAEs均有较好的萃取效率,以乙腈为分散剂时对5种PAEs萃取效率最高,所以实验选择乙腈作分散剂.
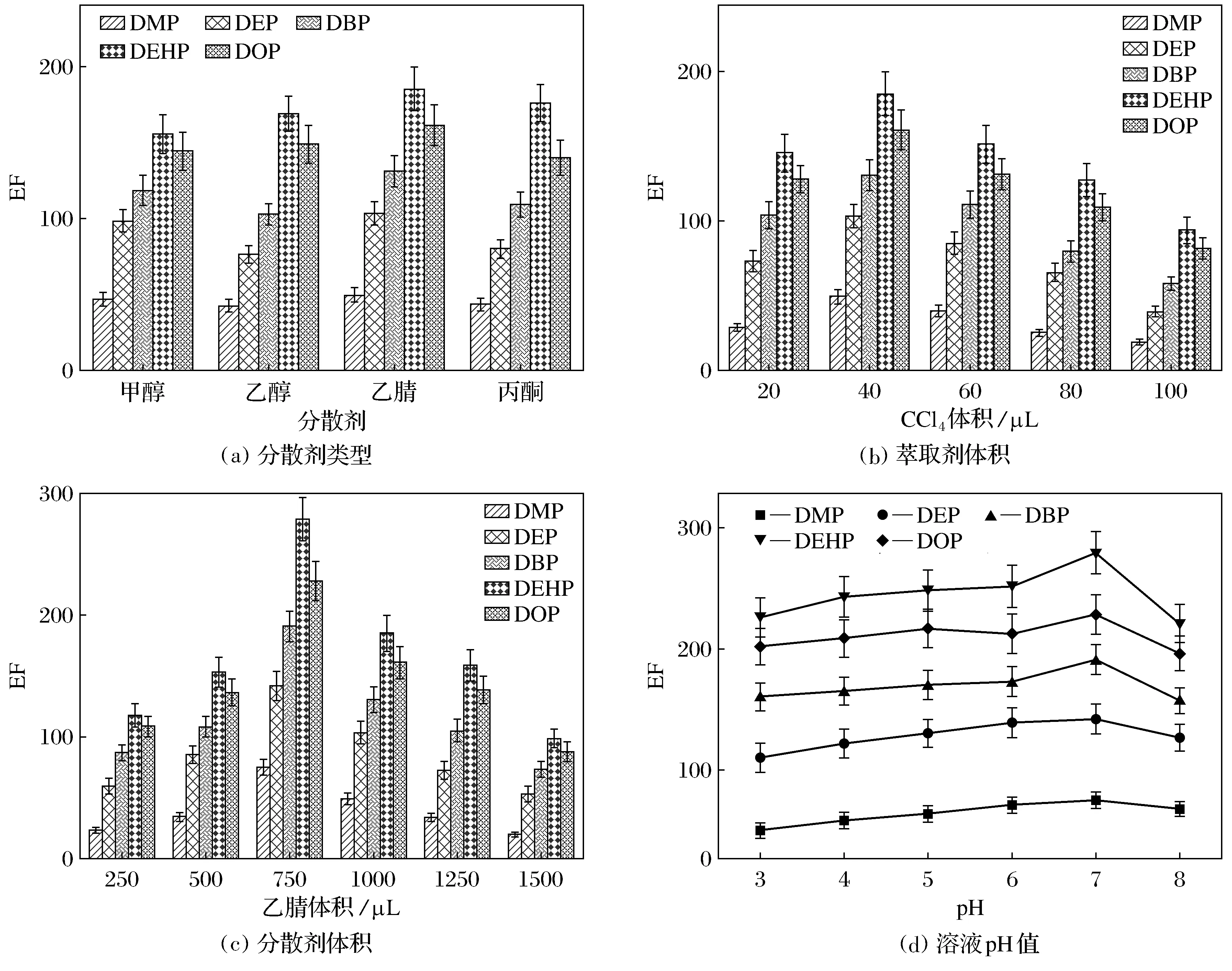
图1 不同萃取条件对萃取PAEs(50 μg·L-1)的影响Fig.1 Effects of different eminating siastles on the extraction of PAEs(50 μg·L-1)
2.2.3 萃取剂体积的优化
萃取剂的体积直接影响方法的富集倍数,用1.0 mL乙腈与不同体积(20,40,60,80和100 μL)的CCl4分别作分散剂和萃取剂,考察了不同体积萃取剂对萃取效率的影响.萃取剂的体积太小,获得的沉积相很少,则无法进样分析.图1b表示的是目标物的萃取效率与萃取剂体积之间的关系.从图可以看出,随着萃取剂的用量从20 μL增加到100 μL,富集倍数先增大后逐渐减小,当萃取剂的体积为40 μL时,萃取效率最高.这可能是因为CCl4为20 μL时,萃取不完全;CCl4体积大于40 μL时,过多的CCl4又会溶解沉积相,导致EF减小.因此,40 μL为CCl4的最佳用量.
2.2.4 分散剂用量的优化
分散剂的量直接影响三相体系乳浊液的形成以及萃取剂在水样中的分散程度,从而影响富集倍数和萃取效率.图1c表示的是分散剂乙腈体积对萃取效率的影响,当乙腈用量少于750L时,萃取效率随着乙腈用量的增加而增大;当乙腈用量多于750L时,萃取效率减小.这是因为乙腈的体积较小时,无法使CCl4很好地分散,从而无法形成稳定的乳浊液;但当乙腈的用量过大时,也会使PAEs和CCl4在水相中的溶解度增加.选择750L为乙腈的最佳体积.
2.2.5 pH值的优化
在DLLME中,溶液的pH值是影响萃取效率的重要因素,样品溶液的pH值决定了目标化合物在溶液中的存在状态,某些目标化合物可能会在酸性或碱性条件下分解,或者发生解离,以离子状态存在.对目标化合物萃取效率的高低与其存在形式直接相关.在该实验中,对pH值从3.0~8.0时对萃取效率的影响进行了研究,结果如图1d所示,pH值在3.0~7.0时,所有目标物的萃取效率变化不大,pH值从7.0~8.0,EF下降较多.可能是因为PAEs在酸性环境中水解程度小,碱性环境中水解程度大,选择pH=7.0为最佳pH值.
2.2.6 离子强度对DLLME的影响
盐的加入可以减小邻苯二甲酸酯在水相中的溶解度,从而提高萃取效率.为此,在同一浓度的标准溶液中,以不同浓度的氯化钠控制样品溶液离子强度,研究了离子强度对DLLME萃取效率的影响.实验结果发现,随着溶液中盐浓度的增大,EF逐渐减小.这可能是因为盐析效应在减小PAEs溶解度的同时,萃取剂在水相中的溶解度也会有所降低,导致离心后沉积相的体积相应增大,PAEs在沉积相的浓度相应减小,反而使EF减小.由于盐的加入对分析物的富集倍数没有显著改善,加入NaCl后,溶液的黏度和密度增大,给离心分离带来不便,因此实验中不加盐.
2.2.7 超声时间的选择
超声是利用超声波在超声过程中产生的空化效应、热效应、机械搅拌、强化扩散、乳化作用等一系列效应,来加快萃取过程中的传质作用,从而提高萃取效率.考察了相同实验条件下超声时间在0~5 min内对5种PAEs萃取效率的影响.实验表明,超声萃取宜在2 min内完成.超声有利于萃取剂在水相的分散和萃取,超声时间过长萃取效率反而下降,可能是由过长超声时间产生的热效应使沉积相溶解所致,实验中选择超声辅助时间为2 min.
2.3 分析方法评价
在最佳实验条件下对质量浓度为1~100 μg·L-1的加标超纯水溶液进行分析,以5种PAEs的峰面积为纵坐标、对应的质量浓度为横坐标绘制标准曲线(见表2),结果表明,5种PAEs的质量浓度在1~100 μg·L-1范围内线性关系良好,相关系数均>0.99.

表2 5种邻苯二甲酸酯的线性方程、检出限Table 2 Linear equations and detection limits of fivekinds of PAEs
对同一质量浓度(50 μg·L-1)进行加标回收实验,考察方法的精密度和准确度见表3.平均加标回收率为94.6%~105.8%,PAEs的检出限(S/N=3)为0.012~0.028 μg·L-1,5种PAEs峰面积的RSD为3.96%~5.38%(n=3),5种PAEs的富集倍数从75到279,可以满足分析要求.
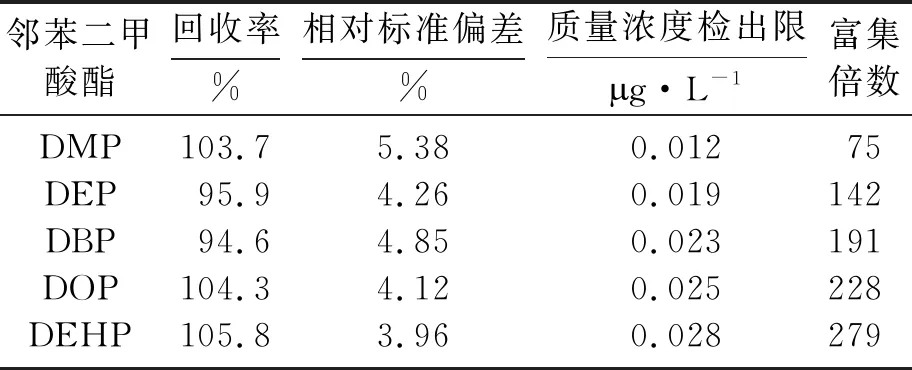
表3 分析方法特性
2.4 实际水样分析
将该方法应用于实际水样PAEs含量的测定,并进行了加标回收实验,结果如表4所示,雨水中未检出PAEs,泾河水样和生活污水中都检测到DBP和DEHP,原因可能是泾河沿岸居民区生活垃圾和高密度蔬菜种植塑料大棚的普遍使用,说明当地环境已被PAEs污染,同时也证明DBP和DEHP是2种使用最为广泛的增塑剂.上述水样中加入浓度均为20g·L-1的DMP、DEP、DBP、DOP和DEHP,泾河水、雨水和废水水样的相对回收率分别为95.2%~104.1%、97.0%~108.2%和92.5%~107.2%,相对标准偏差(RSD)在4.59%和5.81%之间.这些数据表明,基体效应对萃取和测定实际水样中的PAEs影响不大.
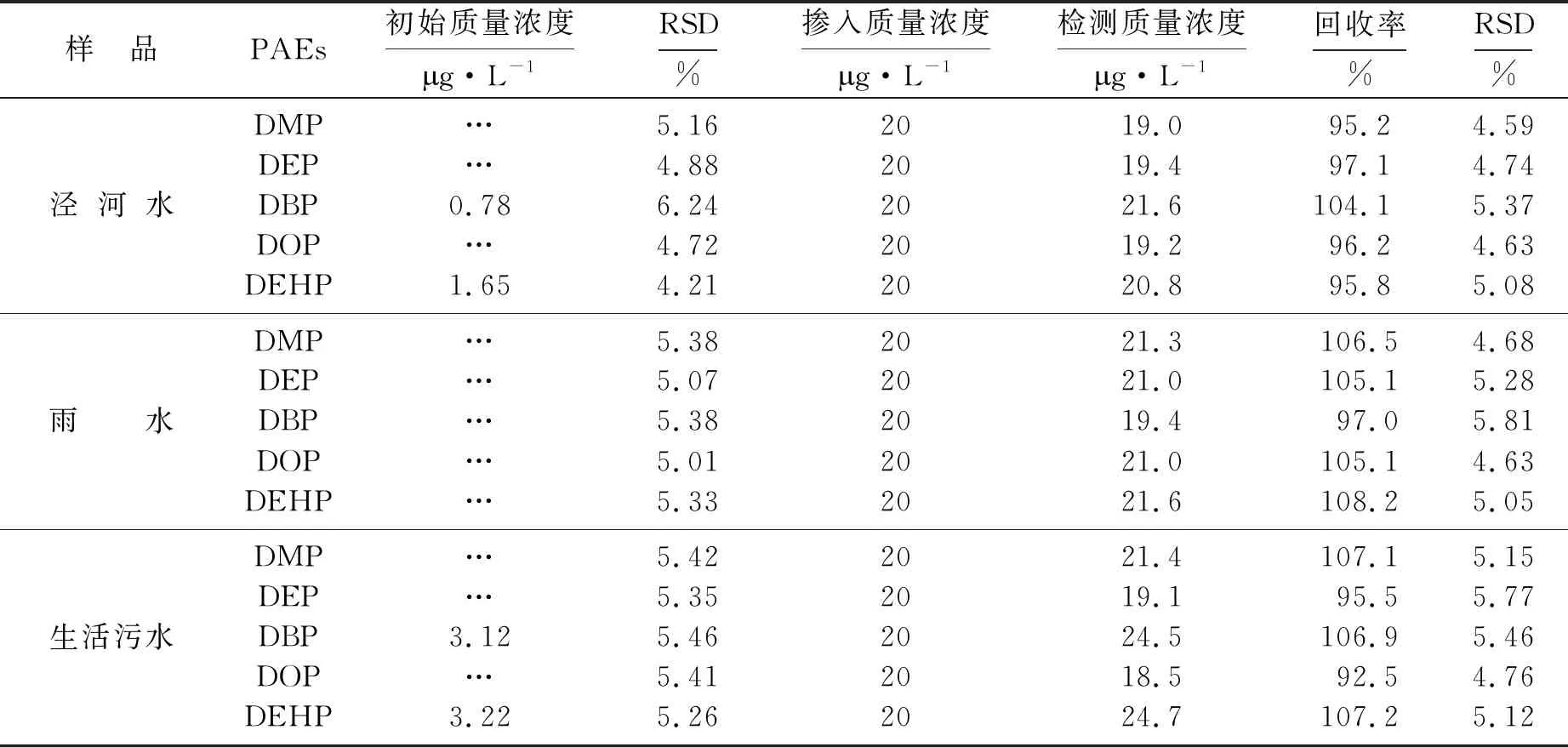
表4 实际水样分析结果Table 4 Analysis of water samples
3 结 论
本实验运用超声辅助,将分散液-液微萃取与高效液相色谱联用,建立了环境水体中PAEs的快速检测方法.样品前处理步骤简单、快速、富集效率高,从而保证了对痕量PAEs的高灵敏分析,由于有机溶剂的使用量很少,所以不会造成有机溶剂污染,是一种操作简单、快速高效、环境友好的样品前处理方法,适用于富集和测定环境水样中的PAEs.
