自愈合水凝胶的应用研究进展
2020-02-14庞相琛
庞相琛

摘要:水凝胶是一种以大量水为分散介质且质地柔软的高分子材料,广泛应用于日常生活。而自愈合是材料能够自动地修复破损、恢复材料原有性能的一种性质。由于水凝胶材料大多力学强度较低,使用过程易发生机械损伤且损伤后性能大大降低,无法继续满足使用要求。因此仿照生物体损伤自愈合的原理, 制备出具有自愈合性质的水凝胶材料具有十分重要的意义,可以延长水凝胶的使用寿命、降低成本、扩大其应用范围。随着技术的不断发展,自愈合水凝胶材料在医用器械、仿生电子皮肤、可注射水凝胶等方面备受关注,因此本文将对自愈合水凝胶材料的实现机理以及应用研究进行综合阐述。
Abstract: Hydrogel is a kind of polymer material with a large amount of water as a dispersion medium and a soft texture. It is widely used in daily life. And self-healing is a property that the material can automatically repair the damage and restore the original properties of the material. Due to the low mechanical strength of most hydrogel materials, mechanical damage is prone to occur during use and the performance is greatly reduced after the damage, which cannot continue to meet the requirements for use. Therefore, following the principle of self-healing of biological damage, it is of great significance to prepare hydrogel materials with self-healing properties, which can prolong the service life of hydrogels, reduce costs, and expand their application scope. With the continuous development of technology, self-healing hydrogel materials have received much attention in medical devices, biomimetic electronic skins, injectable hydrogels, etc.. Therefore, this article comprehensively elaborates the realization mechanism and application study of self-healing hydrogel materials.
关键词:自修复材料;水凝胶;应用研究进展
Key words: self-healing material;hydrogel;application research progress
中图分类号:R318.08 文献标识码:A 文章编号:1006-4311(2020)01-0215-04
0 引言
水凝胶是能保持一定形状的三维网状结构高分子溶胀体,可以吸收、保持大量水或水溶液,在水中发生溶胀而又不会溶解于水,质地柔软(如图1所示)[1]。构成水凝胶的聚合物主链或侧链上有亲水基团(-OH、-COOH等),在溶胀后,相当一部分水与这些亲水基团形成氢键,故水凝胶可以保持大量水分。水凝胶材料具有很多优异特性,其在日常生活、生物医用、药物等方面应用十分普遍。如具有生物相容性的水凝胶可以用于医疗器材、药物载体、止血凝胶、高强度仿生皮肤。但是水凝胶作为一种软物质材料,不足之处主要在于机械强度较低,容易在工作过程中受到机械损伤而缩短使用寿命,所以开发出高强度的水凝胶一直是科学家们的研究方向。除此之外,还可以通过赋予水凝胶自愈合的特性,使得水凝胶在破损后可以自动愈合,则能大大延长水凝胶材料的使用寿命[2]。
自愈合材料是一种“有生命”的材料,具有自动愈合损伤的能力,能够利用固有的资源去恢复原有的功能,自我愈合的过程分为自发的或需要外界刺激(如加热、光照等)。自愈合材料相对传统材料优越性在于损伤后能像人类皮肤一样自行愈合,恢复原有结构和功能,大大延长了材料的使用寿命,提高使用安全性并降低维护成本,可谓安全又环保,为实现材料更加安全化与持久性提供了新途径。自愈性水凝胶因其各自良好的亲水性、渗透性、刺激響应性和优越的生物相容性以及生物组织相似性在生物医用(如止血载药等)、制备柔性电子器件、形状记忆材料等领域有着开阔的发展前景[3]。
1 水凝胶自愈合机理
水凝胶是由亲水性高分子交联而成的三维网络体系,不同的交联方式会赋予水凝胶不同的性质,比如氢键交联、光交联、pH响应交联等。由具有动态特性的交联网络构建形成这种材料具有本征性的自愈性,因此设计动态可逆的交联作用是制备自愈合水凝胶的关键。可逆交联作用一般分为可逆共价键作用(如亚胺键)和可逆非共价键作用(如氢键)[4]。一方面动态化学键对多种环境刺激具有响应性,另一方面可对外界破坏造成的损伤进行自我修复,能自我调节以适应环境变化,为将自愈性水凝胶开发为自适性多功能智能新材料的发展奠定了基础。
1.1 可逆共价键作用
1.1.1 亚胺键和酰腙键
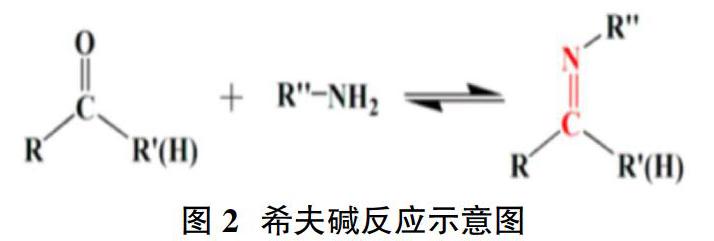
亚胺键,也叫希夫碱,是由伯胺和活性羰基化合物(醛基、酮)发生缩合反应而生成的,具有动态可逆的特性[5](如圖2所示)。因此以亚胺键为交联结构的水凝胶具有一定的自愈合性。目前广泛应用于生物医用材料中的高分子如壳聚糖、聚赖氨酸、聚乙烯亚胺、葡聚糖、蛋白质及多肽等物质含有丰富的氨基,利用这些高分子来设计亚胺键交联制备的自愈合水凝胶在生物医学方面有着巨大的应用前景。
酰腙键也是一种动态可逆的化学键,由酰肼和醛基反应生成。酰腙键在动态共价键中属于结合较稳定的一类,具有明显的pH依赖性。陈咏梅研制了基于酰腙键和亚胺键两种动态共价化学键的多糖基自愈合水凝胶,通过己二酰肼交联氧化海藻酸钠生成可逆酰腙键,同时通过氧化海藻酸钠交联水溶性壳聚糖得到可逆亚胺键。该水凝胶在生理条件下具有较高的自愈合效率,该水凝胶还有可注射性和降解性能[6]。
1.1.2 Diels-Alder反应
Diels-Alder反应,又名双烯加成,由共轭双烯与烯烃或炔烃反应生成六元环的反应,具有热可逆性,可用作自愈合水凝胶的化学交联反应。之前的研究中,科研人员开发了具有弹性、可注射性的多功能水凝胶和基于DA点击化学的组织粘合能力用于软骨组织修复。此外,通过呋喃基和马来酰亚胺之间的DA点击化学形成的环己烯衍生物(氧-降冰片烯基团)可以通过硫醇-烯反应进行有效地与硫醇基团反应,可以用于进一步官能化水凝胶。
1.2 可逆非共价键作用
1.2.1 氢键作用
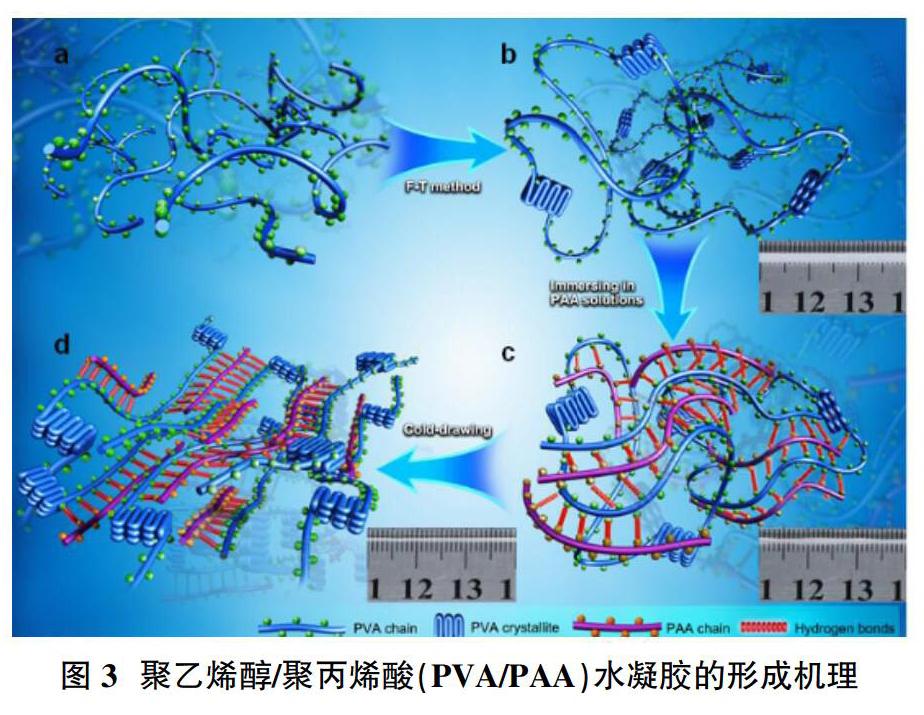
氢键是一种比共价键和离子键作用弱的非共价键力,它普遍存在于生物体和化学分子中。氢键是一种可逆作用,在高温下被破坏,低温下重新形成。因此可以利用氢键这一特性来制备氢键交联的自愈合水凝胶。北京师范大学汪辉亮课题组研究人员利用浸泡和冷拉的方法来增强聚合物之间的氢键相互作用,从而制备了一种力学强度超过塑料的超强韧聚乙烯醇/聚丙烯酸水凝胶。通过冷冻-解冻法制备了物理交联的聚乙烯醇(PVA)水凝胶,然后将PVA凝胶浸泡在聚丙烯酸水溶液中,得到聚乙烯醇/聚丙烯酸(PVA/PAA)水凝胶。随着PAA逐渐迁移进PVA凝胶中,PAA链上的羧基与PVA链上的羟基会形成大量的氢键,增大了水凝胶的交联密度。此外,通过将PVA/PAA水凝胶进行冷拉处理,使得水凝胶内部的高分子链进一步靠近并高度取向,诱导PVA与PAA分子链间更多的氢键形成,使其力学性能得到极大提升,从而制备了一种力学强度超过塑料的超强韧水凝胶(图3)。实验表明,分子链之间的氢键交联作用提升了材料的力学性能并赋予了它优越的自愈合性能。
1.2.2 金属配位键作用
金属配位键是由过渡金属离子(如Fe3+、Zn2+、Cu2+)提供空轨道、配体(如-OH、-COOH等基团)提供孤对电子形成的一类化学键。金属配位键具有动态可逆的性质,是制备剪切变稀和自愈合水凝胶的一种有效分子设计策略。通过在高分子骨架上共价结合配体分子,并向其中引入金属离子,即可形成基于配体-金属配位键的交联点,从而制备出具有自愈合性能的水凝胶。通过选择不同的配体和金属离子,可制备出具有一系列不同力学强度的水凝胶,用以满足不同生物医学应用中的力学需求。基于以上特点,wei等开发出了一种简单的自愈合水凝胶制备方法:在丙烯酸水溶液中加入Fe3+,通过聚合反应形成聚丙烯酸大分子骨架的同时,Fe3+与-COOH发生配位作用形成交联点,从而制备了金属配位交联的自愈合水凝胶(图4所示)。
湖南大学施李杨等利用双膦酸根和金属之间形成的动态配位键开发了一类具有自愈合特性的水凝胶,这种具有动态可逆网络结构的双膦酸-金属配位水凝胶可实现“凝胶-溶胶-凝胶”的转化,注射时间点无窗口期限制[7]。将开发的双膦酸和金属离子交联的水凝胶用作3D打印墨水、组织修复支架以及药物缓释载体[8],并取得了良好的体内外生物学效果。由此可见动态配位键是开发动态可逆性能的水凝胶生物材料的一种重要的化学策略,有着开阔的发展前景。
2 自修复水凝胶的应用研究
2.1 生物医用水凝胶
水凝胶具有良好的生物相容性,其含水量很高,与人体组织具有相似的粘弹性、能够保持软骨细胞表型、可原位成型等多方面优势,已成为一种较为理想的软骨组织工程支架材料,在生物医用材料有广阔的应用前景。
华南理工大学的曹晓东教授通过Diels-Alder点击化学法和动态化学交联酰腙键,制备了可注射成型的愈合型水凝胶。该水凝胶具有自身愈合性,还可与天然软骨组织形成良好的界面结合(如图5所示),有望解决植入体在术后松动或脱落等不良问题。
近日,汪建新教授课题组借鉴了酶催化下盐酸酪氨之间的动态偶联反应,探讨了在温和条件下利用催化剂诱导盐酸酪氨衍生物之间发生偶联反应的可行性,并利用该可逆化学键来构筑兼具良好自愈性能、力学性能以及生物相容性的“自主性”自愈合水凝胶[9]。所得水凝胶自愈合24小时后,接触样品已经完全自愈合,切口消失,最后将水凝胶与细胞进行三维共培养,表征该水凝胶具有良好的生物相容性及在组织工程支架领域的潜在应用。该水凝胶优良的机械性能、超高的自主自愈合性能以及生物相容性为其在组织工程、创伤敷料等领域提供了良好的应用前景,同时通过引入这种温和条件下的偶联反应制备自主自愈材料为设计制备自愈材料提供了新的思路。(图6)
2.2 仿生电子皮肤
随着人工智能和软体机器人等领域的发展,模仿人体皮肤感知能力和力学性能的多功能传感器的研发和制备受到越来越多研究者的关注。在化学领域里,特定结构的高分子水凝胶就可以模拟人的触觉,因为其中的载流子就是电子,和人真实皮肤的工作原理非常接近。
武培怡教授课题组在对高分子的分子内以及分子间相互作用机理的研究基础上,提出了一系列调控凝胶力学、电学和光学性质的设计:
①利用納米级无定形矿物粒子和天然多糖的离子作用,调节物理交联聚丙烯酸的粘弹性,所构筑的仿生皮肤可以快速自修复,并且具有更高的应力响应灵敏度;
②利用刺激响应水凝胶的体积相转变行为,将外界刺激转变为有效电信号,拓宽了水凝胶类仿生皮肤的感知功能;
③以及利用三种分子间非共价相互作用,实现多重动态交联网络,制备的透明超分子水凝胶集合了一系列类似皮肤甚至超越皮肤的力学性质,具有压缩回弹性,可大幅拉伸,可自修复,可在室温下的任意塑形,并通过电阻和电容的两种电信号,同时实现对外界应力应变和温度刺激的感知;
④进一步引入α-甲基,则可以实现对具有相同共聚单体结构的水凝胶相变行为从UCST到LCST的广泛调节,基于此构筑的仿生水凝胶皮肤不仅具有多重电信号感知效果,还可以实现可调节的温度-光学响应效果。极大改善和拓宽了基于凝胶类的仿生皮肤的应用前景。
2.3 电子器件/传感器
可拉伸导电材料在未来各种领域的应用是不可或缺的,例如可拉伸板、柔性储能装置、电极、传感器和可穿戴装置。为了实现这些目标,关键问题是同时引入机械强度和电导率。导电水凝胶由于其优异的柔韧性,良好的电气特性和可调谐的机械性能而具有一体化潜力。迄今为止,各领域的研究人员中已经广泛研究了导电水凝胶,例如,应用于柔性超级电容器和传感器中的导电聚合物水凝胶。
刘明杰教授课题组报道了由PVA网络、导电聚合物PEDOT:PSS和H2O/EG溶剂组成的抗冻导电油水凝胶(图7所示)[9]。EG形成氢键和致密结晶畴使材料具有高的机械强度。此外,氢键和结晶区的物理交联导致防冻导电油水凝胶为热塑性和自愈性,并具有可重塑性和可重复使用性。结合上述所有性质,导电油水凝胶可以在诸如柔性电极、传感器、能量存储装置和可穿戴装置等各种领域中,在零下温度下应用。
3 总结与展望
水凝胶在我们生活中起着不可或缺的作用,凭借各优异性能,为我们的生产生活带来极大的便利。为完善其功能,随着科研人员对水凝胶研究逐渐深入,自愈合水凝胶材料成为一大热点。自愈合水凝胶可广泛使用于生物医用、制备柔性皮肤材料等特殊专业领域。由于其具有良好的亲水性、对多种环境刺激响应性、高强度、高拉伸性、高韧性优异的自修复与循环利用性能,水凝胶在生物组织工程和电子皮肤等方面拥有独到的优势,为各行业提高工作效率、降低了风险,更逐渐走进人们的日常生活。但这种材料的制备技术仍不完善,高含水量使其机械性能差,在提高机械性能上仍有很大的发展空间,加上研发成本和专业技术要求较高,所以还没有广泛投入市场。因此自愈合水凝胶材料未来研究方向主要在降低生产成本,寻找最优方案和配置方法;集中各种机理的水凝胶各自的优势于同一种材料,开拓其用途;研发水凝胶弊端解决方法,提高水凝胶机械性能;继续研发不需修复剂的自修复材料,促成友好型环境的发展。
参考文献:
[1]Shi, L.*; Ding, P.; Wang, Y.; Zhang, Y.; Ossipov, D. *; Hilborn, J. *, Self-Healing Polymeric Hydrogel Formed by Metal-Ligand Coordination Assembly: Design, Fabrication, and Biomedical Applications. Macromol. Rapid Commun. 2019, 1800837.
[2]Gang Wangab, Jiehua Zhuab, Xiaofeng Chenabc, Hua DongORCID logoabc, Qingtao Lid, Lei Zengab and Xiaodong Cao. Alginate based antimicrobial hydrogels formed by integrating Diels Alder “click chemistry” and the thiol–ene reaction. RSC Adv., 2018, 8, 11036-11042.
[3]WEI Z, HE J, LIANG T, et al. Autonomous self-healing of poly(acrylic acid) hydrogels induced by the migration of ferric ions [J]. Polymer Chemistry, 2013, 4(17): 4601-5.
[4]Shi, L.; Wang, F.; Zhu, W.; Xu, Z.; Fuchs, S.; Hilborn, J.; Zhu, L.; Ma, Q.; Wang, Y.; Weng, X.; Ossipov, D. A., Self-Healing Silk Fibroin-Based Hydrogel for Bone Regeneration: Dynamic Metal-Ligand Self-Assembly Approach. Adv. Funct. Mater. 2017, 27,1700591.
[5]JIA Y, LI J. Molecular Assembly of Schiff Base Interactions: Construction and Application [J]. Chemical Reviews, 2015, 115(3): 1597-621.
[6]WEI Z, YANG J H, LIU Z Q, et al. Novel Biocompatible Polysaccharide-Based Self-Healing Hydrogel [J]. Advanced Functional Materials, 2015, 25(9): 1352-9.
[7]Gang Wang, Jiehua Zhu, Xiaofeng Chen, Hua Dong, Qingtao Li, Lei Zeng and Xiaodong CaoAlginate based antimicrobial hydrogels formed by integrating Diels–Alder "click chemistry" and the thiol ene reaction).
[8]Wang Y , Xu Q , Chen T , et al. A dynamic-coupling-reaction-based autonomous self-healing hydrogel with ultra-high stretching and adhesion properties[J]. Journal of Materials Chemistry B, 2019.
[9]Anti‐freezing, Conductive Self-healing Organohydrogels with Stable Strain㏒ensitivity at Subzero Temperatures[J]. Angewandte Chemie, 2017, 129(45):14159-14163.
