生物质碳源制备锂离子电池正极材料Na2MnPO4F/C及其电化学性能研究*
2020-02-13艾慧婷周含子吕奕菊张淑芬
李 伟,刘 峥,艾慧婷,周含子,吕奕菊,张淑芬,2
(1. 桂林理工大学 化学与生物工程学院 电磁化学功能物质广西区重点实验室,广西 桂林 541004;2. 大连理工大学 精细化工重点实验室,辽宁 大连,116024)
0 引 言
近年来,储能设备逐渐成为研究热门,锂离子电池作为最热门的电池之一,对其的需求量日益增加。然而,地壳中锂元素仅为0.0065%,锂资源十分短缺,这对于锂离子电池是个巨大的冲击。
LiCoO2作为商品化锂离子电池中最成功的正极材料,理论容量能达到274 m Ah/g,但在实际的应用当中,有着许多致命的问题。在当电池充放电中需要让锂离子的脱嵌量在0.55个单元以下,否则能使材料发生不可逆的相变,容量快速衰减,因为脱嵌量的改变,最终实验中实际容量只在140 m Ah/g左右。同时地壳中钴元素的含量并不比锂元素的含量多,资源也是十分紧张,钴的毒性也会令其应用受到限制[1-3]。当钴酸锂作为正极材料时,过度充电后,可能会导致电池材料分解,并产生大量的热甚至爆炸。
目前聚阴离子型正极材料因为结构的稳定受到众多人的关注与研究[4]。所谓的聚阴离子型化合物就是指一系列含有八面体或者四面体阴离子结构单元(XOm)n-(Y)k-(X=P、S、Mo和W等,Y=F和OH等)的化合物的总称,在该种结构框架中四面体和八面体进行三维连接,最终形成网状结构[5],结构都十分稳定。用于作正极材料的聚阴离子型磷酸盐(如橄榄石晶体结构LiFePO4[6-8]、LiMnPO4[9]和单斜晶体结构的Li3V2(PO4)3[10-12]等),与传统正极材料相比,比容量较高、低危险性并对环境污染小,但这类聚阴离子型磷酸盐也存在工作电压平台较低(如LiFePO4为3.4 V),锂离子扩散速度较慢等不足。
考虑到锂元素资源的匮乏,人们发现聚阴离子化合物中钠基氟化磷酸盐体系具有良好的电化学性能,可考虑作为锂离子电池正极材料[13-14]。该类化合物具有强电负性的氟元素能够提高充放电电压[2],钠基氟化磷酸盐体系有可能出现两个或两个以上的电子转移,可以大大提高电池的比容量[15-16]。钠基氟化磷酸盐作为锂离子正极材料,打破了传统观念,即锂离子电池中的正极材料必须是锂基化合物,扩大了锂离子正极材料的研究范围[17]。Na、Mn在地球上含量丰富,文献表明,减小颗粒尺寸和增加碳涂层是两种有效改善钠基氟化磷酸盐体系电子电导率低和离子扩散速度慢的方法,所以研究Na2MnPO4F/C复合正极材料意义重大。
本文利用生物质碳材料作为碳源对聚氟阴离子材料进行包覆,可使成本更为低廉,使用原位热解法令有机碳源在烧结过程中分解,最后得到的碳材料比表面积较大,碳材料的包覆也能减小材料的粒径,同时碳材料为高导电性材料,有助于电子的传递。
1 实验
1.1 Na2MnPO4F/C复合正极材料的制备
(1)甘蔗渣预处理方法 :将配制好的5%氢氧化钠溶液倒入甘蔗渣中,在80 ℃恒温加热2 h,再浸泡4 h后,从中取出预处理后的甘蔗渣并用蒸馏水清洗至pH为中性。在鼓风干燥箱中进行烘干,将烘干后的甘蔗渣放入密封式研磨机中进行研磨,研磨成300~400目的粉末,待用。
(2)Na2MnPO4F/C正极材料制备方法:①称取2.4509 g Mn(CH3COO)2·4H2O、0.4199 g NaF、1.1502 g NH4H2PO4和1.3608 gNaCH3COO·3H2O,加入0.538 2 g甘蔗渣作为碳源,加入20 mL无水乙醇作为分散剂,球磨6 h后,然后将研磨后得到的流变相浆体置于65 ℃的鼓风干燥箱保温5 h左右以除去乙醇,获得前驱体粉末。②将干燥后的前驱体粉末装入坩埚在氩气保护的管式炉中300 ℃预热2 h(升温速率为5 ℃/min),将预热好的粉末再次研磨,然后在600 ℃下在充满氩气的管式炉中煅烧6 h(升温速率为10 ℃/min),随管式炉冷却至室温,得到Na2MnPO4F/C复合正极材料(活性物质)。
1.2 样品的表征分析
利用美国TA公司生产的SDT-Q600 型热重分析仪,测试甘蔗渣的热重曲线,获得残碳量,测试条件:用N2保护,升温速率为10 ℃/min,最高温度为900 ℃;采用英国雷尼绍公司in via激光拉曼光谱仪,测定样品的拉曼光谱测试条件:电源为220 V±10%,仪器操作环境温度为20 ℃~25 ℃,仪器操作环境湿度<50%,激光器波长为 514 nm及785 nm;采用荷兰帕纳科公司生产的 X射线粉末衍射仪,测试样品的X射线粉末衍射谱图,分析其相组成和相结构,测试条件:电压40 kV,电流40 mA, Cu(Kα)靶,λ=1.54426,扫描速率16° min-1,扫描范围10~90°;采用日本日立公司生产的场发射扫描电子显微镜,测试样品的SEM照片,对其表面的微观形貌进行观察与分析,测试条件:加速电压3 kV,发射电流10 100 nA,工作距离6 000 μm;采用德国牛津的能谱分析仪,测定样品的元素成份,测试条件:工作距离为 5~40 mm, 空间分辨率 0.5 μm,角度分辨率 0.50。
1.3 Na2MnPO4F/C复合正极材料的电化学性能测试
(1)锂离子电池电极片制备与电池装配:按照m(活性物质)∶m(乙炔黑)∶m(聚偏二氟乙烯)(PVDF)=7∶2∶1的比例,先分别称取一定质量的活性物质,乙炔黑,将这些物质混合并进行研磨,研磨的时间约为60 min,再称取PVDF(粘结剂)加入研钵中,研磨十几分钟使其充分混合,滴加适量N-甲基吡咯烷酮(NMP),调整为适合的稀稠度,将研磨好的物质涂在铝片上,真空干燥12 h,最后压成合适大小的极片待用。将制备好的极片作为研究电极,首先称量极片的质量,再将称好的极片放入事先清洗并烘干的正极壳中,配好垫片、弹片和负极壳,以金属锂片为对电极,以聚丙烯多孔膜为隔膜,以1.0 mol/L LiPF6的碳酸乙烯酯(EC)、碳酸二甲酯(DMC)的混合液(m(EC)∶m(DMC)=1∶1)为电解液,在Ar气保护的米开罗那(中国)有限公司的MIKPROUNA 超级净化手套箱中(氧气及水蒸气含量均小于1×10-6)中进行半电池的组装、压片。
(2)充放电性能曲线的测试:采用新威电池性能测试系统,测试循环性能曲线、倍率性能曲线、库仑效率曲线、充放电平台曲线,分析其充放电性能。测试条件:温度为25 ℃,电压范围为1.5~4.5 V,循环性能电流密度为0.1 C,倍率性能所用倍率为0.1 C、0.2 C、0.5 C、1 C、2 C。
(3)循环伏安曲线和电化学交流阻抗谱的测定:通过上海辰华公司生产的 CHI860D 电化学工作站, 采用半电池体系,测定所组装的纽扣电池的循环伏安曲线,分析其氧化还原峰电位。测试条件:扫描范围为1.5~4.5 V,扫描速率为10 mV/s;以及测定电化学交流阻抗谱,分析其电阻。测试条件:温度为室温,测试参数设置为0.01~10 000 Hz,振幅为5 mV。
2 结果与讨论
2.1 Na2MnPO4F/C正极材料制备条件优化
2.1.1 碳源用量影响
按照1.1方法,温度控制600 ℃,改变碳源用量为5%、10%、15%进行实验,获得的3种Na2MnPO4F/C正极材料样品,利用拉曼光谱对样品进行测试,结果见图1。
拉曼光谱G-band(-1 580 cm-1)是由碳环或长链中的所有sp2杂化振动产生的, D-band(-1 360 cm-1)则是由于晶体缺陷和无序诱导产生,一般用D峰和G峰的强度比值来衡量碳材料的无序度[18]。ID/IG值越小,则表明样品石墨化程度越高。从拉曼光谱图1中可以看出,不同活化温度下,制备的甘蔗渣的D峰都出现在1 360 cm-1,是甘蔗渣石墨中结晶边界区域的拉曼活性,来自结晶大小效应的贡献;G峰出现在1 580 cm-1附近,它在所有碳纤维光谱中都出现[18]。

表1 600 ℃下不同碳源用量Na2MnPO4F/C正极材料样品的R值Table 1 R value of Na2MnPO4F/C cathode material sample with different carbon source dosage at 600 ℃
从表1可知,制备Na2MnPO4F/C正极材料时,当碳源用量为15%的时,R值最小,得到的Na2MnPO4F/C正极材料中碳材料石墨化程度最高,石墨化程度越高,越能增加其电导性。本文确定15%的碳源用量为制备Na2MnPO4F/C正极材料的最佳碳源用量。
2.1.2 煅烧温度的影响
按照1.1方法,在最佳碳源用量下,改变温度为600、650、700 ℃进行实验,获得3种Na2MnPO4F/C正极材料样品,利用拉曼光谱对样品进行测试,结果见图2。

图2 15%碳源用量不同煅烧温度Na2MnPO4F/C正极材料样品的拉曼光谱图Fig 2 Raman spectra of Na2MnPO4F/C cathode material samples at different calcination temperatures of 15% carbon source
依据拉曼光谱图计算R值列于表2。从表2可知,当碳源用量为15%时制备Na2MnPO4F/C正极材料,600 ℃的煅烧温度可以得到石墨化程度最高的碳材料(R值最小)。本文选择600 ℃为Na2MnPO4F/C正极材料的最佳煅烧温度。
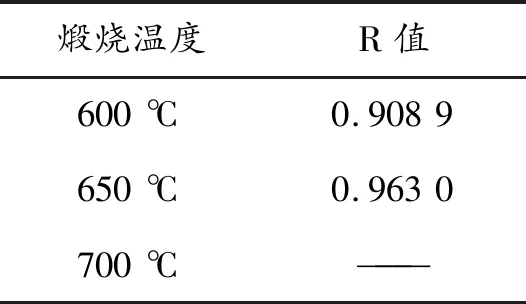
表2 15%碳源用量不同煅烧温度Na2MnPO4F/C正极材料样品的R值Table 2 R value of Na2MnPO4F/C cathode material sample at different calcination temperature of 15% carbon source
综上所述,Na2MnPO4F/C正极材料制备最佳条件为碳源用量为15%,煅烧温度为600 ℃。
2.2 Na2MnPO4F/C正极材料表征分析
2.2.1 SEM分析
按1.2的测试条件,进行Na2MnPO4F/C正极材料的扫描电镜测试,结果见图3。

图3 Na2MnPO4F/C正极材料的扫描电镜图Fig 3 Scanning electron micrograph of Na2MnPO4F/C cathode material
从图3可以看出Na2MnPO4F/C正极材料的结晶性较为良好,粒子尺寸通过观察图中与标尺进行对比,大概在400~500 nm范围内。这主要是由于甘蔗渣高温分解时所产生的碳有效地抑制了Na2FePO4F晶粒在煅烧过程中的生长,并且剩余的碳有助于粒子之间的分散。
2.2.2 EDS分析
按1.2的测试条件,进行Na2MnPO4F/C正极材料的EDS能谱分析,结果见图4。

图4 Na2MnPO4F/C正极材料的EDS谱图Fig 4 EDS diagram of Na2MnPO4F/C cathode material
由图4可知,EDS谱图中发现正极材料中所有的元素,所有元素含量之和接近百分之百,证明正极材料中杂质较少,碳均匀的分布在所制得的Na2MnPO4F/C正极材料表面,证明碳材料成包覆成功。
2.2.3 XRD分析
按1.2的测试条件,进行Na2MnPO4F/C正极材料和Na2MnPO4F材料样品的X射线粉末衍射测试,结果见图5。
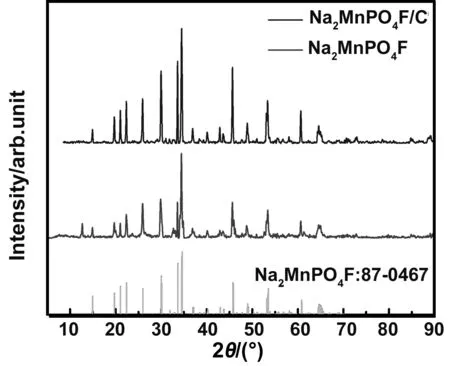
图5 碳包覆Na2MnPO4F正极材料的 XRD 图Fig 5 XRD patterns of carbon coated Na2MnPO4F cathode material
图5中可以看出,未包覆碳以及包覆碳的Na2MnPO4F材料样品的XRD衍射谱图均能与Na2MnPO4F标准卡片(PDF#87-0467)图谱吻合,基本没有出现多余的杂峰,这说明制得的样品为Na2MnPO4F ,且其晶型结构并没有因为碳包覆而改变。
2.3 Na2MnPO4F/C正极材料电化学性能
2.3.1 循环性能曲线分析
按照1.3的方法制备碳包覆样品的纽扣电池,利用新威电池测试系统,恒流下(0.1 C)进行循环性能测试,与未进行碳包覆的对照材料样品同时进行测试,结果图6所示。

图6 不同样品材料的循环性能曲线Fig 6 Cycle performance curves of different sample materials
图6为Na2MnPO4F/C正极材料、Na2MnPO4F材料的循环性能曲线图。从图6中可以看出,Na2MnPO4F/C在0.1 C倍率下经过充放电循环,首圈放电比容量为8.71 m Ah/g,在30圈循环后容量衰减至5.75 m Ah/g;而未包覆碳材料放电比容量首圈为1.94 m Ah/g ,循环30圈后衰减为1.56 m Ah/g,由此可知碳包覆可以增强正极材料的放电比容量。经计算可知,Na2MnPO4F的理论比容量为135 m Ah/g,与本文所测得数据有差异,可能因为当锰的平均价态低于+3.5价时会发生Jahn-Teller效应,晶体结构将发生畸变使晶胞单元体积变大,使材料结构变得不稳定,容量减低并加快衰减。另一个原因可能是锰在Na2MnPO4F中为+2价,Mn2+可以溶于电解液中,当电解液中存在痕量的水时,电解质LiPF6就会与水反应生成HF,而HF会加速Mn2+的溶解,使得活性物质减少,造成比容量大大减小[2]。同时,在高温的影响下,Mn2+的溶解量将会增加,导致比容量更小。
2.3.2 倍率性能曲线分析
图7为Na2MnPO4F/C正极材料、Na2MnPO4F对比材料样品的倍率性能曲线图。

图7 不同样品材料倍率性能曲线Fig 7 Different sample material rate performance curve
由图7可以看出,Na2MnPO4F/C材料样品和其对比材料在0.1 C、0.2 C、0.5 C、1 C和2 C 5个倍率下的放电容量为8.7至3.7 m Ah/g,放电容量不高,可能是因为Na2MnPO4F/C正极材料中Mn2+溶解在电解液中,导致容量变低。但与碳包覆相比,碳包覆还是可以提高其电导性,使容量提高。
2.3.3 库伦效率曲线分析
图8为Na2MnPO4F/C正极材料、Na2MnPO4F对比样品材料的库伦效率曲线图。

图8 不同样品材料的库伦效率曲线Fig 8 Coulombic efficiency curves of different sample materials
由图8可看出,两个样品的首次库伦效率都较低,可能是因为首次脱Na+后,Li+并不能顺利地嵌入。在后面的循环中,库伦效率逐渐增加,最后Na2MnPO4F/C的库伦效率增至98.98%,要比未包覆碳材料稍高。
2.3.4 循环伏安曲线分析
图9为Na2MnPO4F/C正极材料、Na2MnPO4F对比材料样品的循环伏安曲线图。

图9 不同样品材料的循环伏安图Fig 9 Cyclic voltammograms of different sample materials
图9为材料在1.5~4.5 V电压区间,10 m V/s扫描速率下的循环伏安曲线。图9(a)和图9(b)可知,Na2MnPO4F/C正极材料循环伏安曲线所围的面积较Na2MnPO4F对比材料样品的面积大,表明Na2MnPO4F/C正极材料的容量要比Na2MnPO4F对比材料样品大。
3 结 论
(1)通过拉曼光谱测试分析,获得Na2MnPO4F/C正极材料最优条件为碳源用量在15%,煅烧温度在600℃;在最优条件下,制备的正极材料R值最小,证明其中碳的石墨化程度最高,电导性最好。
(2)通过SEM、EDS、XRD等表征手段,证明所制备材料结晶性较好,碳材料可以均匀包覆在聚氟阴离子材料表面上。
(3)将正极材料组装成CR2032型纽扣电池进行循环伏安曲线的测试,证明进行碳包覆材料比未进行碳包覆材料的电化学性能更好,其表现为前者比容量更大。
(4)进行充放电曲线测试,发现Na2MnPO4F/C正极材料比容量与理论值差距较大,主要原因是因为Na2MnPO4F/C正极材料颗粒粒径较大,并且材料中的Mn2+溶解在电解液中,导致容量的衰减。
