藏药“佐太”的研究进展
2020-02-04周自强孙芳云
周自强 孙芳云
【摘 要】 佐太的最主要原料是汞,经过洗、涤、煮等多道复杂炮制工艺后,再加以多种重金属,煅炭存性而成。佐太是制作多种珍宝类藏成药的重要原材料,也是藏药中诸多重金属元素的主要的存在形式。对佐太的深入研究为开发治疗心脑血管疾病、消化系统疾病和肿瘤等的新药研发提供新思路。文章根据近年来佐太研究的相关文献,从药物成分、药效学、药代动力学、毒理学及临床进展进行分析与总结。
【关键词】 藏药;佐太;重金属;药效学;毒理学
【中图分类号】R29 【文献标志码】 A【文章编号】1007-8517(2020)23-0055-05
Research Progress of Tibetan Medicine “Zuo Tai”
ZHOU Ziqiang SUN Fangyun*
Engineering research center of Tibetan medicine testing technology of ministry of education,xianyang 712082,China
Abstract:The key raw material of Zuotai is mercury, which is made by forging a variety of heavy metals after washing, cleaning, cooking and other complex processing processes. Zuotai is not only an important raw material for making a variety of precious Tibetan medicines, but also the main form of many heavy metal elements in Tibetan medicines. Recent studies have reported Zuotai from the perspectives of pharmaceutical ingredients, pharmacodynamics, pharmacokinetics, toxicology and clinical effects. Therefore, in-depth research on Zuotai will provide novel ideas for the development of new medicines for the administration?of cardiovascular and cerebrovascular diseases, digestive diseases and tumors.
Keywords:Tibetan Medicine; Zuotai; Heavy Metal;Pharmacodynamics;Toxicology
佐太,藏名为“仁青欧曲佐珠钦木”[1],又称“佐台”“佐塔”“甘露精王”等,在藏药中应用广泛且历史悠久,为珍宝类藏成药“仁青常觉”“七十味珍珠丸”“大月晶丸”等药的核心配伍成分[2]。佐太在藏药组份中常起提升治疗效果、降低毒副作用的功能。由于佐太中含有诸多有毒重金属物质,以至于很多藏药在临床的推广和应用上受到限制。为了更好地继承与发展这一传统藏药,现将其药物成分、药效学研究、药代动力学研究、毒理学研究和临床研究进展进行总结归纳,为基于佐太的药物研发提供参考依据。
1 佐太成分分析
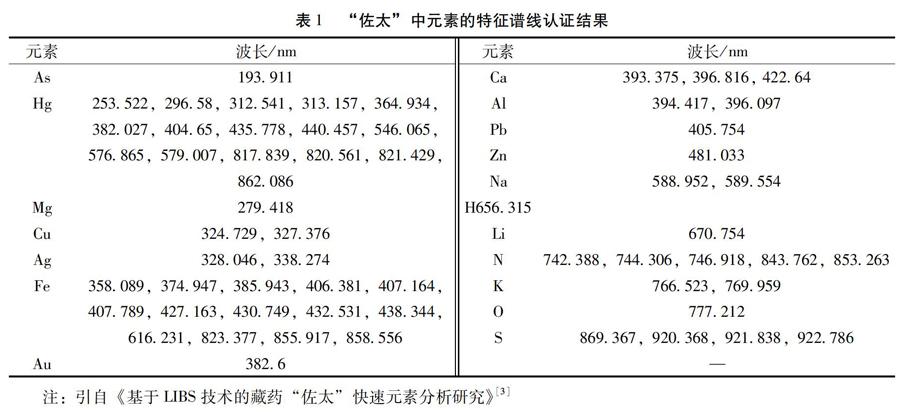
1.1 化学元素分析 刘晓娜等[3]运用LIBS技术对佐太进行了定性元素分析,并得到它的光谱图。分析结果表明,佐太主要由14种元素组成,分别是汞(Hg)、铁(Fe)、钾(K)、钙(Ca)、钠(Na)、以及含量较少的铅(Pb)、银(Ag)、金(Au)等,同时还在佐太中发现了硫(S)元素的存在(如表1)。李岑等[4]发现,佐太中主要存在的元素为汞(Hg)和硫(S),此外还有氧(O)、铁(Fe)、铝(Al)、铜(Cu)、钾(K)、银(Ag)、钙(Ca)、镁(Mg)等元素。
1.2 微观结构分析 李岑等[4]采用多种实验方法对佐太进行微观结构分析发现,在佐太中以正2价形式存在的汞元素,其配位原子为硫,配位数是4。佐太的结晶度在59%左右,且存在空间群为F-43 m216的立方晶系β- HgS、空间群为Fddd70的斜方晶系单质硫S8,空间群为P63/ mmc194的六方晶系碳C、空间群为P63/ mmc194的六方晶系铁Fe1.05 S0.95、空间群为P63/mmc194的六方晶系铜Cu6S6、空间群为F-43 m216的立方晶系Cu1.8 S等。此外,佐太中微粒多在100~600nm,部分低于100nm,它们可形成1~20μm松散不规则型的颗粒。佐太中不规则型物质占总体的41%左右,因此佐太应为古代微纳米药物,此微观结构的分析对佐太的认识与发展具有重要的意义。
1.3 有机物成分分析 文献中对于佐太有机物成分的报道比较少见,有研究用石油醚和乙醇各对佐太做有机成分提取,液相检测后发现石油醚可提出极少量的非极性化合物,而醇提物中化合物則相对较多,对于佐太中的有机物的发现还需要更多的实验来论证[5]。
2 药效学研究
2.1 佐太的解热镇痛作用 蒋婀娜等[6]研究表明佐太可以降低接种伤寒疫苗后产生发热现象的新西兰兔体温;可以使小鼠的惊厥潜伏期及死亡潜伏期显著延长;对于二甲苯所导致小鼠外耳肿胀,佐太可使其症状有效减轻;可显著提高小鼠的廓清指数以及吞噬指数。说明佐太具有解热、抗惊厥、抗炎和增强机体免疫力等作用。
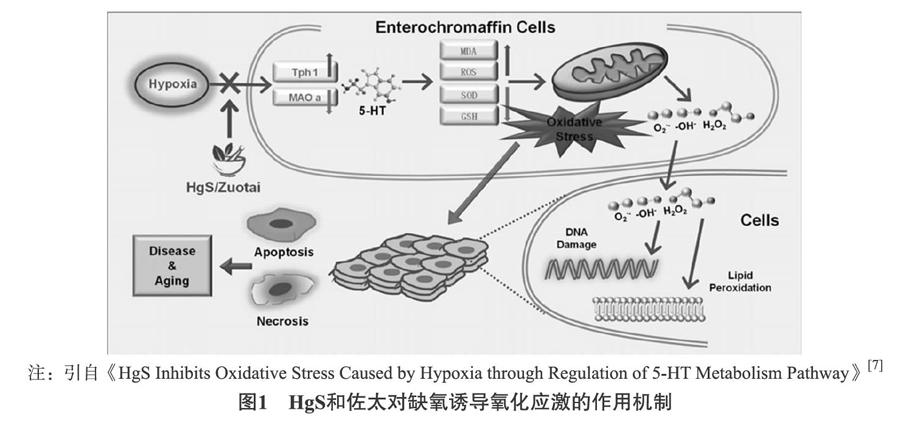
2.2 佐太对细胞氧化应激的作用 He等[7]细胞体外实验发现,缺氧使细胞处于氧化应激状态时,外源性5-羟色胺可加重氧化应激,在使用佐太后可以减轻细胞氧化应激现象。此外,体内实验显示,在斑马鱼体内使用佐太可降低缺氧诱导的活性氧(ROS),并可治愈行为异常。因此,生物缺氧诱导氧化应激5-羟色胺水平被发现异常升高,表明5-羟色胺能调节氧化应激,在进行佐太给药后,5-羟色胺含量降低,行为异常得到缓解。研究说明: 佐太可能基于5-羟色胺的代谢来调节和缓解氧化应激现象(如图1)。尽管目前佐太的剂量对细胞系没有显示出毒性,但它们的剂量依赖性仍有待评估。
2.3 佐太的中枢抑制作用 曾勇等[8]研究发现佐太具有降低正常小鼠自发活动量的趋势、对镇静催眠药物所致小鼠的睡眠潜伏期有缩短趋势,对其所致睡眠时间具有延长的趋势、可以增加士的宁所致惊厥诱导时间且减低惊厥率。说明佐太有一定的中枢抑制作用。
文献报道佐太可影响钟基因的表达,使神经元PAS域蛋白2(Npas2)、脑肌肉Arnt- like蛋白1(Bmal1)在10: 00时的振幅降低。在时钟驱动的靶基因中,佐太增加了PAR- bZip家族成员d- box结合蛋白(Dbp)的振荡幅度,降低了核因子白细胞介素3(Nfil3)[9],結果有助于对佐太的部分药理和毒理作用机制作出解释。
Zhang等[10]发现佐太具有良好的治疗小鼠抑郁样行为的能力,通过对小鼠进行强迫游泳试验、悬尾试验和野外试验,发现佐太可明显提高小鼠的运动能力;在小鼠的蔗糖偏好试验中,佐太显著增加了小鼠的体重和蔗糖偏好比;佐太可显著降低HPA轴皮质激素释放激素、促肾上腺皮质激素和皮质酮水平,并使CUMS小鼠血清中5-羟色胺和去甲肾上腺素水平升高。然而,由于佐太中少量汞在鼠的下丘脑和海马中沉积,这可能对中枢神经系统造成潜在的危险。
3 药代动力学研究
李向阳等[11]研究发现分别给予大鼠佐太7d和21d后,显示短期内佐太中的汞在大鼠体内吸收较少,但明显蓄积于肝肾组织中,维持原剂量持续给予大鼠佐太,可发现蓄积于肝脏中的汞含量明显降低,肾脏中的汞却显著增多,说明汞在大鼠肝脏中的蓄积只是暂时的,最终会在肾脏产生大量的蓄积; 在对粪便和尿液的检测中发现,只有极少量的汞存在于尿液中,却有大量的汞存在于粪便中,证明通过粪便排出体外是佐太的一种重要的排泄形式。
4 毒理学研究
4.1 佐太的肝肾毒性 Zhou等[12]通过评估佐太对肝细胞和斑马鱼的毒性作用发现佐太可使L-02细胞、HepG2细胞和RBL-2 A细胞的存活率随剂量和时间的变化而降低。佐太(0.1mg/mL)诱导HepG2细胞收缩、凝集、破碎,增加凋亡细胞数量。Caspase-3和 bax的表达活动水平增加,并且bcl-2的表达水平在HepG2细胞暴露于佐太(10-4-0.1mg/mL)24h后会减少。此外,佐太(0.2mg/mL)可诱导幼年的斑马鱼深色肝脏颜色改变和成年斑马鱼肝脏形态学改变。佐太(0.2mg/mL)能提高成年斑马鱼肝脏中CYP1A1、CYP1B1以及MT-1的mRNA水平。结果显示,佐太在一定剂量下可有效诱导肝毒性,但其肝毒性可能是通过其它不依赖于HgS的机制发生的。
李岑等[13]通过多种长期试验观察证实了传统藏药佐太的毒性极低,在其参与临床配伍的药物中安全性良好,在临床剂量用药下以及临床服药周期内未发现不良作用,但长时间大剂量用药可能会给肾脏造成一定的毒副作用。朱洪梅等[14]通过小鼠以临床等效剂量长期给予藏药佐太进行观察,结果显示小鼠以临床等效剂量给药佐太4.5个月后,其生长发育情况、大体外观、脑组织形态学结构、各种生理生化指标均无明显影响,但可损伤到小鼠肝脏、脾脏以及肾脏等的组织学结构,表明不能长期服用含有佐太成分的药物。
张国英等[15]以昆明种小鼠作为研究对象,连续给予4.5个月等效剂量的佐太,停止给药1.5个月后,发现长时间将临床等效剂量的佐太灌胃小鼠后,汞在肾脏和脑组织中会发生蓄积,但在停止给药后几个月内可逐渐恢复到正常水平,而汞的蓄积现象并不明显发生于血液、肝脏和脾脏等组织器官。
张炜等[16]研究发现大鼠在给予佐太和佐太制剂之后,血液以及其它重要器官中会出现汞的蓄积,且呈剂量和时间依赖性。同时,对大鼠各重要组织器官内蓄积的汞进行分析后发现,大鼠体内蓄积的汞主要是毒性较小的无机汞,而具有剧毒的有机汞则含量较低。表明佐太制剂在服用时,应该考虑以短期、低剂量的形式使用。
Cen等[17]使用x光吸收光谱和基于同步辐射x射线荧光成像研究汞化学形式和汞特殊分布,分别给予不同分组小鼠以佐太、β-HgS 以及HgCl2一段时间后,对肾脏进行病理组织学观察。发现汞主要沉积在肾皮质,肾髓质的汞含量很低。而肾脏的含汞量最高的是给予HgCl2饲养的老鼠,其次是给予β-HgS饲养的老鼠,肾脏含汞量最低的是给予佐太饲养的小鼠。这些发现阐明了汞元素在小鼠体内的毒性差异与其化学性质、空间分布密切相关。
4.2 佐太的细胞毒性 耿卢婧等[18]研究发现佐太、β- HgS对神经细胞株 PC12细胞的毒性远小于HgCl2,佐太、β- HgS可能会引起促凋亡基因Bax、Bak及死亡受体Fas/ FasL通路信号传导阻滞,这可为研究佐太等含汞药物的药理活性、毒理作用提供新思路。
朱婷等[19]实验发现当佐太浓度在0.125g/ L的时候人胚肾细胞的增殖速度显著,通过对凋亡相关因子caspase-3在基因水平和蛋白水平下的检测也证实了在这两个浓度下caspase-3不表达或是表达量明显降低,表明佐太可以限制 caspase-3表达来促进人胚肾细胞增殖,并且存在剂量效应关系。由于佐太中含有高剂量的汞化合物可能会对细胞产生毒性作用,基于对人体用药安全健康方面的考虑,佐太的使用程度对细胞的毒性作用还需要更多的实验结果来验证。
综上,佐太以及其制剂安全性高,在正常剂量和正常服药周期内服用对机体不会产生明显的毒副作用,但长时间服用后,会对肾功能造成一定的损伤,表明佐太及其制剂不适用于长疗程大剂量服用。
5 临床研究进展
目前,将佐太独自用于临床治疗的病例未见文献报道。佐太主要被当作复方佐剂成分,与多种药物配伍,以增强药物疗效,并减低毒性[20-21]。含有佐太的复方制剂在临床上应用很广泛,在消化性溃疡的治疗中常用藏药大月晶丸,大月晶丸的应用对于消化性溃疡患者可以保证治疗有效性[22]。萎缩性胃炎等消化系统疾病用仁青常觉有显著疗效[23]。对慢性萎缩性胃炎患者予以仁青常觉、帕朱丸两种藏药联合使用,其药物疗效显著优于西药联合用药[24]。对于脑出血患者,脑卒中、阿尔兹海默症等脑血管疾病及其后遗症用七十味珍珠丸治疗,可明显提升临床治疗效果[25-27]。藏药七十味松石丸常用治疗于乙型肝炎及肝硬化等肝脏疾病[28]。佐太在藏药体系中发挥重要的治疗及辅助作用。
藏医药学是千百年来藏族人民对自然、健康和生命的求索,同时又是藏民族战胜各种疾病的经验汇聚,其理论体系的完整性、治愈疾病的有效性、施治药物的独特性是藏医药学得以传承下来和继续发展的根本所在[29]。千百年临床实践证明,藏医药具有简、便、廉、验的鲜明特点,在治疗心脑血管、肝炎、高原病等某些疑难疾病时作用独特、疗效确切,在民族地区尤其是高海拔地区的防病治病中发挥了不可替代的作用,受到了世界医药行业的关注。2018年国家中医药管理局将藏医药防治肝纤维化、脑中风后遗症选入重大专项课题指南。
但当前藏药的开发研制、生产加工以及质量标准制定等方面仍然存在着很多困难,其中备受人们关注的是藏药中含有的重金属成分[30]。从西医的观点来看,重金属是对机体有毒的物质,同时也是西药在质量控制中的重要指标之一。佐太中的重金属在炮制时会通过很多的特殊工艺进行去毒处理,但这些重金属在藏药中所起的作用仍需要更深入的科学验证来解释。因此对佐太进行更深入的化学成分研究、药效学研究、药代动力学研究以及毒理学研究是必不可少的。以期对佐太的有效性和安全性做出进一步的阐释,从而对促进藏药规范的生产具有重要而深远的意义。
参考文献
[1]诸国本.中国民族医药散论[M].北京:中国医药科技出版社,2006:334.
[2]孙元化.雪域奇葩藏医药[J].西北民族大学学报(哲学社会科学版),1992(3):92-94.
[3]刘晓娜,史新元,贾帅芸,等.基于LIBS技术的藏药“佐太”快速元素分析研究[J].世界科学技术-中医药现代化,2014,16(12):2582-2585.
[4]李岑,占堆,楞本才让,等.藏药佐太的化学成分、汞配位结构及微观形貌分析[J].光谱学与光谱分析,2015,35(4):1072-1078.
[5]蓝高武,陈忠杰,李文虎,等.藏药“佐塔”的成分分析[J].时珍国医国药,2010,21(12):3209-3211.
[6]蒋婀娜,张春光,王建华,等.藏药“佐太”主要药效学研究[J].时珍国医国药,2009,20(8):2113-2114.
[7]HE Q Q,MA J,KUMAR K P,et al.HgS Inhibits Oxidative Stress Caused by Hypoxia through Regulation of 5-HT Metabolism Pathway. [J]. International journal of molecular sciences,2019,20(6):1364-1378.
[8]曾勇,何毓敏,劉颖,等.藏药“佐塔”对中枢神经系统的部分药理作用研究[J].四川中医,2005(11):36-37.
[9]LI H,LI W K,LU Y F,et al.The Tibetan medicine Zuotai influences clock gene expression in the liver of mice.[J].PeerJ,2016(4):1632-1643.
[10]ZHANG B B,LIU Y M,HU A L,et al.HgS and Zuotai differ from HgCl2 and methyl mercury in intestinal Hg absorption,transporter expression and gut microbiome in mice[J].Toxicology and Applied Pharmacology,2019:379.
[11]李向阳,冯伟力,马祁生,等.藏药佐太中的汞在大鼠体内吸收和排泄的初步研究[J].时珍国医国药,2010,21(2):290-292.
[12]ZHOU L L,CHEN H J.Evaluation of hepatotoxicity potential of a potent traditional Tibetan medicine Zuotai.[J].Journal of ethnopharmacology,2018:234.
[13]李岑,王东平,多杰,等.藏药佐太安全性研究及其复方当佐的临床安全观察初探[J].中国中药杂志,2014,39(13):2573-2582.
[14]朱洪梅,魏立新,杜玉枝,等.藏药佐太长期给药对小鼠毒性的初步研究[J].时珍国医国药,2013,24(8):2022-2024.
[15]张国英,王东平,李岑,等.藏药佐太中汞的长期蓄积性实验研究[J].时珍国医国药,2012,23(9):2146-2147.
[16]张炜,刘海青,骆桂法,等.佐太及珍宝类藏成药中汞在大鼠体内的蓄积研究[J].中国药事,2020,34(2):195-201.
[17]CEN L,WEI X,SHENG Q C,et al.The chemical speciation, spatial distribution and toxicity of mercury from Tibetan medicine Zuotai,β-HgS and HgCl2 in mouse kidney[J].Journal of Trace Elements in Medicine and Biology,2018:45.
[18]耿卢婧,李岑,夏政华,等.佐太、β-HgS、HgCl2对PC12细胞活性和凋亡相关基因表达影响的比较[J].中成药,2019,41(3):543-548.
[19]朱婷,沈蓓,王新为,等.藏药“佐太”通过抑制caspase-3促进293细胞增殖[J].中国民族医药杂志,2013,19(5):47-49.
[20]黄海波,王奇志,王新为,等.藏药“左太”的研究进展[J].中国中药杂志,2013,38(17):2886-2888.
[21]杨梦,周雪姣,李向阳.藏药佐太的研究现状与进展[J].药学研究,2016,35(11):663-667.
[22]卓玛措.藏药大月晶丸治疗消化性溃疡症有效性[J].全科口腔医学电子杂志,2019,6(25):144.
[23]贾宝珠.分析藏药治疗慢性萎缩性胃炎的临床疗效[J].世界最新医学信息文摘,2019,19(41):206.
[24]兰有文.藏药仁青常觉治疗萎缩性胃炎45例临床观察[J].中国民族民间医药,2016,25(7):7.
[25]增太吉.观察藏药七十味珍珠丸治疗脑出血(脑溢血)的临床疗效[J].智慧健康,2019,5(28):179-180.
[26]陈红霞,裴晋云,潘锐焕,等.七十味珍珠丸治疗63例脑卒中恢复期患者临床疗效研究[J].时珍国医国药,2018,29(12):2968-2970.
[27]才让吉.应用藏药七十味珍珠丸改善阿尔茨海默病患者认知功能、氧化应激状态[J].临床医药文献电子杂志,2017,4(69):13613.
[28]久美彭措.久美七十味松石丸治疗病毒性甲型肝炎临床分析[J].青海医药杂志,2008(9):86-87.
[29]乌仁其其格.萨满巫医术与蒙古族传统医疗文化关系探析[J].内蒙古师范大学学报(哲学社会科学版),2009,38(1):13-17.
[30]朱俊博,史彦斌,李向阳.珍宝类藏药“佐塔”的现代研究[J].亚太传统医药,2014,10(9):8-9.
(收稿日期:2020-06-11 编辑:刘斌)
基金项目:西藏自治区教育厅藏医药区域协同创新中心项目(2018XTCX003)。
作者简介:周自强(1993-),男,汉族,硕士,研究方向为藏药药理学研究。E-mail:505838681@qq.com
通信作者:孙芳云(1963-),女,汉族,本科,教授,研究方向为藏药药理学与毒理学。E-mail:xzmysfy@163.com
