瑶药芦山藤化学成分初步研究
2020-02-04黄颖蒋艳华杨小良李兵
黄颖 蒋艳华 杨小良 李兵


【摘 要】 目的:对芦山藤的化学成分进行研究。方法:采用系统预试验法对芦山藤药材化学成分进行预试验,采用硅胶柱色谱、重结晶等分离方法对芦山藤的化学成分进行分离、纯化,并根据化合物的理化性质、波谱方法等进行结构鉴定。结果:从瑶药芦山藤中分离得到4个化合物,鉴定为:肉豆蔻酸(Myristic acid,1),豆甾醇(stigmasterol,2),山萮酸(Behenic acid,3),綠原酸(chlorogenic acid,4)。结论:化合物1、3、4为首次从该植物中分离得到,为进一步研究其化学成分提供参考。
【关键词】 芦山藤;化学成分;结构鉴定
【中图分类号】R284.1 【文献标志码】 A【文章编号】1007-8517(2020)23-0036-04
A Preliminary Study on Chemical Composition from Yao Medicine Cissampelopsis spelaeicola
HUANG Ying1 JIANG Yanhua2 YANG Xiaoliang1 LI Bing2*
1.Faculty of Chinese Medicine Science Guangxi University of Chinese Medicine,Nanning 530222,China;
2.Guangxi University of Chinese Medicine,Nanning 530200,China
Abstract:Objective To study the chemical constituents from Yao medicine Cissampelopsis spelaeicola. Methods The chemical components of C. spelaeicola were pretested by systematic pretest method. Constituents were isolated by silica gel column chromatography and recrystallization, et al. And their structures were identified by physicochemical properties and spectral methods. Result Four compounds were isolated from C. spelaeicola,and identified as Myristic acid(1),Stigmasterol(2),Behenic acid(3)and chlorogenic acid (4)。Conclusion Compounds 1, 2and 4 were isolated from the plant for the first time, and providing reference for further study of their chemical constituents.
Keywords:Cissampelopsis spelaeicola; Chemical Composition; Structural Identification
芦山藤是菊科植物岩穴千里光Cissampelopsis spelaeicola(Vant)C. Jeffrey et Y. L.Chen的干燥茎叶,具有祛风除湿、活血止痛等功效,用于治疗小儿惊风、风湿骨痛、跌打损伤等症[1]。该药始载于《中国高等植物图鉴》,《贵州植物志》中记载芦山藤的别名叫岩生藤菊,产于四川、贵州、云南、广西[2]。据前期的瑶药调查发现,芦山藤在广西除了分布于友谊关外,在广西壮族自治区金秀瑶族自治县境内多数地方也有分布。但通过查阅国内外文献,发现瑶药芦山藤的化学成分、药理活性、质量控制等方面的研究较少。仅有梁爽等[3]从糯米风75%乙醇提取物中共分离鉴定出12个化合物。同属植物研究也较少,仅有Ongkarn Vanijajiva1等[4]对藤菊属植物的历史沿革进行考证并进行完整的的修订。然而其同科植物化学成分及药理作用研究较多[5-13],显示出较好的活性及应用价值,其主要含有生物碱类、酚酸类、黄酮类、挥发油类、萜类以及其他成分,其药理作用包括抗菌、抗炎、抗病毒及抗肿瘤、抗氧化及清除自由基和毒理等作用。为了进一步研究芦山藤的化学成分,本研究利用多种色谱方法对广西瑶药芦山藤进行化学成分研究。
1 实验材料
1.1 药材及鉴定 芦山藤,2019年购于广西金秀县,经广西中医药大学壮医药学院韦松基教授鉴定为菊科植物岩穴千里光Cissampelopsis spelaeicola(Vant)C.Jeffrey et Y. L. Chen的干燥茎叶。
1.2 仪器与试剂 旋转蒸发器RE-52AA(上海亚荣);低温冷却液循环泵DLSB-5L/20(郑州长城科工贸);循环水式多用真空泵SHB-ⅢA(郑州长城科工贸有限公司);电热恒温水浴锅HWS-26(上海齐欣科学仪器有限公司);冷却水循环装置CCA-1112A(上海爱郎仪器有限公司);各种不同规格的普通玻璃柱(上海欣维尔有限公司)。柱色谱硅胶(国药集团化学试剂有限公司);硅胶板(青岛海洋化工有限公司);乙醇、石油醚(60~90℃)、乙酸乙酯、正丁醇、氯仿、丙酮、甲醇等试剂(国药集团化学试剂有限公司)。
2 芦山藤的化学成分预试验
为初步了解芦山藤中所含化学成分的类型,从而有目的地设计出提取和分离的路线,采用系统预试法对其进行化学成分预试验。
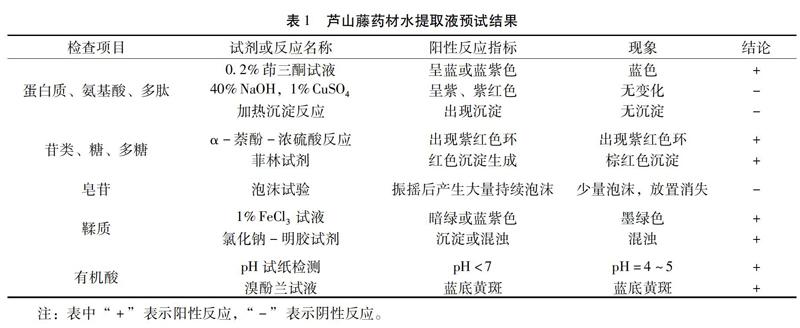
2.1 水提取液 取芦山藤药材粗粉10g加水100mL,冷浸24h,滤取10mL滤液做蛋白质、多肽、氨基酸检查。剩余药渣,于60℃水浴上加热30min,过滤,滤液作皂苷、糖、苷类、多糖、有机酸、鞣质检查,结果见表1。
2.2 乙醇提取液 取芦山藤药材粗粉10g加100mL乙醇,加热回流1h,过滤,滤液分成两个份,一份做黄酮、蒽酚类、内酯等化合物的检查。另一份回收溶剂至浸膏,15mL 5%HCl溶解,过滤,滤液做生物碱检查,结果见表2。
2.3 石油醚提取液预试 取芦山藤药材粗粉1g,加5mL石油醚,放置3h,过滤,取少许滤液做挥发油和油脂检查,结果见表3。
2.4 化学成分预试小结 化学成分预试验结果表明,瑶药芦山藤药材中可能含有糖类、苷、鞣质、有机酸、甾醇、三萜、黄酮、蒽醌、香豆素、酚类、生物碱、油脂等类型成分。
3 瑶药芦山藤化学成分的提取和分离
3.1 提取与分离过程 瑶药芦山藤药材粗粉8.4kg,用10倍量90%乙醇回流提取三次,10倍量70%乙醇回流三次,合并提取液,减压回收溶剂得到乙醇总提取物692.6g,取400g提取物,加水混悬后,依次用石油醚(60~90℃)、乙酸乙酯、正丁醇进行萃取分离,减压回收溶剂,得石油醚部位41g,乙酸乙酯部位112g,正丁醇部位62g,剩余水部位。
取石油醚部位35g,经硅胶柱色谱分离,用石油醚-乙酸乙酯梯度洗脱8组分, Fr.s3(石油醚-乙酸乙酯(10∶1))合并浓缩后所得流份再经硅胶柱色谱分离,石油醚-丙酮梯度洗脱,重结晶,得到白色结晶化合物1(3.3mg)。
Fr.s4瓶检识合并后,取2.3g浓缩物加硅胶拌样后,经硅胶柱色谱再次分离,氯仿-甲醇梯度洗脱,合并浓缩后,析出白色粉末,经重结晶,得到白色结晶化合物2(1.9mg)。三氯甲烷-甲醇(10∶1)组分再次经硅胶柱色谱分离,重结晶,得到化合物3(1.3mg)。乙酸乙酯(0∶10)组分后经反复硅胶柱色谱分离及重结晶得化合物4(白色固体2mg)。
3.2 图谱解析及结构推断 对芦山藤中分离得到的化合物通过理化检验、13C-NMR、1H-NMR等波谱方法进行结构鉴定,确定其化学结构。
3.3 结构鉴定 化合物1:白色粉末,易溶于乙酸乙酯、氯仿。1H-NMR(500MHz,CDCl3)δ:0.87 (3H,t,J= 6.94Hz),为末端甲基信号峰;1.31(22H,m),1.62(2H,m)一系列亚甲基信号; 2.34(2H,t,J=7.50 Hz)与吸电子基团相连的亚甲基信号,提示该化合物为长链脂肪族化合物。13C-NMR(500MHz,CDCl3)δ:180.42为羧基信号,34.11为羰基α位碳信号,31.94、29.71、29.68、29.66、29.61、29.45、29.38、29.26、29.07、24.68、22.70为一系列的亚甲基碳信号,14.12为末端甲基碳信号。以上数据与文献[14]报道基本一致,确定化合物2为肉豆蔻酸(Myristic acid),分子式为C14H28O2,不饱和度为1。
化合物2:白色细针状结晶,易溶于氯仿、丙酮,难溶于水。Libermann-Burchard反應呈阳性。1H-NMR(500MHz, CDCl3 )δ:0.67-1.54范围内,高场区出现多个甲基信号峰,,3.50(1H,m)为活泼氢,5.35(1H,m),5.14(1H,m),5.12(1H,m)为烯氢信号峰,13C-NMR(500MHz, CDCl3)高场区也出现多个甲基信号峰;71.82为连氧碳信号峰,140.76,138.34,129.28,121.73为烯碳信号峰,初步推断为甾体类化合物。具体氢谱数据、碳谱数据与文献[15]报道的豆甾醇数据基本一致,故鉴定化合物2为豆甾醇(stigmasterol),分子式为C29H48O。
化合物3:白色粉末,易溶于石油醚、乙酸乙酯,可溶于热丙酮,难溶于水、甲醇。1H-NMR(500MHz,CDCl3)δ:0.84 (3H,t,J=6.70Hz),为末端甲基信号峰;2.26,1.58和1.25为系列亚甲基氢信号,提示该化合物为长链脂肪族化合物。13C-NMR(500MHz,CDCl3)δ:176.48为羧基信号,33.96为羰基α位碳信号,31.90、29.67、29.63、29.59、29.46、29.33、29.27、29.13、24.88、22.66为一系列的亚甲基碳信号,14.07为末端甲基碳信号。因此该化合物应该是脂肪烷酸类化合物。根据以上数据分析,化合物3的碳谱和氢谱数据与文献报道[16]的山俞酸数据基本相同,因此确定化合物3为山萮酸(Behenic acid),分子式为 C22H44O2。
化合物4:白色粉末,mp:206~209℃,红外光谱与绿原酸标准图谱一致,将绿原酸对照品与其共薄层色谱,分别以石油醚-乙酸乙酯-甲酸、氯仿-甲醇-甲酸、乙酸丁酯-甲醇-甲酸共三种系统展开,二者的Rf均相等,且二者混合熔点不下降,故确定化合物4为绿原酸(chlorogenic acid)。
4 讨论
从瑶药芦山藤中分离得到4个化合物,鉴定为肉豆蔻酸(Myristic acid,1),豆甾醇(stigmasterol,2),山萮酸(Behenic acid,3),绿原酸(chlorogenic acid,4)。化合物1、3、4为首次从该植物中分离得到,本课题初步研究了芦山藤的化学成分,为进一步研究与开发芦山藤提供依据。
芦山藤研究较少,民间调研发现其治疗风湿骨痛、跌打损伤等疗效较好,从本实验分离所得的成分来看,豆甾醇具有抗肿瘤、抗炎、抗氧化、降低胆固醇和改善记忆等作用[17],而绿原酸具有抗菌、抗病毒、抗肿瘤、抗氧化、抗炎、调节代谢等药理作用[18-20],在食品、医药和化工等领域都有广泛的应用[21]。故很有必要继续开展其化学成分和药效物质基础研究,以便进一步阐明其发挥疗效的作用机制及控制药材的质量,确保其临床使用规范及安全。
参考文献
[1]《中华本草》编委会.中华本草(第七册)[M].上海:上海科学技术出版社,1999:953.
[2]中国科学院中国植物志编辑委员会.中国植物志[M].北京:科学出版社,1999: 222.
[3]梁爽,马雯芳,梁可文,等.瑶药糯米风醇提物的化学成分研究[J].中国药房,2019,30(20) :2835-2839.
[4]VANIJAJIVA O,W. KADEREIT J. A revision of Cissampelopsis (Asteraceae: Senecioneae)[J]. Kew bulletin,2008(63): 213-226.
[5] 林生, 张中晓, 沈云亨,等. 菊叶千里光的一个新木脂素苷[J]. 中国中药杂志, 2011, 36(13) :1755-1762.
[6] 朱立刚, 李志峰. 千里光的化学成分研究[J]. 黑龙江医药, 2014,27(3) : 543-544.
[7] 李卓, 刘科峰, 于洋, 等. 全叶千里光化学成分的研究(Ⅰ)[J]. 长春中医药大学学报, 2008, 24(2):158-158.
[8] 吴斌, 吴立军. 千里光属植物的化学成分研究进展[J]. 中国中药杂志, 2003,28(2) :97-100.
[9] 徐定平, 周鑫堂, 郜红利, 等. 千里光化学成分和药理作用研究进展[J]. 中国药师, 2014,17(9) :1562-1565.
[10]陈曦,任华忠,宋成英,等.蒌蒿地上部分化学成分研究[J].中药材,2019,42(4) :794-797.
[11]昝珂,陈筱清,屠鹏飞.多花蒿中愈创木内酯类成分研究[J].中国中药杂志,2018,43(11) :2295-2299.
[12] YU Y,SONG Y,LIU L, et al. Chemical constituents from Nannoglottis yuennanensis[J]. Biochemical Systematics and Ecology,2018:80.
[13] 姜海,杨柳,邢绪东,等.苍耳子的化学成分研究[J].中草药,2017,48(1) :47-51.
[14] 徐丹丹,周洪波,房志坚 . 粗叶悬钩子的化学成分研究[J]. 广东药学院学报,2012,28(2):142-144.
[15] 邝嘉乐,张德志. 紫茉莉根化学成分研究[J]. 广东药学院学报,2007,23(1):1-2.
[16] 郑宗平,梁敬钰,胡立宏.柳杉茎皮化学成分研究[J]. 中国天然药物,2004,2(5):272-275.
[17] 周志远,卢群,刘洋,等.豆甾醇的研究及开发进展[J].中国当代医药,2015,22(24):15-17.
[18] NAVEED M, HEJAZI V, ABBAS M, et al. Chlorogenic acid (CGA): a pharmacological review and call for further research [J]. Biomed Pharmacother, 2018(97):67-74.
[19] BAGDAS D, GUL Z, MEADE J A, et al. Pharmacologic overview of chlorogenic acidand its metabolites in chronic pain and inflammation [J]. Curr Neuropharmacol, 2020(18):216-228.
[20] LI Y, WANG Q, YAO X, et al. Induction of CYP3A4 and MDR1 gene expression by baicalin, baicalein, chlorogenic acid, and ginsenoside Rf through constitutive androstane receptor- and pregnane X receptor-mediated pathways [J]. Eur J Pharmacol, 2010(640):46-54.
[21] SANTANA-GLVEZ J, LUIS C Z, JACOBO-VELZQUEZ D A. Chlorogenic acid: recent advances on its dual role as a food additive and a nutraceutical against metabolic syndrome [J]. Molecules, 2017(22):358.
(收稿日期:2020-07-01 編辑:刘斌)
基金项目:2016年度广西高校中青年教师基础能力提升项目(KY2016YB828)。
作者简介:黄颖(1984-),女,汉族,硕士,讲师,研究方向为中药及其制剂质量分析。E-mail:77869160@qq.com
通信作者:李兵(1982-),男,汉族,硕士,副教授,研究方向为中药活性成分与质量标准研究。E-mail:215811180@qq.com
