基于浸出物和特征图谱的熵权TOPSIS法综合评价仙鹤草药材质量
2020-01-11曾昭君洪婉敏钟如帆胡瑶潘玲干丽
曾昭君 洪婉敏 钟如帆 胡瑶 潘玲 干丽


摘 要 目的:基于浸出物和特征图谱建立仙鹤草药材的整体质量评价模型,为该药材的综合质量评价和优质种源筛选提供依据。方法:参照2015年版《中国药典》(四部)通则采用不同的提取方法和溶剂条件,以浸出物含量和浸出物高效液相色谱(HPLC)特征图谱总峰面积为指标,通过加权综合评分优选仙鹤草浸出物的提取工艺。建立15批仙鹤草药材的HPLC特征图谱,并进行相似度评价和特征峰指认。采用SPSS 25.0软件对不同产地仙鹤草浸出物含量、药材特征峰总峰面积进行单因素方差分析和Pearson相关性分析,比较不同产地药材的质量优劣。以15批仙鹤草药材的特征峰峰面积和浸出物含量为指标,采用熵权逼近理想解排序法(TOPSIS)进行该药材综合质量评价。结果:优选出以50%乙醇为溶剂、热浸法提取的仙鹤草浸出物提取工艺。15批仙鹤草药材的相似度均大于0.92,并指认了4个特征成分(鞣花酸、槲皮苷、芹菜素、山柰酚)。不同产地的仙鹤草浸出物平均含量、药材特征图谱平均总峰面积均有显著差异(P<0.05或P<0.01),且两者呈正相关(r=0.86,P<0.01)。熵权TOPSIS法评价结果显示,安徽、浙江、四川、河南、江苏产仙鹤草药材质量评价中的贴近度(Ci)均值依次为0.689、0.351、0.218、0.308、0.361。结论:各批样品以安徽产仙鹤草药材质量最优,江苏、浙江产药材质量次之,河南产药材质量再次之,四川产地药材质量相对较差。所建立的仙鹤草浸出物提取工艺、药材特征图谱测定方法稳定可行;用于仙鶴草药材综合质量评价的熵权TOPSIS法客观、可量化,能有效评价该药材质量。
关键词 仙鹤草;浸出物;特征图谱;熵权TOPSIS法;质量评价
ABSTRACT OBJECTIVE: To establish an overall quality evaluation model for Agrimonia pilosa based on extract and characteristic spectrum, and to provide evidence for comprehensive quality evaluation of the medicinal material and screening of high-quality provenance. METHODS: Referring to different extraction method and solvent condition stated in 2015 edition of Chinese Pharmacopoeia (part Ⅳ), using the content and total peak area of HPLC characteristic chromatogram of extract as indexes, and the extraction technology was optimized by weighted comprehensive score. HPLC characteristic spectrum of 15 batches of A. pilosa was established, and similarity evaluation and characteristic peak identification were performed. SPSS 25.0 software was used to conduct single factor analysis and Pearson correlation analysis for the extract content and total peak area of A. pilosa from different origins. The quality of medicinal materials from different origins were compared. Entropy weight TOPSIS method was adopted to evaluate comprehensive quality of A. pilosa using the extract content and total peak area of 15 batches of A. pilosa. RESULTS: The extraction technology of A. pilosa extract, which was extracted with hot dip plating using 50% ethanol as solvent, was optimized. The similarity of 15 batches of A. pilosa was higher than 0.92, and 4 characteristic components were identified (ellagic acid, quercetin, apigenin, kaempferol). There were significant differences in average extract content and total peak area of characteristic chromatogram of A. pilosa from different origins (P<0.05 or P<0.01), and there was a certain positive correlation between them (r=0.86, P<0.01). Results of entropy weight TOPSIS evaluation showed that the average Ci values of A. pilosa in Anhui,Zhejiang,Sichuan,Henan and Jiangsu provinces were 0.689,0.351,0.218,0.308 and 0.361 respectively. CONCLUSIONS: The quality of A. pilosa from Anhui was the best,that from Zhejiang and Jiangsu was better,that from Henan was the second,and that from Sichuan was poor. Established extraction technology and characteristic spectrum determination method of A. pilosa are stable and feasible. The entropy weight TOPSIS model is objective and quantifiable for comprehensive quality evaluation of A. pilosa, and can effectively evaluate its quality.
KEYWORDS Agrimonia pilosa;Extract;Characteristic spectrum; Entropy weight TOPSIS method; Quality evaluation
仙鹤草为蔷薇科植物龙芽草Agrimonia pilosa Ledeb.的干燥地上部分,主产于我国浙江、江苏、湖北、安徽等地,多在夏秋两季茎叶茂盛时采收;具有收敛止血、截疟、止痢等功效,多用于治疗咯血、吐血、崩漏下血、疟疾、血痢等[1]。仙鹤草中主要含有黄酮类、三萜类、鞣质类以及酚类等化学成分,以黄酮类、鞣质类成分居多[2-5]。现代药理研究表明,仙鹤草中的黄酮类成分具有抗菌、抗病毒、降血糖、抗氧化等重要药理活性[6-8];鞣质类成分能在体外抑制肝癌、胃癌细胞增殖,其收敛止血及广谱抗菌等作用显著[8-15]。该药材临床使用量较大,控制其质量对确保临床疗效有着重要意义[6]。
浸出物测定系指用水或其他适宜的溶剂对药材和饮片中的可溶性物质进行测定[16],是中药材质量控制的重要部分,但2015年版《中国药典》(一部)“仙鹤草”项下仅记载其鉴别和检查等方法[1],而未对浸出物含量进行限定,也未采用液相色谱法等分析手段进行质量评价。中药特征图谱是一種能较全面反映药材质量的重要方法,被广泛应用于药材的质量评价[17]。基于此,本研究拟优选仙鹤草浸出物的提取工艺并测定其浸出物含量;同时,建立仙鹤草药材特征图谱,并基于其浸出物含量和药材特征图谱,采用熵权逼近理想解排序法(TOPSIS)综合评价15批不同产地仙鹤草药材的质量,为进一步确保该药材质量的有效、稳定以及优质种源的筛选提供参考依据。
1 材料
1.1 仪器
ARC型高效液相色谱(HPLC)仪,含二极管阵列(PDA)检测器(美国Waters公司);KQ-700DE型数控超声波清洗器(昆山市超声仪器有限公司);ME204E型万分之一分析天平(瑞士Mettler Toledo公司);111B型二两装高速中药粉碎机(瑞安市永历制药机械有限公司);DHG-9147A型电热恒温干燥箱(上海精宏实验设备有限公司);HWS28型电热恒温水浴锅(上海一恒科学仪器有限公司)。
1.2 药品与试剂
槲皮苷对照品(批号:111538-201606,纯度:≥90.6%)、芹菜素对照品(批号:111901-201603,纯度:≥99.2%)、山柰酚对照品(批号:110861-201611,纯度:≥95.5%)、鞣花酸对照品(批号111959-201903,纯度:≥89.3%)均购自中国食品药品检定研究院;磷酸、甲醇、乙腈均为色谱纯,乙醇为分析纯,水为超纯水。
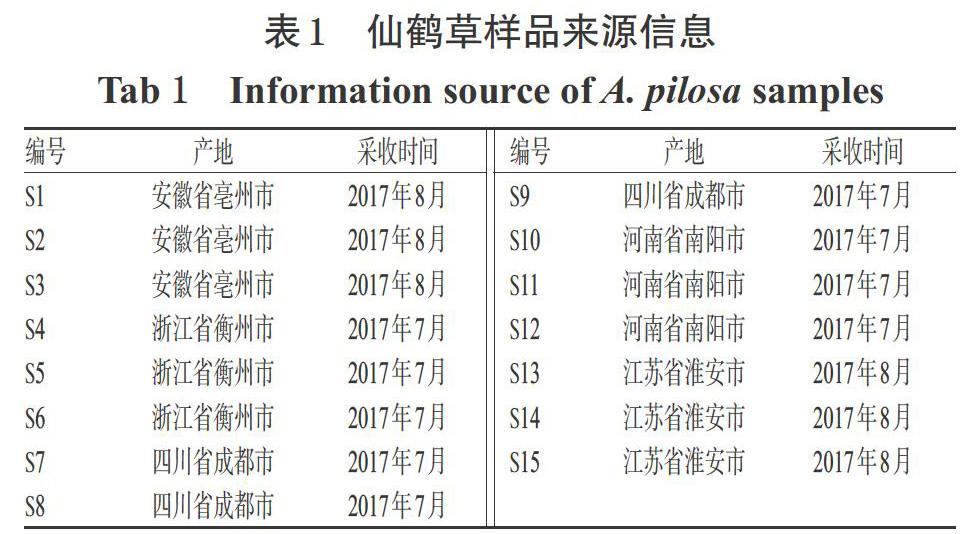
15批仙鹤草药材分别于2017 年采集自安徽亳州市、浙江衡州市、四川成都市、河南南阳市、江苏淮安市,并于同市不同乡镇各采集3批,经过广东一方制药有限公司魏梅主任药师鉴定为蔷薇科植物龙芽草A. pilosa Ledeb.的干燥地上部分,且符合2015年版《中国药典》(一部)要求[1]。12批仙鹤草样品来源信息见表1。
2 方法与结果
2.1 仙鹤草药材HPLC特征图谱测定方法的建立
2.1.1 色谱条件 色谱柱:Eclipse XDB-C18(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.1%磷酸水溶液(B),梯度洗脱(0~30 min,13%A;30~65 min,13%A→22%A;65~80 min,22%A→30%A;80~100 min,30%A);流速:1.0 mL/min;柱温:30 ℃;检测波长:254 nm;进样量:10 μL。
2.1.2 溶液的制备 ①混合对照品溶液:分别称取鞣花酸、槲皮苷、芹菜素、山柰酚对照品适量,精密称定,加甲醇制成每1 mL分别含鞣花酸10.72 μg、槲皮苷70.65 μg、芹菜素6.96 μg、山柰酚4.18 μg的混合对照品溶液,用0.22 μm微孔滤膜滤过,取续滤液,即得。②供试品溶液:取仙鹤草药材粉末(过三号筛,下同)1.0 g,精密称定,置于具塞锥形瓶中,精密加入50%乙醇25 mL,密塞,称定质量,加热回流45 min,取出,放冷,再次称定质量,用50%乙醇补足减失的质量,用0.22 μm微孔滤膜滤过,取续滤液,即得。
2.1.3 精密度试验 取仙鹤草药材(编号:S14)粉末适量,按“2.1.2②”项下方法制备供试品溶液,再按“2.1.1”项下色谱条件连续进样6 次测定,结果得12个特征峰。以峰面积较大、分离度较好的6号色谱峰作为参照峰(S)进行计算,其余11个特征峰相对保留时间的RSD均小于1.0%(n=6)、相对峰面积的RSD均小于2.0%(n=6),表明方法精密度良好。
2.1.4 重复性试验 取同一批仙鹤草药材(编号:S14)粉末适量,共6份,按“2.1.2②”项下方法平行制备供试品溶液,再按“2.1.1”项下色谱条件进样测定。以6号色谱峰作为参照峰(S)进行计算,其余11个特征峰相对保留时间的RSD均小于1.0%(n=6)、相对峰面积的RSD 均小于2.0%(n=6),表明方法重复性较好。
2.1.5 稳定性试验 取仙鹤草药材(编号:S14)粉末适量,按“2.1.2②”项下方法制备供试品溶液,再按“2.1.1”项下色谱条件分别于室温下放置0、2、4、8、12、24 h时进样测定。以6 号色谱峰作为参照峰(S)进行计算,其余11个特征峰相对保留时间的RSD均小于1.0%(n=6)、相对峰面积的RSD均小于2.0%(n=6),表明供试品溶液在室温下放置24 h内稳定性良好。
2.2 仙鹤草浸出物提取工艺的建立
2.2.1 仙鹤草浸出物的提取条件 取仙鹤草药材(编号:S14)粉末(过三号筛,下同)约4 g,共24份,精密称定,置于250 mL锥形瓶中,分别按2015年版《中国药典》(四部)通则“2201冷浸法和热浸法”[16],均分别以水、50%乙醇、75%乙醇、95%乙醇各100 mL为溶剂进行提取(不同提取方法、溶剂条件均平行3份样品操作),用干燥滤器迅速滤过,备用。
2.2.2 不同提取方法和溶剂对仙鹤草浸出物含量的影响 精密量取“2.2.1”项下所得样品滤液25 mL,分别置于已干燥至恒质量的蒸发皿中,水浴蒸干,再于105 ℃干燥3 h后置于干燥器中冷却30 min,迅速精密称定质量,以干燥品计算仙鹤草浸出物含量[浸出物含量(%)=(干燥品质量×稀释体积)/(取样质量×取样体积)×100%],结果见表2。如表2所示,以不同溶剂采用热浸法提取后所测得的仙鹤草浸出物含量均高于以相应溶剂采用冷浸法提取所得的浸出物含量,且相同提取方法、不同溶剂所得浸出物的含量排序均为50%乙醇>75%乙醇>水>95%乙醇。
2.2.3 不同提取方法和溶剂对仙鹤草浸出物特征图谱总峰面积的影响 取“2.2.1”项下仙鹤草浸出物滤液适量,以0.22 μm微孔滤膜滤过,取续滤液,按“2.1.1”项下色谱条件进样测定,记录峰面积。采用Origin 2018软件绘制其HPLC叠加特征图谱,详见图1;浸出物特征峰总峰面积见表3。如图1、表3所示,在不同体积分数乙醇提取条件下,冷浸法和热浸法所得仙鹤草浸出物的主要色谱峰个数均基本一致;以水为提取溶剂时,所得部分浸出物的色谱峰无法检出,且特征峰总峰面积存在较大差异;此外,不同溶剂热浸法较之于相应溶剂冷浸法提取所得浸出物的特征峰总峰面积更高,且相同提取方法、不同溶剂提取所得浸出物的特征峰总峰面积排序均为50%乙醇>75%乙醇>95%乙醇>水。
2.2.4 仙鹤草浸出物提取工艺优化 以浸出物的含量、浸出物特征峰总峰面积再结合过滤速度(即浸出物提取液用干燥滤器滤过的快慢)为评价指标,采用综合加权评分法进行仙鹤草浸出物提取工艺评价。分别计算浸出物含量、特征峰总峰面积、过滤速度的得分(某指标得分=该指标测定值/该指标最大值×100),并拟定浸出物含量、特征峰总峰面积、过滤速度的权重分别为0.4、0.4、0.2,计算综合评分(综合评分=浸出物含量/浸出物含量最大值×40+特征峰总峰面积/特征峰总峰面积最大值×40+过滤速度/过滤速度最大值×20),结果见表4。如表4所示,热浸法所得综合评分总体高于冷浸法,表明热浸法用于提取仙鹤草浸出物的效果更优。选择综合评分最高(94.0分)的工艺为仙鹤草浸出物的最优提取工艺,即以50%乙醇为溶剂、采用热浸法提取。
2.3 仙鹤草药材HPLC特征图谱的建立
2.3.1 HPLC特征图谱的生成 取15批仙鹤草药材粉末,按“2.1.2②”项下方法制备供试品溶液,再按“2.1.1”项下色谱条件进样测定,记录色谱图,使用《中药色谱指纹图谱相似度评价软件(2012版)》进行共有峰匹配。以编号为S1的仙鹤草药材的色谱图为参照图谱,将时间窗宽度设为0.1 min,采用多点校正法进行色谱峰匹配,选择中位数法生成对照图谱(R)。15批仙鹤草药材的HPLC叠加特征图谱见图2,对照图谱(R)见图3A。
2.3.2 相似度评价 采用《中药色谱指纹图谱相似度评价系统(2012 版)》,以仙鹤草药材对照图谱为参照进行15批样品的整体相似度评价。结果显示,15批仙鹤草(编号:S1~S15)的相似度依次为0.965、0.993、0.992、0.993、0.990、0.994、0.977、0.946、0.954、0.966、0.985、0.995、0.926、0.984、0.964,均大于0.92,且与对照图谱具有较好的一致性,表明药材批间差異较小、质量稳定性较好。
2.3.3 特征峰的指认 15批仙鹤草药材样品共有12个共有特征峰,取“2.1.2①”项下混合对照品溶液,按“2.1.1”项下色谱条件进样测定,记录色谱图。通过与此对照品图谱比对,指认了仙鹤草对照图谱(R)中的2号峰为鞣花酸、6号峰为槲皮苷、11号峰为芹菜素、12号峰为山柰酚。混合对照品溶液色谱图见图3B。
2.4 15批仙鹤草浸出物含量和药材特征图谱总峰面积的测定和两者相关性分析
2.4.1 15批仙鹤草浸出物含量和药材特征图谱总峰面积的测定 取15批不同产地仙鹤草药材,采用“2.2.4”项下所得最佳提取工艺(50%乙醇、热浸法)提取,并按“2.2.2”项下方法测定并计算浸出物含量;同时,取上述不同产地仙鹤草药材,按“2.3”项下方法检测,获得特征图谱总峰面积,结果见表5。
采用SPSS 25.0软件对不同产地的15批仙鹤草的浸出物含量、药材特征图谱总峰面积进行单因素方差分析,P<0.05为差异有统计学意义。对不同产地仙鹤草样品(每个地区各3批)的测定结果取平均值后显示,其浸出物平均含量、药材平均特征总峰面积均有显著差异:安徽、江苏产仙鹤草的浸出物平均含量、药材特征图谱平均总峰面积均显著高于四川产仙鹤草,差异均有统计学意义(P<0.05或P<0.01);安徽产药材特征图谱平均总峰面积也显著高于浙江、河南产仙鹤草,差异均有统计学意义(P<0.05或P<0.01)。不同产地的仙鹤草浸出物平均含量排序为:安徽>江苏>浙江≈河南>四川;药材特征图谱平均总峰面积排序为:安徽>江苏≈浙江>河南>四川。综上,以安徽产仙鹤草药材质量整体较优,详见图4。
2.4.2 相关性分析 采用SPSS 25.0软件对15批仙鹤草浸出物含量、药材特征峰总峰面积进行Pearson相关性分析。结果显示,浸出物含量与药材特征峰总峰面积呈显著相关(P<0.01)。以浸出物含量为横坐标(X,%)、药材特征图谱总峰面积为纵坐标(Y),采用Prism 8.01软件绘制线性曲线(见图5),并求得线性关系方程:Y=13 159X-81 273(r=0.86)。结果表明,仙鹤草浸出物含量与药材特征图谱总峰面积呈正相关。
2.5 熵权TOPSIS法综合评价仙鹤草药材质量
采用熵权TOPSIS法[18-20]综合评价仙鹤草药材质量。15批仙鹤草药材中共有12个共有特征峰(4个特征峰被指认),以其中的6号峰(槲皮苷)作为参照峰(S),计算得各特征峰的相对峰面积和相对保留时间,详见表6、表7。
将15批仙鹤草药材中的12个特征峰的峰面积和浸出物的含量数据等13个指标进行同向标准化处理:假设m个样本(m=15)有n个指标(n=13),根据以下公式(1)(2)对原始试验数据建立标准决策矩阵,后进行归一化处理,计算越大越优型指标和越小越优型指标的标化值(Rij)。由于本研究中13个指标均为越大越优型指标,故采用公式(1)计算:
Rij=[Xij-min(X1j,X2j,…,Xmj)
max(X1j,X2j,…,Xmj)-min(X1j,X2j,…,Xmj)] … (1)
Rij=[max(X1j,X2j,…,Xmj)-Xij
max(X1j,X2j,…,Xmj)-min(X1j,X2j,…,Xmj)] … (2)
利用熵权法评价指标的熵值(Eij),来反映样品数据的离散程度并体现评价指标的重要性,并计算得出1~12号特征峰的峰面积和浸出物含量这13个指标的权重(Wj)=(0.124,0.095,0.052,0.081,0.054,0.068,0.084,0.059,0.033,0.056,0.097,0.134,0.062)。熵值(Ej)和权重(Wj)按公式(3)(4)计算:
Ej=-k[∑][i=1][m]RijlnRij…(3)
Wj=[1-Ej
[∑][j=1][n](1-Ej)] [([∑][j=1][n]Wj=1)]……………………(4)
以权重赋值标准化决策矩阵,进一步构建加权决策矩阵(Z),并确定最优向量(Z +)与最劣向量(Z-)。按公式(5)(6)(7)计算,得Z +=(0.124,0.095,0.052,0.081,0.054,0.068,0.084,0.059,0.033,0.056,0.097,0.134,0.062),Z-=(0,0,0,0,0,0,0,0,0,0,0,0,0);并按公式(8)(9)计算每个样本与Z+和Z-的距离(Di+、Di-)及最优方案的的贴近度(Ci),其中Ci取值为0~1,越接近1表示评价样本越接近最优水平,越接近0则越接近最劣水平,结果见表8。
如表8所示,安徽、浙江、四川、河南、江苏产仙鹤草药材质量评价中Ci均值依次为0.689、0.351、0.218、0.308、0.361(n=3),以安徽产药材的Ci均值最接近1,表明其质量最优;其次为江苏、浙江产药材,再次为河南产药材,而四川产地药材质量相对较差。其中,安徽产的3批药材Ci值排前3位,表明该产地的仙鹤草药材整体质量更优,可作为优良种质资源进一步研究与开发。
3 讨论
浸出物的测定是用于鉴别、检查中药及其饮片质量的重要方法之一。由于中药成分复杂,部分中药中有效成分尚不明确,故以浸出物作为质量评价的指标之一,对于中药质量标准的建立具有重要意义。2015年版《中国药典》(一部)未对仙鹤草浸出物含量进行规定,因此本研究采用不同提取方法和提取溶剂,优选仙鹤草浸出物最佳提取工艺并进行含量测定。
中药特征图谱现已被广泛应用于整体反映中药成分复杂性的研究中,可对某些特征成分进行指认及分析,是中药的有效质量控制与评价方法。因此,本研究在测定仙鹤草浸出物含量的基础上,同时建立了仙鹤草药材的特征图谱,共得到12个特征峰,并指认了鞣花酸、槲皮苷、芹菜素、山柰酚等4个化合物。近年來,越来越多研究发现,鞣花酸可抑制乳腺癌细胞的增殖、迁移和侵袭[21];山柰酚、槲皮苷能有效降低糖尿病模型小鼠的血糖水平[22],也是治疗结肠癌的潜在活性成分[23];槲皮苷及其衍生物也可用于阿尔茨海默病的治疗[10];芹菜素具有舒张动脉血管、降血压、抗炎、杀菌等多种药理活性[24-26]。所以,本研究以特征图谱对不同产地的仙鹤草药材进行的测定分析,可为仙鹤草药材质量差异所引起的药理、药效研究提供一定的数据支撑。
本研究测定了15批不同产地仙鹤草浸出物含量和药材特征图谱总峰面积。结果显示,不同产地浸出物含量均值排序为:安徽>江苏>浙江≈河南>四川;不同产地特征峰总峰面积均值排序为:安徽>江苏≈浙江>河南>四川。同时发现,浸出物含量和药材特征图谱总峰面积具有一定的正相关性,即浸出物含量越高,相应批次药材的特征峰总峰面积越大。但仅从浸出物含量或特征峰的峰面积分析仙鹤草药材质量较单一,故本研究进一步以浸出物含量和药材特征图谱峰面积为指标,采用熵权TOPSIS法建立整体质量评价模型,对15批仙鹤草药材进行质量评价。结果显示,5个产地样品的Ci均值排序为:安徽>江苏≈浙江>河南>四川,3批安徽产样品(S1~S3)的Ci值排前3位。由此可见,仙鹤草浸出物含量、药材特征图谱总峰面积与熵权TOPSIS法综合评价结果基本一致,均以安徽产仙鹤草药材质量整体较高。本文采用的熵值法对各指标进行客观权重赋值,能避免主观意识对评价结果的影响,降低主观性[19];再结合TOPSIS法通过计算各指标对最优方案的贴近度,提高整体综合分析的科学性与准确性[19],可实现对不同产地仙鹤草整体质量评价以及优质种源筛选的目的。
综上所述,本研究基于浸出物和药材HPLC特征图谱,采用熵权TOPSIS法建立了仙鹤草药材整体质量评价模型,以多个测定指标对不同产地仙鹤草药材进行综合质量评价,符合中药的整体性概念;所采用的熵权TOPSIS评价法客观、可量化,能做出比较科学、全面的判断。今后有待进一步对该药材尚未指认的特征峰进行液质联用分析,以期对不同产地仙鹤草药材中化学成分进行更全面的差异分析。
参考文献
[ 1 ] 国家药典委员会.中华人民共和国药典:一部[S]. 2015年版.北京:中国医药科技出版社,2015:102-103.
[ 2 ] KATO H,LI W,KOIKE M,et al. Phenolic glucosides from Agrimonia pilosa[J]. Phtochemistry,2010,71(16):1925-1929.
[ 3 ] 路芳,巴晓雨,何永志.仙鹤草的化学成分研究[J].中草药,2012,43(5):851-855.
[ 4 ] 刘红霞,刘召喜,姜清华.仙鹤草的酚类化学成分[J].沈阳药科大学学报,2010,27(4):286-289.
[ 5 ] 潘娅,刘红霞,庄玉磊,等.仙鹤草中黄酮类化学成分研究[J].中国中药杂志,2008,33(24):2925-2927.
[ 6 ] 刘位杰,梁敬钰,孙建博,等.仙鹤草化学成分及药理作用研究进展[J].海峡药学,2016,28(2):1-7.
[ 7 ] 王希,张焜,陈优生.仙鹤草降糖活性成分的提取分离[J].中国实验方剂学杂志,2010,16(6):85-87.
[ 8 ] 田露露,包永睿,王帅,等.仙鹤草总黄酮提取纯化工艺及体外抗肝肿瘤药效研究[J].中药材,2019,42(2):380- 384.
[ 9 ] 丛慧源,王颖,邓雁如. 2种近缘中药翻白草和仙鹤草的化学成分和降血糖活性比较[J].中草药,2015,46(16):2484-2491.
[10] HE CH,JI XW,PAN YM,et al. Antioxidant activity of alcoholic extract of Agrimonia pilosa Ledeb[J]. Med Chem Res,2010,19(5):448-461.
[11] 程艳刚,谭金燕,叶文冲,等.基于Plackett-Burman设计和Box-Behnken响应面法优化仙鹤草总黄酮超声提取工艺及其抗氧化抗肿瘤活性研究[J].中华中医药学刊,2018,36(10):2414-2419.
[12] 蔡田恬,赵敏,王建平.仙鹤草水提液对胰腺癌细胞 BXPC-3和PANC-1增殖的抑制作用研究[J].中国现代应用药学,2018,35(8):1208-1211.
[13] 王青,苏聪平,张惠敏,等.从炎性反应角度探讨清热解毒药的作用机制[J].中国中药杂志,2018,43(18):3787- 3794.
[14] 田露露,包永睿,王帥,等.基于人肝癌细胞HepG2的仙鹤草挥发性成分体外抗肝肿瘤活性评价研究[J].中南药学,2019,17(1):15-19.
[15] 于莉,金哲雄.仙鹤草中鞣质成分的抗氧化作用[J].黑龙江医药,2009,22(5):625-627.
[16] 国家药典委员会.中华人民共和国药典:四部[S]. 2015年版.北京:中国医药科技出版社,2015:30、202.
[17] 路东波,孔静,李思潼,等.基于有效基准特征图谱质量表征模式的中药紫苏叶质量评价研究[J].北京中医药大学学报,2020,43(2):148-162.
[18] 张亚亚,王亚丽,顾志荣,等.熵权TOPSIS法综合评价直播与移栽当归药材的质量[J].时珍国医国药,2016,27(11):2741-2743.
[19] 李运,张霁,徐福荣,等.多指标决策分析TOPSIS对三七的质量评价研究[J].中草药,2017,48(22):4764-4771.
[20] 马天翔,顾志荣,许爱霞,等.基于OPLS结合熵权TOPSIS法对不同产地锁阳的鉴别与综合质量评价[J].中草药,2020,51(12):3284-3291.
[21] 韦柳霞,何美玲,黄俊清,等.鞣花酸对BRCA1沉默的三阴性乳腺癌MDA-MB-231细胞生物学行为的影响及其作用机制[J].中国癌症防治杂志,2019,11(6):485-491.
[22] 张家瑞.槲皮苷和山柰酚对糖尿病小鼠血糖及血脂水平的影响[J].现代食品科技,2013,29(3):459-462.
[23] 杨云英,何莎莎,王岩,等.基于网络药理学探讨仙鹤草治疗结肠癌的作用机制[J].消化肿瘤杂志,2019,11(3):282-289.
[24] ANDUEZA A,GARCIA-GARZON A,DE GALARRETA MR,et al. Oxidation pathways underlying the pro-oxidant effects of apigenin[J]. Free Radical Bio Med,2015. DOI:10.1016/j.freeradbiomed.2015.06.003.
[25] WANG Q,ZENG P,LIU YL,et al. Inhibition of autophagy- ameliorates atherogenic inflammation by augmenting apigenin-induced macrophage apoptosis[J]. Int Immunopharmacol,2015,27(1):24-31.
[26] PAREDES MD,ROMEC?N P,ATUCHA NM,et al. Mo- derate effect of flavonoids on vascular and renal function in spontaneously hypertensive rats[J]. Nutrients,2018,10(8):1107-1118.
(收稿日期:2020-07-09 修回日期:2020-10-15)
(编辑:段思怡)
