酚酞遇酸溶液都不变色吗
2020-01-09甘肃省兰州市教育科学研究所730046吴正帅
甘肃省兰州市教育科学研究所(730046) 吴正帅
甘肃省兰州市西固区福利东路第三小学(730060) 郭红霞
1 问题的提出
在化学实验教学中,偶尔会出现异常现象,认真对待任何一个异常现象是每一位教师需要做的事情。酚酞指示剂遇酸不变色,遇碱变红色是常见的酸碱指示剂变色规律。对于酚酞遇到浓度较大的碱溶液会先变红后褪色的异常现象及机理的研究论文屡见不鲜,但有关酚酞与酸溶液混合的报道却鲜有耳闻。那么,酚酞遇到酸溶液后一定不显色吗?
2 实验探究
2.1 实验
酚酞与不同种类的酸溶液的显色实验探究。
2.1.1 实验药品以及仪器
酚酞固体、浓度为95%的乙醇、10mol/LHCl、10mol/L H2SO4、10 mol/L HNO3、10 mol/L H3PO4、1 mol/L HCl、1 mol/L H2SO4、1 mol/L HNO3、1mol/L H3PO4、浓度为20%的NaOH 溶液、蒸馏水、烧杯、玻璃棒。
2.1.2 实验步骤
取酚酞固体1g,加入95%的乙醇溶解并稀释至100mL,摇匀后得到浓度为1%的酚酞指示剂;分别取HCl、H2SO4、HNO3和H3PO410mol/L浓溶液和1mol/L稀溶液各2mL,溶液无色;向上述酸的溶液各滴加1滴酚酞指示剂,然后加水稀释,再逐渐滴加20%的NaOH 溶液直至过量,实验现象见表1。
2.2 实验结论
酚酞遇很多浓度较大的酸时均可发生不同程度的变色。
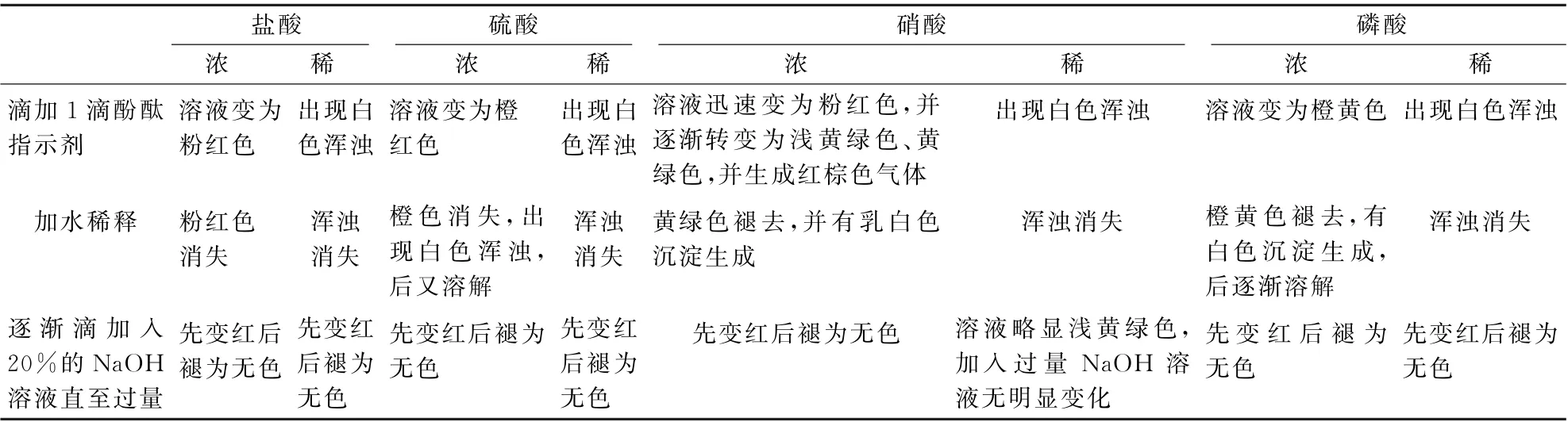
表1 不同种类酸的溶液遇到酚酞显色的实验结果
3 结论
酚酞为白色或微带黄色的细小晶体,微溶于水而易溶于酒精。实验室通常将酚酞配制成浓度为1%的酒精溶液后使用。表1中将酚酞试剂滴入稀酸水溶液会出现白色浑浊物,是由于酚酞微溶于水,使酚酞乙醇溶液中部分酚酞析出的缘故。
实验时,酚酞遇很多浓酸时均可发生不同程度的变色,其中遇浓硝酸时颜色变化非常丰富,这是由于酚酞在浓硝酸中被氧化分解,生成了难溶性硝基化合物并产生红棕色NO2气体的缘故。因此,当溶液稀释后会出现乳白色悬浊液,而继续加碱时则不再出现红色。酚酞遇到其他一些浓酸时会发生从无色结构向橙色结构的转化,但该过程是可逆的,因此继续加碱时溶液仍可显红色。各酚酞结构间的转化关系可表示为:

由于常用的酚酞指示剂一般使用乙醇溶液溶解配制,因此酚酞遇浓酸时,在强酸的催化作用下,酚酞分子中酰基和乙醇发生了酯交换反应,并再度失水使中心碳原子发生sp2杂化,与3个碳环组成共体系,使溶液呈现红色。该过程发生的化学反应如下:

为此,设计如下验证实验。在烧杯中加入0.5g酚酞固体、200mL蒸馏水,用玻璃棒充分搅拌得到酚酞悬浊液。充分静置后取清液(饱和酚酞水溶液)作指示剂,并加入到浓硫酸中发现溶液仍能显橙红色。可见,酚酞遇浓硫酸的显色机理应与浓HCl、浓H3PO4等变色机理相同,而与溶剂乙醇及浓硫酸自身的强氧化性等因素无关。如果使用酚酞的水溶液就不会出现这样的问题,即遇浓酸时不会出现显色,遇到稀的酸溶液时也不会出现白色浑浊,遇NaOH溶液则显色效果良好。实验室常选用乙醇作溶剂,但这样的酚酞指示剂在稀酸或中性溶液中易产生沉淀变浑浊的现象,在浓酸溶液中又会有不同程度的显色干扰酸碱性判断。因此,中学实验室可以尝试使用酚酞的水溶液作指示剂。
