碳酸钠催化超声波去除水样残留H2O2的动力学探究
2020-01-01曹浩然兰健马春燕刘振鸿李子真王奇义超
曹浩然,兰健,马春燕,刘振鸿,李子真,王奇,义超
(东华大学 环境科学与工程学院,上海 201600)
高级氧化法(AOPs)中强氧化剂·OH能够有效的降解有机污染物和去除某些无机污染物,所以被广泛地用来处理不同类型的污水[1]。H2O2作为自然产生的一种物质,通常在AOPs工艺中用来提供·OH,而残留的H2O2可以引起化学需氧量(COD)测定的误差[2-3]。因此,在测定AOPs废水的COD时必须去掉H2O2对COD值的影响。
本课题组前期已经对碳酸钠催化超声波分解H2O2的可行性和条件进行探究,此方法作为监测方法中的预处理方法是可行的[4]。本研究利用超声波结合催化剂碳酸钠对邻苯二甲酸氢钾模拟废水中的H2O2进行去除,更深入地探究超声波结合碳酸钠催化分解H2O2的影响条件并对H2O2分解过程进行动力学分析。
1 实验部分
1.1 试剂与仪器
重铬酸钾、1,10-菲罗啉、六水合硫酸亚铁铵、七水合硫酸亚铁、硫酸银、硫酸(ρ=1.84 g/mL)、过氧化氢(30%)、邻苯二甲酸氢钾、碳酸钠、碳酸氢钠、草酸钛钾均为分析纯。
SCOD-100标准COD消解器;UV-7504紫外可见分光光度计;IT 12A型超声波发生器(三档可调,39 kHz,功率分为75,112.5 W和150 W);赛多利斯BSA1245-CW电子天平;Titrette数字瓶口滴定器;Multi N/C3100 TOC/TN TOC测定仪。
1.2 实验方法
用邻苯二甲酸氢钾配制COD为100 mg/L的水样。取水样800 mL,投加已知浓度的H2O2溶液、碳酸钠溶液后缓慢搅拌均匀,立即取样测定H2O2浓度,同时开始进行超声处理。每隔5 min分别取10 mL和5 mL水样立即测定COD和H2O2。
COD测定采用重铬酸钾法。在10 mL水样中加入5 mL的重铬酸钾溶液后,加入15 mL硫酸-硫酸银溶液后沸腾回流2 h,以试亚铁灵为指示剂,用硫酸亚铁铵滴定水样,最终计算出消耗氧的质量浓度。
H2O2测定采用钛盐光度法[5]。在5 mL水样中分别加入5 mL的稀硫酸和草酸钛钾,反应10 min后,在最大吸收波长400 nm处,测定吸光度,根据吸光度确定H2O2的浓度。
2 结果与讨论
2.1 超声+Na2CO3去除H2O2的效果
为了探究超声和碳酸钠对H2O2的去除效果,向COD为100 mg/L的邻苯二甲酸氢钾水样中加入5 mmol/L的H2O2,探究超声功率为150 W,碳酸钠浓度为5 g/L条件下,H2O2的去除效果,H2O2的去除和COD值随时间的变化见图1。
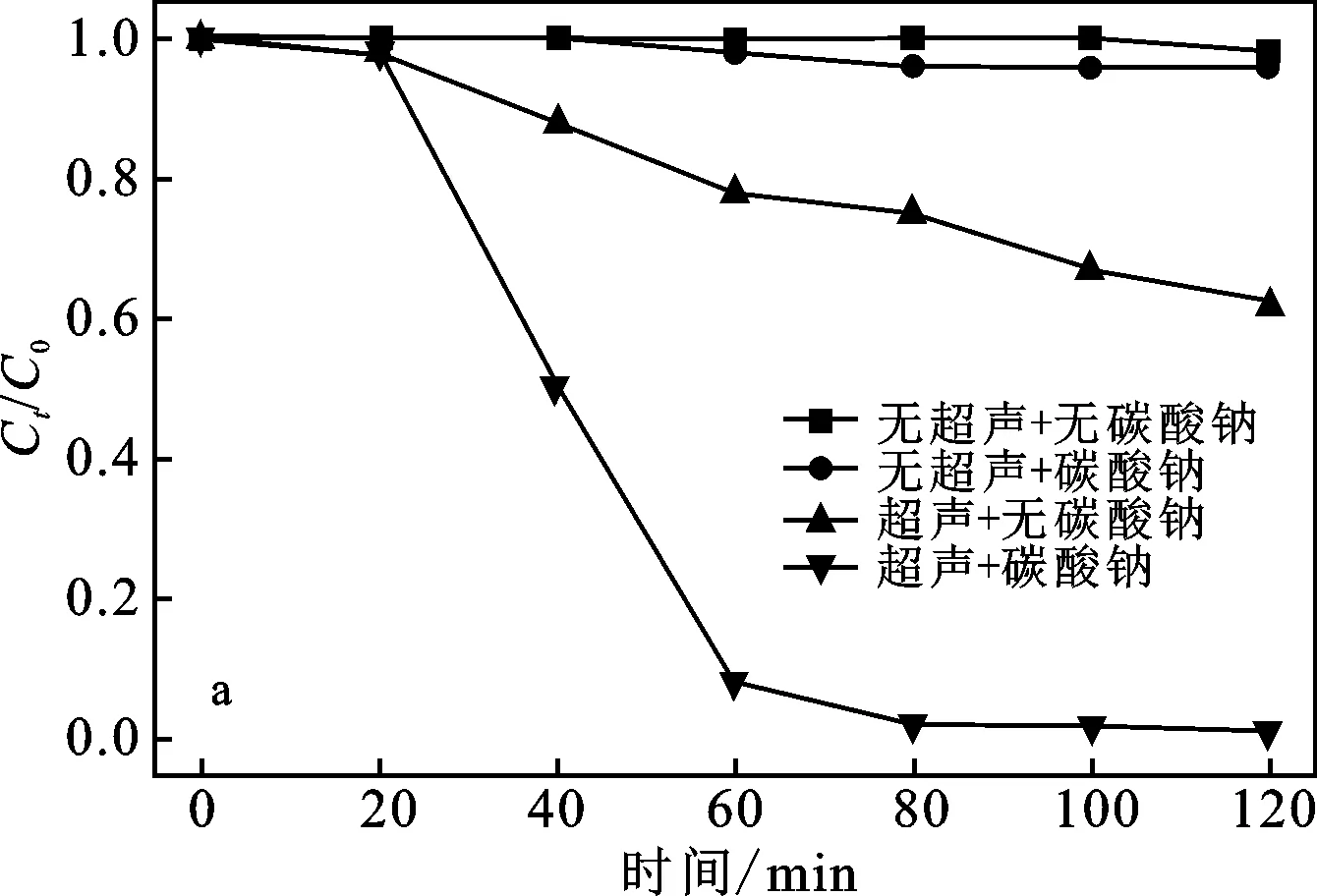

图1 超声和碳酸钠对H2O2的去除效果Fig.1 Removal of hydrogen peroxide by ultrasound and sodium carbonate a.H2O2;b.COD
由图1a可知,当没有超声时,加不加入碳酸钠对H2O2都几乎没有去除;当有超声但不加入碳酸钠时,超声2 h后仍有60%的H2O2残留,但加入碳酸钠后,在超声80 min后就可以有效去除水样中残留的H2O2。并且图1b中水样的COD值也在减小,同时实验过程中测定发现水样的TOC并没有发生改变,说明邻苯二甲酸氢钾没有被分解,COD的降低是因为溶液中的H2O2被去除。实验结果表明,在低功率超声波和碳酸钠作用下可以不降解有机物并有效分解H2O2。
超声可以分解H2O2的原因是,溶液在超声波周期性的压缩稀疏作用下有微气泡的形成、生长和突然崩塌,产生“声空化”和超临界区域,空化气泡内产生局部高温高压环境,分别可达到5 000 K和1 000 atm以上[6],这些极端的结果维持时间极短,但是会产生高活性的自由基,包括羟基(·OH)、氢基(H·)和过氧羟基(HO2·)[7-9]。当含有H2O2并超声时溶液中会发生下列反应[10-11]:
H2O→H+·OH
(1)
H2O2→2HO·
(2)
2HO·→H2O2
(3)
H2O2+·OH→H2O+HO2·
(4)
HO2·+H2O2→H2O+·OH+O2
(5)
超声可以分解H2O2,但是不加碳酸钠对H2O2的去除效果较差,原因是水样中不加入碳酸钠,H2O2的去除主要是靠与·OH和HO2·反应,虽然H2O2会分解生成·OH,但是由于·OH不稳定,存在的时间很短,很快又会相互结合生成H2O2,因此H2O2的去除效果不佳。但是超声时向溶液中加入碳酸钠,溶液可能在发生(1)~(5)反应的同时还发生了(6)~(11)反应[12-13]:
(6)
(7)
(8)
(9)
(10)
(11)

(12)
2.2 初始H2O2浓度对去除H2O2的影响
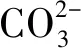
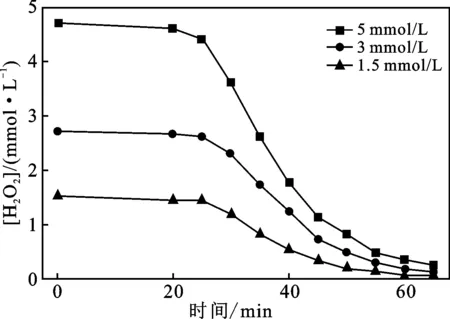
图2 H2O2浓度对H2O2去除的影响Fig.2 Effects of hydrogen peroxide concentration on removal of hydrogen peroxide
根据反应动力学的基本原理,H2O2分解反应速率方程可表示为:
(13)

(14)
为了更好的反映H2O2分解动力学关系,不考虑实验的预反应阶段,根据反应30 min后的实验数据,使用积分法求反应级数,结果见图3。
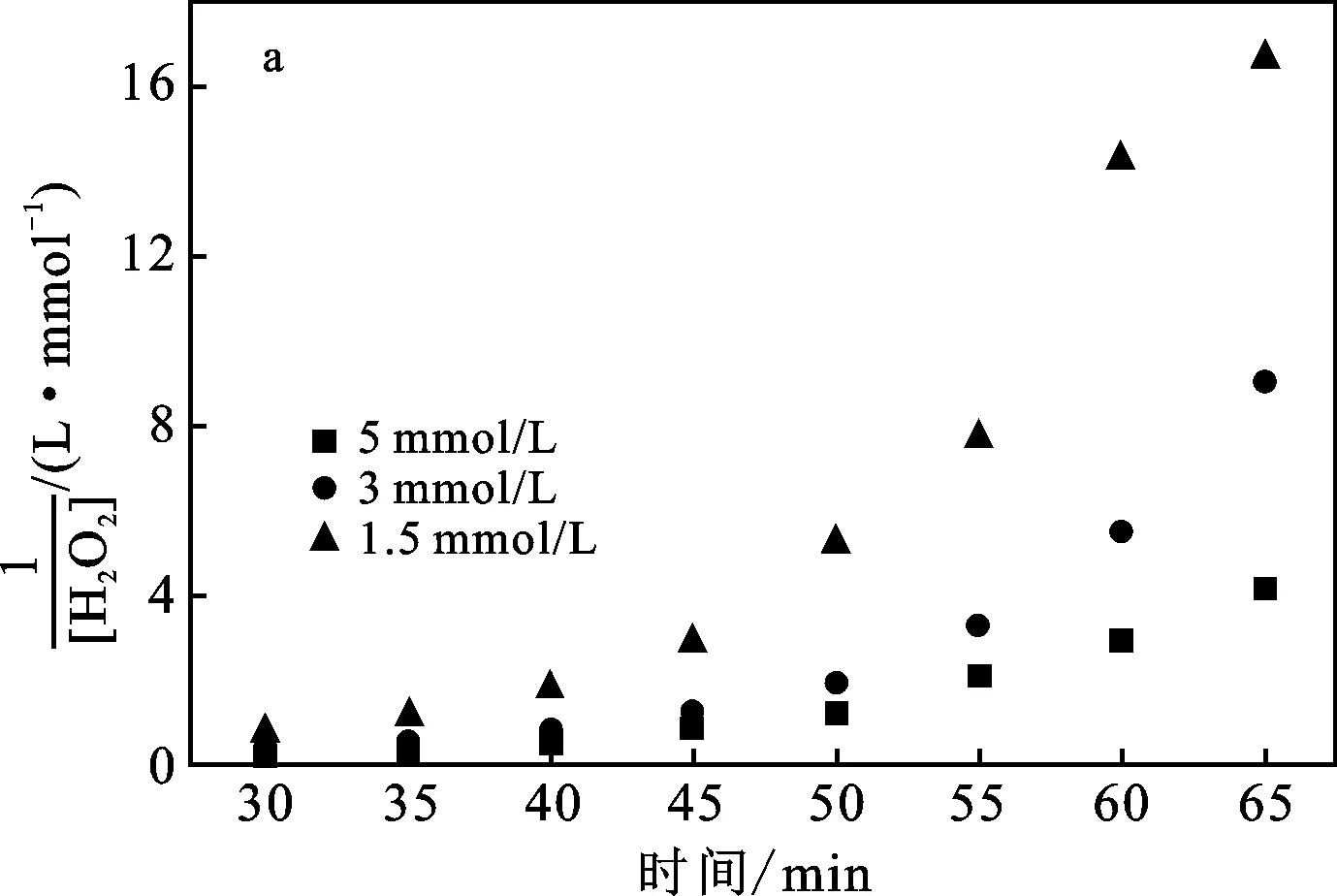
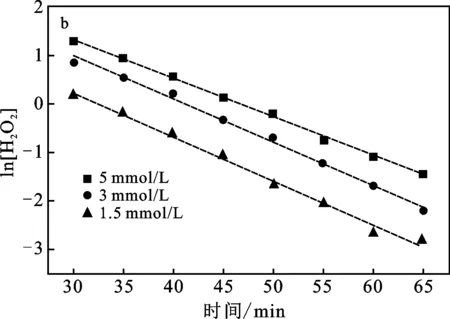
图3 反应级数拟合Fig.3 Integral method for the number of reaction stages a.1/[H2O2]与时间的关系;b.ln[H2O2]与时间的线性拟合
由图3可知,ln[H2O2]~t为直线关系,1/[H2O2]~t不为直线关系,所以该反应是一级反应。根据线性拟合得到不同初始浓度下H2O2分解的反应速率方程,见表1。

表1 不同初始浓度H2O2分解反应速率方程Table 1 The different initial concentration H2O2 decomposition reaction rate equations
由表1可知,当已知碳酸钠浓度时,H2O2的分解速率与当时存在的H2O2的量呈正比。
上述的讨论是在同一CO32-浓度下进行的,反应速率方程反映的是在一定的CO32-下H2O2的分解速率与其浓度的关系。在实验过程中测定溶液的pH并未发生改变,因此前文假设CO32-在反应过程中起到催化剂的作用,浓度不变是合理的。
2.3 Na2CO3投加量对H2O2去除的影响
根据反应动力学原理,催化剂的存在不改变反应平衡,但同时会显著改变反应速率,即碳酸钠的投加量变化时,k值出现变化。为探讨投加量对H2O2分解的影响,在此选定超声波功率为(150 W)和H2O2浓度(5 mmol/L),分析k值的变化规律,结果见图4。
由图4可知,随着初始投加量的增大,H2O2分解的速率增大,表明碳酸钠的增加会加剧H2O2的分解。但当碳酸钠的投加量>5 g/L时,H2O2催化分解的速率几乎不发生变化,说明碳酸钠催化H2O2分解的效果达到一个饱和点。将ln[H2O2]~t线性拟合,得到不同碳酸钠投加量下H2O2分解的速率常数,见表2。
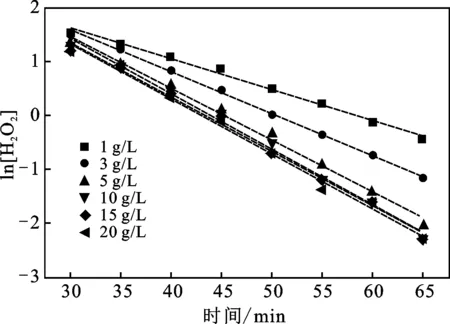
图4 不同Na2CO3投加量对超声去除H2O2的影响Fig.4 Effects of different concentrations of Na2CO3 on ultrasonic removal of hydrogen peroxide

表2 不同碳酸钠投加量下的-k值Table 2 -k values under different sodium carbonate dosage
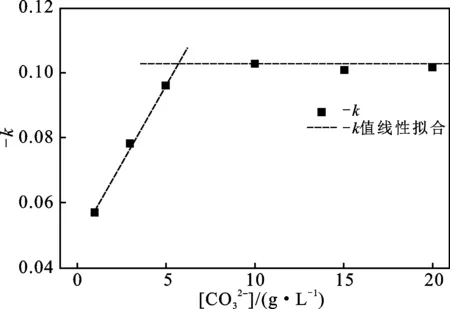
图5 -k与之间的关系Fig.5 Relationship between-k
由图5可知,-k值先随碳酸钠投加量的增加呈直线变化,随后随着碳酸钠浓度的增大,-k值保持恒定。
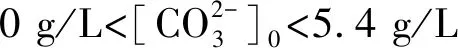
(15)
(16)
3 结论
(1)超声和碳酸钠可以在不分解有机物的前提下有效去除测试COD的水样中残留的H2O2。超声是去除H2O2的必备条件,碳酸钠作为催化剂可以提高超声分解H2O2的速率。
(2)H2O2初始浓度和碳酸钠投加量都会影响H2O2去除的速率,并且H2O2分解速率符合一级反应动力学方程。碳酸钠的投加量有一个饱和点5.4 g/L,在一定的超声条件和H2O2的初始浓度下,投加量不高于5.4 g/L时,随着投加量的增加,H2O2分解速率增加;当碳酸钠的投加量高于5.4 g/L时,H2O2分解速率不随投加量的增加而增加。
(3)相同的条件下,不同的超声波功率也会导致H2O2分解速率的不同。因此,超声波的作用对H2O2分解的影响是今后研究的方向之一。
