内括约肌切除术在低位直肠癌保肛中的应用
2020-01-01刘佳文汤东王道荣
刘佳文 汤东 王道荣
结直肠癌在全球癌症中的发病率高居第三位,而在中国,直肠癌又以低位多见,占全部直肠癌的65%至70%[1]。低位直肠癌暂无统一定义,一般认为肿瘤下缘距离肛缘小于5 cm 的为低位直肠癌[2]。距离肛缘5 cm 以内的直肠癌过去常规行腹会阴联合切除术(abdomino perineal resection, APR),不仅手术创伤大,还使患者承受永久性造口的痛苦。目前选择性地对低位直肠癌的患者行内括约肌切除术(intersphincteric resection,ISR),既可以取得较好的根治效果,又能保留一定的肛门功能,提高患者术后的生活质量。
一、ISR 的提出及其适应证、禁忌证
ISR 手术起初由Parks 提出用于需行全结直肠切除的炎性肠病患者,该术仅切除至直肠内括约肌,保留外括约肌及其周围组织,从而避免了巨大的手术创伤致会阴部切口的愈合困难[3]。1992 年,Braun 等[4]将ISR 手术应用于距肛5 cm 以下的低位直肠癌的保肛治疗中,为低位直肠癌患者提供了更多保肛的可能。根据文献报道,ISR 自开展以来,局部复发率从0%至22.7%、5 年总生存率从79%至97%不等[5],其生存和功能的预后结果是可接受的,但ISR 毕竟是低位直肠癌保肛的极端术式,需对患者进行充分的术前评估以选择符合指征的患者。
目前推荐ISR 的主要适应证有:①肿瘤下缘距离肛缘2 cm~5 cm;②病理确诊为癌,且组织学分级为中高级分化;③经影像学分期评估为早期(cT1-T2 期);④部分cT3 期直肠癌,在接受新辅助放化疗后能降期至cT1-T2 期者; ⑤肛门括约肌紧张度尚可,肛门功能良好者。
ISR 的主要禁忌证有:①病理结果提示肿瘤高度恶性或组织分化为低分化或未分化癌;②cT3 期直肠癌经新辅助放化疗后未能实现降期;③晚期直肠癌(T4 期或已有远处脏器转移);④肛门功能较差者。
目前直肠癌的临床分期主要依靠MRI 及直肠超声内镜。在手术前,有必要充分评估肿瘤下缘与肛缘之间的距离,TNM 分期,CRM(环周切缘)及周围血管是否被侵犯。由于低位直肠解剖上的特殊,如无腹膜覆盖等,其临床分期与中高位直肠癌有所不同。位于肛直肠环上方的低位直肠癌,T 分期与腹膜返折下的中位直肠癌相同。而外科肛管的直肠癌T 分期则为:T1 期指肿瘤侵犯黏膜或黏膜下层;T2 期指肿瘤仅侵犯内括约肌;T3 期指肿瘤侵犯联合纵肌;T4 期指侵犯外括约肌和/或肛提肌。
二、ISR 的临床研究进展
ISR 手术既往多采用开放经腹联合经肛路径,近年来,随着腹腔镜甚至机器人手术的应用、新辅助放化疗的开展、吻合器等手术器械的不断更新,ISR 在低位直肠癌的保肛治疗中有了越来越大的“发挥空间”。腹腔镜在直肠癌手术中充分发挥了其视野的优势,术者可在狭小的盆底空间中游离层次更为精准,向下分离的平面往往较传统开腹手术更低,甚至可在腔镜下完成内外括约肌间隙的分离,并能更好地识别、保护自主神经丛。目前的研究表明,腹腔镜ISR 手术的安全性及其预后是可接受的[6-7]。Saito 等[8]分析了228 例腹腔镜ISR 手术的病例,其5 年生存率为91.9%,5年无病生存率为83.2%,而5年局部复发率为6.7%,没有发现吻合口复发的患者。Chi 等[9]分析了137 名接受ISR 手术的低位直肠癌患者,开腹组与腹腔镜组的局部复发率,3 年无病生存率,术后肛门功能Wexner 评分无显著差异;腹腔镜手术组术中出血量较少,术后平均住院时间较短。
(一)ISR 手术的分型
根据内括约肌切除的范围可分为(图1A):①部分内括约肌切除术(partial-ISR),即在齿状线附近切除上1/3内括约肌;②次全内括约肌切除术(subtotal-ISR),即在齿 状线与白线之间切除中上2/3 内括约肌;③完全内括约肌切 除术(total-ISR),即经括约肌间沟完全切除内括约肌。
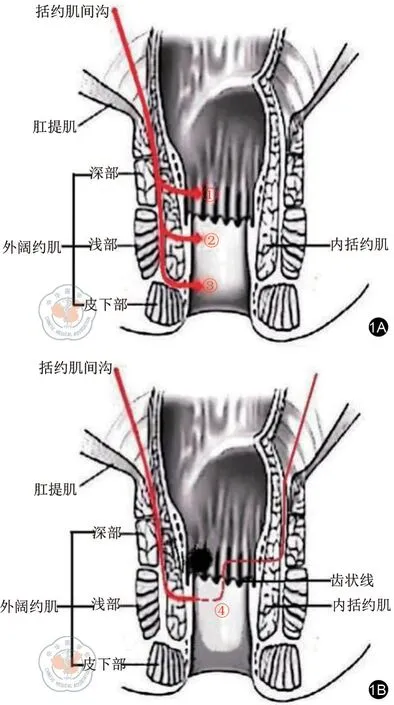
图1 ISR 手术分型。1A:①部分ISR;②次全ISR; ③完全ISR;1B:④保留部分齿状线的改良ISR
根据Rullier 等[10]提出的低位直肠癌Bordeaux 分型 (图2),分别为:I 型 肛管上型,指肿瘤距肛直肠环上缘 >1 cm,可行直肠前切除术;Ⅱ型 近肛管型,指肿瘤距肛直肠环上缘≤1 cm,可行部分ISR;Ⅲ型 肛管内型,指肿瘤下缘位于外科肛管内、仅浸润内括约肌,可行完全ISR;Ⅳ型 经肛管型,指肿瘤侵犯外括约肌和(或)肛提肌,多须行APR[11]。
内括约肌切除的范围被认为是影响术后肛门功能的主要因素,为进一步改善术后肛门功能,王振军等[12]和 Han 等[13]在部分ISR 手术的基础上提出了改良的方法 (图1B)。即如果肿瘤较早期,侵犯环周肠壁较少,保证肿瘤一侧肠管的安全切缘后,可于对侧的齿状线上缘离断直肠,在切缘术中快速病理阴性条件下适当保留部分齿状线。他们研究结果也提示经改良的部分ISR 手术明显改善患者术后短期内的肛门功能,但该术式尚缺乏大宗数据证实其安全可行。
(二)ISR 入路
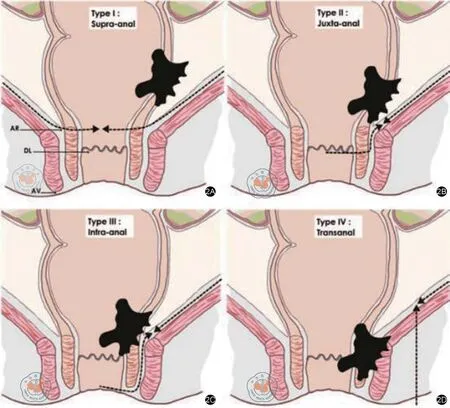
图2 低位直肠癌Bordeaux 分型[14]。2A:Type I:肛管上型;2B:Type Ⅱ:近肛管型;2C:Type Ⅲ:肛管内 型;2D:Type Ⅳ:经肛管型。AR 表示肛直肠环;DL 表示齿状线;AV 表示肛缘
1. 经腹经肛联合入路:开腹或腹腔镜下完成直肠及系膜游离(严格遵循TME 原则),直肠游离尽可能低至盆底水平并完成预防性肠造口。然后再经肛门,在直视下,于肿瘤远端1 cm~2 cm 处切开直肠黏膜及内括约肌,进入内外括约肌间隙,沿此间隙向上游离直至与腹腔组会师。最后经肛门或腹部切口离断标本,并经肛门直视下间断缝合结肠-肛管。
2. 完全经腹入路:在腹腔镜下,按TME 原则将直肠及其系膜游离至盆底平面(为保证吻合口无张力,多数情况需充分游离脾区结肠),继续向下游离开内外括约肌间隙,拥有足够的切缘后,可在腔镜下离断直肠,移除标本后采用器械吻合;若无法保证安全切缘,可在腹腔镜下完成括约肌间的分离后,经肛门于癌肿远端安全切缘处离断直肠,并行手工的结肠-肛管吻合。此法由池畔等[15]报道,其最为显著的优点即经腹入路括约肌间分离较传统ISR 手术更省时省力,并且在进一步的研究中显示该法有较满意的中期疗效[9]。
(三)ISR 手术的消化道重建
传统的ISR 手术强调在直视下手工吻合结肠-肛管,经肛门手工缝合技术费时费力,且术后易出现出血、感染、吻合口漏、吻合口狭窄等并发症。随着腹腔镜与吻合器的发展,近年来国内外也报道了ISR 手术中行器械吻合的研究,与手工缝合比较,运用吻合器行结肠-肛管吻合技术安全、简单,且未增加术后并发症[9]。
双吻合器吻合技术已经成为腹腔镜直肠癌手术中被推荐使用的消化道重建技术[16]。经腹入路,当直肠及系膜尽可能游离至齿状线水平后,再次行直肠指检,明确肿瘤下缘位置。若肿瘤下缘距离齿状线≥2 cm,则可在盆腔内以直线切割闭合器离断闭合远端直肠,再用圆形吻合器行结肠-肛管吻合。研究认为位于齿状线上方0.45 cm 处的直肠肛管移行上皮区(anal transitional zone,ATZ)可触发排便反射,为尽可能地保留ATZ,可选择25 mm 的圆形吻合器进行吻合[17]。吻合时需要注意保护周边组织,如耻骨直肠肌及阴道壁等,避免将其卷入吻合器中。
如肿瘤下缘距离齿状线小于2 cm,可选择在其近端离断乙状结肠,将直肠经肛门外翻后直视下闭合离断,残端还纳行器械吻合。或是经肛门入路离断肠管,拖出移除肿瘤后,手工缝合结肠-肛管。该吻合方式发生吻合口漏的风险较大,需行预防性造瘘。黄平[18]结合改良Bacon 术的方法,即移除肿瘤肠段后,将结肠经肛门拖出3 cm~5 cm (必要时需充分游离脾区结肠),无需缝合,待肠壁与肛管肌鞘愈合后,即可切去多余的肠段。此法无需行预防性造瘘,无吻合口漏的风险。但拖出的结肠可能发生回缩、缺血坏死,愈合处肠段易发生狭窄,术后需常规行扩肛治疗,预防吻合口狭窄。
三、ISR 手术的并发症及其预后
(一)术后并发症
ISR 术后常见的并发症有出血、感染、吻合口漏、吻合口狭窄、排便失禁等,其中以吻合口漏最为常见。根据文献报道[5,19-20]ISR 术后并发症发生率为7.5%~38.3%,吻合口漏和吻合口狭窄的发生率分别为4.5%~13%和8.4%~16%不等,对比其他的直肠癌手术,并未有明显上升。若因吻合口缺血造成吻合口漏,有时需行经腹会阴联合切除手术。 Zhang 等[21]针对腹腔镜ISR 与开放ISR 手术做了荟萃分析,研究发现腔镜组的术后并发症总发生率较开放组显著降低(P=0.01),但两组在切口感染(P=0.14),盆腔脓肿(P=0.57),吻合口漏(P=0.44),吻合口狭窄(P=0.54),尿路并发症(P=0.85)等方面差异无明显统计学意义。
关于预防性肠造口,过去认为其可降低吻合口漏的发生率。但近年来的研究表明预防性肠造口在降低吻合口漏的发生上并无帮助,不过在吻合口漏相关死亡率和再手术率上显著低于未造口组,也就是说预造口可明显降低吻合口漏的严重程度[22]。同时ISR 术后早期肛门功能往往较差,预防性肠造口可帮助患者行肛门功能的锻炼和恢复,减轻术后可能出现的排便失禁或大便次数过多的症状,一定程度上改善患者近期的生活质量[11,23]。
ISR 术后患者需定期来院复诊,特别是行预防性肠造口的患者,每月至少行一次直肠指检来评估吻合口的情况,若患者存在吻合口狭窄,医师须教会患者及家属使用医用扩肛器,每天坚持扩肛,半年内基本可解决这个问题[17]。
(二)肿瘤学预后
Akagi 等[5]的研究表明,ISR 手术的R0 切除率可达92.0%。Kim 等[24]对624 例行直肠癌低位前切除术和ISR手术的两组患者进行了回顾性分析,结果显示直肠癌低位前切除术组与ISR 组的5 年总生存率、无病生存率以及局部复发率等差异无统计学意义。另外Chi 等[9]对腹腔镜ISR 与开放ISR 手术患者进行对比分析,两组局部复发率相似(3.2%:6.1%;P=0.652),3 年无病生存率差异也无统计学意义(83.2%:83.8%;P=0.857)。一系列的研究均显示ISR 手术可以获得较好的肿瘤学预后,关键在于严格把握手术指征。直肠癌术后局部复发最重要的因素即环周切缘阳性,术中在括约肌间隙解剖的基础上,尽可能保证切缘>1 cm~2 cm,环周切缘>2 mm,可有效降低局部复发[24]。对于进展期侵犯外括约肌的肿瘤,应果断放弃ISR手术,改行APR 手术,以确保远期生存效果。
(三)肛门功能及生活质量
ISR 手术的目的即保留一定肛门功能,避免永久性造口带来的痛苦。虽然各文献评估术后肛门功能的标准有所差异(Wexner 失禁评分、Kirwan 分级以及Williams 标准等),但均表明不论是哪种ISR 手术的分型,其术后早期肛门功能均有明显受损表现,术后6~12 个月肛门功能可有不同程度的改善,以部分ISR 恢复效果最佳[25]。一项纳入1 289 名 ISR 术后患者的调查显示,51.2%的患者术后肛门功能恢复较好,每日排便次数平均约为2.7 次,29.1%的患者出现过排便急迫、污染衣物的情况,23.8%的患者无法控制排气,18.6%的患者则出现排便失禁或每日排便次数过多[26]。Koyama 等[27]分析比较了ISR 和LAR 术后的肛门功能,平均随访6 年,ISR 和LAR 的平均排便分别为每天3.7 次和3.2 次,Wexner 评分平均为8.1 分和4.9 分,两组的排便功能和生活质量差异并无统计学意义。
ISR 术后早期排便失禁,其主要因素是内括约肌切除所造成的括约肌功能不全,Pachler 等[28]发现新辅助放化疗、吻合口位置距肛缘低于2 cm 为影响ISR 术后肛门功能恢复的独立危险因素。此外,术中切除过多的内括约肌、电凝灼伤、过度扩肛等不当操作可能损伤外括约肌或其支配的神经。因而严格把握术前新辅助放化疗及手术的适应证是关键,术中谨慎操作是保证,应尽量避免损伤需保留的部分内括约肌、外括约肌、耻骨直肠肌以及盆底神经丛。
四、展望
低位直肠癌的手术治疗在根治性原则上,保留肛门功能以改善患者生活质量已然成为新时代的重要目标。内括约肌切除术应用于低位直肠癌的保肛治疗,若能合理选择患者、术前准确评估、术中精细操作、术后功能锻炼,不仅可以取得较好的根治效果,还能为患者保留较满意的肛门功能,明显地改善术后的生活质量。我们期待有更多的研究来验证其疗效,使内括约肌切除术成为低位直肠癌手术治疗的重要选择之一。
