红果樫木叶化学成分研究
2019-12-25闫慧娇陈雨洁李兵崔莉刘伟耿岩玲王晓
闫慧娇,陈雨洁,李兵,崔莉,刘伟,耿岩玲,王晓*
(1.齐鲁工业大学(山东省科学院)山东省分析测试中心 山东省中药质量控制技术重点实验室,山东 济南 250014;2.山东省食品药品审评认证中心,山东 济南 250014;3.鲁南制药集团股份有限公司,山东 临沂 276006)
樫木属 (Dysoxylum)是楝科 (Meliaceae)楝亚科的一个属,包括约75种植物,分布于中南半岛、印度、印度尼西亚、马来半岛、澳大利亚和新西兰。我国分布有15种和1个变种,主要发现于云南省、广东省、海南省、广西省和台湾省等地区[1]。樫木属许多种植物是斐济、巴布亚新几内亚及新西兰等地的传统药物,用于治疗发烧、出血、惊厥、四肢僵硬、痉挛面部变形等[2]。樫木属植物次级代谢产物丰富,国内外学者从该属植物中陆续发现了包括三萜类化合物[3-4]、Limonoids 类化合物[5]、倍半萜类化合物[6]、二萜类化合物[7]、甾体类化合物[8]和生物碱类[9]等在内的化学成分,其中一些具有较好的杀虫、生长抑制[10-11]、抑菌[12]及针对肿瘤细胞的细胞毒活性[13]。前期从红果樫木(Dysoxylumbinectariferum)中发现了新颖的活性三萜和甾体类化合物[14-15]。为了进一步系统研究红果樫木的化学成分,本文应用多种色谱方法从中分离得到3个化合物,并通过波谱学方法和化学方法,鉴定为5, 7-二羟基-2-甲基色原酮(Ⅰ)、滨蒿内酯(Ⅱ)和对羟基苯甲酸甲酯(Ⅲ)。化合物Ⅰ~Ⅲ 均首次从樫木属植物中分离得到,其结构式见图1。。

图1 化合物Ⅰ~Ⅲ 结构式
1 仪器与材料
1.1 实验仪器
Bruker AVANCE III 400 NMR型核磁共振波谱仪(德国Bruker公司,以TMS为内标);Agilent 6520型质谱仪(美国Agilent公司);Agilent 1160 型高效液相色谱仪(配有自动进样器和DAD检测器,美国Agilent 公司);Shimadzu LC-6AD型高效液相色谱仪(日本岛津公司);R201 型旋转蒸发仪(上海申生科技有限公司);FA1104 型电子天平(上海精天电子仪器厂)。
硅胶(青岛海洋化工);D101大孔树脂(沧州宝恩树脂);ODS(UniSil 30-120 C18 EC,纳微);Sephadex LH-20 (美国GE Healthcare);乙醇(分析纯,德州恒业化工有限公司);甲醇、二氯甲烷、石油醚、乙酸乙酯(分析纯,天津市化学试剂厂);甲酸、乙腈(色谱纯,山东禹王试剂有限公司)。
1.2 实验材料
红果樫木叶,2018年8月采集于云南西双版纳,并由西双版纳热带植物园张顺成老师鉴定为楝科樫木属植物红果樫木(Dysoxylumbinecteriferum),叶标本凭证(HG201808L)存放于山东省中药质量控制技术重点实验室。
2 方法与结果
2.1 提取与分离

图2 D1~D6组分TLC图
2.2 化合物纯度检测
纯度检测条件,采用Agilent 1120 型高效液相色谱仪,色谱柱为纳微 Nano-Micro C18柱(250 mm×4.6 mm,5 μm),体积流量1.0 mL/min,进样量10 μL,检测波长210 nm,以乙腈-0.1%甲酸水溶液为流动相,梯度洗脱参数为0~30 min、10%~100%乙腈。化合物Ⅰ、Ⅱ、Ⅲ高效液相色谱(high performance liquid chromatography,HPLC)及紫外吸收图见图3,检测结果表明化合物纯度均大于95%。
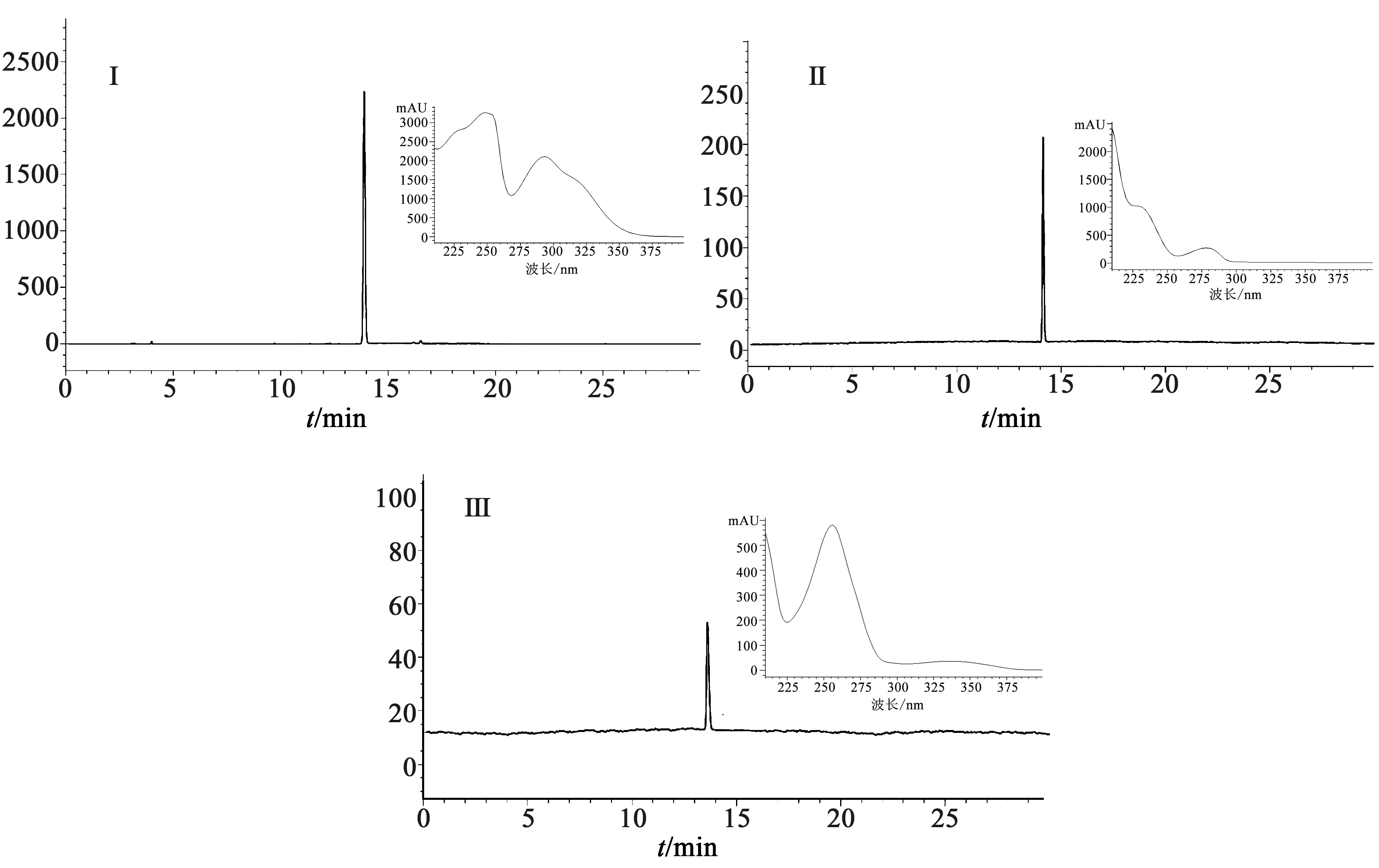
图3 单体化合物HPLC色谱图
2.3 结构鉴定
化合物1:白色固体(甲醇)。ESI-MSm/z:192 [M]+,推测其分子式为C10H8O4。1H NMR (DMSO,400 MHz):dH6.32 (1H, d,J= 1.9 Hz, H-8), 6.17 (1H, d,J= 1.9 Hz, H-6), 6.16 (1H, s, H-3), 2.34(3H, s, 2-CH3);13C NMR (DMSO, 100 MHz):dC158.27 (C-2), 108.39 (C-3), 182.18 (C-4), 103.81 (C-4a), 164.77 (C-5), 99.26 (C-6), 168.06 (C-7), 94.20 (C-8), 161.97 (C-8a),20.37 (2-CH3)。1H NMR及13C NMR数据与文献[16]报道对照基本一致。综合以上信息,鉴定化合物为5, 7-二羟基-2-甲基色原酮。
化合物2:白色粉末(甲醇)。ESI-MSm/z: 206 [M]+,推测其分子式为C11H10O4。1H NMR (DMSO, 400 MHz):dH6.30 (1H, d,J= 9.4 Hz, H-3), 7.96 (1H, d,J= 9.4 Hz, H-4), 7.26 (1H, s, H-5), 7.07(1H, s, H-8), 3.86 (OCH3), 3.81 (OCH3);13C NMR (DMSO, 100 MHz):dC161.06 (C-2), 109.42 (C-3),144.84 (C-4), 113.12 (C-5), 146.34 (C-6), 149.89 (C-7), 100.51(C-8), 153.02 (C-9), 111.66 (C-10), 56.64 (OCH3), 56.37 (OCH3)。1H NMR及13C NMR与文献[17]报道对照基本一致。综合以上信息,鉴定化合物为滨蒿内酯。
化合物3:无色结晶(甲醇)。ESI-MSm/z: 153 [M+H]+,推测其分子式为C8H8O3。1H NMR (DMSO, 400 MHz):dH7.81 (2H, d,J= 8.8 Hz, H-2, 6), 6.85 (2H, d,J= 8.8 Hz, H-3, 5);13C NMR (DMSO, 100 MHz):dC120.68 (C-1), 131.87 (C-2, 6), 115.81 (C-3, 5), 162.44 (C-4), 166.54 (C-7), 52.09(-OCH3)。1H NMR及13C NMR数据与文献[18]报道对照基本一致。综合以上信息,鉴定化合物为对羟基苯甲酸甲酯。
3 结论
樫木属植物以富含各种类型的三萜化合物为特征[3-4],本文通过对其分离,发现了色原酮类化合物5,7-二羟基-2-甲基色原酮、香豆素类化合物滨蒿内酯和苯甲酸类化合物对羟基苯甲酸甲酯,丰富了樫木属植物次级代谢产物类型。色原酮类化合物具有抗氧化、抗炎等活性[19],对羟基苯甲酸甲酯具有一定抗菌活性,滨蒿内酯具有保肝利胆、抗肿瘤等[20-21]活性,也为解释樫木属植物药用物质基础提供了一定参考。
