JS-K对人结肠癌细胞HCT116增殖及凋亡的影响*
2019-12-21范旋燕孙锦辉黄帅叶石才喻才元周宇全娟花
范旋燕,孙锦辉,黄帅,叶石才,喻才元,周宇,全娟花
(广东医科大学附属医院 消化内科,广东 湛江 524001)
结肠癌的发病率呈逐年升高趋势,当前治疗手段以手术结合化疗为主,辅以基因治疗、靶向治疗等,但随治疗时间延长及耐药细胞的出现,其疗效并不理想[1]。JS-K 作为一氧化氮前体药物通过与细胞内谷胱甘肽-S-转移酶结合并释放一氧化氮,进而调控机体多种生命活动,包括舒张血管、抗病毒及抗肿瘤等[2-4]。JS-K 对多种肿瘤细胞增殖有抑制作用,但对人结肠癌细胞HCT116 的影响尚未明确。本研究采用不同浓度JS-K 处理HCT116 细胞,观察其对细胞增殖及凋亡的影响,为临床治疗人结肠癌提供理论依据。
1 材料与方法
1.1 试剂与仪器
JS-K(西格玛奥德里奇上海贸易有限公司),胎牛血清(fetal bovine serum,FBS)(乌拉圭Lonsera 公司),100X 抗菌-抗真菌剂、0.25%胰蛋白酶(美国Gibco 公司),RPMI 1640 培养基(美国Hyclone 公司),细胞冻存液CELLBANKER 2(日本ZENOAQ 公司),Trizol、Texas Red-X 鬼笔环肽(美国Life Technology公司),实时荧光定量聚合酶链反应(quantitative realtime polymerase chain reaction,qRT-PCR) 引 物( 上海生工生物工程股份有限公司),M-MLV cDNA 合成试剂盒、酶标仪及细胞培养箱(中国赛默飞世尔科技有限公司),CellTiter 96®AQueous 单溶液细胞增殖检测试剂盒(北京普洛麦格生物技术有限公司),细胞周期检测试剂盒(上海翊圣生物科技有限公司),Annexin V-FITC/碘化丙啶(propidium iodide,PI)凋亡检测试剂盒(日本Dojindo 公司),抗荧光淬灭封片剂封片(美国Vector Laboratories 公司),倒置荧光显微镜(日本Olympus 公司),FACS Canto II 流式细胞仪(美国BD 公司)。
1.2 细胞培养
将人结肠癌细胞株HCT116(北京北纳创联生物科技有限公司)接种于10 cm 培养皿,培养体系为含10% FBS、1%抗菌-抗真菌剂(青霉素、链霉素JI 两性霉素B)的RPMI 1640 培养基,使用饱和湿度细胞培养箱于37℃、5%二氧化碳CO2环境下培养,待细胞融合度达70%~80%时,用0.25%胰蛋白酶-EDTA 消化、传代后冻存备用。
1.3 JS-K 对HCT116 细胞增殖的影响
将对数生长期的HCT116 细胞,按每孔3 000 个细胞均匀接种于96 孔板中,待细胞贴壁12 h 后,加入含有不同浓度JS-K 的培养基100μl,使培养体系JS-K 药 物浓 度 分别 为0.0、1.0、2.5、5.0、10.0 及20.0μmol/L,并分别作为0.0、1.0、2.5、5.0、10.0 及20.0μmol/L 组。各组设置5 个复孔,分别处理12、24、48 及72 h 后检测细胞增殖情况。参照MTS 说明书,于不同时间点加入20μl/孔MTS,在37℃培养箱中孵育2 h,酶标仪测定490 nm 处的吸光度,计算细胞增殖抑制率。
1.4 细胞周期检测
取对数生长期的HCT116 细胞接种于6 孔板中(3×105个/孔),培养12 h 后,用不同浓度JS-K 处理细胞48 h,用PI 单染色流式细胞术检测细胞周期收集各组上清液,贴壁细胞用0.25%胰蛋白酶消化,1 500 r/min 离心10 min,预冷磷酸盐缓冲液(phosphate buffered saline,PBS)重悬细胞,离心沉淀细胞,弃上清液,预留50μl PBS,用预冷75%乙醇于4℃固定过夜。用预冷PBS 洗涤、重悬细胞后转移至流式管,每管加入20μl RNase A Solution,37℃水浴30 min,每管加入400μl PI Staining Solution,轻轻混匀,4℃避光孵育30 min,用流式细胞仪检测。
1.5 细胞凋亡检测
参照1.4 的方法收集细胞,加入500μl 预先配好的1×Annexin V Binding Buffer 重悬细胞,使细胞浓度为1×106个/ml。取100μl 细胞悬液到流式管中,每管加入5μl FITC Annexin V 和PI 溶液,室温避光孵育15 min。补加400μl 1×Annexin V Binding Buffer,用流式细胞仪检测。
1.6 细胞形态观察
将对数生长期的HCT116 细胞接种于置有灭菌盖玻片的12 孔板(8×104个/孔),培养12 h 后,不同浓度JS-K 处理细胞48 h,弃培养基,用预冷PBS 洗涤2 次,加入免疫荧光固定液室温固定30 min。用0.1% Triton X-100 透化10 min,免疫荧光洗涤液洗2 次,滴加200μl Texas Red-X 鬼笔环肽(1 ∶100 稀释),暗盒室温放置30 min,染色细胞骨架。用10μl DAPI 抗荧光淬灭封片剂封片,在倒置荧光显微镜下观察细胞形态。
1.7 凋亡基因mRNA 表达检测
取对数生长期的HCT116 细胞接种于10 cm 培养皿(2.5×106个/皿),培养12 h,不同浓度JS-K 处理细胞48 h。用Trizol试剂提取样本总RNA,利用M-MLV试剂盒合成cDNA。设计引物并用10μl qRT-PCR 反应体系进行扩增(见表1)。以GAPDH 为内参,采用2-ΔΔCT法分析基因转录水平。
1.8 统计学方法
数据分析采用Graphpad Prism 7.0 统计软件。计量资料以均数±标准差(±s)表示,比较用单因素方差分析或重复测量设计的方差分析,进一步的两两比较用LSD-t法,P<0.05 为差异有统计学意义。

表1 Bcl-2 家族凋亡基因引物序列
2 结果
2.1 各组HCT116 细胞的生长抑制率比较
不同浓度JS-K处理HCT116 细胞12、24、48及72 h 后,检测细胞生长抑制率,采用重复测量设计的方差分析,结果如下:①不同时间点细胞生长抑制率比较,差异有统计学意义(F=364.450,P=0.000);②各组HCT16 细胞生长抑制率比较,差异有统计学意义(F=138.237,P=0.000);③各组细胞生长抑制率的变化趋势比较,差异有统计学意义(F=29.835,P=0.000)。在同一时间点,HCT116 细胞的生长抑制率随JS-K 浓度的增加而升高;在JS-K 浓度相同时,HCT116 细胞的生长抑制率随暴露时间的延长而升高,提示JS-K 对HCT116 细胞增殖的抑制作用呈剂量-时间依赖性。见表2和图1。
表2 各组HCT116 细胞生长抑制率比较 (%,±s)

表2 各组HCT116 细胞生长抑制率比较 (%,±s)
组别 12 h 24 h 48 h 72 h 0.0μmol/L 组 0.00±0.00 0.00±0.00 0.00±0.00 0.00±0.00 1.0μmol/L 组 7.19±2.20 7.86±3.96 16.49±6.87 17.17±7.03 2.5μmol/L 组 10.47±1.95 15.21±6.05 33.71±7.31 57.53±4.48 5.0μmol/L 组 12.03±2.54 19.97±4.73 49.53±7.26 68.16±5.92 10.0μmol/L 组 13.78±2.59 23.09±5.61 58.93±5.43 76.04±3.74 20.0μmol/L 组 14.96±2.15 32.43±6.47 63.26±3.69 85.03±6.08
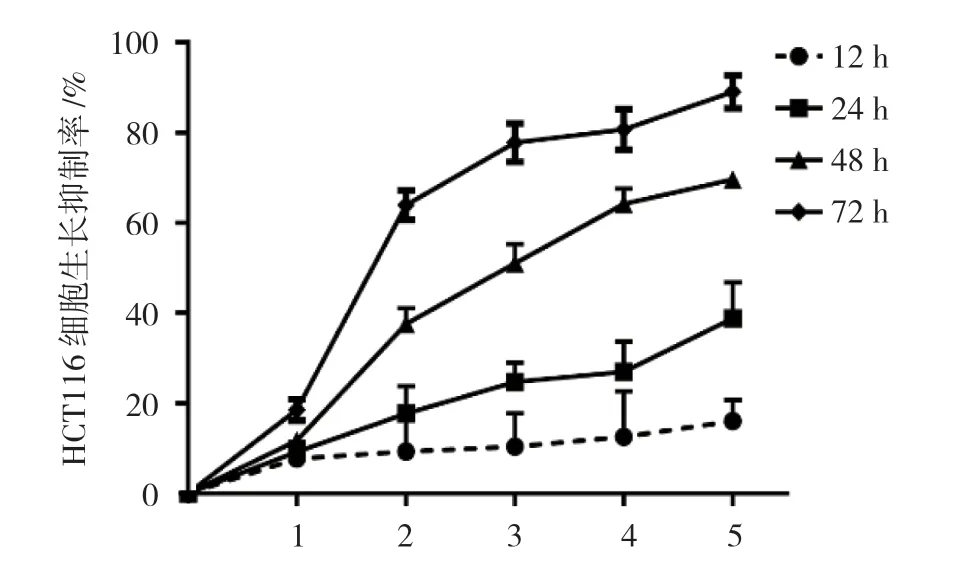
图1 各组HCT116 细胞生长抑制率的变化趋势 (±s)
2.2 不同浓度JS-K 对HCT116 细胞周期的影响
各组G0/G1 期细胞比例比较,经单因素方差分析,差异有统计学意义(P<0.05);1.0、2.5、5.0、10.0及20.0μmol/L 组G0/G1 期细胞比例较0.0μmol/L 组下降。各组G2/M 期细胞比例比较,经单因素方差分析,差异有统计学意义(P<0.05),1.0、2.5、5.0、10.0 及20.0μmol/L 组G2/M 期细胞比例较0.0μmol/L 组上升,提示JS-K可阻滞HCT116细胞G2/M 期。见表3和图2。
表3 各组G0/G1 期、G2/M 期HCT116 细胞比例比较 (%,±s)
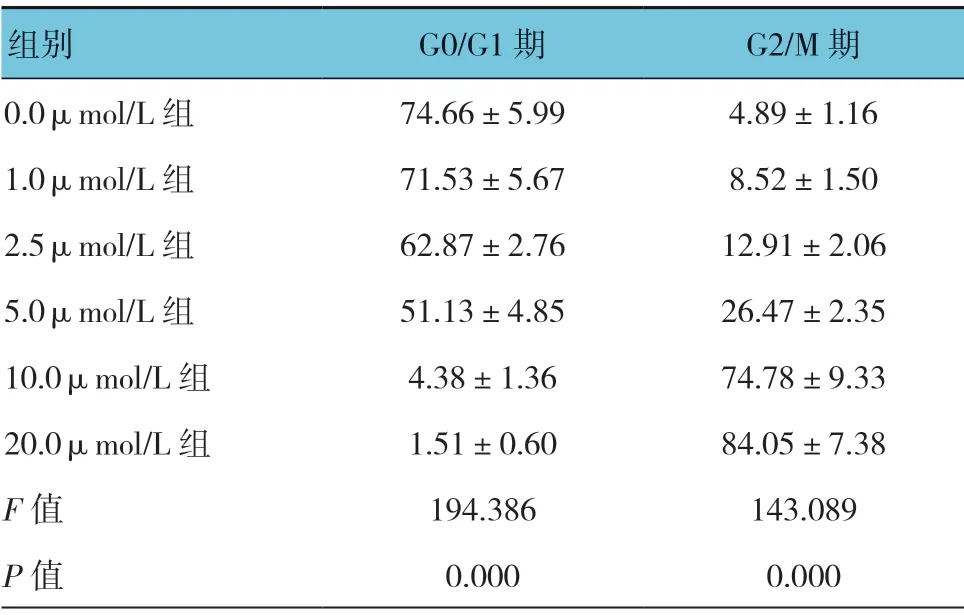
表3 各组G0/G1 期、G2/M 期HCT116 细胞比例比较 (%,±s)
组别 G0/G1 期 G2/M 期0.0μmol/L 组 74.66±5.99 4.89±1.16 1.0μmol/L 组 71.53±5.67 8.52±1.50 2.5μmol/L 组 62.87±2.76 12.91±2.06 5.0μmol/L 组 51.13±4.85 26.47±2.35 10.0μmol/L 组 4.38±1.36 74.78±9.33 20.0μmol/L 组 1.51±0.60 84.05±7.38 F 值 194.386 143.089 P 值 0.000 0.000
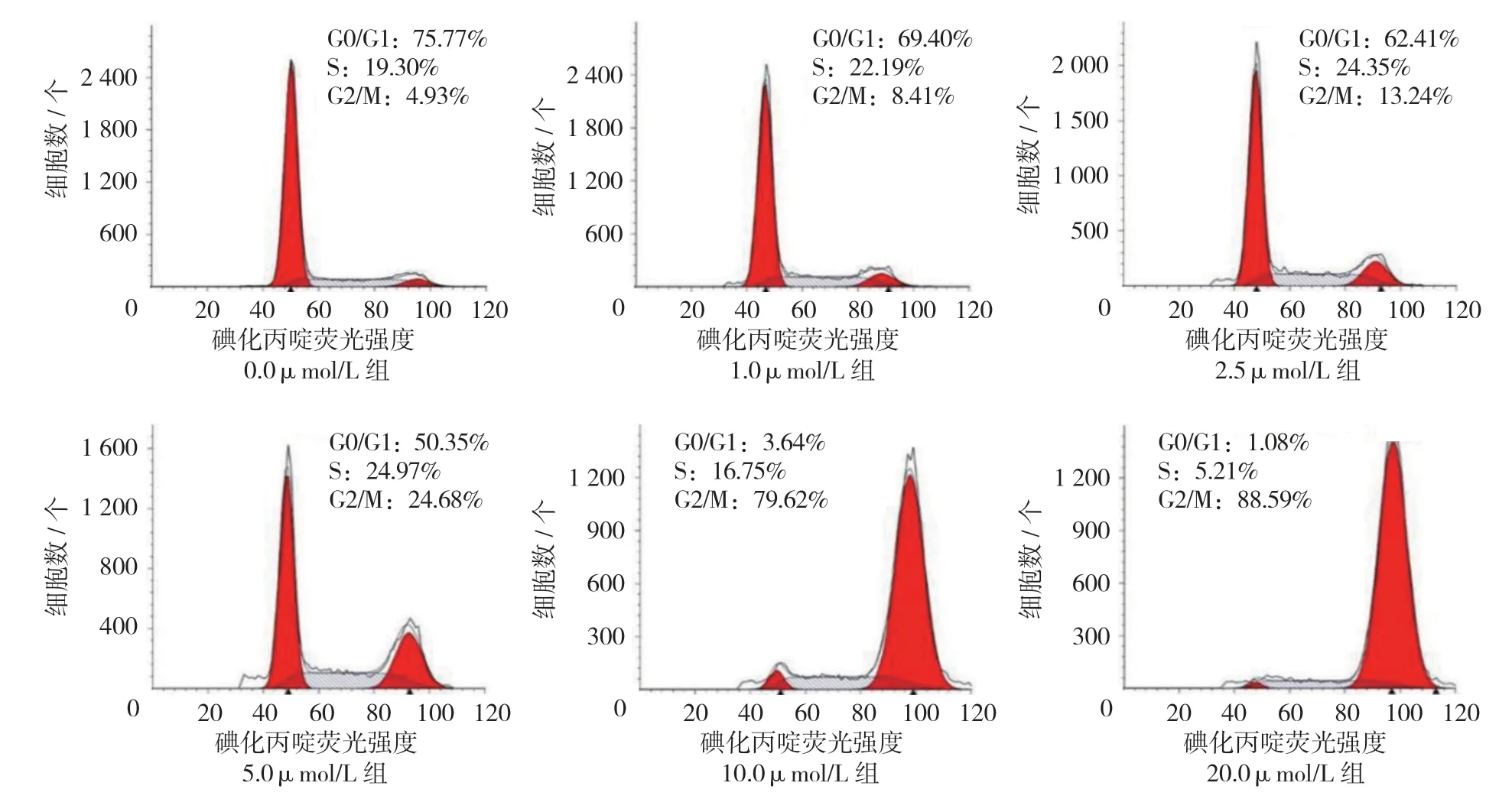
图2 JS-K 处理HCT116 细胞48 h 后周期分布
2.3 各组细胞晚期凋亡率比较
0.0、1.0、2.5、5.0、10.0 及20.0μmol/L 组 细 胞晚期凋亡率分别为(5.4±0.8)%、(28.8±3.0)%、(31.1±2.3)%、(35.2±6.1)%、(36.9±4.5)% 和(71.6±6.9)%,经单因素方差分析,差异有统计学意义(F=71.069,P=0.000)。进一步两两比较,1.0、2.5、5.0、10.0 及20.0μmol/L 组细胞晚期凋亡率逐渐递增,且均高于0.0μmol/L 组(P<0.05),提示JS-K呈浓度依赖性促进HCT116 细胞的晚期凋亡。见 图3。
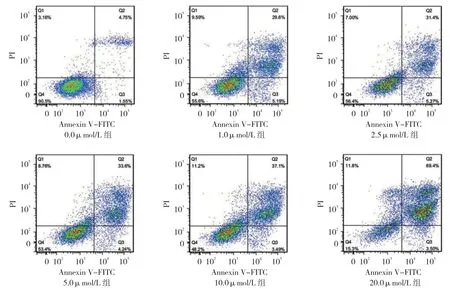
图3 细胞凋亡流式细胞图
2.4 不同浓度JS-K 对HCT116 细胞核及细胞骨架微丝结构的影响
0.0μmol/L 组细胞微丝结构分布相对均匀,相互连成网状,周围边界清晰,有少量微丝触角。JS-K 处理后,DAPI 染色呈核浓缩,核碎裂成大小不等的圆形小体;细胞骨架微丝网状结构不清晰,局部呈现溶解或者断裂现象。以上结果提示,JS-K 可诱导HCT116细胞核碎裂及改变骨架微丝结构的分布。见图4。
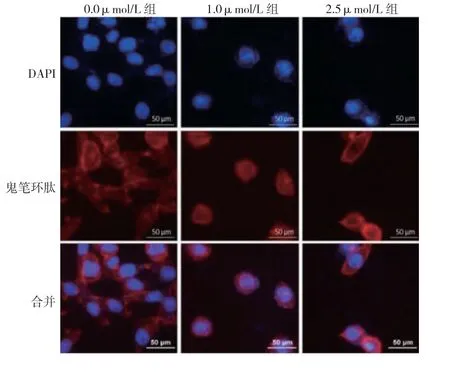
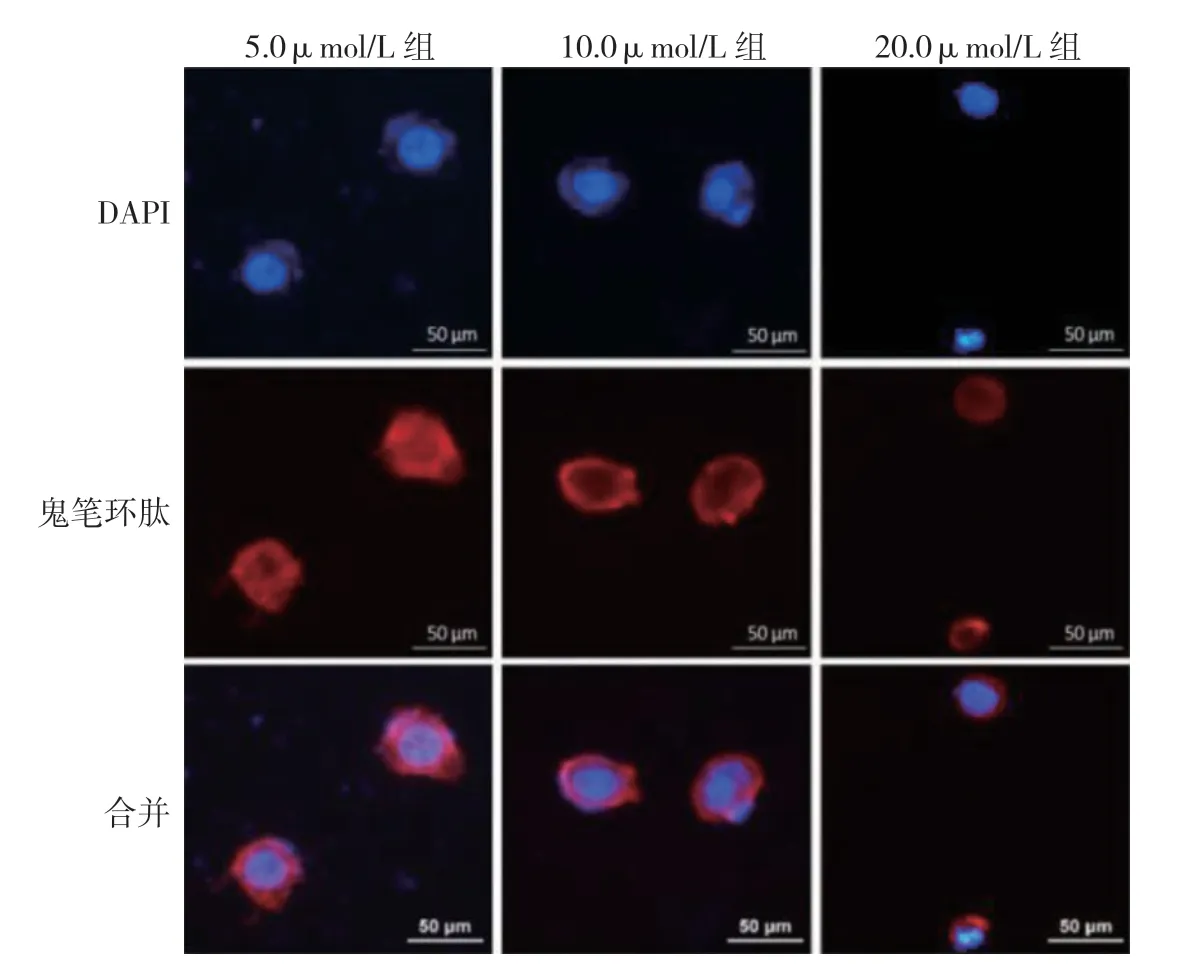
图4 HCT116 细胞核及细胞骨架微丝结构变化
2.5 各组Bcl-2 家族基因 mRNA 相对表达量 比较
各 组Bax、Bik、Bim、Puma、Bcl-xL 和Mcl-1 mRNA 相对表达量比较,差异有统计学意义(P<0.05)。0.0、1.0、2.5 和5.0μmol/L 组Bax、Bik 及Bim mRNA 相对表达量呈上升趋势;5.0μmol/L 组Puma mRNA 相对表达量最高;0.0、1.0、2.5 和5.0μmol/L 组Bcl-2 和Bcl-xL mRNA 相对表达量呈下降趋势;5.0μmol/L 组Mcl-1 mRNA 相对表达量最低。见表4和图5。
表4 各组Bcl-2 家族基因mRNA 相对表达量比较 (±s)
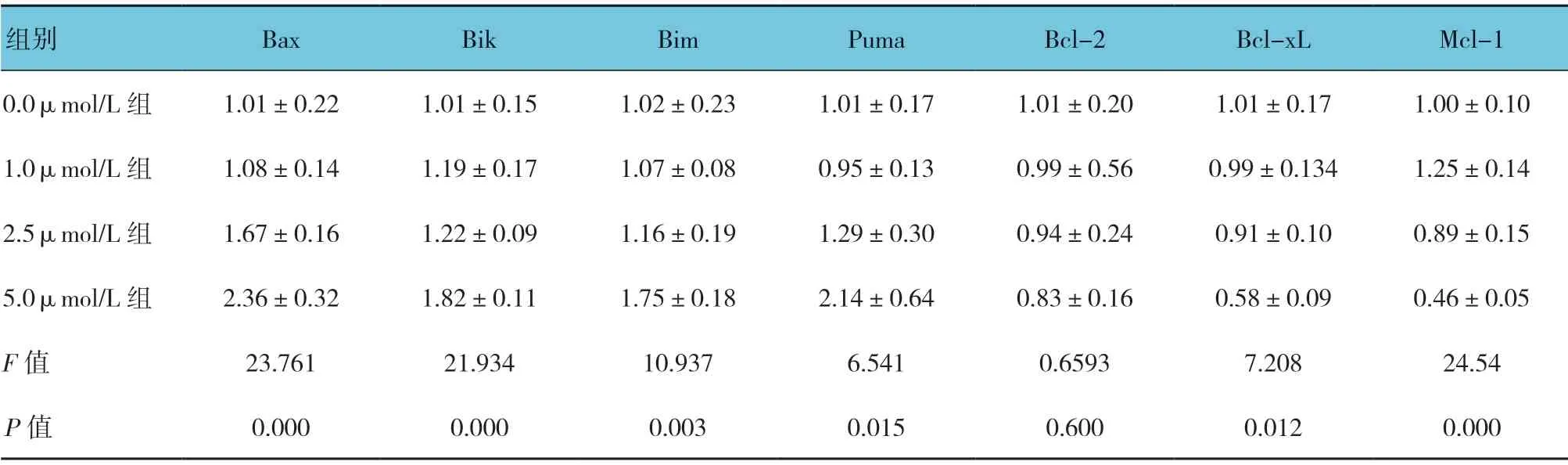
表4 各组Bcl-2 家族基因mRNA 相对表达量比较 (±s)
组别 Bax Bik Bim Puma Bcl-2 Bcl-xL Mcl-1 0.0μmol/L 组 1.01±0.22 1.01±0.15 1.02±0.23 1.01±0.17 1.01±0.20 1.01±0.17 1.00±0.10 1.0μmol/L 组 1.08±0.14 1.19±0.17 1.07±0.08 0.95±0.13 0.99±0.56 0.99±0.134 1.25±0.14 2.5μmol/L 组 1.67±0.16 1.22±0.09 1.16±0.19 1.29±0.30 0.94±0.24 0.91±0.10 0.89±0.15 5.0μmol/L 组 2.36±0.32 1.82±0.11 1.75±0.18 2.14±0.64 0.83±0.16 0.58±0.09 0.46±0.05 F 值 23.761 21.934 10.937 6.541 0.6593 7.208 24.54 P 值 0.000 0.000 0.003 0.015 0.600 0.012 0.000
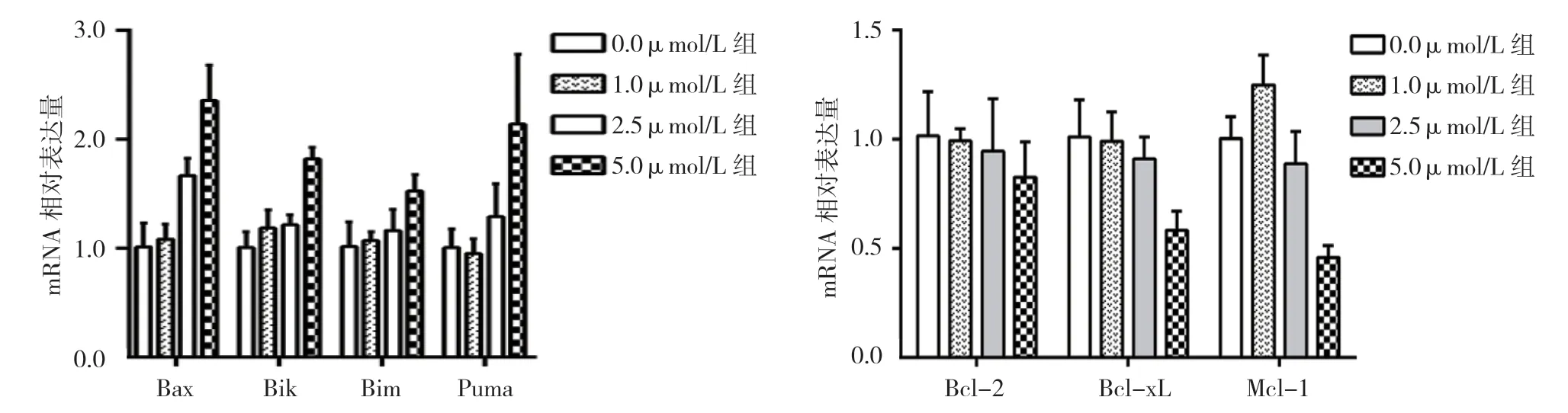
图5 各组Bcl-2 家族基因mRNA 相对表达量比较 (±s)
3 讨论
结肠癌作为一种常见的消化道恶性肿瘤,在世界范围内严重威胁着人类的身心健康。尽管随着各项研究的深入和技术的进步,结直肠癌的诊断和治疗手段都有了显著提高,但是肿瘤诊断和治疗仍然面临诸多挑战[5]。临床治疗以根治手术联合化疗为主,但患者的5年生存率仍不理想,多药耐药性是影响结直肠癌患者化疗疗效的主要原因[6]。因此,开发高效、低毒的药物是治疗肿瘤的有效途径之一。有研究报道,一氧化氮前体药JS-K 对前列腺癌、肝癌、肺癌、乳腺癌、白血病、多发性骨髓瘤及神经胶质母细胞瘤等生长有抑制作 用[3,7-12]。本研究结果表明,JS-K 对人结肠癌HCT116细胞增殖和凋亡有明显影响,且呈浓度依赖性。
有研究报道,JS-K 可抑制白血病细胞G2/M 期,诱导细胞早期凋亡[13]。本研究显示,JS-K 主要阻滞HCT116 细胞G2/M 期,并诱导晚期凋亡,且呈浓度依赖性。细胞凋亡时细胞骨架发生相应变化,表现为微丝结构降解凝集和分布不均匀[14]。本研究荧光双标记结果提示,JS-K 处理HCT116 细胞后,诱导核浓缩和核碎裂;细胞微丝结构和分布发生变化,局部出现溶解或断裂现象,表明JS-K 促进HCT116 细胞凋亡。
JS-K 主要通过诱导细胞凋亡对肿瘤细胞产生抑制作用,在调控凋亡的众多基因中,Bcl-2 家族与凋亡发生、发展最为密切。Bcl-2 家族分为2 大类:一类是抗凋亡蛋白,包括Bcl-2、Bcl-xL 及Bcl-w 等;另一类是促凋亡蛋白,包括Bax、Bak、Bid、Bik 及Bad等[15]。LIU 等[16]发现,JS-K 通过Bcl-2 家族蛋白调控诱导人肝癌HepG2 细胞凋亡。本研究结果提示,JS-K可通过上调促凋亡蛋白Bax、Puma,下调抗凋亡蛋白Mcl-1 蛋白表达,促进HCT116 细胞凋亡。
综上所述,本实验证实JS-K 对人结肠癌细胞HCT116 增殖有明显抑制作用,同时JS-K 通过上调HCT116 细胞中Bax 和下调Bcl-2 表达,阻滞细胞G2/M 期,促进细胞的晚期凋亡。目前证实JS-K 通过以下3 条途径抑制肿瘤细胞:①MAPK/JNK 通路;②Wnt/β-catenin 信号通路;③胱天蛋白酶信号通路。其中胱天蛋白酶信号通路是JS-K 诱导凋亡最重要的信号通路,JS-K 诱导人结肠癌细胞HCT116 凋亡的作用机制还有待研究。
