中药抗炎合剂干预全身炎性反应综合征的临床疗效研究*
2019-12-17陈思思朱海勇
王 颖 陈思思 朱海勇
浙江省台州市中心医院 浙江 台州 318000
全身炎性反应综合征(SIRS)是继发于炎症、创伤、感染和组织缺血—再灌注损伤等之后所出现的以全身持续高代谢、高动力循环状态及过度炎症反应为临床特征,伴有多种炎症介质及细胞因子释放失控的全身性瀑布式炎症反应综合征,若未能有效控制,最终可发展为多脏器功能衰竭(MSOF)。笔者结合多年来临床经验,在西药综合治疗基础上配合我院自制中药抗炎合剂,在控制SIRS向MSOF发展中取得一定疗效,现将结果报告如下。
1 资料与方法
1.1 一般资料:采取前瞻性研究方法,选择2016年9月~2018年9月本院重症监护室(ICU)及急诊病区收治的57例SIRS患者,其中男31例,女26例,年龄44~76岁,平均61.09±10.4岁。其中重症肺炎34例,胃肠道感染8例,泌尿道感染8例,皮肤软组织感染7例。如表1所示,两组患者治疗前原发病构成、性别、年龄、急性生理学与慢性健康状况评分(APACHE-Ⅱ)差异无统计学意义(P>0.05),具有可比性。见表1。

表1 两组基础资料比较
1.2 SIRS诊断标准:根据1991年美国胸科医师学会和危重病医学会公布的诊断标准:①体温>38℃或<36℃;②心率>90次/min;③呼吸>20次/min或动脉二氧化碳分压(PaCO2)<32mmHg(4.3kPa);④白细胞(WBC)计数>12.0×109/L或<4.0×109/L,或不成熟WBC>10%。符合两项及以上者,诊断为SIRS。其中符合两项、三项和四项的分别有29例、17例和11例。
1.3 中医证候入选标准:参照GB/16751.2—1997《中医临床诊疗术语证候部分》基本实症类的邪毒炽盛证(发热汗多不解、口渴饮冷、脘腹胀满、便结尿黄、舌红苔黄、脉数或洪)的诊断标准,入选患者经2名资深主治医生及中医师同时判定其中医证候满足入选标准。中医证候根据主症(发热汗多不解、口渴饮冷、舌红苔黄)和次症(脘腹胀满、便结尿黄、脉数或洪等)分为轻、中、重度,分别记为2、4、6分,治疗前后分别给予评分。
1.4 治疗方法:两组患者入组后均进行西医常规综合治疗,包括抗感染、维持内环境平衡、脏器功能支持、强化胰岛素、营养支持、氧疗及对症处理等,但在治疗过程中不应用低分子肝素等抗凝药物及活血药物。治疗组入组后即开始加用中药抗炎合剂(由本院制剂室提供)治疗组方含大黄、连翘、瓜蒌各15g,苦杏仁、滑石各8g,黄芩、厚朴各10g,败酱草30g。每次浓煎100ml,每日2次,12小时1次,口服或鼻饲,连服用7天。治疗过程中未有患者死亡,57例患者均完成本研究。
1.5 观察指标:两组患者确诊当天及治疗3天、治疗7天分别测定肿瘤坏死因子-α(TNF-α)、C反应蛋白(CRP)、血小板(PLT)、D-二聚体水平,并在治疗前后进行APACHE-Ⅱ评分和中医证候总分评估,并计算中医证候总有效率。随访28天病死率。
1.6 统计学处理:采用SPSS22.0统计软件,计量资料以均数加减标准差(±s)表示,组内采用配对t检验,组间采用独立样本t检验,计数资料采用卡方检验。P<0.05为差异具有统计学意义。
2 结果
2.1 中医证候疗效判定:疗效判定根据《中药新药临床研究指导原则》。临床治愈:症候积分减少率≥95%;显效:证候积分减少率为70%~94%;有效:证候积分减少率为30%~69%;无效:证候积分减少率<30%。
2.2 炎症反应指标:两组治疗前后TNF-α和CRP水平 比较见表2。
表2 两组治疗前后TNF-α和CRP水平比较(±s)

表2 两组治疗前后TNF-α和CRP水平比较(±s)
注:与本组治疗前比较,△P<0.01;与对照组同期比较,#P<0.01。
组别治疗组对照组TNF-α(ng/L)CRP(mg/L)7d 50.92±24.10#△90.40±36.71△例数30 27 0d 6.10±2.28*5.49±1.76 3d 3.40±1.84#5.22±2.10 7d 2.91±1.14#△4.66±1.11△0d 193.03±33.57 180.31±32.91 3d 114.67±33.09#156.17±51.08
2.3 凝血指标:两组治疗前后PLT和D-二聚体水平比 较见表3。
表3 两组治疗前后PLT和D-二聚体水平比较(±s)
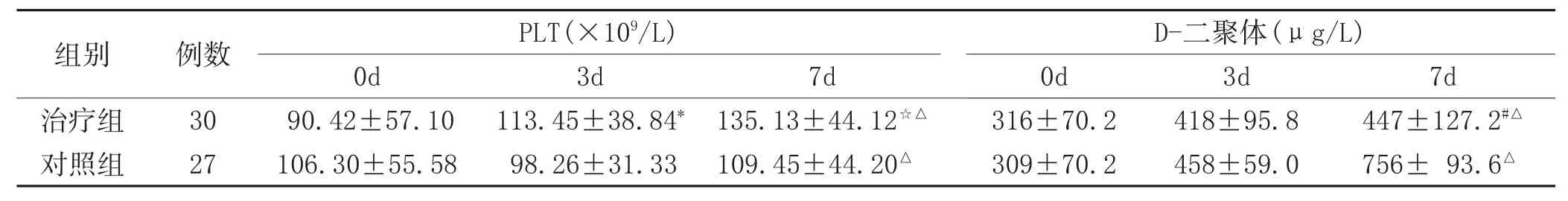
表3 两组治疗前后PLT和D-二聚体水平比较(±s)
注:与本组治疗前比较,△P<0.01;与对照组同期比较,☆P<0.05,#P<0.01。
组别治疗组对照组PLT(×109/L)D-二聚体(μg/L)7d 447±127.2#△756± 93.6△例数30 27 0d 90.42±57.10 106.30±55.58 3d 113.45±38.84*98.26±31.33 7d 135.13±44.12☆△109.45±44.20△0d 316±70.2 309±70.2 3d 418±95.8 458±59.0
2.4 中医证候总有效率:见表4。

表4 两组治疗前后中医证候总有效率的比较
2.5 APACHE-Ⅱ评分和28天病死率:见表5。
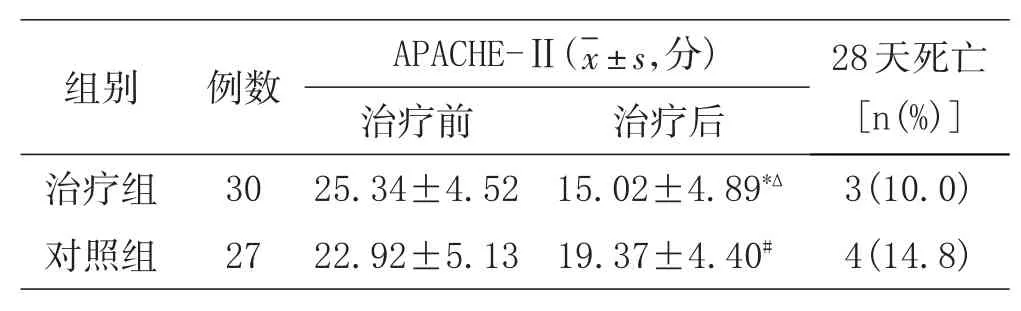
表5 两组治疗前后APACHE-Ⅱ评分和28天病死率比较
2.6 不良反应:治疗组未见明显出血等不良反应。
3 讨论
我院自制抗炎合剂含有大黄、苦杏仁、黄芩、连翘、厚朴、败酱草、滑石和瓜蒌,此小样本临床研究证明,其可有效降低炎症因子水平,促进凝血功能的改善,有利于控制SIRS的进展。大黄清热解毒,具有抗炎、泻下、解毒、保护胃肠屏障,减少肠毒素和细菌移位作用,其主要成分大黄素有抑制体内炎症相关分子表达的作用[1]。苦杏仁祛风热、润肠通便,其成分苦杏仁苷还有镇痛作用,可以帮助炎症患者减轻疼痛而不成瘾。黄芩苦寒,善清热泻火解毒,其主要成分黄芩苷及苷元黄芩素等,具有抑菌抗炎等活性,可在多个环节影响白细胞的功能。连翘苦寒泄热毒,具有疏肝理气,抗病毒抗炎的功效,从而减轻SIRS的内热炽盛的症状。厚朴行气消胀、理气和中、不伤脾阳,其主要成分厚朴酚具有镇痛、抗炎、抗菌的作用,有利于控制抗炎反应。败酱草味辛、苦,有清热解毒,祛瘀排脓等功效,具有镇静、保肝利胆、抗菌消炎等作用,可提高组织耐缺氧性,减少缺血-再灌注损伤。滑石因其质地,有利于祛除体内湿气且利下,减轻胃肠道负担,利脾而有益于消化系统的症状缓解。且滑石、连翘可以协同黄芩的作用,进一步加强其抗炎作用。瓜蒌皮清热解燥,是理气消渴的良药,能抑制血小板聚集和血栓形成,减轻再灌注损伤,减缓SIRS进展,有利于机体的修复[2]。本研究中,中药抗炎合剂对SIRS患者的血浆TNF-α、CRP值降低效果优于对照组,可能机制在于抗炎合剂通过多个环节(保护胃肠功能,减少内毒素和细菌移位等)降低了患者的血浆TNF-α等炎症因子水平,有效阻止炎性介质的扩增及其生物学作用的发挥,
减少了相关环节炎症反应的进一步加剧和对机体的损害。CRP水平下降和炎症因子水平下降有关,还可能和中药合剂对机体免疫系统的调节有关,促进炎症—抗炎之间的平衡,减轻对机体器官的损害。治疗组血小板计数上升同时伴有D-二聚体水平变化不明显,可能和炎症因子水平下降,炎症反应减轻,血小板损耗降低,组织缺血缺氧减轻,对机体凝血-纤溶系统起到保护作用有关。本研究中随访28天病死率两组间无统计学差异,可能与样本量过小或中药合剂疗程较短,剂型单一有关。综上所述,中药抗炎合剂对SIRS有保护作用,其机制可能与其对炎症反应的抑制和凝血-纤溶功能的保护有关。
