吸光光度法同时测定食品中的苯甲酸和山梨酸
2019-12-16白海鑫刘小花陈华梅
白海鑫 刘小花 陈华梅

摘要:基于吸光度的加和性原理,在选定波长254、224 nm下,通过对苯甲酸/山梨酸的吸光度与浓度间的标准曲线进行线性回归分析所得的斜率,建立了苯甲酸和山梨酸吸光度D与浓度C的关系方程组,最终获得起1种无需分离即可同时测定食品中的苯甲酸和山梨酸含量的方法。结果表明:苯甲酸的回收率为91.83%~102.10%,RSD(相对标准偏差)为0.885%,最小检出限为0.13 mg/L,山梨酸的回收率为91.81%~92.67%,RSD为3.01%,最小检出限为0.096 mg/L,除了具有成本低、操作简单、快速、高效、重现性好等优点外,该方法最大的优点是可不经分离而直接测定混合样品中的苯甲酸与山梨酸的浓度。
关键词:吸光光度法;同时测定;苯甲酸;山梨酸
中图分类号: TS255.7文献标志码: A
文章编号:1002-1302(2019)19-0224-03
收稿日期:2018-07-21
基金项目:国家自然科学基金(编号:31501213);河南省高等学校青年骨干教师资助计划(编号:2014GGJS-083)。
作者简介:白海鑫(1973—),男,河南中牟人,博士,副教授,主要从事吸收光谱及荧光光谱的分析方法研究。E-mail:haixin_bai@aliyun.com。
通信作者:刘小花,博士,副教授,主要从事光谱分析与材料化学方面的研究。E-mail:xiaohualiu78@aliyun.com。
科学技术的迅速发展使食品工业快速崛起,食品添加剂得以广泛应用。部分商家为追求食品的色、香、味俱全,延长保质期,往往会在食品中添加大量食品添加剂。《食品添加剂使用卫生标准》对食品添加剂用量和使用范围都有严格的规定和要求[1]。但仍有厂家为了降低生产成本和延长保质期等,在食品中加入过量食品添加剂,而食品添加剂摄入过量会危及人体健康。苯甲酸和山梨酸是较常用的食品添加剂,它们在食品中含量的测定方法的研究显得尤其重要。测定苯甲酸和山梨酸含量的方法有气相色谱法[2-3]、高效液相色譜法[4-6]、薄层色谱法[7]、滴定法[8]、吸光光度法[9-10]。虽然气相色谱法和高效液相色谱法被较多地用于食品中苯甲酸与山梨酸的测定,但其仪器昂贵,分析成本高和操作繁杂等,不利于其应用与普及。鉴于吸光光度法操作简单、快速、成本低等优点[11-13],本研究通过对不同选定波长下的吸光度与浓度间的标准曲线进行线性回归分析,并基于吸光光度法中吸光度具有加和性原理建立了对样品中的苯甲酸和山梨酸不经分离而直接同时测定的方法。
1 材料与方法
1.1 试剂与仪器
分析纯级的苯甲酸和山梨酸购自上海阿拉丁试剂有限公司;其余试剂均为分析纯。试验用水为去离子水,试验用山楂片购自当地超市。
吸收光谱及光度分析试验所用分光光度仪系配有1 cm光程的石英比色皿的TU-1901型双光束紫外可见光谱仪(北京普析通用仪器有限责任公司)。
1.2 苯甲酸及山梨酸溶液的配制
准确称取一定质量的苯甲酸,用5% Na2HPO4或0.01 mol/L NaOH溶液溶解,定容为1 mg/mL苯甲酸溶液储备液,用时稀释到所需浓度;山梨酸溶液的配制方法与此相同。
1.3 食品样品的预处理
准确称取一定质量研碎的山楂片于适量蒸馏水中,超声提取20 min,离心,过滤,将滤液转入容量瓶并用蒸馏水定容。取部分滤液于分液漏斗中,加入一定量HCl及饱和NaCl溶液,用乙醚萃取4次,弃无机相,合并有机相于另一分液漏斗中,再用5% Na2HPO4溶液进行反萃取多次,弃有机相,合并无机相于小烧杯中[14]。在70 ℃磁力搅拌下去除乙醚,将去除乙醚的溶液转入容量瓶中,用5% Na2HPO4溶液定容。以试剂空白为参比溶液,在200~300 nm范围内进行光谱扫描,测定样品的吸光度。
2 结果与分析
2.1 溶剂的选择
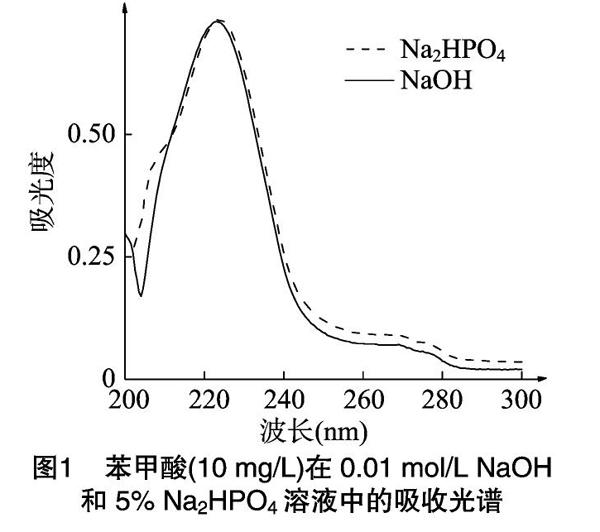
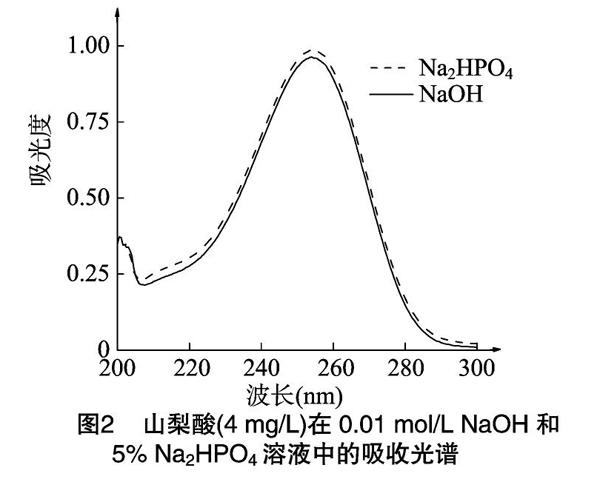
苯甲酸和山梨酸微溶于水,易溶于有机溶剂。常用 0.01 mol/L NaOH溶液溶解苯甲酸和山梨酸[10,15]。本试验发现,在室温下用0.01 mol/L NaOH溶液溶解苯甲酸和山梨酸至少要搅拌15 min,放置时间长,且有白色浑浊沉淀生成;当用5% Na2HPO4溶解苯甲酸和山梨酸时,溶解时间较短,不需搅拌,立即溶解。
从苯甲酸和山梨酸在0.01 mol/L NaOH和5% Na2HPO4溶液中的吸收光谱可看出,苯甲酸和山梨酸在5% Na2HPO4和0.01 mol/L NaOH溶液中的吸收光谱基本相同,苯甲酸和山梨酸的最大吸收峰无明显变化(图1、图2),该试验结果表明,苯甲酸和山梨酸的吸收光谱不受这些溶剂的影响。在提取食品样品中的苯甲酸和山梨酸时,一般是先酸化样品,再用乙醚萃取有机物质,最后用5% Na2HPO4溶液反萃取并定容[14]。综合考虑苯甲酸的溶解性及后续试验等因素,本试验选用5% Na2HPO4溶液作为溶解苯甲酸和山梨酸的溶剂。
2.2 测定波长的选择
准确移取一定量的储备液,以5% Na2HPO4溶液为溶剂分别测定10 mg/L苯甲酸和4 mg/L山梨酸溶液在200~300 nm 范围内的吸收光谱。由图3可知,苯甲酸、山梨酸的最大吸收波长分别为224、254 nm。苯甲酸和山梨酸在200~300 nm波长范围具有较强的吸收,光谱重叠。由于两者的吸收光谱双向重叠,互相干扰,因此不能直接利用吸光度D与浓度C的关系对苯甲酸和山梨酸进行单组分测量,在该范围内测得的吸光度均为苯甲酸与山梨酸吸光度之和。如苯甲酸、山梨酸在224、254 nm处的吸光度可表示为下式:
D224,x+y=k224,xCx+k224,yCy;
D254,x+y=k254,xCx+k254,yCy。
式中:x、y分别指苯甲酸与山梨酸。上式中浓度项的4个系数k可通过苯甲酸与山梨酸单独存在时相应波长下的吸光度D与浓度C的标准曲线的斜率求得,将4个k值代入上方程组即可求出苯甲酸与山梨酸的浓度。苯甲酸与山梨酸在224、254 nm处均有一定的灵敏度,故本试验选择在224、254 nm 处进行苯甲酸与山梨酸单独存在时吸光度D与浓度C的标准曲线测定及二者共存时的吸光度的测定。
2.3 标准曲线试验
准确移取苯甲酸或山梨酸储备液,加入5% Na2HPO4溶液,分别配成一系列准确浓度的标准溶液,测定其吸收光谱,取224、254 nm处的D224 nm、D254 nm对浓度C作图得标准曲线(图4至图7),并对标准曲线进行线性拟合以求得其线性回归方程及斜率。
由图4及图5可知,苯甲酸在254 nm处吸光度D254 nm对浓度C的线性回归方程为D254 nm=0.006 35C苯甲酸-0.002 29,相关系数r=0.989 3,线性范围为0.00~30.00 mg/L。山梨酸在254 nm处的线性回归方程为D254 nm=0.250 87C山梨酸-0.007 69,相关系数r=0.998 6,线性范围为0.00~8.00 mg/L。由于吸光度具有加和性,所以二者共存的样品溶液在254 nm处的吸光度如下:
D254 nm=0.250 87C山梨酸+0.006 35C苯甲酸-0.009 98。(1)
同理,由图6及图7可知,苯甲酸在224 nm处的线性回归方程为D224 nm=0.070 38C苯甲酸-0.009 64,相关系数r=0.998 6,线性范围为0.00~30.00 mg/L。山梨酸在224 nm处的线性回归方程为D224 nm=0.080 38C山梨酸+0.014 36,相关系数r=0.991 0,线性范围为0.00~8.00 mg/L。因此,苯甲酸与山梨酸混合样品溶液在224 nm处的吸光度如下:
D224 nm=0.080 38C山梨酸+0.070 38C苯甲酸+0.004 72。(2)
由上述标准曲线相关系数可知,在其线性范围内,苯甲酸和山梨酸在224、254 nm处的吸光度D与浓度C之间有着良好的线性关系。对于苯甲酸与山梨酸混合样品,可通过测定混合样品在224和254 nm处的吸光度D,联立得方程组:
D254 nm=0.250 87C山梨酸+0.006 35C苯甲酸-0.009 98;(3)
D224 nm=0.080 38C山梨酸+0.070 38C苯甲酸+0.004 72。(4)
求解该方程组,即可不经分离求得苯甲酸和山梨酸的混合样品中各自浓度。鉴于试验测定时一般选择200~300 nm波长下的吸光度D=0.434为试驗测值,此时光度法误差最小。然而,该方程组中常数项(0.009 98及0.004 72)数值相对于0.434的相对误差小于光度法的最小误差(约为2.7%)。因此方程组中的常数项在准确度要求不太高的计算中可忽略,故以上方程组可简化为下式:
D254 nm=0.250 87C山梨酸+0.006 35C苯甲酸;(5)
D224 nm=0.080 38C山梨酸+0.070 38C苯甲酸。(6)
3 讨论
3.1 样品测定
准确移取5.00 mL山楂样品溶液,按预处理方法处理样品溶液,在相同条件下,平行测定6次样品溶液,计算苯甲酸和山梨酸含量以及它们的相对标准偏差RSD(%)。
由表1可知,苯甲酸的RSD为0.885%,在线性范围有较好的精密度,山梨酸的RSD为3.01%,在线性范围内,精密度低于苯甲酸。
3.2 加标回收率试验
分别用苯甲酸和山梨酸的标准溶液配制不同浓度的混合液,每种浓度进行6次平行测定试验,将测得的吸光度代入回归方程,测定值与理论值之比即为回收率。苯甲酸的回收率为91.83%~102.10%,山梨酸的回收率为91.81%~92.67%,回收率符合试验要求,分析方法具有良好的准确度。
4 结论
本研究基于吸光光度法中吸光度具有加和性,通过对不同选定波长下的吸光度与浓度间的标准曲线进行线性回归分析所得的斜率,建立了苯甲酸和山梨酸在波长254、224 nm下的吸光度D与浓度C的关系方程组:
D254 nm=0.250 87C山梨酸+0.006 35C苯甲酸;
D224 nm=0.080 38C山梨酸+0.070 38C苯甲酸。
通过测定苯甲酸与山梨酸混合样品在上述2个波长处的吸光度D,并代入该方程组即可直接求出样品中苯甲酸与山梨酸的浓度。结果表明,苯甲酸的线性范围为0.00~30.00 mg/L,最小检出限为0.13 mg/L,山梨酸的线性范围为0.00~8.00 mg/L,最小检出限为0.096 mg/L,该方法得到苯甲酸的回收率为91.83%~102.1%,RSD为0.885%,山梨酸的回收率为91.81%~92.67%,RSD为3.01%。该方法除操作简单、快速、高效外,最大的优点就是无需分离苯甲酸与山梨酸就可测定二者共存样品中各自的浓度。鉴于大多数食品中的添加剂都不止1种,而是2种或多种添加剂共存,故本方法的建立对测定食品中添加剂含量具有较大借鉴意义。
参考文献:
[1]食品添加剂使用卫生标准GB2760—2007[S]. 北京:中国标准出版社,2007.
[2]鲍忠定,许佳飞,许荣年,等. 毛细管气相色谱内标法同时测定食品中8种防腐剂[J]. 分析化学,2004,32(2):270.
[3]庞楠楠,迪丽努尔·马力克,牛 蓓,等. 快速气相色谱法测定食品中的常见防腐剂[J]. 分析试验室,2005,24(3):48-52.
[4]陈青川,于文莲,王 静. 高效液相色谱法同时测定多种食品添加剂[J]. 色谱,2001,19(2):105-108.
[5]刘莉萍,毕思远,龚达浩,等. HPLC法测定食品中的防腐剂和合成着色剂[J]. 食品工业,2018,39(1):266-269.
[6]许金伟,周晓红. 超高效液相色谱法测定蜜饯中苯甲酸、山梨酸及糖精钠方法研究[J]. 现代农业科技,2018(8):245-246.
[7]肖学成. 薄层色谱法同时测定食品中4种添加剂的方法介绍[J]. 实用预防医学,1998,5(2):122-123.
[8]金 薇,尤献民,张曦弘. 电位滴定法测定复方板蓝根冲剂中总有机酸的含量研究[J]. 中医药学刊,2004,22(3):574.
[9]茅周祎. 葡萄皮红色素在风味饮料中应用探究[J]. 食品工业,2018,39(4):40-42.
[10]汪晓璇,汪念秋,刘晓曦,等. 紫外光度法同时测定酱油中苯甲酸和山梨酸含量[J]. 中国调味品,2015,40(8):108-110.
[11]Zhou L,Liu X H,Bai H X,et al. A simple method for determining water content in organic solvents based on cobalt(Ⅱ) complexes[J]. Chinese Chemical Letters,2011,22(2):189-192.
[12]Bai H X,Yang X R. Spectrophotometric determination of water content in alcohol organic solvents[J]. Journal of the Chinese Chemical Society,2007,54(3):619-624.
[13]汪顯阳,冯 伟,胡岩岩,等. 两种吸收光度法同时测定果味饮料中苯甲酸钠和山梨酸钾含量的比较研究[J]. 食品科学,2009,30(24):337-339.
[14]马盛龙,罗 浩,李巧琪. 食品添加剂中苯甲酸和山梨酸的检测与分析[J]. 现代食品,2017,7(14):113-115.
[15]吴勤民. 荧光光谱法和紫外分光光度法在发酵调味品中苯甲酸含量测定中的应用和比较[J]. 中国调味品,2010,35(1):78-84.
