基于表面等离子体共振和电化学联用的DNA传感器研究进展
2019-12-11张玉昆安娜刘卫晓宛煜嵩金芜军李亮张晓
张玉昆,安娜,刘卫晓,宛煜嵩,金芜军,李亮*,张晓
1.长春理工大学生命科学技术学院,长春 130022;2.中国农业科学院生物技术研究所,北京 100081
脱氧核糖核酸(DNA)是已知的主要且最有研究意义的生物有机化合物,具有生物相容性和生物可降解性[1-2],因此,DNA杂交反应在分子检测领域具有很重要的研究价值。了解非生物表面与功能性生物分子(如蛋白质、DNA、适体等)之间存在的相互作用,在开发用于生物传感器和分子传递等的功能性生物界面方面起着至关重要的作用。例如,生物传感器的发展需要各个生物分子识别元件的适当分配、定向和改变构象,以实现最佳活性、结合亲和力和长期稳定性[3-6]。然而,由于待结合分子的复杂性和异质性,研究界面是具有挑战的。固体基质上的固定/定位方法和较弱的亲和力导致动力学检测的不稳定性[7-8]。
在过去的几十年中,随着纳米材料的研发和联用技术的飞速发展,研究界面性质的先进光谱电化学方法越来越受到关注。纳米技术与纳米材料科学的新成就,使不同大小(1~100nm)、形状与组成(成分)的众多纳米材料介入生物传感领域。纳米粒子的小体积突破了结构微型化的限制,导致了更低的检测限,甚至可达到zmol(1 zmol=10-21mol)的水平。而且,生物功能化纳米粒子可以产生催化性能、传导性能与生物相容性能的协同作用,并加快信号传导。更为重要的是,纳米材料与环境直接接触,可以直接作为化学与生物传感器,实现生物分子的单分子检测,从而使其广泛应用于生物体系。纳米生物传感的进一步发展也为多种生物技术的联用提供了有用工具。
光谱电化学可以通过电化学(electrochemical,EC)和光学技术的结合实现原位界面表征。单独的电化学方法通常不适合识别界面上发生的结合事件和构象变化,因此需要额外的光学技术,例如表面等离子体共振(surface plasmon resonance,SPR)。SPR作为无标记技术,便于研究界面上的相互作用[9-13]。然而,它对低浓度、小分子的检测和非特异性结合的识别存在限制[14-17]。另外,由于衰减长度的限制,SPR仅对距离金表面几百纳米距离内的折射率变化具有检测效应。EC的设备简单,试验成本低。然而,对于许多生物分子,在电极上没有发生直接的电子转移,因此需要通过标记分子的间接电子转移,这增加了检测的复杂性和费用。同时,与法拉第电流一起产生的电容电流也会导致信号干扰。此外,EC难以鉴定中间体或产物的未知物质。而SPR与电化学的耦合通常有利于它们相互弥补这些缺陷。因此,以SPR为主的EC-SPR联用引起了极大的关注。本文综述了近年来SPR和EC联用的DNA传感器应用研究进展,包括技术原理、联用方法(CV-SPR、EIS-SPR、CV/EIS-SPR)与未来展望,以期为相关研究提供参考。
1 电化学/表面等离子体共振(EC-SPR)技术基本原理
1.1 SPR基本原理
SPR光谱法是一种光学技术,可监测固体表面上的折射变化,并与其他小分子或生物分子一起进行修饰。折射率的变化反映了溶液中的分析物与固定在表面上的与配体结合的分析物质的量[18]。SPR原理如图1所示。
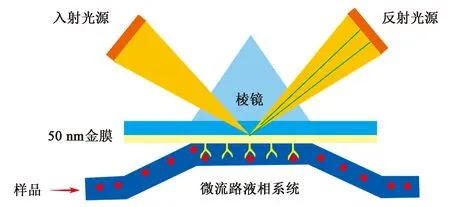
图1 表面等离子共振(SPR)原理图[18]Fig.1 Theory of surface plasmon resonance (SPR)[18].
偏振光以一定角度范围入射到镀在玻璃表面的薄膜上发生全反射,会形成消逝波进入光疏介质,而在光疏介质中又存在等离子波,当符合表面等离子体共振波的激发条件时,两波相遇就可能发生共振(图1)。入射光的能量被吸收,使反射光能量急剧下降,在反射光谱上出现反射强度最低值,即共振吸收峰,所对应的波长为共振波长,对应的入射角为共振角,当金属薄膜表面介质不同时,共振角或共振波长将改变,由此可获得相关信息。SPR对附着在金属薄膜表面的介质折射率非常敏感,当表面介质的属性改变或者附着量改变时,共振角会发生变化。因此,SPR谱(共振角的变化vs时间)能够反映与金属膜表面接触的体系的变化[9-13]。
1.2 EC基本原理
EC检测依托于三电极体系:工作电极(working electrode)、参比电极(reference electrode)和对电极(auxiliary electrode)。在电化学反应中,反应物在电解液或电极修饰层溶液的界面中得失电子,其大多是一种界面反应。电极电流可以看作工作电位的函数,工作电极的电位相对于参比电极,电流流经工作电极和对电极(图2)。
1.3 EC-SPR联用
在EC-SPR中,玻璃或石英基底上的金膜既被用来产生表面等离子体共振的介质,又可以用作电化学测试的工作电极。在产生电化学反应的时候,电极溶液界面内发生的任何性质的变化都会引起SPR共振角(折射率)发生变化,这就是EC-SPR技术的基本原理(图2)[19-21]。
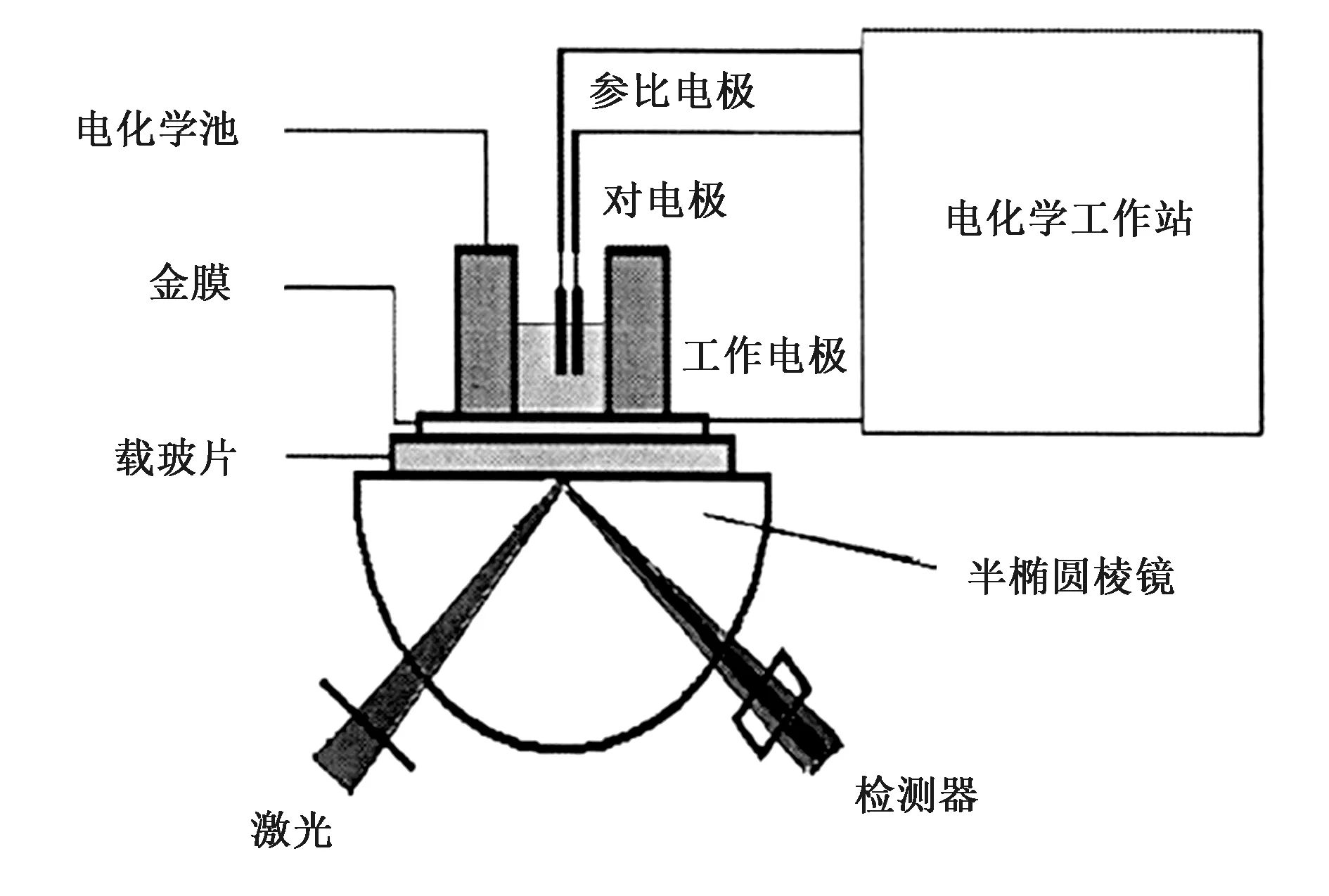
图2 EC-SPR原理图[21]Fig.2 Theory of electrochemical surface plasmon resonance[21].
2 EC-SPR在DNA分析及其他方面的应用进展
2.1 循环伏安法(cyclic voltammetry,CV)与SPR联用在DNA检测中的应用研究
CV除了作为定量分析方法外,更主要的是作为电化学方法,可用于研究电极反应的性质、机理及电极过程中的动力学参数等。在一个典型的循环伏安实验中,工作电极一般为浸在溶液中的固定电极。为了尽可能降低欧姆电阻,建议采用三电极系统。在三电极系统中,电流流经工作电极和对电极。工作电极电位是一个分开的参比电极(如饱和甘汞电极,SCE)为基准的相对电位。在循环伏安测试实验中,工作电极的电位以10~200 mV/s的扫描速度随时间线性变化,与此同时记录在不同电位下的电流。表面等离子共振技术旨在检测表面附近折射率的变化。众所周知,SPR是一种无标记、实时、灵敏和快速的方法,用于研究分子相互作用[22-25]的动力学和效率常数、大分子的构象变化[26-27]等。传统的SPR由于无法测量折射率的极小变化而在超灵敏检测中的应用受到限制。而这两者的结合,可以监测电化学反应中的大范围氧化还原反应过程,不但可以研究聚合物的电化学行为,还可以分析电极表面的结合、解离和扩散过程。Liu等[28]报道了一种基于二茂铁-链霉抗生物素蛋白(Fc-Stv)缀合物的灵敏方法,用于将EC和SPR的DNA靶标同时杂交至金表面修饰的肽核酸上。Fc-Stv与生物素化的互补靶DNA的连接不仅放大了SPR信号,而且由于每个Stv具有许多Fc标记物,也增强了电化学信号。二茂铁氧化还原峰电流随靶DNA浓度的增加而增加。因此,可以通过CV估计杂交的靶DNA的量。该传感器还显示出高选择性(在单碱基错配水平下)和良好的重现性。Patskovsky等[29]以亚甲基蓝(MB)有机染料为例,通过CV进行表征,研究了电化学SPR(ESPR)传感的理论和实验参数。他们还评估了在溶液中以及在由标记有MB的茎环寡核苷酸形成的均匀界面薄膜中用于MB传感的最佳ESPR实验方法。光学SPR响应的电化学激活依赖于局部MB浓度,可用于设计敏感和高选择性的生物传感方法。
2.2 电化学阻抗谱(electrochemical impedance spectroscopy,EIS)与SPR联用在DNA检测中的应用研究
EIS描述了系统对周期性小幅度交流信号的应用的响应,用于分析由表面上带电生物分子结合诱导的修饰电极和半导体的界面特性的变化,是SPR的一个有用的无标记检测工具。EIS可以在导电聚合物[30-31]、金属[32-37]、半导体界面[37-41]以及异质结构如半导体/介电界面(例如硅/二氧化硅)[40,42-45]上进行。Vogt等[46]在两个镀金的SPR玻片上单独进行了EIS和SPR联合测量,证明了从FeRi/亚铁氰化物氧化还原偶中释放的游离CN-会蚀刻金表面的猜测。Wang等[47]报道了一种基于石墨烯的无标记、再生和灵敏的表面等离子共振(SPR)和电化学适体传感器,用于检测α-凝血酶。无标记的EIS适体传感器表现出高选择性,证实了适体传感器良好的灵敏度和选择性,可用于制备灵敏的EIS适体传感器检测α-凝血酶,从而为设计高性能电化学适体传感器提供了一种新方法。值得一提的是,与CV相比,EIS的优势在于其非侵入性[48]。在CV的情况下应用潜在的斜坡会导致与表面相连的分子发生不可逆的氧化。因此,通过研究氧化还原探针在缓冲溶液中的扩散或通过记录杂交前后DNA层的阻抗变化,EIS已成功应用于DNA杂交研究[49-50]。但是在EIS中经常遇到的一个问题是难以确定从实验数据获得的电路模型的唯一性。与SPR测量(SPR/EIS)的联合应用有助于克服这一缺陷。因此,使用EIS检测双分子的相互作用已被应用于生物传感器的开发[51-52]。
2.3 CV/EIS与SPR联用在DNA检测中的应用研究
CV和EIS都是研究电极过程的最常用方法,除了单独和SPR技术联用外,近些年来CV、EIS共同与SPR联用的方法也逐渐成为研究的热点。Lee等[53]利用电化学方法(EC)和局域表面等离子体共振(LSPR)方法,通过CV/EIS技术在Au纳米晶体(AuNC)上制备了由多功能DNA(MF-DNA)组成的双模心肌钙蛋白I(CTnI)生物传感器。这种简单的纳米结构提供了更高的表面覆盖率,便于增加固定化时间,以实现更大的靶标-生物探针结合。此外,该工艺不需要复杂的生物传感器制造方法,最终减少了生物传感器的制造时间。Zhang等[54]报道了CV/EIS与SPR联用方法在检测大肠杆菌细胞表面上贴壁细胞和DNA吸收的应用,通过原子力显微镜(AFM)、CV和EIS表征活细胞在表面上的附着,并计算CV和SPR信号获得吸收的动态参数。在这项工作中,利用多肽RGD对金颗粒的结合特异性,将大肠杆菌细胞靶向结合在金表面。然后通过电化学方法以及该固定化方案的表面等离子体共振光谱研究细胞外鲱鱼精子DNA在大肠杆菌上的吸附动力学。重要的是,这是第一项使用电化学方法表达大肠杆菌对DNA吸附作用的研究。最终结果表明,联用方法适用于检测微生物表面上的DNA结合,并且平衡常数的结果是精确可靠的。
2.4 EC-SPR在其他方面的应用
综上,可以看出电化学和SPR两种技术的联用呈现出多样化的趋势,随着EC-SPR研究的不断深入,应用范围也在逐渐扩大。本小节将根据EC-SPR在研究细胞色素C(Cyt C)的氧化还原对和细胞色素C氧化酶(COX)之间的相互作用、癌细胞以及水中氨苄青霉素的检测等方面的应用对其研究进展进行评述。
Hou[55]等通过电化学表面等离子共振(EC-SPR)系统在模拟氧化还原调节的界面上研究细胞色素C(Cyt C)的氧化还原对和细胞色素C氧化酶(COX)之间的相互作用。在该研究中,原位EC-SPR有望更好地模拟COX嵌入线粒体内膜的体内条件。而且,利用Cyt C在流动相中充当电子穿梭物,是研究氧化还原依赖性生物分子相互作用的有效方法。Wu等[56]采用EC-SPR研究的策略来评估在SPR芯片界面上用DNR处理的癌细胞。从SPR记录的信号变化是由吸附的HepG2细胞的形态和质量变化以及培养基溶液的折射率变化引起的。培养基中细胞外的DNR残留浓度可通过电化学方法测定。光学显微镜图像和MTT测试的结果还证明,相关细胞的释放或解吸是由DNR处理后癌细胞的凋亡引起的。SPR信号幅度的降低与细胞存活率线性相关。观察表明SPR与电化学研究的组合可用于评估细胞中生物活性剂的治疗效率。因此,这种无标记的实时EC-SPR方法在监测相关临床治疗过程和药物分析方面具有巨大的应用潜力。Wu等[57]建立了一种基于SPR的检测方法,应用EC对氨苄青霉素检测中使用的适体平台进行精制和表征。基于APT修饰的金芯片的新型SPR方法被开发用于AMP的选择性、灵敏、实时和无标记测定。通过潜在的脉冲电化学方法改善了在特定APT的金芯片上的固定。通过SPR、CV、EIS和石英晶体微天平分析表征了适体传感器精制的每个步骤。经开发的适体传感器被证明对AMP检测具有选择性,且几乎不受其他抗生素和药物的影响,并已成功用于河水中AMP的检测。
3 展望
SPR对金属膜上发生的各种反应高度敏感,并且已经成为研究在表面上发生的分子结合过程的强有力的无标记方法。另一个重要但较少探索的应用领域是使用EC-SPR联合,该方法将EC与光学方法结合,使EC和SPR技术特点相互补充,虽然二者都是研究界面及界面附近物质的变化,但信号的来源各不相同,EC为电子转移过程,SPR为折射率的变化。EC-SPR联用技术相比于单一技术,能够得到综合且全面的信息。而SPR芯片的金膜又可以作为EC的工作电极,通过对样品流动池的简单改造便可搭建三电极电化学池。两种技术联用对于研究在电极表面上发生的非均相反应,以及用于测量反应物质的光学性质具有独特的优势,这可以帮助识别反应机理从而更好地监测和理解生化过程。同时,EC-SPR联合跳出了SPR联用技术中简单结合的思路,能够在更深层次上认识SPR信号与EC信号的关系,搭建起两种信号之间的纽带。
值得一提的是,近期SPR技术相关的研究多数依赖于成熟的商业化设备,由于此类设备系统较为封闭,且芯片试剂等材料均为设备公司提供,阻碍了EC-SPR联用方面的研究,且仪器昂贵,不便于推广。随着功能纳米材料微型化、新特性和新功能的需求日益增长,多技术联用方面的应用前景越来越广阔。EC-SPR和其他技术(例如:高效液相色谱、光学显微技术、原子显微镜等)进一步联用的相关研究会逐步深入,EC-SPR的应用范围也会进一步扩大。接下来EC-SPR的仪器集成化、微型化和检验自动化或将成为未来开发的重点。
