干旱和复水对4种咖啡叶片叶绿素荧光特性和SPAD的影响①
2019-12-10武瑞瑞黄家雄李亚男张晓芳吕玉兰沈正松何红艳李贵平
武瑞瑞 黄家雄 杨 阳 李亚男 张晓芳 吕玉兰 沈正松 何红艳 李贵平
(云南省农业科院热带亚热带经济作物研究所 云南保山678000)
植物适应干旱的机制基本分为:避旱性、抗旱性及耐旱性3种[1]。抗旱性机理主要是减少蒸腾、根系加强吸水能力、储藏水分;耐旱机理主要是保持绿色的耐脱水性,保持正常的代谢水平,延迟组织器官衰老;避旱性机理为通过改变自身的生长史等方式躲避干旱。作物抗旱性评价指标有:形态指标、生长发育指标、生理生化指标、产量指标等。生理生化指标包括水分生理指标、光合作用指标等,叶绿素荧光分析技术是反映光合作用“内在性”的特点。当干旱胁迫发生时,植物叶片叶绿素荧光参数也会发生规律性变化,从而间接地指示不同干旱程度时植物光合生理的变化。
从叶绿素荧光参数入手研究植物抗旱性相关的报道比较多,如吴甘霖等[2]对草莓在不同干旱胁迫和复水下叶绿素荧光测定研究结果表明,低中度干旱胁迫复水后草莓的叶绿素荧光参数恢复到正常水平,而重度干旱胁迫时未能恢复;李威等[3]对东北红豆杉实生苗和扦插苗在干旱和复水条件下的叶绿素荧光特性进行了研究,结果表明,在干旱条件下扦插苗的叶绿素荧光参数变化程度大,对干旱敏感,但复水后两者都恢复到正常水平;刘永安等[4]研究了麻疯树幼苗在干旱和复水条件下叶绿素荧光的变化,结果表明基质含水量在8.70%时,叶绿素荧光参数发生变化,基质含水量降至4.22%复水48 h后,叶绿素荧光较快恢复,说明麻疯树有极强的干旱适应能力;谢东锋[5]对干旱胁迫和复水后金银花叶绿素荧光参数的变化进行了研究,结果表明,随着干旱胁迫时间的延长,金银花的叶绿素荧光参数发生变化,复水后各参数先快速恢复后缓慢恢复,直到稳定状态,但是不同干旱程度和胁迫时间,恢复的程度和速度均不同。目前,从叶绿素荧光参数等方面入手开展咖啡抗旱性研究的报道较少,王睿芳等[6]通过对小粒种咖啡叶片的解剖研究咖啡的抗旱性,结果发现,栅栏组织和叶片组织结构紧密度是迅速反应抗旱性的叶片解剖性状;张珍贤等[7]通过小粒种咖啡在干旱胁迫下施肥对其光合特性的影响研究,发现氮肥和磷肥在增强抗旱性方面有很大效果,且磷肥作用更强。笔者从叶绿素荧光参数最大光化学效率(Fv/Fm)、实际光化学效率(ΦPSII)、光合电子传递速率(ETR)等方面开展不同小粒种咖啡在干旱胁迫下的表现,分析其对干旱逆境的响应规律及适应能力,以及复水后各品种叶绿素荧光参数的恢复情况,明确不同咖啡品种的抗旱性,为加强抗旱育种的针对性和节水栽培的有效性提供理论依据。
1 材料与方法
1.1 材料
试验地点位于云南省保山市隆阳区潞江镇(21°59′N,98°53′E),属南亚热带半干旱季风气候,年均温21.3℃,绝对最高气温40.4℃,绝对最低气温0.2℃,>10℃积温7 694℃,年均降雨量751.4 mm,降雨集中在6~10月份,年均蒸发量2 101.9 mm,年日照时数2 328 h,相对湿度70%。
材料:小粒种咖啡(Coffea arabicaL.)卡蒂姆系列的4个品种(卡蒂姆1、卡蒂姆2、卡蒂姆3、卡蒂姆4),各品种均为2年生咖啡苗。
仪器:叶绿素荧光参数用调制叶绿素荧光仪(英国汉莎FMS-2),手持叶绿素测定仪(浙江托普TYS-B)。
1.2 方法
1.2.1 干旱处理
采用疼痛视觉评估方法(VAS)进行评价,分值分布在0-10分,0分表示患者无疼痛感,10分表示患者疼痛剧烈,无法忍受,分数越高表示患者疼痛程度越深。采用QLQ-C30生活质量量表对患者进行评价,总分为100分,分数越高则表示患者的生活状况越好。
试验时间于2018年4~5月,采用盆栽方式进行,规格为上口直径24 cm、底部直径20 cm、高20 cm的塑料盆。盆栽用的土壤为0~30 cm试验地点大田表层土,风干过筛后混匀。土壤为冲积母质发育的沙壤土,pH7.11,有机质含量10.30 g/kg,全氮0.074%,水解氮71.60 mg/kg,有效磷17.70 mg/kg,速效钾83 mg/kg。每盆底部用纸封口,装入6 kg土和60 g羊粪,混匀。每盆种植1株,每个品种6株,共24株。整个试验在温室中进行,温室中有通风措施。试验材料在温室中培养2周,适应温室中的环境,每天下午浇透水。2周后干旱处理,采用持续不浇水。持续干旱15 d后,分为二组,A-1组和A-2组,每组每个品种3棵。A-1组直接复水,复水6 d后结束;A-2组再持续干旱3 d,然后复水,复水6 d后结束。
1.2.2 功能性状测定
叶绿素含量测定:用手持叶绿素测定仪(浙江托普TYS-B)测定第4对叶子的叶绿素含量(Soil and Plant Analyzer Development,SPAD),每株测10次,取平均值。
叶绿素荧光参数测定:每次早上9:00开始测定,用饱和脉冲100 μmol/(m2·s)测定光适应下的实际光化学效率(ΦPSII)、光合电子传递速率(ETR),暗适应下15 min后光系统II的最大光化学效率(Fv/Fm),各参数直接从仪器FMS-2中直接导出,每株测定从顶端数第4对叶子,重复3次,取平均值。
1.3 数据统计
采用Excel 2003进行数据整理和制图,测定指标用SPSS 19.0进行分析。
2 结果与分析
2.1 咖啡叶片SPAD值的变化
2.1.1 干旱15 d及复水对咖啡叶片SPAD的影响
由表1可知,在试验干旱前,4个卡蒂姆品种的SPAD有一定的差异,卡蒂姆2和4无显著差异,与卡蒂姆1、3有显著差异(p<0.05)。干旱15 d后测得SPAD值,除了卡蒂姆1外,其他3个品种均比试验开始时有增加,卡蒂姆3增幅最大;卡蒂姆1、2无显著差异,卡蒂姆3和4与它们之间有显著差异。复水后第3天测得的SPAD值,较试验开始及干旱15 d测得的SPAD值下降,卡蒂姆3下降幅度最大;卡蒂姆2、3、4间无显著差异,与卡蒂姆1有显著差异。复水后第6天所测得的SPAD值,比复水后第3天有所增加,卡蒂姆2增加数值最大,且卡蒂姆2恢复到试验开始的98.41%,其他品种分别为84.05%、86.64%和96.28%,卡蒂姆2、3、4无显著差异,卡蒂姆1、4无显著差异(p<0.05)。

表1 A-1组干旱15 d及复水后SPAD变化
2.1.2 干旱18 d及复水对咖啡叶片SPAD的影响
由表2可知,干旱18 d后所测的SPAD值均比试验开始时降低,各品种较原始值下降幅度分别为20.45%、10.88%、20.46%和9.04%,卡蒂姆1和3降低幅度最大,卡蒂姆2、3、4无显著差异,与卡蒂姆1有显著差异(p<0.05);复水后第3天,除了卡蒂姆4外,其他3个品种的SPAD值均有所降低,卡蒂姆2降低幅度最大,卡蒂姆3、4无显著差异,卡蒂姆1、2无显著差异,卡蒂姆1、2和卡蒂姆3、4有显著差异;复水后第6天,较复水后第3天均有所增长,卡蒂姆3增长幅度大,各品种的恢复到初始值的79.12%、82.39%、86.62%和95.26%,卡蒂姆3、4无显著差异,卡蒂姆1、2无显著差异,卡蒂姆1、2和卡蒂姆3、4有显著差异。
SPAD值的大小是衡量叶片中叶绿素含量变化情况。干旱胁迫15 d后SPAD值增加,但干旱胁迫18 d后SPAD值下降,所以适度的干旱胁迫可以使SPAD值上升,但是过度胁迫后SPAD值降低;从干旱胁迫15 d后复水的情况和干旱胁迫18 d后复水的情况,SPAD增长情况也有所不同。表明不同干旱胁迫程度,植物生长恢复速度也有所不同,适度干旱对植株生长有促进作用,严重干旱时叶绿素含量才减少。

表2 A-1组干旱18 d及复水后SPAD变化
2.2 咖啡叶片叶绿素荧光参数的变化情况
2.2.1 干旱及复水对咖啡叶片叶绿素荧光参数Fv/Fm的影响
由图1可知,未胁迫前各咖啡品种的Fv/Fm值均在0.7以上,数值分别为,0.72、0.71、0.71、0.76,卡蒂姆4和卡蒂姆2、3有显著差异,卡蒂姆1和其他品种无显著差异(p<0.05)。干旱胁迫后各咖啡品种的Fv/Fm值不同程度降低,且随着干旱时间的延长呈继续下降趋势;干旱15 d时,卡蒂姆1和2的Fv/Fm值下降幅度较大,卡蒂姆3和4下降幅度较小;品种间差异:卡蒂姆1(数值为0.34)和卡蒂姆3(数值为0.52)、4(数值为0.58)显著差异,卡蒂姆2(数值为0.41)和4(数值为0.58)显著差异(p<0.05)。由图2可知,干旱18 d时,各品种的Fv/Fm值继续下降,与干旱15 d相比,下降最大的是卡蒂姆1,下降幅度为57.01%(数值为0.15),其他3个品种的下降幅度分别为36.21%(数值为0.26)、22.16%(数值为0.41)和15.76%(数值为0.49),各品种间差异显著(p<0.05)。
复水后,各品种的Fv/Fm值恢复速度也不相同,恢复的程度也有所不同,且均没恢复如初。由图1可知干旱15 d后复水6 d,各品种的Fv/Fm值均有不同程度回升,分别恢复到初始值的97.65%(数值为0.70)、98.98%(数值为0.68)、92.57%(数值为0.65)、88.85%(数值为0.68),各品种间无显著差异(p<0.05)。由图2可知,干旱18天后复水6 d,各品种的Fv/Fm值都有所回升,分别恢复到初始值的 72.81%、93.66%、84.41%、89.51%,卡蒂姆1(数值为0.52)和3(数值为0.60)显著差异,卡蒂姆2(数值为0.66)和4(数值为0.68)无显著差异,卡蒂姆1、3和卡蒂姆2、4显著差异(p<0.05)。
整个试验过程中,干旱胁迫时和复水后卡蒂姆4的Fv/Fm值波动不大,且Fv/Fm值一直居高,变幅也较缓慢。
2.2.2 干旱及复水以后咖啡叶片叶绿素荧光参数ΦPSII的变化
由图3可知,未胁迫前各咖啡品种的ΦPSII数值分别为0.74、0.71、0.73、0.74,卡蒂姆2和其他3个品种有显著差异(p<0.05)。干旱胁迫导致各咖啡品种ΦPSII值不同程度的降低,且随着干旱时间的延长呈快速下降趋势。由图3可知,干旱15 d时,卡蒂姆1(数值为0.28)和2(数值为0.33)快速下降,卡蒂姆3(数值为0.58)和4(数值为0.55)降幅降幅较小,降幅较初始值分别为 61.82%、53.97%。20.98%、26.09%;品种间差异:除了卡蒂姆2和3无显著差异外,品种间存在显著差异(p<0.05)。由图4可知干旱18 d时,各品种的ΦPSII值继续下降,降幅较初始值分别为75.97%(数值为0.18)、47.94%(数值为0.37)、43.66%(数值为0.41)和28.32%(数值为0.53);卡蒂姆3较干旱15 d时下降明显,不同品种间差异显著(p<0.05)。
复水后各品种ΦPSII值都有所回升。从图3看出,干旱15 d复水6 d后卡蒂姆3(数值为0.64)和4(数值为0.69)恢复缓慢,卡蒂姆1(数值为0.72)和2(数值为0.69)恢复较快;各品种复水6 d后分别恢复到初始值的98.24%、97.23%、86.99%和93.19%;除了卡蒂姆2和4无显著差异外,品种间存在显著差异(p<0.05)。由图4可看出,干旱18 d复水6 d后各品种ΦPSII值都有了明显的回升;卡蒂姆1(数值为0.55)、2(数值为0.69)、3(数值为0.61)和4(数值为0.72)分别恢复到初始值75.13%、96.22%、83.35%和97.79%;各品种间存在显著差异(p<0.05)。
整个试验过程中,干旱15 d卡蒂姆3的ΦPSII值变化波动较小,干旱18 d时卡蒂姆4的波动较小。卡蒂姆4的ΦPSII值在整个试验过程中居高。
2.2.3 干旱及复水后咖啡叶片叶绿素荧光参数ETR的变化
由图5可知,未胁迫前各咖啡品种的ETR数值分别为3.85、2.88、3.08、3.91,卡蒂姆1、4和卡蒂姆2、3有显著差异(p<0.05)。干旱15 d时各品种光合电子传递速率ETR值较初始值下降幅度分别为61.29%、45.78%、21.23%和35.98%,数值分别为1.12、1.56、2.43、2.50,各品种间存在显著差异(p<0.05);由图6可知,随干旱时间延长,各品种ETR值继续降低,干旱18 d时较初始值降幅为74.30%、51.20%、43.29%和41.30%,数值分别为0.74、1.41、1.75、2.29,各品种间存在显著差异(p<0.05)。

图1 A-1组干旱及复水后咖啡叶片叶绿素荧光参数Fv/Fm的变化
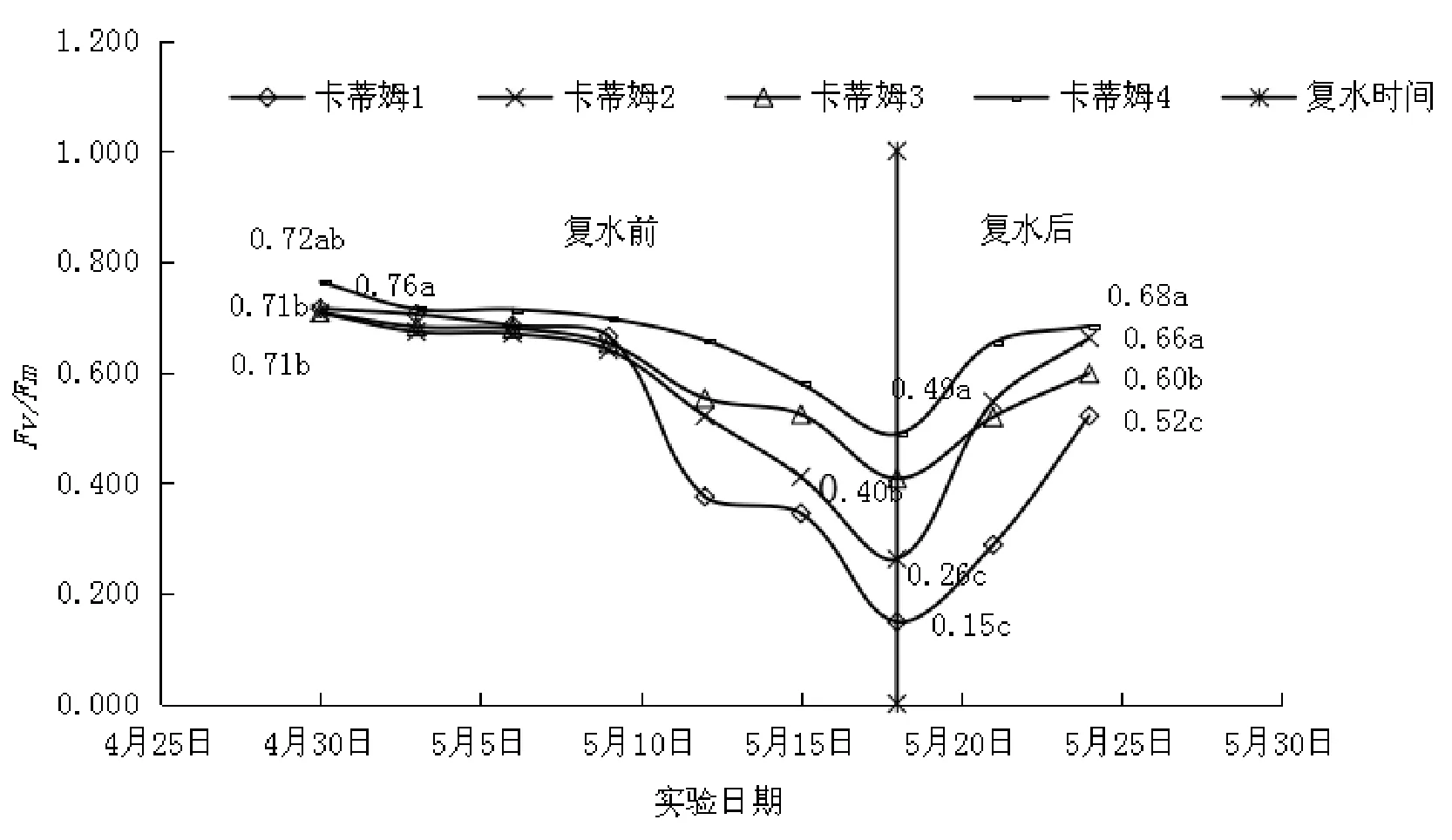
图2 A-2组干旱及复水后咖啡叶片叶绿素荧光参数Fv/Fm的变化
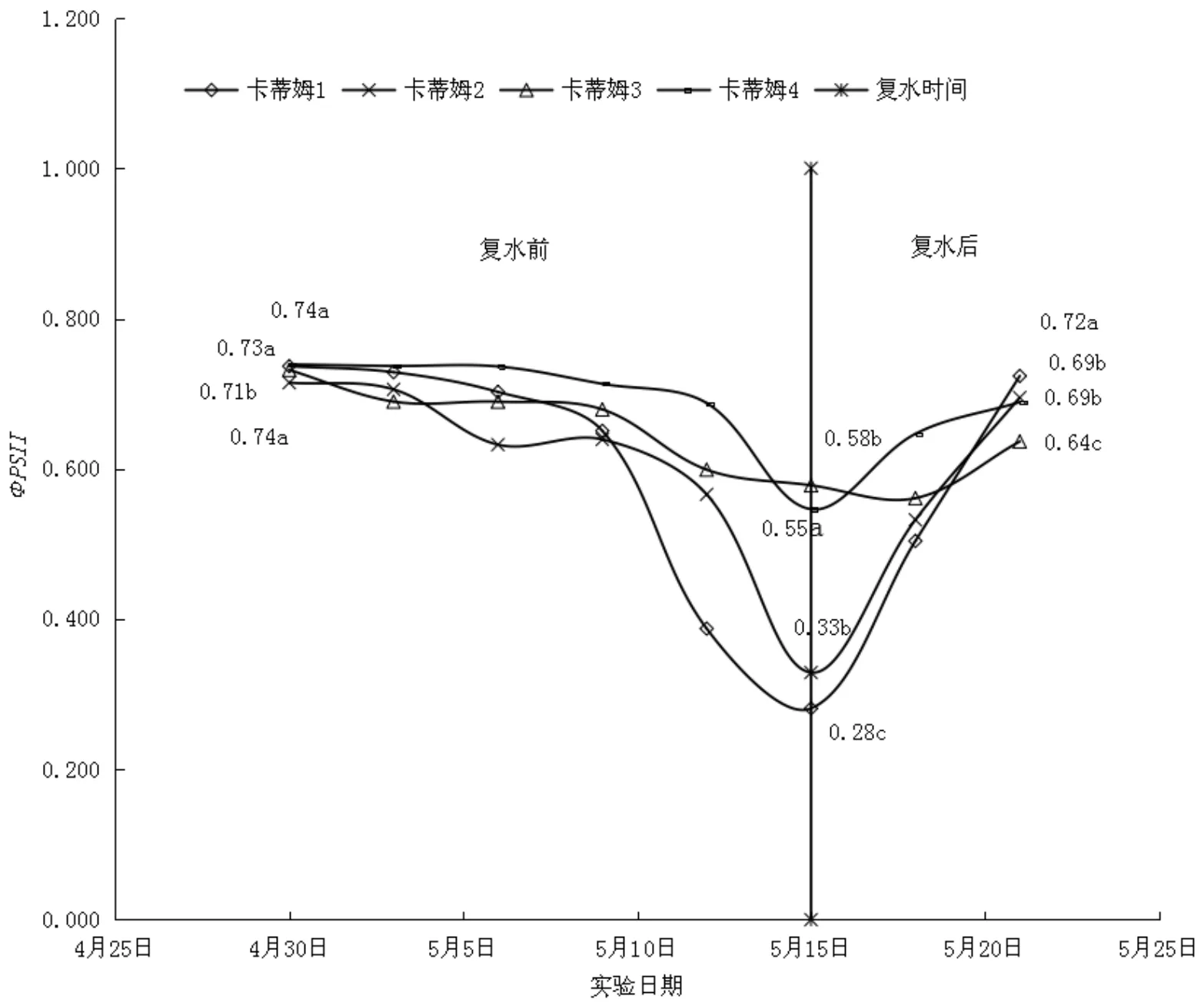
图3 A-1组干旱及复水后咖啡叶片叶绿素荧光参数ΦPSII的变化
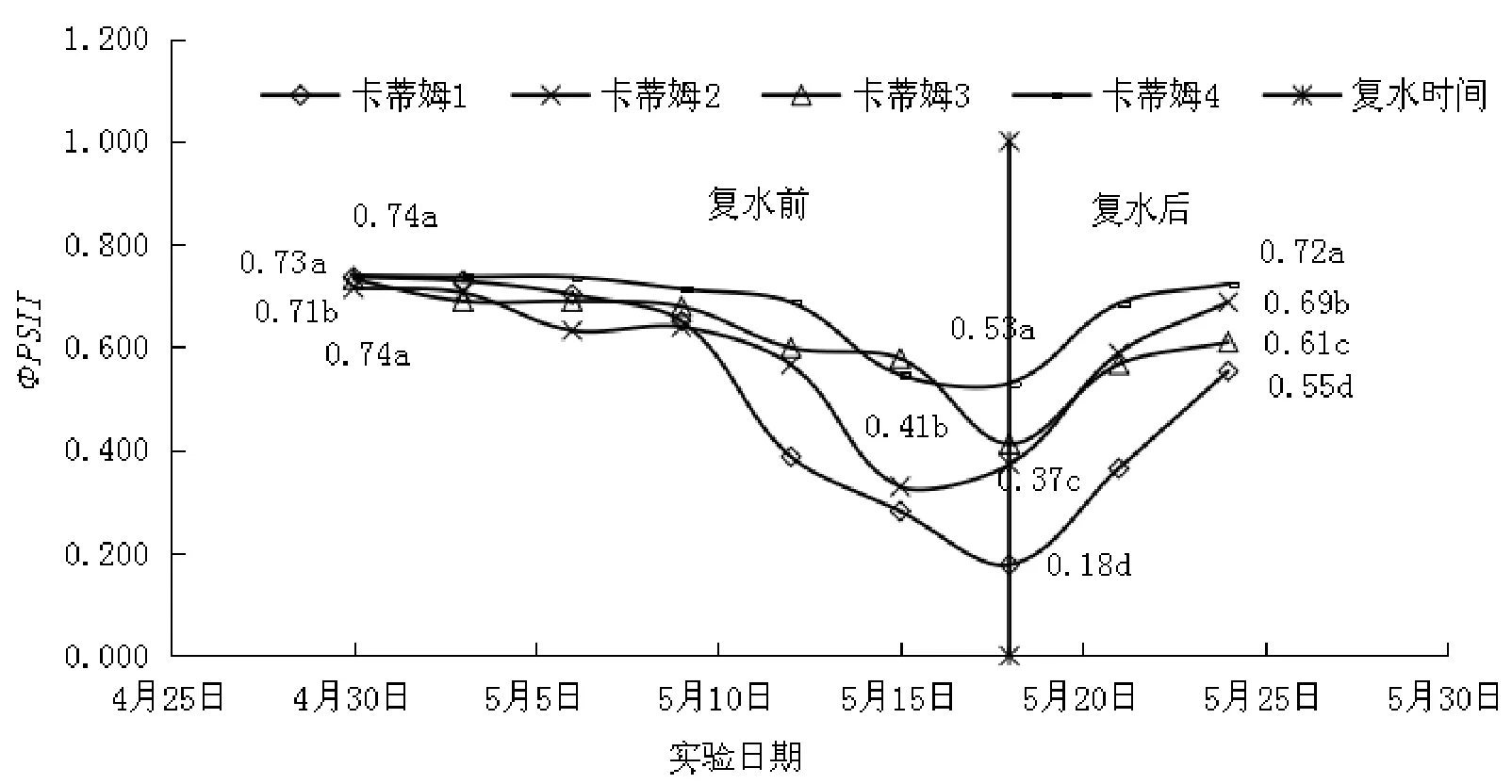
图4 A-2组干旱及复水后咖啡叶片叶绿素荧光参数ΦPSII的变化
由图5可知,复水后第3天卡蒂姆1、2和4的ETR值上升幅度较大,复水第6天时各品种恢复到初始值的 90.88%、121.53%、103.98%和 88.84%,数值分别为3.50、3.50、3.21、3.47;卡蒂姆2、3的ETR值超过了初始值,表明复水后ETR值恢复能力较强。由图6可看出,复水后第3天卡蒂姆2恢复速率最大;复水后第6天各品种恢复到初始值的84.36%、105.26%、91.36%和85.46%,数值分别为2.44、3.03、2.82、3.34,卡蒂姆2恢复超过原有水平。
整个试验过程,卡蒂姆4的ETR值都高于其他品种,表明其光能转化效率和光电子传递效率较强。
3 讨论与结论
3.1 讨论
叶绿素是绿色植物参与光合作用的重要色素,其含量的高低反映了植株光合能力和生长状况[8],故通过研究干旱胁迫对植物叶绿素含量的影响,可分析抗旱性能的差异[9]。SPAD值是一项表征叶片光合活性的指标,它与单位叶面积的叶绿素含量及叶绿素的密度显著正相关[10-11],因此常用SPAD值的大小来衡量叶片中叶绿素含量的情况[12]。本次试验中,干旱15 d时卡蒂姆1的SPAD值略小于试验开始所测得数值,而卡蒂姆2、3、4的SPAD值均高于试验开始所测得数值,和吴际友对红椿的试验结果相似[13];干旱18 d时各品种均低于试验开始和干旱15 d所测得数值,与陈雪妮对蓝莓的研究结果一致[14]。试验结果表明,在一定范围内的干旱胁迫,咖啡叶片的SPAD值先增加,超过范围后SPAD值减少;在一定程度的干旱胁迫下,植物体内水分降低,造成单位叶面积的叶绿素含量升高[9,15-16],干旱胁迫加深时,叶绿体遭到破坏[17-18],或叶绿体合成受到阻碍或抑制,从而使叶绿素含量降低[19],降低了对光能的利用。本次试验中复水后4种咖啡的叶绿素含量相对于干旱胁迫时数值均有所增加,说明复水对这些植物均有不同程度的补偿作用。
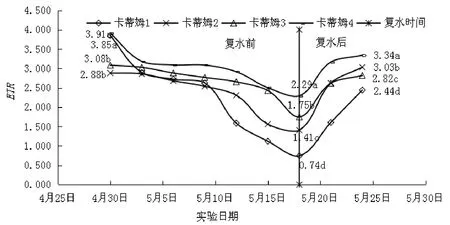
图6 A-2组干旱及复水后咖啡叶片叶绿素荧光参数ETR的变化
Fv/Fm是PSⅡ的最大光化学效率,常用于说明植物叶片PSⅡ原初光能转换效率。一般来说,植物在非胁迫生长条件下,叶绿素荧光参数Fv/Fm值一般在0.70以上。Fv/Fm值越高,光化学效率越高,叶片的光合作用越强[11]。植物在胁迫生长条件下,叶绿素荧光Fv/Fm低于 0.7[2,20],说明植物受到光抑制,反应中心受到不可逆破坏或可逆失活[21-22],下降程度越高,抑制作用越大,胁迫程度越高。
ΦPSII表示PSII实际光能转化效率,表示进入PSII反应中心的光能中用于光化学反应的光能所占比例,可以作为植物叶片光合电子传递速率快慢的相对指标。高的ΦPSII有利于提高作物的光能转换效率,为暗反应的碳同化积累更多的能量,其值降低说明光合机构受到抑制[23-24]。
由本研究结果可知,干旱胁迫均使各参度品种的ΦPSII、Fv/Fm和ETR降低,说明捕光蛋白复合体被破坏,使得电子传递受阻,光能转化效率降低[5],参数的下降幅度越大,抗旱性越弱[17]。干旱15 d时Fv/Fm、ΦPSII和ETR的降低程度顺序为:卡蒂姆1>卡蒂姆2>卡蒂姆4>卡蒂姆3;干旱18 d时Fv/Fm、ΦPSII和ETR的降低程度顺序为:卡蒂姆1>卡蒂姆2>卡蒂姆3>卡蒂姆4。表明卡蒂姆1和2对干旱敏感,受到水分限制较大[5];干旱时间越长,各参数下降程度越大;复水后ΦPSII、Fv/Fm和ETR升高,说明干旱胁迫并未对光系统造成不可逆的抑制[10],但未恢复到未胁迫前,可能是恢复时间不够或此时的干旱胁迫对咖啡品种光系统还是带来了一定的损伤,且不同程度的干旱,各参数恢复情况也不同。
随着干旱程度的加深,叶绿素荧光参数ΦPSII和Fv/Fm的变化趋势与李伟成等[25]对浙江楠的研究结果一致,叶绿素荧光参数ETR和Fv/Fm的变化趋势与李晓梅等[26]对辣椒的研究结果一致。植物的抗旱性是植物在干旱条件下的生存能力,以及在干旱解除以后迅速恢复的能力,理想抗旱作物品种,不但要求植物在操受干旱胁迫过程中能够尽量减少干旱胁迫对植物的伤害,而且要求一旦有降水或灌溉,又能够从干旱伤害中迅速恢复生长[20]。
3.2 结论
SPAD是植株抗旱指标之一[9]。本研究结果得出,适度干旱时,卡蒂姆2和4均表现良好,而干旱程度再加深时,卡蒂姆4表现良好。根据干旱胁迫时叶绿素荧光参数的变化,得出干旱15 d时,卡蒂姆3和4表现良好,抗旱性强;干旱18 d时,卡蒂姆4抗旱性更好一些,结合复水后不同咖啡品种的恢复情况,卡蒂姆4抗旱性较好。
