磁场作用下葡萄糖近红外光谱检测技术研究
2019-12-05陈剑虹刘泽晨朱凌建
陈剑虹 ,刘泽晨,朱凌建
(西安理工大学 机械与精密仪器工程学院,陕西 西安 710048)
糖尿病是由于体内胰岛素缺乏或作用缺陷而出现的一种以高血糖为特征的代谢性综合疾病,是严重威胁人类的四大疾病之一[1]。目前近红外光谱分析技术得到了日益发展,已被广泛应用于农业、食品卫生、石油化工、生命科学等诸多领域[2]。近年来,国内外有众多学者致力于应用近红外光谱进行血糖分析的研究[3-5]。
庞小峰等[12]研究了磁场对乙醇和乙醇-水溶液红外光谱的影响,发现磁场可增强乙醇溶液分子间氢键,进而影响分子基团的振动;Chang等[13]利用分子动力学模拟研究外部磁场对液态水结构的影响,发现随着磁场强度的增加,氢键的数量略有增加;李滚等[14]研究了静磁场曝露作用30 d后对大鼠脑组织红外光谱特征的影响,发现大鼠脑组织部分红外吸收峰发生位移。上述研究说明磁场影响有机物分子的物理特性与近红外光谱。在磁场作用下,一方面分子可能获得附加能量,另一方面,可以对物质分子间力产生影响,使分子的受力方向和自由能发生改变。关于磁场作用对葡萄糖红外光谱检测的影响尚未见报道。本文采用傅立叶变换红外光谱(FTIR)对不同磁场强度下不同浓度葡萄糖溶液的近红外光谱进行采集,分析了磁场对葡萄糖溶液近红外光谱吸收的影响,并运用偏最小二乘回归(PLS)建立葡萄糖溶液定量分析模型进行验证,对不同磁场强度下的模型参数进行了对比分析,以期在外加磁场的作用下提高测量精度。

图1 静磁场Fig.1 Static magnetic field
1 实验部分
1.1 仪器与试剂
采用德国布鲁克公司生产的Tensor 37傅立叶变换近红外光谱仪,卤素灯近红外光源,BT100-1F蠕动泵(保定兰格恒流泵有限公司),光谱仪扫描次数设置为16次,仪器分辨率为4 cm-1,波数范围为800~2 500 nm;光程为1 mm样品池安放在恒温装置内(PIKE公司),整个测量过程中保持25 ℃恒温。静磁场由钕铁硼磁铁构成,采用PCE-MFM3000高斯计测量,磁场中心强度范围为100~1 000 mT,磁场夹持在蠕动泵进样管上,如图1所示。BSA124S微量电子天平(精确至0.1 mg,北京赛多利斯仪器有限公司)。
采用天津巴斯夫化工有限公司生产的分析纯级葡萄糖和蒸馏水配制相关溶液。
1.2 实验方法
配制质量浓度为100~2 000 mg/dL的葡萄糖溶液样品作为对照组(第1组)。第2、3、4组溶液质量浓度不变,分别在蠕动泵的进液管上加持0~870 mT的静磁场。
样品池采用蠕动泵进样。整个样品池被置于光谱仪内,测量在25 ℃恒温下进行,每组样品随机抽取。单个样品扫描3次。随机选取60个样品光谱作为校正集,其余20个样品光谱作为预测集建模,以消除人工操作对测量结果的影响。
2 结果与讨论
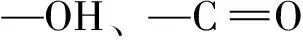
2.1 磁场对葡萄糖溶液近红外光谱的影响
800 mT静磁场作用前后1 000 mg/dL葡萄糖的近红外光谱(扣除水背景)如图2所示。可以观察到,经磁场作用后,葡萄糖溶液的近红外光谱发生了显著改变(红色光谱),不仅在整个近红外范围内吸收强度明显增加,而且部分特征吸收峰的峰位也发生了偏移。
红外光谱谱带强度的影响因素主要有两个:一是偶极矩变化程度,二是能级跃迁概率。偶极矩变化与分子(或基团)本身的偶极矩有关,振动方式不同的相同基团的各种振动,其分子电子云分布不同,偶极矩变化也不同。通常情况下,伸缩振动的吸收强度比变形振动的吸收强度大。当葡萄糖分子处于磁场中时,外加磁场作用于葡萄糖分子内的原子核和核外电子,改变了分子电子云分布的形状,产生诱导偶极矩,导致偶极子矩跃迁的变化和分子的振动态以及电子跃迁概率的变化,葡萄糖分子因此获得附加能量。表1给出了葡萄糖不同基团分子振动频率吸光度与浓度变化线性关系的斜率,在磁场作用下,不同振动方式均得到增强,其中第一倍频区斜率的增长率大于合频区,这主要是因为第一倍频区吸收完全由C—H键伸缩振动产生,而合频区吸收则是由葡萄糖分子中O—H键的伸缩和C—H键伸缩和弯曲振动产生的。
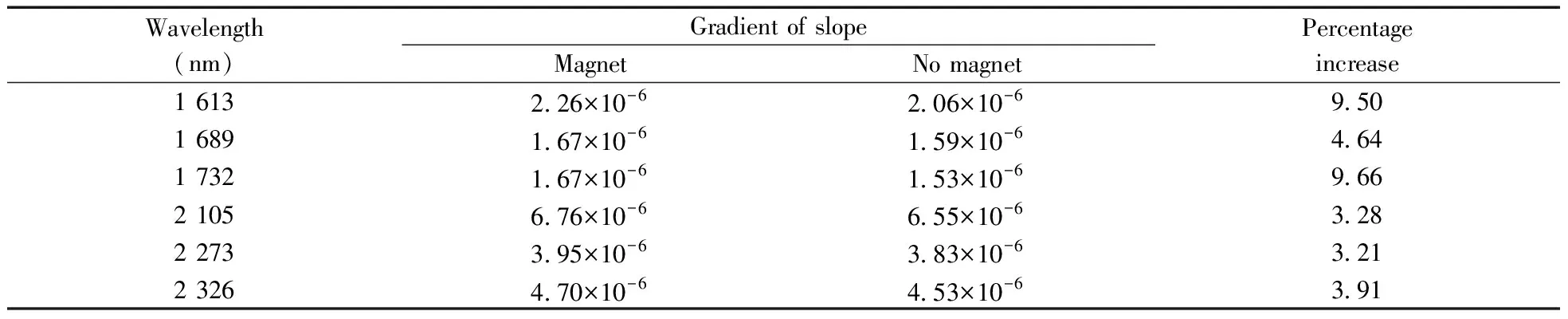
表1 磁场作用下葡萄糖特征吸收峰的吸光度增长率Table 1 Increasement of glucose absorbance at characteristic wavelengths due to effect of magnetic field
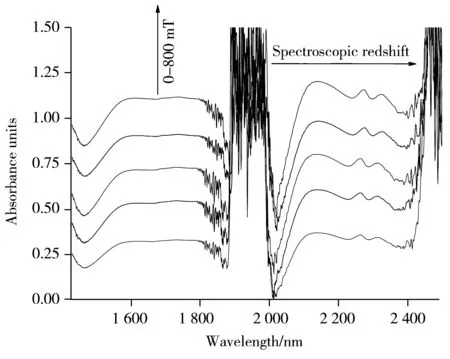
图3 不同磁场强度下同一浓度葡萄糖溶液归一化吸收光谱Fig.3 Normalized absorption spectra of glucose solution of the same concentration under different magnetic fields intensity

2.2 磁场对葡萄糖预测模型精度的影响
为了定量分析磁场对葡萄糖溶液浓度预测模型的影响,利用偏最小二乘回归法进行建模分析,选取80组光谱数据进行建模(60个样品光谱作为校正集,其余20个样品光谱作为预测集),分别分析无磁场、460 mT、800 mT磁场作用下的预测模型。
选择2 088~2 353、1 550~1 835、834~1 333 nm波长区间,不同磁场条件下模型参数比较如表2所示。

表2 不同磁场强度下模型参数比较Table 2 Comparison of model parameters under different magnetic fields intensity
通过比较建模预测结果(表3),发现无磁场25 ℃恒温条件下最大误差为-129.74 mg/dL,最小误差为2.23 mg/dL,平均误差为-13.46 mg/dL;800 mT磁场条件下最大误差为-34.41 mg/dL,最小误差为-0.10 mg/dL,平均误差为-0.55 mg/dL。可以看出,在磁场作用后预测模型的精度高于无磁场条件。进一步分析计算葡萄糖不同基团分子振动频率(特征吸收峰)的吸光度与浓度变化的线性关系,发现在静磁场的作用下,两者的线性关系得到极大改善。这是因为磁场改变了葡萄糖分子的受力方向和自由能[15-16],葡萄糖分子趋向于沿平行于磁场的方向排列,并且随着磁场强度的增强,越来越多的分子排列倾向于平行磁场方向,分子结构规整性变好,最终使得葡萄糖分子相对于外加磁场方向择优取向,证实磁场可对葡萄糖分子近红外光谱吸收强度产生影响,并有助于提高建模精度。
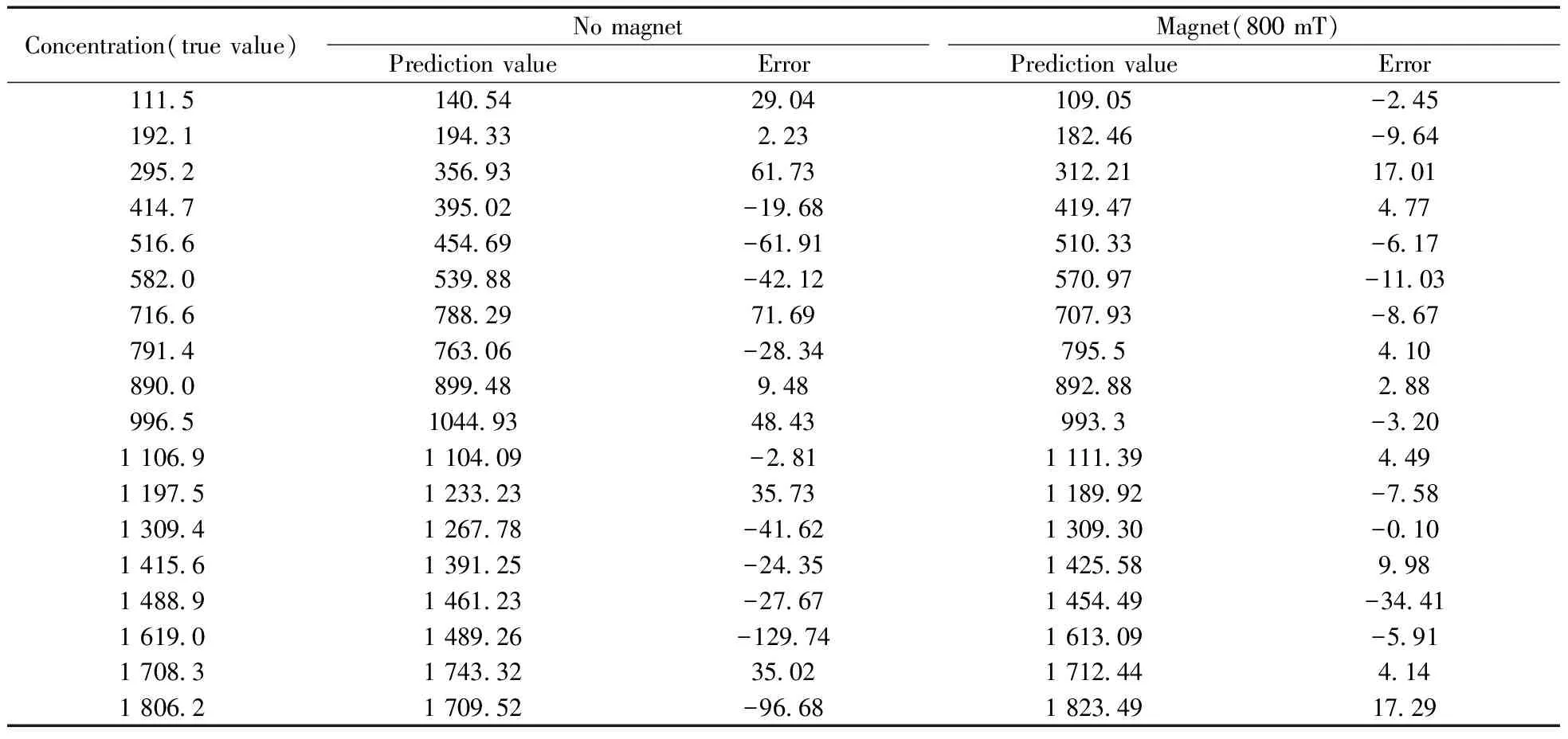
表3 不同磁场强度下建模结果比较Table 3 Comparison of modeling results under different magnetic field intensity (mg/dL)
(续表3)

Concentration(true value)No magnetMagnet(800 mT)Prediction valueErrorPrediction valueError1 901.51 880.51-20.991 916.1214.621 983.31 916.76-66.541 982.20-1.10
3 结 论
磁场作用于葡萄糖溶液,葡萄糖分子的近红外吸收强度明显提高,其羟基与水分子间的氢键缔合得到加强,分子特征吸收峰吸光度与浓度变化线性关系一致性得到极大的改善,并且随磁场强度增强到一定程度后达到饱和。本研究有助于提高葡萄糖分子近红外光谱吸收强度及测量精度。
