多孔SnO2空心球材料的合成及甲醛气敏性能研究
2019-11-26程知萱王晓红徐甲强
李 娜,向 群,程知萱,王晓红,徐甲强
(1.上海大学 理学院化学系, 上海 200444; 2.上海民航职业技术学院 基础教学部,上海 200232)
0 引言
甲醛广泛存在于装修家居、纺织品和食品中,是对人体危害最严重的物质之一,人类如果经常接触甲醛则可能引发再生障碍性贫血、白血病等严重疾病,甚至患上癌症[1].目前检测甲醛的传感器主要为半导体金属氧化物气体传感器,SnO2(Eg=3.6 eV)作为一种宽带隙半导体金属氧化物,是半导体气体传感器领域中研究较为广泛的气敏材料[2].Xu等[3]通过在传统工艺中引入拓扑转换方法合成了SnO2微棒,在330 ℃下可以检测较低浓度的甲醛.但低维SnO2材料普遍存在高温下易团聚、性能不稳定以及重复性差等缺点,因此需要设计新型纳米结构的材料来满足气体传感器的市场需求[4].三维纳米材料由低维材料堆积而成,既有低维材料的优点,又能提高传感器的稳定性;其次,三维纳米材料比表面积大,气体分子在其表面扩散性好,这些特点都有利于优化传感器的气敏性能.Huang等[5]通过多步法获得了中空多孔SnO2立方块材料;Gu等[6]对花状Cu3SnS4材料进行退火来制备多孔花状SnO2纳米结构;Ren等[7]采用水热、煅烧和酸洗相结合的方法得到了三维SnO2材料,以上几种三维材料由于结构和形貌等因素提升了传感器的气敏性能.但值得注意的是,上述实验过程步骤复杂,因此需要开发简单便捷的方法来制备敏感材料.
笔者通过一步溶剂热法设计合成了三维多孔SnO2空心球纳米材料.气敏测试表明:该材料在210 ℃时对甲醛的响应值高达52.5,选择性较好.浓度梯度测试也表明:该材料在高温下性能稳定,可用于实际生活中甲醛气体的检测.
1 实验部分
1.1 实验方法
将0.384 g锡酸钾和0.48 g尿素加入到80 mL乙醇与水的混合溶液中(V乙醇∶V水=2.5∶5.5,3.0∶5.0,3.5∶4.5,4.0∶4.0),搅拌30 min后将溶液转移至100 mL反应釜中190 ℃反应15 h.反应后用乙醇和去离子水清洗所得产物并离心干燥.在本文中,按照V乙醇∶V水=2.5∶5.5,3.0∶5.0,3.5∶4.5,4.0∶4.0所得的样品分别命名为S-1,S-2,S-3,S-4.
1.2 气体传感器制造以及气敏测试过程
如图1(a)所示,测试所用的气敏元件为旁热式气体传感器.传感器制备工艺如下:将制备好的样品与松油醇在研钵中分别研磨以形成白色糊状物,然后将这些膏体均匀地涂覆在气敏元件表面.将涂覆好的气敏元件放在马弗炉中300 ℃下进行干燥以加速松油醇的挥发并提高气体传感器的稳定性,随后将Ni-Cr合金线圈作为加热器插入气敏元件内以调节气体传感器的工作温度.最后,把涂覆好的气敏元件焊在六孔底座上并在4.0 V的加热电压下老化7 d.通过WS-30 A气敏测量系统来测试材料的敏感性能,测试电路图如图1(b)所示,负载电阻(RL)与气体传感器组成串联电路.图中,Uc为电路电压;Uout为输出电压,通过Uout的改变来反映传感器电阻Ra和Rg的变化;Vh为加热电压.响应值R定义为:R=Ra/Rg(还原性气体)或R=Rg/Ra(氧化性气体),Ra和Rg分别为空气和气体中的电阻.把气体传感器从接触(脱离)被测气体开始到总体阻值变化的90%所用时间定义为响应(恢复)时间[8].
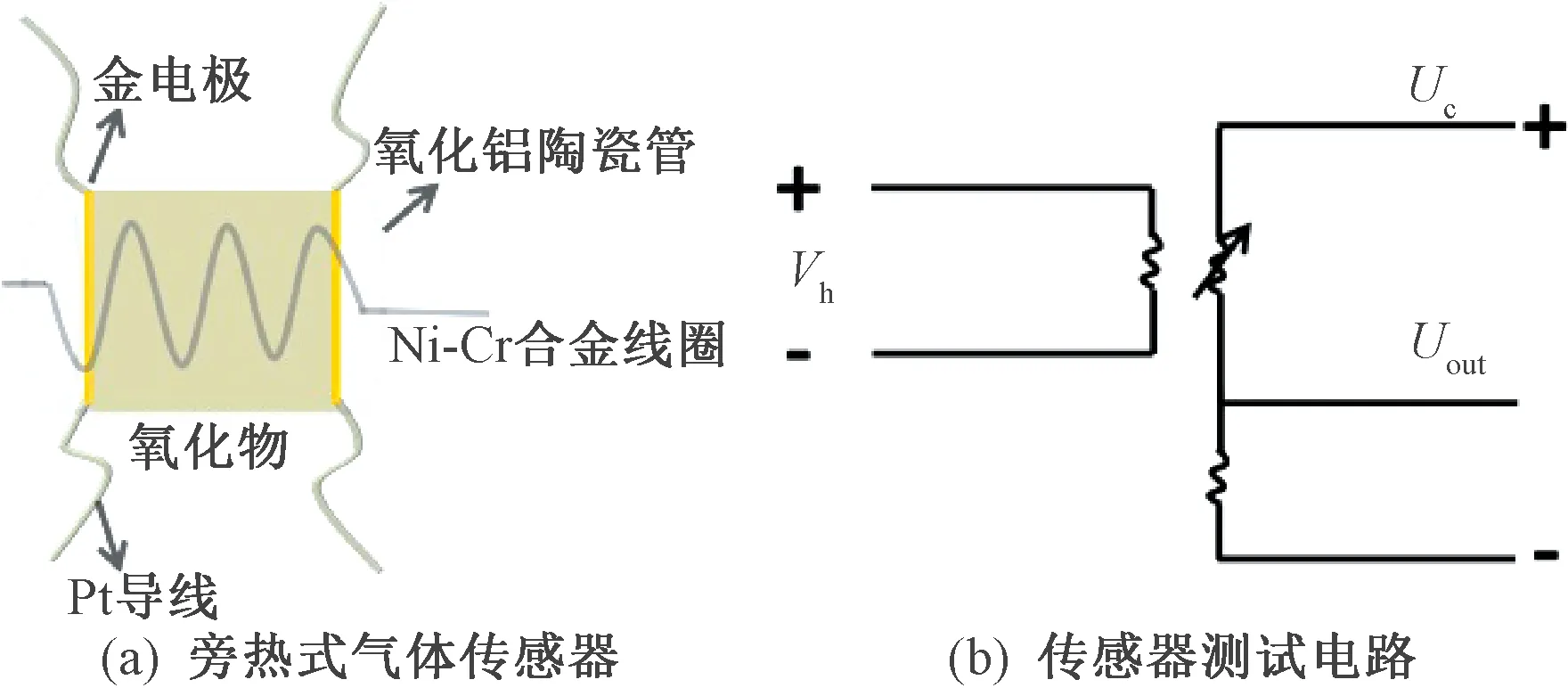
图1 气敏元件及测试电路
2 分析与讨论
2.1 XRD分析
合成样品的物相表征如图2所示.图中4种材料的主要衍射峰出现在26.71°、33.51°、52.11°和65°处,分别对应于金红石SnO2(JCPDS,No.41~1445)的(110)、(101)、(211)和(112)晶面[9].有趣的是,合成4种材料所用的溶剂配比不同,产物组分却大致相同,这表明溶剂配比对产物组成的影响较小.
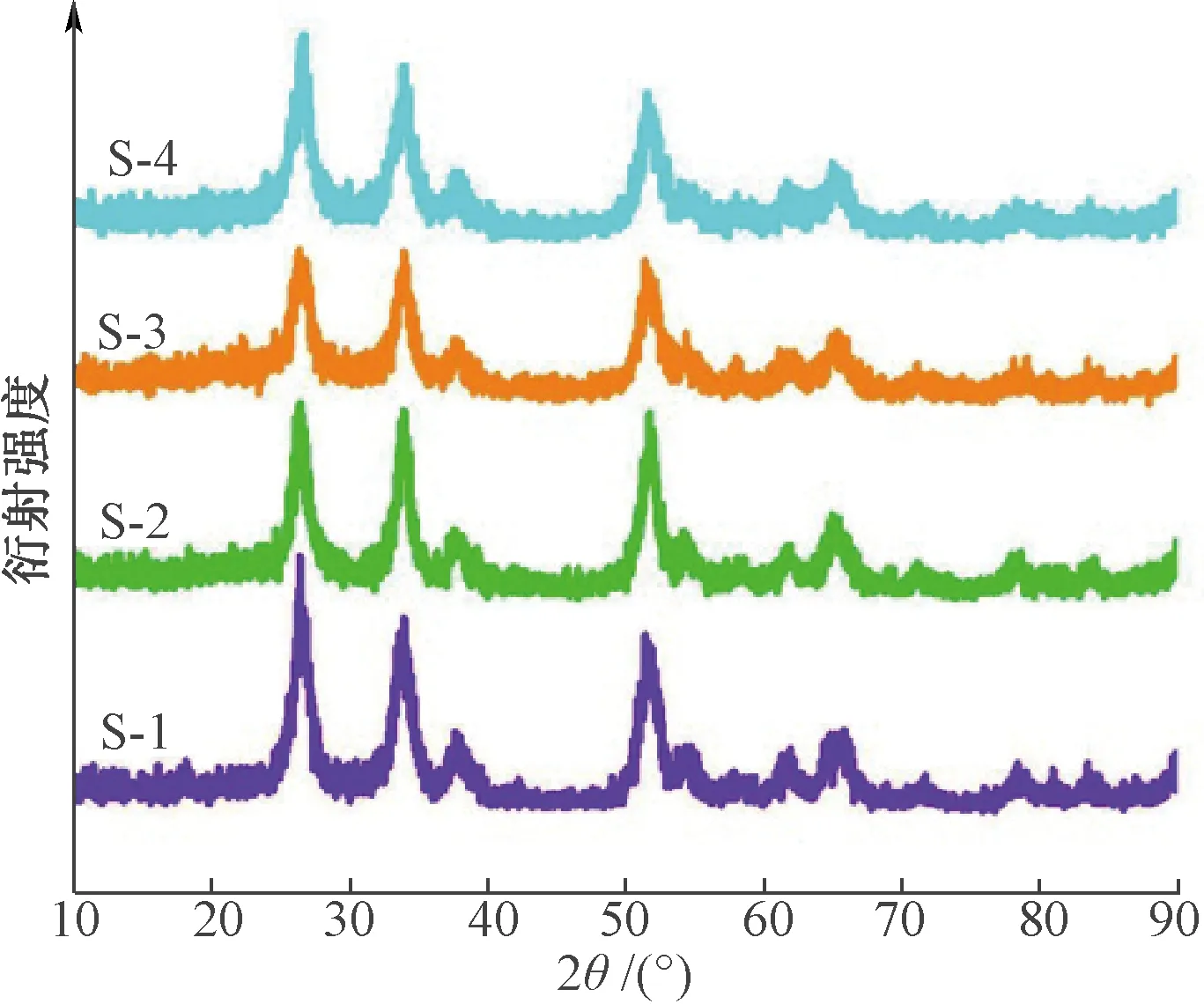
图2 样品的XRD图谱

图3 样品的SEM图像
2.2 SEM和TEM分析
图3为4种材料的扫描电镜图(SEM).图中,S-1呈块状堆积模式且无固定形貌,S-2为均一的球形结构,直径大约为400 nm.继续改变反应的溶剂比得到S-3和S-4,可以发现,两种材料的颗粒尺寸增大,且无序性增加.换句话说,乙醇与水配比的改变在很大程度上会影响产物的形貌.在乙醇的占比由小到大的过程中,样品的颗粒尺寸分布规律为大→小→大,而样品的均一性分布规律为低→高→低.故S-2材料形貌调控最为合适,形貌均一,颗粒尺寸较小,有助于提高材料的气敏性能.
图4为S-2材料的高分辨透射电镜(TEM)表征图.由图4(a)可以看出,S-2材料为均一的空心结构,壳层厚度大约为70 nm.在图4(b)中,S-2材料表面粗糙,且具有疏松多孔的三维结构,这种结构将有利于传感过程中的气体吸附,从而改善气敏性能[10].

图4 S-2样品的TEM图像
2.3 比表面积测试
图5为S-2材料的N2吸脱附曲线和BJH孔径分布图.吸脱附曲线中滞后环的出现表明材料中有孔的存在.在S-2材料的孔径分布图中,主要的峰位于19.92 nm处,表明材料中存在介孔结构.另外,计算出来的S-2材料的比表面积为107.25 m2·g-1,其数值远远大于一般的金属氧化物,这是由于材料的疏松多孔结构中存在大量的介孔,因此材料的比表面积较大,这也为传感过程中的气体接触提供了更多的表面.
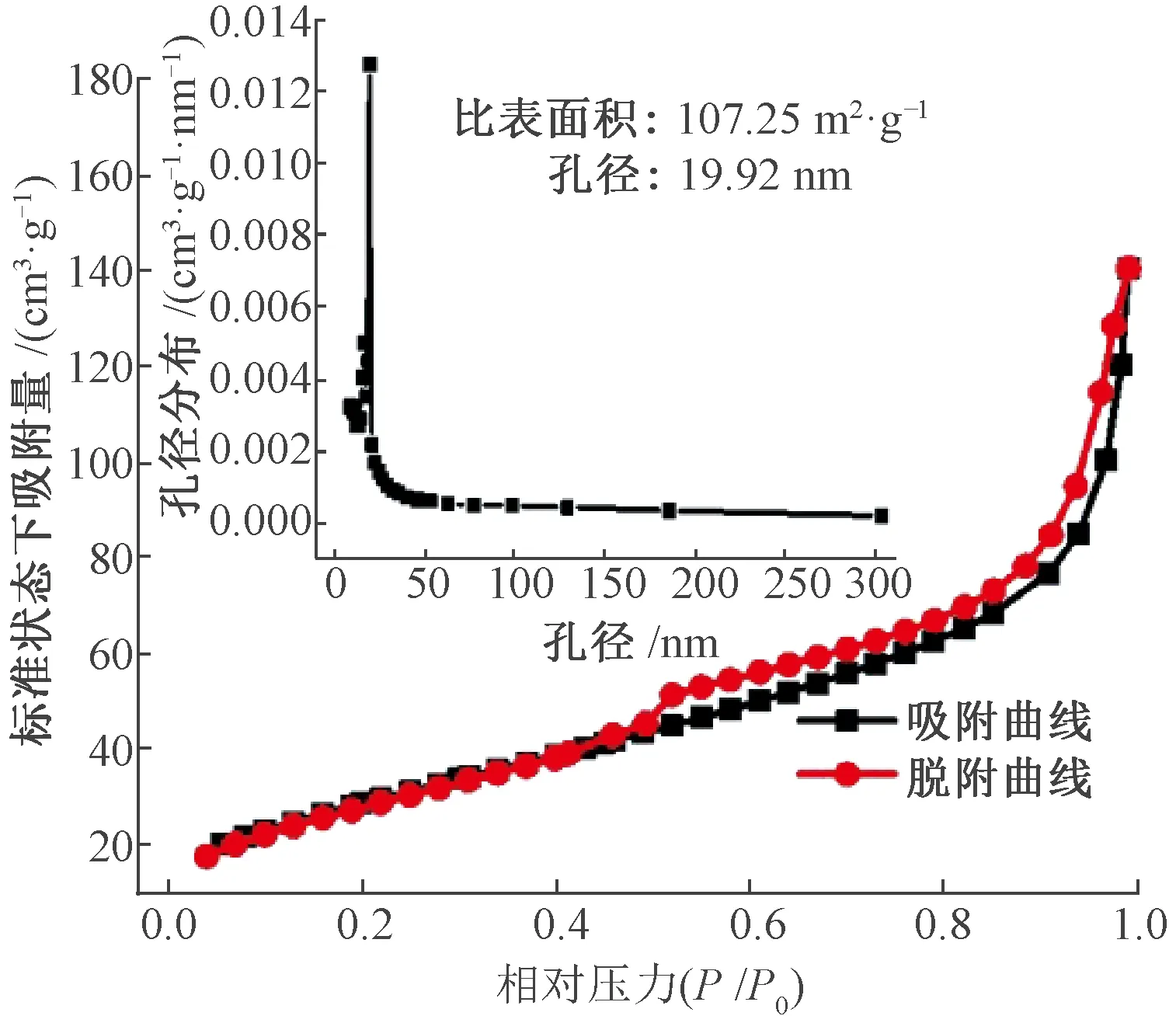
图5 S-2样品N2吸附-脱附等温线和BJH孔径分布
2.4 气敏性能测试
图6为4种材料的工作温度与响应值的关系(检测气体为50 mg/L甲醛).从图6可以看出,传感器的响应值很大程度上取决于工作温度.在210 ℃之前,传感器的响应值随着工作温度的增加而增大;在210 ℃以后,响应值呈现降低的趋势.因此,在接下来的测试中将4种材料进行气敏测试的最佳工作温度确定为210 ℃.
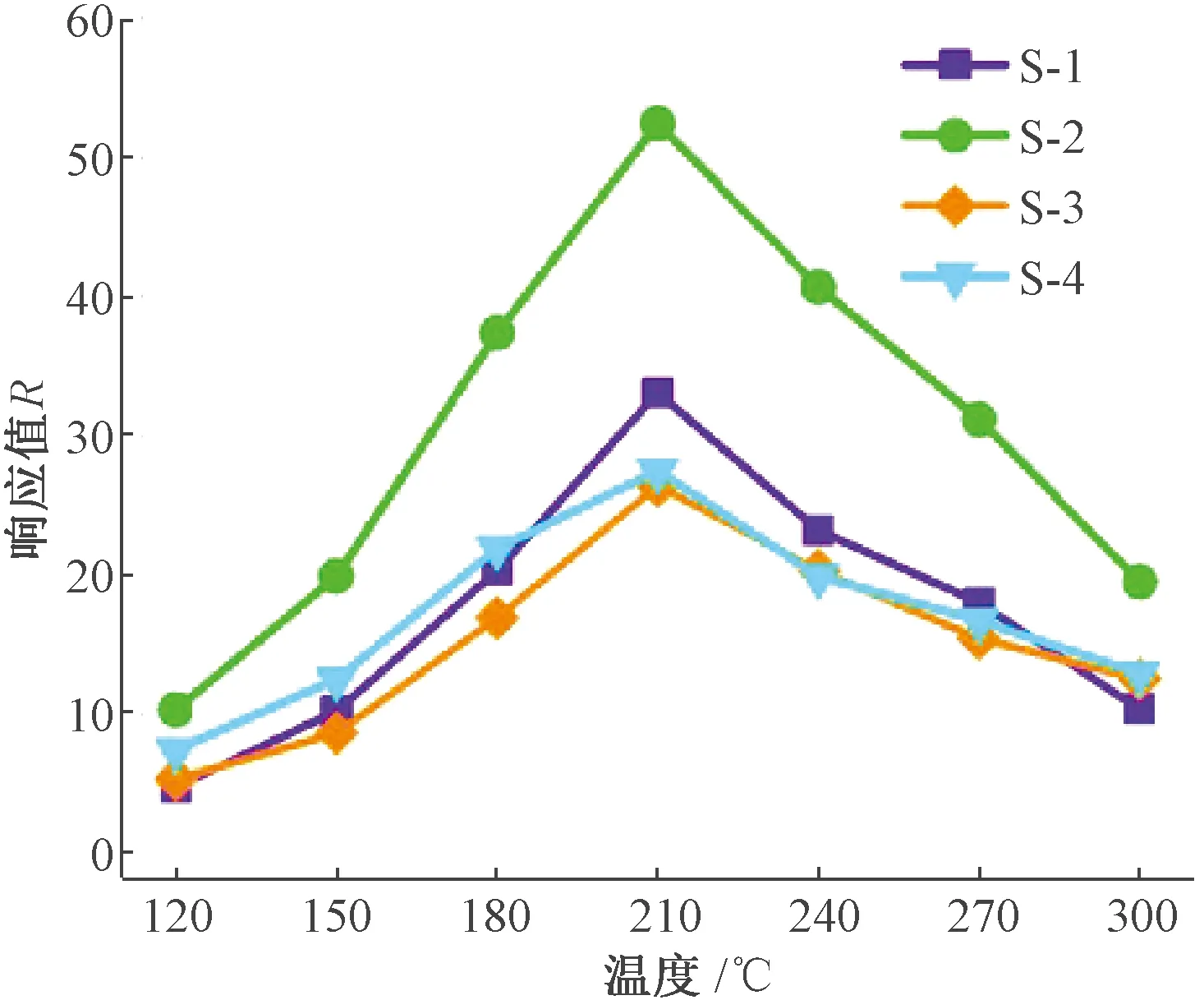
图6 传感器在不同温度下对50 mg/L 甲醛的响应值
S-1、S-2、S-3和S-4 4种气体传感器对1~50 mg/L甲醛的响应如图7所示.可以看出,随着气体浓度的增加,传感器的响应值也在逐渐增大.其中,S-2气体传感器对甲醛的响应值大约为其他传感器的1.5~2.0倍.当甲醛浓度低至1 mg/L时,S-2传感器的响应值仍为4.6.这一结果表明:S-2气体传感器可以用于低浓度甲醛的定量检测.插图为S-2气体传感器响应值与甲醛浓度的函数曲线,响应值R和气体浓度c之间的关系如下:
R=0.97c+5.31.
(1)
从拟合曲线中可以发现:实验数据和理论曲线具有较好的一致性,相关系数r2为0.987 44.
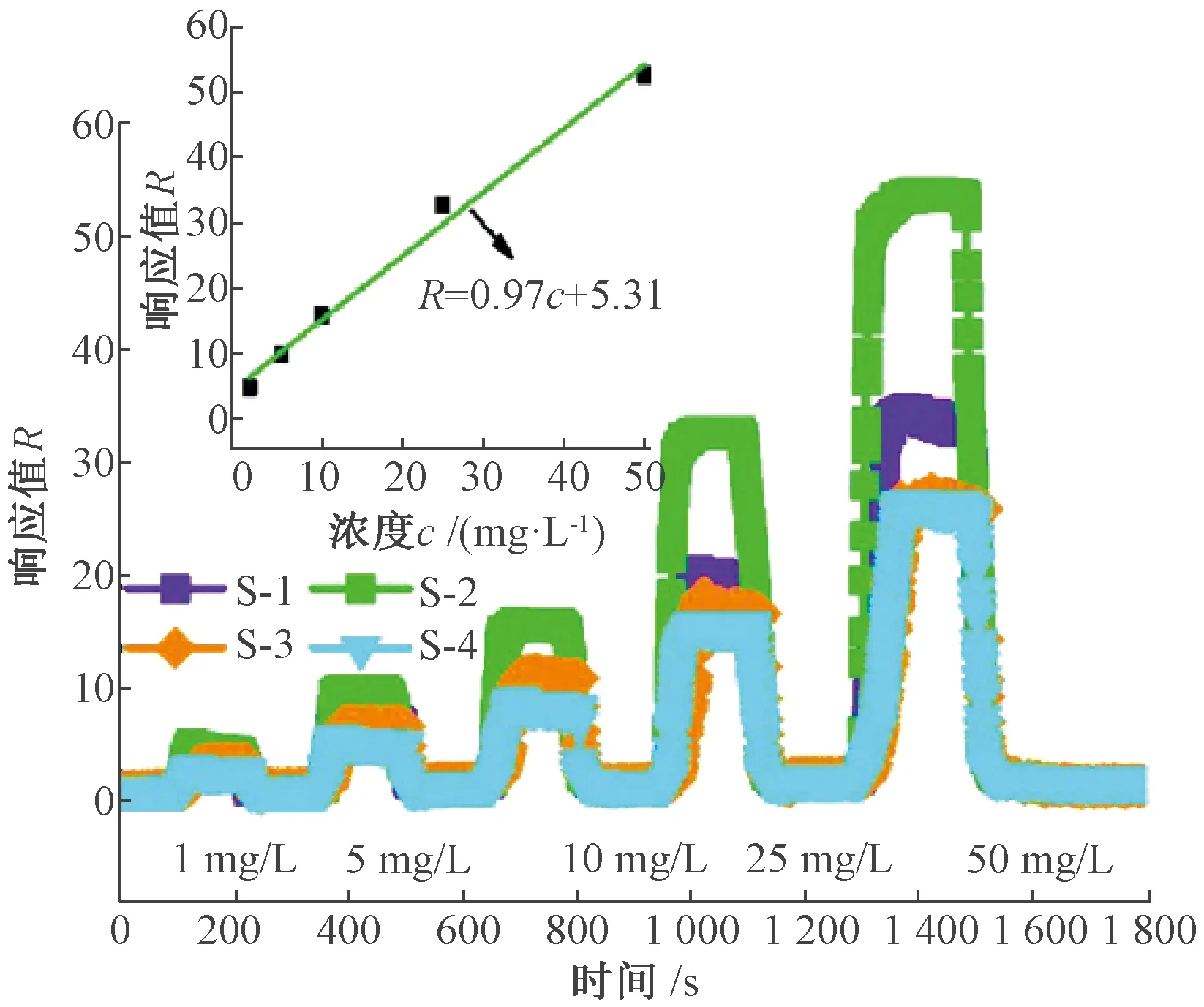
图7 传感器在不同甲醛浓度下的动态响应和线性拟合图
响应和恢复特性是用来评估气体传感器性能好坏的重要参数.图8给出了S-2气体传感器在210 ℃时的响应-恢复曲线,对于50 mg/L甲醛来说,传感器的响应和恢复时间分别为14 s和33 s.此种优异的响应-恢复特性是由于S-2材料的球形结构可以提供足够的活性表面,而且粗糙的球面和多孔结构具有良好的渗透性,这样有利于气体的快速吸附和扩散.
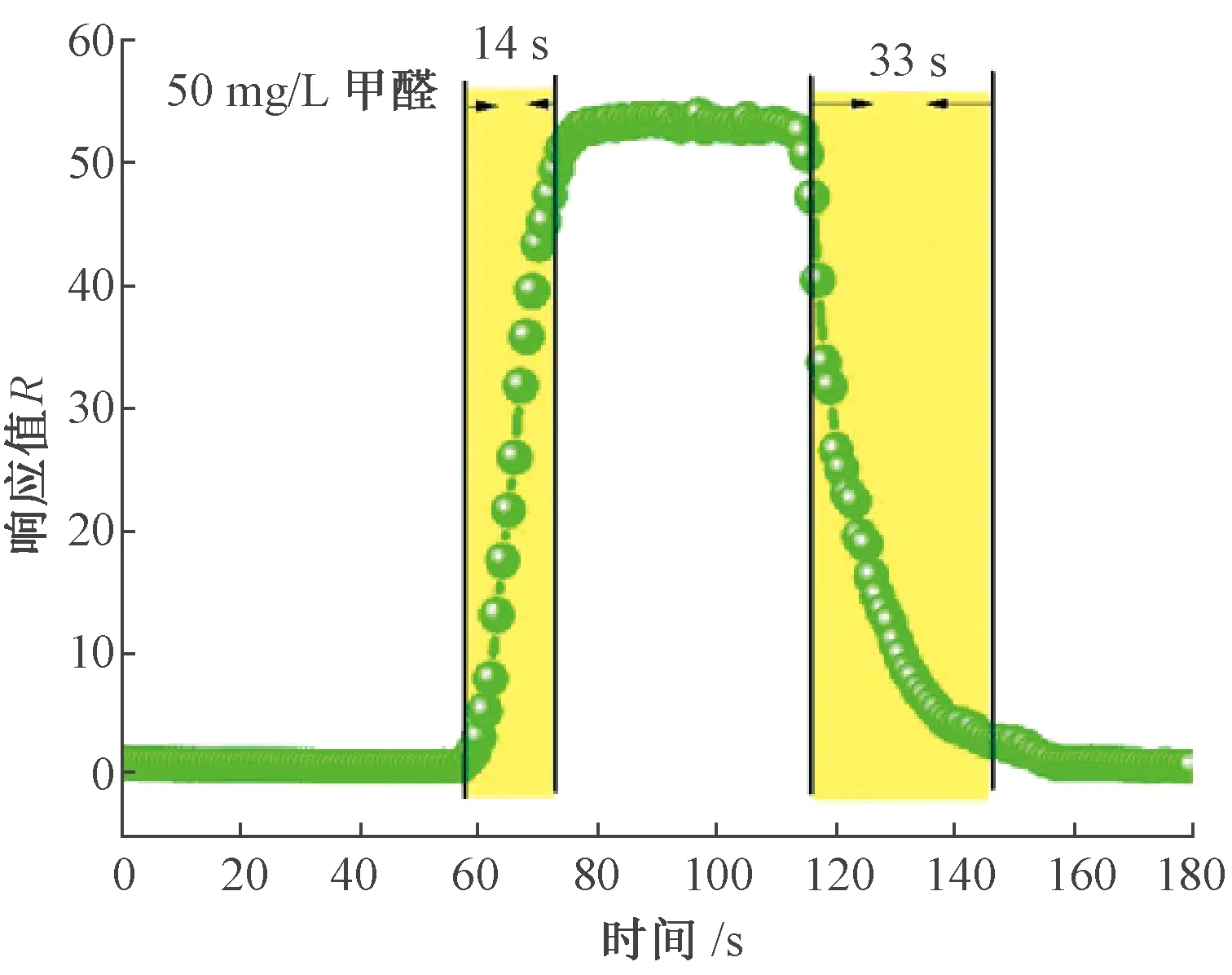
图8 S-2传感器在210 ℃下的响应-恢复曲线
图9 为S-2传感器在210 ℃时对50 mg/L甲醇、苯、丙酮、甲醛、乙醇、硫化氢和氨水的响应值.从图中可以看出S-2传感器对甲醛有较高的响应,对其他气体响应值较低.其中,S-2气体传感器对甲醛的响应值为乙醇响应值的1.6倍,表明其对甲醛具有更好的选择性.对比其他文献可知,S-2气体传感器具有响应值高、响应和恢复时间短、选择性好等优点,是一种潜在的甲醛检测敏感元件.

图9 S-2传感器在210 ℃时对不同气体的响应值
2.5 气体传感机理解释
SnO2的气体传感机制属于表面控制型,气敏性能取决于检测气体与化学吸附氧相互作用引起的电阻变化.图10(a)为SnO2气体传感器暴露在空气中,氧气分子吸附在SnO2表面并通过捕获来自SnO2导带的电子形成化学吸附氧(O2-,O-,O2-).这种吸附过程降低了SnO2的电子浓度,并在其表面形成电子耗尽层,同时也意味着材料中载流子的减少,所以电阻增加,从而获得稳定的高电阻Ra.如图10(b)所示,当SnO2气体传感器暴露于甲醛中时,甲醛分子和氧离子之间的氧化还原反应发生在敏感材料的表面,反应式如下:
HCHO(gas)→HCHO(ads);
(2)
HCHO(ads)+2O(ads)2-→CO2+H2O(g)+4e-.
(3)
这时,耗尽的电子又会被释放回到SnO2导带,导致表面耗尽层宽度的减小和SnO2传感器的电阻(Rg)降低.当甲醛脱离SnO2传感器后,氧气分子会重新吸附在SnO2表面,传感器可以恢复其原有的高电阻,从而完成整个响应恢复过程.一般来说,材料的气敏性能与其表面的电子耗尽层厚度有关.当材料的晶粒尺寸与表面电子耗尽层厚度的2倍接近时,材料的气敏性能便会极大提高.对于空气气氛中的SnO2材料,它表面的电子耗尽层厚度约为3 nm,而本文中S-2纳米材料平均晶粒尺寸约为6.7 nm,该数值接近于空气气氛中电子耗尽层厚度的2倍,这意味着合成的S-2材料在与空气接触时几乎完全耗尽了电子,这样有助于提高化学吸附氧与甲醛分子之间的反应速率,从而产生较快的响应恢复特性.
3 结论
笔者采用一步溶剂热法合成了一系列SnO2纳米材料,并通过气敏测试来比较材料形貌对气敏性能的影响.测试结果表明:多孔和空心球状结构的存在提升了SnO2材料的气敏性能,该材料在210 ℃下对50 mg/L甲醛的响应值为52.5,且选择性较好,响应-恢复时间分别为14 s和33 s,最低检测限为20 μg/L.由此可知,多孔SnO2空心球材料是一种理想的可应用于甲醛检测的敏感材料.
