延胡索咀嚼片质量标准研究
2019-11-22姜黎赵森纪开一邹明孙涌津徐保利
姜黎 赵森 纪开一 邹明 孙涌津 徐保利
[摘要]目的 建立延胡索咀嚼片的薄层及高效液相测定方法。方法 采用1% NaOH制备硅胶G板上,以正己烷-氯仿-甲醇(7.5:4:1)为展开剂,利用延胡索乙素对延胡索咀嚼片进行鉴别。采用反相高效液相色谱(RP-HPLC)进行测定,色谱柱为Hypersil BDS C18(5 μm,4.6 mm×150 mm);流动相为甲醇-0.1%磷酸(用三乙胺调节pH至6.0)(60:40);检测波长为280 nm。结果 延胡索咀嚼片薄层鉴别,置紫外灯(365 nm)下检视,在供试品色谱中,与对照品相同位置上,显相同颜色荧光斑点,阴性对照无此斑点。利用HPLC法对延胡索咀嚼片中的延胡索乙素进行测定,延胡索咀嚼片中延胡索乙素的线性范围为0.0832~0.4160 μg,r=0.9997,平均回收率为99.94%(RSD=0.52%)。结论 所建立的延胡索咀嚼片定性及定量质量控制方法,操作简单、重现性好、专属性高,可作为质量控制的方法。
[关键词]延胡索咀嚼片;延胡索乙素;薄层色谱;高效液相
[中图分类号] R282.1 [文献标识码] A [文章编号] 1674-4721(2019)9(c)-0044-04
[Abstract] Objective To establish thin layer and high performance liquid phase determination methods for Corydalis Rhizoma Chewable Tablets. Methods The silica gel G plate was prepared with 1% NaOH, and the Corydalis Rhizoma Chewable Tablets were identified by tetrahydropalmatine, with n-hexane-chloroform-methanol (7.5:4:1) as the developing agent. It was determined by reversed phase high performance liquid chromatography (RP-HPLC). The column was Hypersil BDS C18 (5 μm, 4.6 mm×150 mm), the mobile phase was methanol-0.1% phosphoric acid (pH adjusted to 6.0 with triethylamine) (60:40), and the detection wavelength was 280 nm. Results The thin layer of Corydalis Rhizoma Chewable Tablets was identified and placed under ultraviolet light (365 nm). In the chromatogram of the test sample, the same color fluorescent spot was displayed at the same position as the reference substance, and the negative control did not have this spot. The content of tetrahydropalmatine in the Corydalis Rhizoma Chewable Tablets was determined by HPLC. The linear range of tetrahydropalmatine was 0.0832-0.4160 μg, r=0.9997, and the average recovery rate was 99.94% (RSD=0.52%). Conclusion The qualitative and quantitative quality control methods of the Corydalis Rhizoma Chewable Tablets are easy to operate with good reproducibility and high specificity, and can be used as quality control methods.
[Key words] Corydalis Rhizoma Chewable Tablets; Tetrahydropalmatine; Thin layer chromatography; High performance liquid phase
延胡索咀嚼片(Corydalis Rhizoma Chewable Tablets)是由醋延胡索、枯礬、海螵蛸(去壳)组成的。原方安胃片,为《中国药典》2015年版一部收载品种[1]。具有行气活血、制酸止痛的功效,用于气滞血瘀所致的胃脘刺痛、吞酸嗳气、脘闷不舒,胃及十二指肠溃疡、慢性胃炎见上述症候者[2]。本方原为吞服片剂,每次服用5~7片,服用剂量大,患者依从性较差,因此本研究将其剂型改为咀嚼片,并验证了新剂型疗效稳定、方便服用。方中君药为延胡索(Corydalis Rhizoma),为罂粟科植物延胡索的块茎,性温、味苦,归肝、心、脾经,功效为活血、行气、止痛[3]。现代药理作用研究表明,延胡索具有抗溃疡作用,对胃及十二指肠溃疡有可靠的疗效[4]。延胡索乙素可安定中枢,尤适用于疼痛引起的失眠[5]。因此本研究利用延胡索乙素为对照品,采用薄层色谱法对延胡索咀嚼片进行定性鉴别[6-7],并采用高效液相色谱法(HPLC)测定延胡索咀嚼片中延胡索乙素含量[8-9],结果表明,上述两种方法操作简便、快速、准确、重现性好、结果直观,可用于该产品的质量控制。
1仪器与试药
1.1仪器
日本岛津LC-10Atvp高效液相色谱仪;Kromasil-C18(150 mm×4.6 mm,5 μm)色谱柱;N-2000色谱工作站;ZF-2型三用紫外分光光度仪(上海市安亭仪器厂);十万分之一分析天平(瑞士);KQ3200超声波清洗器(昆山市超声仪器有限公司)。
1.2试药
延胡索乙素对照品(批号:110726-201819)采购自中国食品药品检定研究所;乙醇、甲醇为色谱纯;水为纯水;延胡索咀嚼片(自制);其余均为分析纯。
2方法与结果
2.1延胡素咀嚼片薄层鉴别
2.1.1对照品溶液制备 取延胡素乙素对照品2.08 mg,精密称定,加甲醇50 ml溶解,即得。
2.1.2供试品溶液制备 取延胡索咀嚼片3 g,粉碎,药粉加甲醇50 ml,超声30 min后,滤过,蒸干滤液,残渣用水溶解后,以浓氨液调至pH值为碱性,乙醚提取3次,每次10 ml,合并乙醚液,蒸干,用甲醇1 ml溶解,即得。
2.1.3阴性溶液制备 取处方中除延胡索外的两味药材,按供试品溶液制备方法制备,即得。
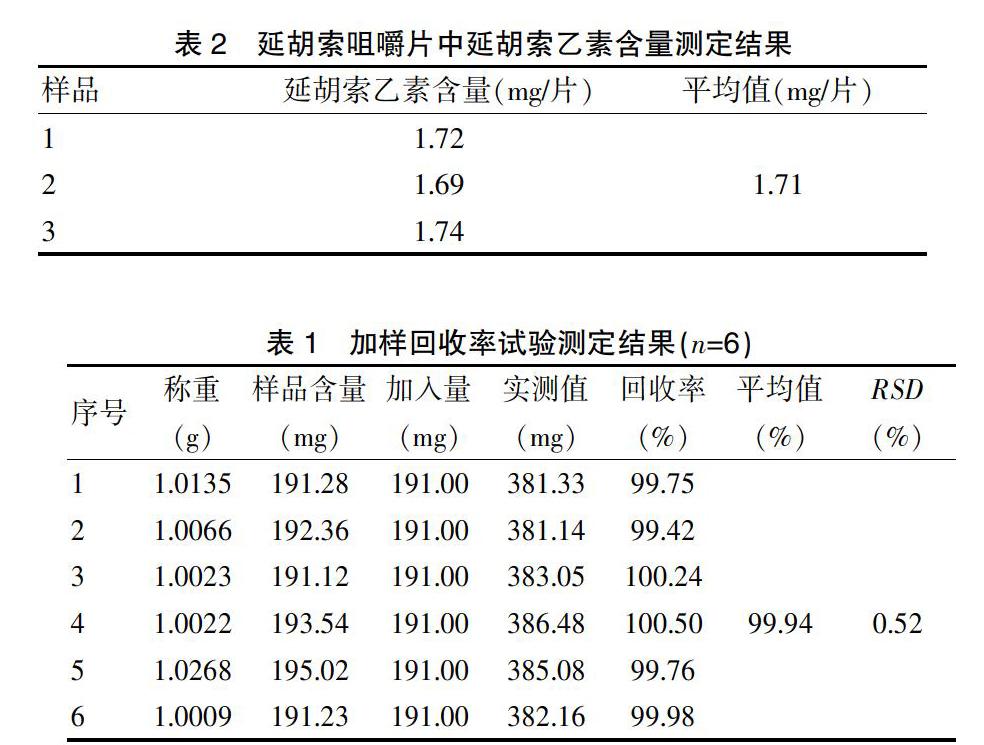
2.1.4薄层色谱条件 分别吸收上述溶液10 μl,点于同一硅胶G板上,以正己烷-氯仿-甲醇(7.5:4:1)为展开剂,展开,晾干后,置碘缸中约3 min后取出,挥尽板上吸附的碘后,置紫外灯下(365 nm)检视,在供试品色谱中,与对照品溶液相同的位置上,显相同颜色的荧光斑点,阴性液无斑点,结果如图1所示。
1:延胡索乙素对照品;2:供试品溶液;3:阴性对照液
2.2延胡素咀嚼片中延胡素乙素的含量测定
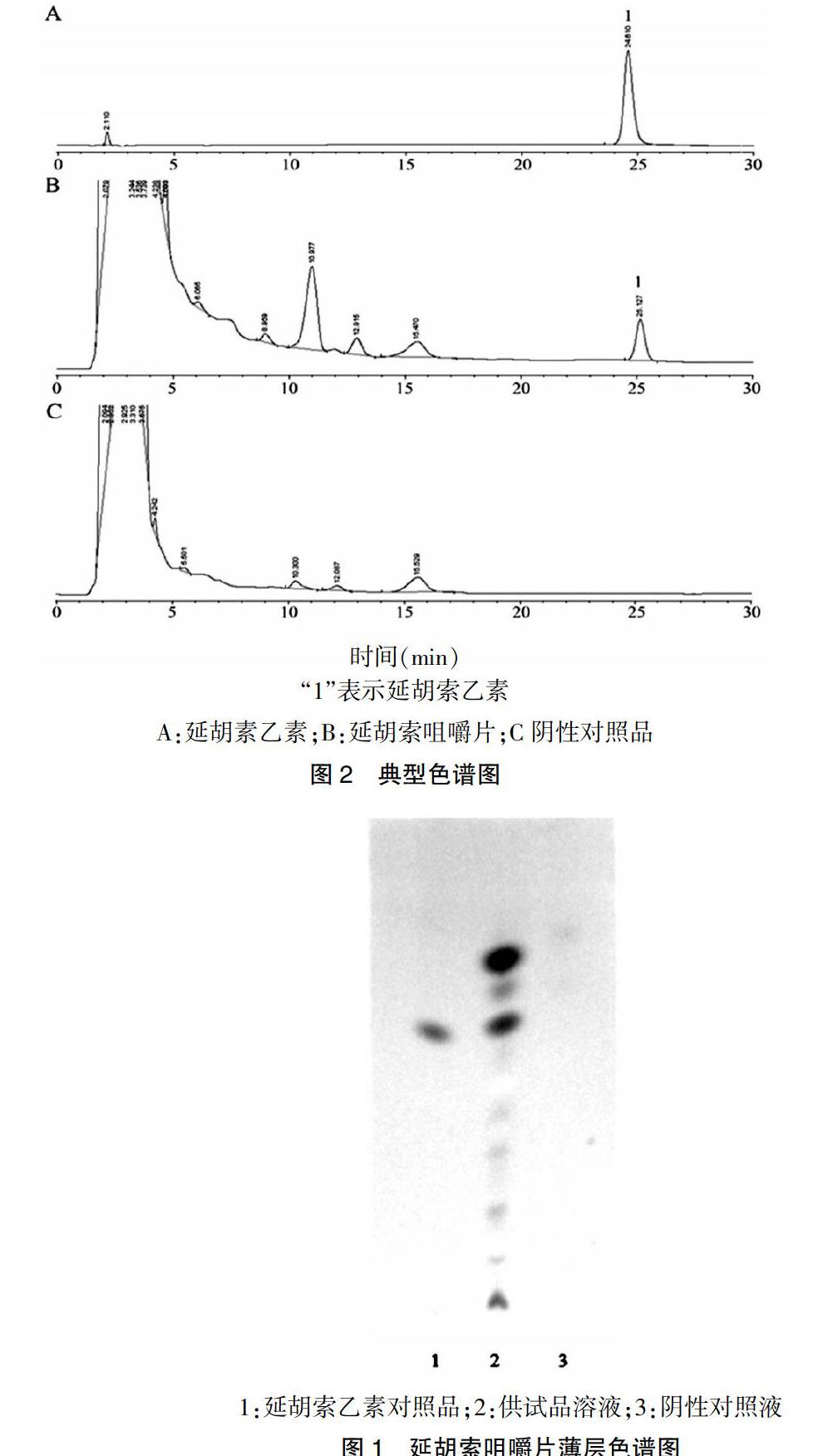
2.2.1色谱条件 采用反相高效液相色谱(RP-HPLC)法,Hypersil BDS C18(5 μm,4.6 mm×150 mm),流动相为甲醇-0.1%磷酸(60:40)(用三乙胺调节pH至6.0),体积流速1.0 ml/min,检测波长为280 nm,进样量为10 μl。典型色谱图具体见图2。
“1”表示延胡索乙素
A:延胡素乙素;B:延胡索咀嚼片;C阴性对照品
2.2.2对照品溶液的制备 精密称取延胡索乙素对照品适量,加甲醇制成41.6 μg/ml的对照品溶液。
2.2.3供试品溶液的制备 取延胡索咀嚼片30片,研细,精密称定,采用以下三种方法分别进行处理,作为供试品溶液,进行测定,结果进行比较。
方法1[10]:取2 g,精密称定,置索氏提取器中,加入乙醚适量,浓氨液2 ml浸泡过夜,加热回流提取,取乙醚液,水浴蒸干,残渣加甲醇1 ml溶解后转移至10 ml容量瓶中,定容后,以0.45 μm微孔滤膜滤过,取续滤液,即得。
方法2[11]:置具塞三角瓶中,精密加入浓氨试液-甲醇(1:15)混合溶液50 ml,称定重量,冷浸1 h后,回流提取60 min,放凉,精密称定,以浓氨试液-甲醇(1:15)补足减少重量,滤过后,取续滤液25 ml蒸干,残渣加水30 ml溶解,并移至分液漏斗中,加盐酸调pH值至2~3,用石油醚(60~90℃)洗涤2次,每次20 ml,弃去石油醚层。水层加浓氨试液调pH值至9~10,用氯仿提取4次,30 ml/次,合并氯仿层,用水20 ml洗涤,氯仿层置水浴蒸干,残渣加甲醇使溶解,转移至10 ml容量瓶中,定容后,以0.45 μm微孔滤膜滤过,取续滤液,即得。
方法3[12]:精密加水50 ml,水浴加热温浸1 h使溶解,用氨水调节pH值至10后,至分液漏斗中,乙醚萃取4次(30、30、20、20 ml),合并乙醚液,水浴挥干,残渣加甲醇定容至10 ml,摇匀,滤过,以0.45 μm微孔滤膜滤过,取续滤液,即得。
取以上三种不同方法制备的供试品溶液各10 μl,分别注入高效液相色谱仪,经实验观察结果显示,方法1中成分分离较好,延胡索乙素含量较高;方法2分离较好,但延胡索乙素含量低;方法3种杂质成分多,不能完全分离。比较决定采用方法1的处理方法作为样品溶液的制备方法。
2.2.4阴性对照溶液的制备 取处方中除延胡索外的两味药材,按供试品溶液制备方法制备,即得。
2.2.5线性关系考察 精密吸取0.1664 mg/ml延胡索对照品溶液5、10、12.5、15、20 μl,分别注入高效液相色谱仪,以浓度为横坐标,对照品锋面积为纵坐标,进行线性回归,得回归方程y=13794x+4042.9,r=0.9997(n=5),结果显示,在0.0832~0.4160 μg内线性关系良好。
2.2.6精密度试验考察 精密吸取对照品溶液10 μl,按上述色谱条件,连续进样(n=6),计算色譜峰面积,对照品及供试品RSD分别为1.01%和1.79%,结果符合规定。
2.2.7重复性试验考察 取延胡索咀嚼片,研细,精密称定6份,按“2.2.3供试品溶液的制备”项下的方法制备,分别精密吸取10 μl注入高效液相色谱仪。测得延胡索乙素含量RSD为1.00%,重复性良好,结果符合规定。
2.2.8稳定性试验考察 取同一供试品溶液,分别于0、2、4、6、8、10 h进样,结果表明,10 h内稳定,RSD为1.30%,结果符合规定。
2.2.9回收率试验考察 分别取样品6份,每份1 g,精密称定,加入一定量的延胡索乙素的对照品溶液,按“2.2.3供试品溶液的制备”项下制备方法制备,进样,测定含量,并计算加样回收率,结果见表1。
2.2.10样品测定 取3批次延胡索咀嚼片,按上述供试品制备方法,制备延胡索咀嚼片供试品溶液,分别精密吸取10 μl注入HPLC进行分析,记录峰面积,计算测得各批次延胡索乙素的含量,结果见表2。根据上述测定结果,暂定本品每片含延胡索以延胡索乙素计算,不得少于1.71 mg。
3讨论
3.1指标成分选择
延胡索咀嚼片中君药为延胡索,且药理活性强[13],主要指标成分为延胡索乙素,以HPLC测定延胡索咀嚼片中延胡索乙素含量[14],方法简单、专属性强、准确度高、重现性良好,可作为延胡索咀嚼片的质量控制依据。
3.2提取條件优化
查阅文献对延胡索咀嚼片的提取条件进行优化[15],对比回流提取法与索氏提取法的提取效率,结果提示,索氏提取法提取效率高,提取完全,故采用索氏提取法进行提取。同时对提取溶媒进行考察,对比氨水及乙醚混合液[16]、氨水及氯仿混合液两种溶媒[17],结果提示,氨水及乙醚混合液提取效率较高,故选用氨水及乙醚混合液作为提取溶媒。
综上所述,对延胡索咀嚼片进行质量标准研究,采用薄层色谱法对延胡索咀嚼片中对延胡索进行定性鉴别,采用HPLC对处方中的延胡索乙素进行含量测定,该方法操作简单、重现性好、专属性高,可作为含量测定的指标。
[参考文献]
[1]国家药典委员会.中华人民共和国药典一部[M].北京:化学工业出版社,2015:139,877-878.
[2]赵丽沙,董宇,寿旦.延胡索生物碱类化学成分及质量控制研究进展[J].中华中医药学刊,2017,35(2):299-302.
[3]杨波,纪宏宇,郑东友,等.中药延胡索的炮制工艺和药理作用的研究进展[J].药学实践杂志,2017,35(2):112-115.
[4]颜晶晶,俸珊,何丽娜,等.延胡索乙素对映体对人肝微粒体细胞色素P450酶抑制作用机制研究[J].中草药,2015, 46(4):534-540.
[5]何晓凤,张晶,张梅.延胡索化学成分、药理活性及毒副作用研究进展[J].上海中医药杂志,2017,51(11):97-100.
[6]张丹,王昌利,卜雕雕,等.高效液相色谱法同时测定延胡索中5种生物碱含量的方法学研究[J].中南药学,2018, 16(12):1759-1762.
[7]黄传奇,熊鑫,马浩然,等.醋延胡索饮片及其混伪品零余子的系统鉴别[J].时珍国医国药,2018,29(6):1363-1366.
[8]杜颖川.高效液相色谱法对复方健胃分散片中延胡索乙素的含量测定及分析[J].中国民康医学,2018,30(21):79-81.
[9]胡珂,何忠臻,彭华胜,等.延胡索块茎中延胡索乙素含量分布的研究[J].中国现代中药,2018,20(7):825-828.
[10]龚青,周蒂,王碧娟.HPLC法测定延胡索中延胡索乙素的含量[J].中国现代应用药学,2000,17(4):177-179.
[11]赵君颖.胃安舒颗粒质量标准的研究[J].中医学报,2007, 22(5):24-25.
[12]房方,丁选胜.延胡索药材中延胡索乙素的含量测定[J].现代中药研究与实践,2005,19(1):54-56.
[13]李凯,杨靖,彭晶晶,等.中药延胡索研究进展[J].陕西农业科学,2018,64(6):93-96.
[14]冯自立,赵正栋,刘建欣.延胡索化学成分及药理活性研究进展[J].天然产物研究与开发,2018,30(11):2000-2008.
[15]唐逸丰.延胡索化学成分与药理作用研究概况[J].中国临床研究,2018,10(23):144-146.
[16]接强,贺吉香.延胡索提取工艺研究[J].辽宁中医药大学学报,2017,19(2):49-52.
[17]徐忠坤,陈广波,殷洪梅,等.延胡索药材提取工艺研究[J].世界科学技术-中医药现代化,2015,17(11):2318-2321.
(收稿日期:2019-03-28 本文编辑:任秀兰)
