一株小脆柄菇的分离培养及木质素降解酶活性
2019-11-04刘子璐胡渤洋王文平陈青君张国庆
刘子璐,胡渤洋,王文平,陈青君,孙 悦,张 娇,张国庆*
(北京农学院a.生物与资源环境学院/农业农村部华北都市农业重点实验室;b.植物科学技术学院/北京林木分子设计育种高精尖创新中心,农业应用新技术北京市重点实验室,北京 102206)
白腐真菌(White rot fungi)是一类能够降解木材并造成白色腐朽的真菌,它们能够分泌多种降解木质纤维素的胞外酶,且降解木质素能力强于降解纤维素的能力[1]。白腐真菌作为木质纤维素分解者,在自然界碳循环中扮演着极其重要的作用,它们的木质素降解酶系统(Ligninolytic enzyme system)主要包括3种酶:锰过氧化物酶(Manganese peroxidase,MnP)、木质素过氧化物酶(Lignin peroxidase, LiP)和漆酶(Laccase, Lac),它们共同作用将木质素最终降解为二氧化碳和水。由于它们能够降解芳香、杂环类化合物,目前已在造纸、堆肥、环保等领域广泛应用[2-4]。
白黄小脆柄菇(Psathyrellacandolleana),又称黄盖小脆柄菇、垂幕菇、薄花边伞等,是小脆柄菇属常见种之一,常见于林中地上、草地、路旁或腐木等,群生或近丛生,可食用,分布于亚洲、欧洲、北美等地区[5]。傅恺等利用白黄小脆柄菇进行液体深层发酵获得胞外漆酶,产量达到9 100 IU/L[6]。李学梅等从白黄小脆柄菇发酵液提取物中分离到一种新的血苋烷型倍半萜[7]。该研究前期从北京农学院校园内采集并分离的一株小脆柄菇属真菌,菌丝体未测得漆酶活性,与前人文献报道不同,可能具有不同的木质素降解酶系。因此,拟开展菌株分类鉴定、菌丝体培养条件以及木质素降解酶活性测定研究,明确其木质素降解酶系,为其开发利用奠定理论和试验基础。
1 材料与方法
1.1 材 料
小脆柄菇子实体采集自北京农学院,由生物与资源环境学院食药用菌课题组分离与保藏。
菌株分离与保藏利用马铃薯葡萄糖琼脂(PDA)培养基。液体发酵利用马铃薯葡萄糖(PD)培养基,液体发酵使用250 mL锥形瓶,每瓶装50 mL培养基。菌丝最适培养条件基础培养基参考王寿南等的报道[8]。
1.2 方 法
1.2.1 菌株的分离、培养与保存 菌株分离采用组织分离法[8]。菌株编号为F1734,于25 ℃避光培养7 d,于4 ℃保藏。
1.2.2 形态与分子鉴定 观察子实体形态并记录。菌丝显微观察采用插片培养法。分子鉴定采用内转录间隔区(ITS)鉴定法,引物为通用引物ITS1和ITS4。目的序列比对采用BLAST在线比对分析(http://blast.ncbi.nlm.nih.gov/Blast.cgi),利用MEGA 7.0软件、采用邻接法(Neighbor-Joining, NJ)构建系统发育树,确定目标菌株的分类学地位[8]。

1.2.4 液体发酵产木质素降解酶活性 以新鲜的F1734菌饼接种于PDA平皿(9 cm)上,25 ℃避光培养至刚刚长满平皿,无菌条件下将其转移至无菌组织匀浆器中,加入50 mL 无菌液体发酵培养基,充分匀浆,制成种子液,以5%(V/V)的接种量将种子液添加到液体发酵培养基中,28 ℃,150 r/min振荡培养。在接种第3至第9天随机取3瓶,4 ℃、8 000 r/min、30 min离心,将菌丝体和上清液分离。菌丝体于35 ℃烘2 h、55 ℃烘至恒重,测量干重。取上清液分别测定胞外Lac、MnP和LiP酶活。Lac活性测定采用2,2’-连氮-双-3-乙基苯并噻唑-6-磺酸(ABTS)法[9]。酶活单位(Unit, U)定义为:在420 nm处,每1 min催化1 μmol ABTS生成产物所需的酶量[10]。MnP活性测定采用MnSO4作为底物。酶活单位定义为:在240 nm处,每1 min催化1 μmol Mn2+转化为Mn3+所需的酶量[11]。LiP酶活性测定采用藜芦醇作为底物。酶活单位定义为:在310 nm处,每1 min催化1 μmol藜芦醇转化为藜芦醛所需的酶量[12]。
1.2.5 统计学分析 所有数据采用SPSS 23.0统计软件进行处理和分析。结果用平均值±标准差(mean ±SD)表示,对不同处理进行单因素方差分析,P<0.05代表数据存在显著性差异。
2 结果与分析
2.1 形态特征鉴定结果
F1734菌株子实体形态如图1-A所示。其子实体发生于道路旁腐木落叶层、群生,子实体小至中型,菌盖幼嫩时圆锥形、成熟后平展,初期边缘附有白色菌幕残片、后渐脱落,菌盖边缘污白至米黄色、中央黄褐色,菌褶直生、密、不等长、污白、灰白至深紫褐色,菌柄细长、中生、中空、质地极脆、表面具白色纤毛,白色至污白色。其子实体形态特征与前人报道白黄小脆柄菇一致[13]。纯培养菌落形态如图1-B所示,菌落白色、不产色素,菌丝致密浓白。菌丝显微形态如图1-C所示,营养菌丝无色透明,薄壁,有隔,多核,偶见锁状联合。

A.子实体;B.菌落;C.菌丝体图1 F1734菌株形态特征A. Fruiting body; B. Colony;C. MyceliaFig.1 Morphological characteristics of F1734 strain
2.2 分子鉴定结果
经PCR扩增获得F1734菌株ITS序列片段,经测序获得长度为695 bp的目的序列片段。利用Blast在线比对确定其为小脆柄菇属。以小脆柄菇属相近种、利用MEGA 7.0软件构建系统发育树(图2)。聚类分析结果表明,F1734菌株与白黄小脆柄菇(P.candolleana)(EU622272.1)的相似性最高,为99%,遗传距离为0.008。结合形态和分子鉴定,确定F1734菌株为白黄小脆柄菇。
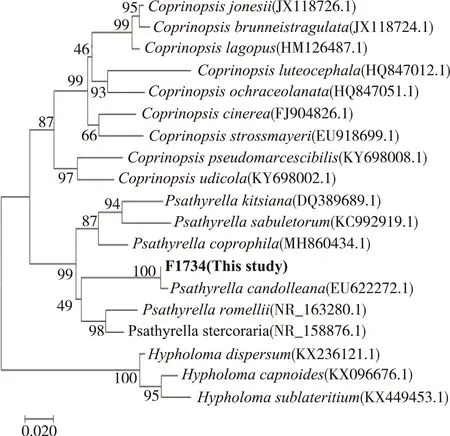
图2 基于ITS序列的F1734菌株与相近属真菌的系统发育分析Fig.2 Polymeric analysis of strain F1734 and other strains from closegenera based on ITS sequences
2.3 最适培养条件
F1734菌株在蔗糖、淀粉等7种碳源及无碳源基础培养基(CK)上均能生长(表1),菌落均为白色,无色素产生。菌丝在蔗糖培养基上生长速率最快(1.52 ± 0.03)mm/d,但长势较浓密,菌落产生絮状气生菌丝及同心圆结构。菌丝在麦芽糖培养基上生长速率为(1.34 ± 0.03) mm/d,长势最佳,菌落致密、浓白、均一,无同心圆结构。菌丝在羧甲基纤维素钠培养基上长势最弱,表明F1734菌株纤维素酶活性较低。综合菌丝生长速率和菌丝长势,F1734菌丝体最适碳源为麦芽糖。
表1 不同碳源、氮源和C/N比对F1734菌株菌丝体生长的影响
Tab.1 Effect of carbon, nitrogen, and C/N ratioon mycelial growth of strain F1734
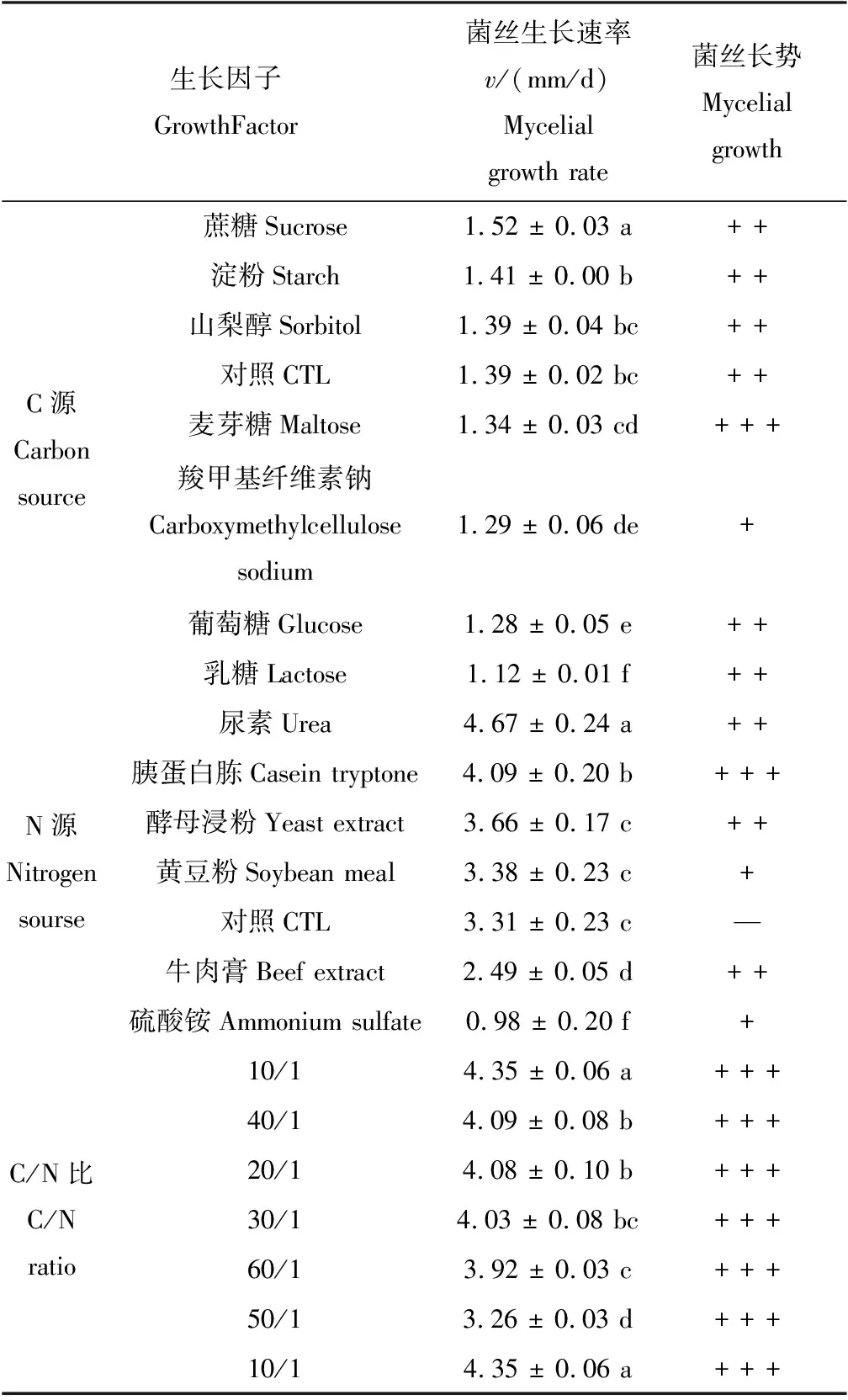
生长因子GrowthFactor菌丝生长速率v/(mm/d)Mycelial growth rate菌丝长势Mycelial growthC源Carbon source蔗糖Sucrose1.52 ± 0.03 a+ +淀粉Starch1.41 ± 0.00 b+ +山梨醇Sorbitol1.39 ± 0.04 bc+ +对照CTL1.39 ± 0.02 bc+ +麦芽糖Maltose1.34 ± 0.03 cd+ + +羧甲基纤维素钠Carboxymethylcellulose sodium1.29 ± 0.06 de+葡萄糖Glucose1.28 ± 0.05 e+ +乳糖Lactose1.12 ± 0.01 f+ +N源Nitrogen sourse尿素Urea4.67 ± 0.24 a+ +胰蛋白胨Casein tryptone4.09 ± 0.20 b+ + +酵母浸粉Yeast extract3.66 ± 0.17 c+ +黄豆粉Soybean meal3.38 ± 0.23 c+对照CTL3.31 ± 0.23 c—牛肉膏Beef extract2.49 ± 0.05 d+ +硫酸铵Ammonium sulfate0.98 ± 0.20 f+C/N比C/N ratio10/14.35 ± 0.06 a+ + +40/14.09 ± 0.08 b+ + +20/14.08 ± 0.10 b+ + +30/14.03 ± 0.08 bc+ + +60/13.92 ± 0.03 c+ + +50/13.26 ± 0.03 d+ + +10/14.35 ± 0.06 a+ + +
—:不生长;+:生长稀疏;+ +:生长较致密;+ + +:生长旺盛。不同小写字母表示差异显著(P< 0.05)
—:No mycelia growth; +: mycelial growth weak; + +: mycelial growth ordinary; + + +: mycelial growth strong. Different small letters indicate significant differences (P< 0.05)
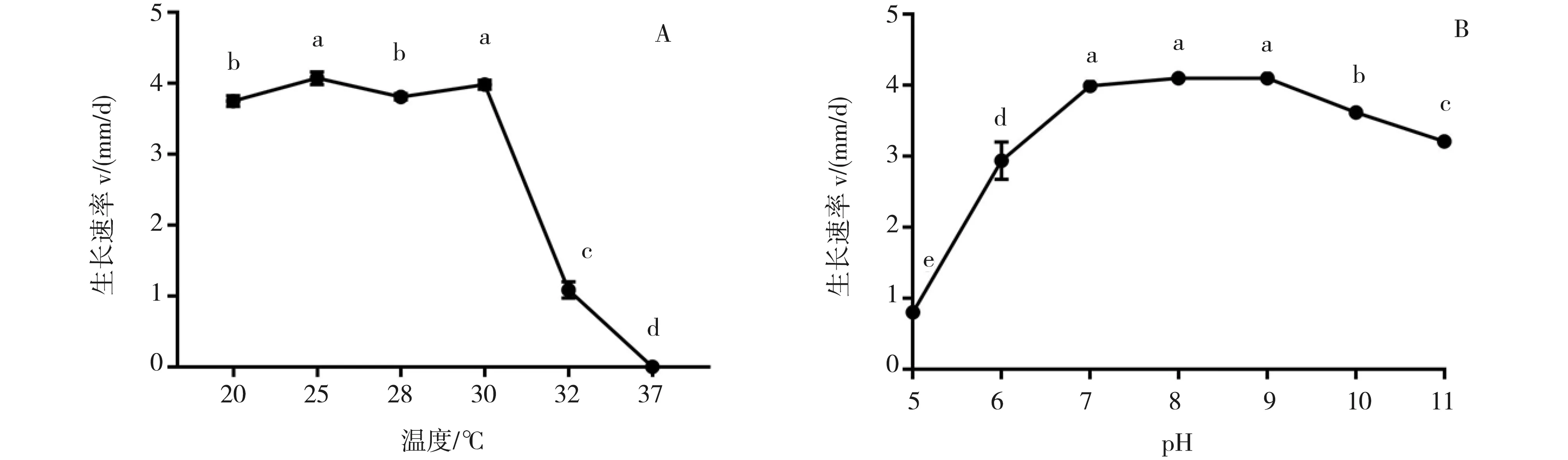
图3 温度和pH对F1734菌株菌丝生长的影响Fig.3 Effect of temperatureandpHon mycelial growth of strain F1734
F1734菌株在尿素、胰蛋白胨等6种氮源培养基上均能生长(表1)。而在无氮源基础培养基(CK)上几乎不生长,除硫酸铵培养基外,菌落均为白色,无色素产生。菌丝在以尿素为氮源的培养基上生长速率最快(4.67 ± 0.24) mm/d,其次是胰蛋白胨(4.09 ± 0.20) mm/d,但后者菌丝长势最佳,菌丝浓白。在硫酸铵的培养基上生长速率最慢(0.98 ± 0.20) mm/d,长势最弱,菌落边际不均一,且分泌黄色色素。综合菌丝生长速率及菌丝长势,F1734菌丝生长最适氮源为胰蛋白胨。
F1734菌株在C/N比10/1至60/1范围均能生长良好(表1),菌丝致密浓白。菌丝在C/N比为10/1培养基上生长速率最快(4.35 ± 0.06) mm/d,其次为40/1培养基(4.09 ± 0.08) mm/d,在50/1培养基上生长速率最慢(3.26 ± 0.03) mm/d。综合菌丝生长速率及菌丝长势,F1734菌丝生长的最适C/N比为10/1。
F1734菌株在20~32 ℃下均能生长,在37 ℃时无法生长(图3-A),菌落白色。20 ℃培养时菌丝生长速率较快,但菌丝长势较25~30 ℃培养时稍弱;菌株在25~30 ℃培养时生长速率最快(3.75 ± 0.07)~(3.98 ± 0.06) mm/d,菌丝浓白致密。当温度高于30 ℃时,菌丝生长速率下降、长势变弱,32 ℃培养时生长速率仅为(1.09 ± 0.11) mm/d。而当温度达到37 ℃时,菌株无法生长。综合菌丝生长速率及菌丝长势,F1734菌丝体生长最适温度范围为25~30 ℃。
F1734菌株在pH 6.0~11.0时均能生长,在pH 7.0~9.0时生长速率最快、长势最佳,而当pH低于7.0或高于9.0时菌丝生长速率迅速下降(图3-B)。pH 7.0~9.0时生长速率最快(3.99 ± 0.06)~(4.10 ± 0.05) mm/d,菌丝致密浓白;而pH 5.0时生长速率最慢(0.80 ± 0.02) mm/d,长势最弱,且菌落形状不规则。综合菌丝生长速率和菌丝长势,F1734菌丝体生长最适pH值在7.0~9.0之间。
2.4 液体发酵产木质素降解酶活性
F1734菌株液体发酵时,在第3~7天呈线性生长,在第7天菌丝干重达到最大,50 mL发酵液中菌丝干重达到(25.63 ± 5.12) mg,在7~9 d菌丝生物量保持相对稳定(图4-A、图4-B~D)。F1734菌株液体发酵产Lac、MnP和LiP结果如图4-B~D所示。在发酵培养的第3~9天,发酵液中均未检测出Lac活性,表明该条件下F1734菌株无胞外漆酶活性(图4-B)。MnP酶活在第4天开始出现,随后逐渐增加,在第7天时达到峰值,为(186.32±7.29) U/mL,随后迅速下降(图4-C)。LiP在第3天时表现出较高的活性,达到(3 787.90±283.43) U/mL,后缓慢上升,在第5天时酶活达到最高,为(4 890.20±979.37) U/mL,随后在第5~7天时逐渐下降,在7~9 d酶活达到相对稳定,为(2 823.18 ~3 106.33) U/mL(图4-D)。
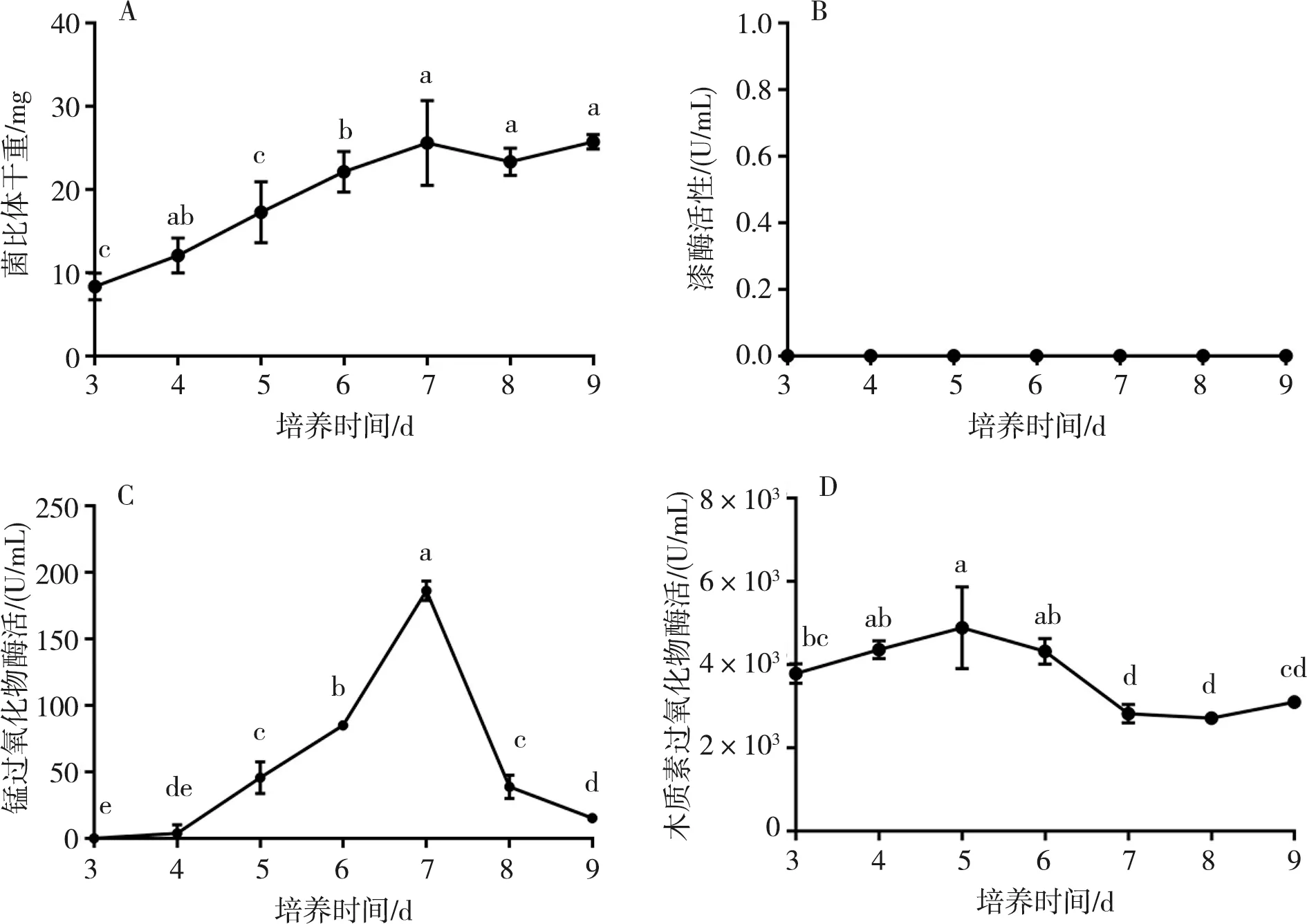
A.生物量;B.漆酶;C.锰过氧化物酶;D.木质素过氧化物酶图4 F1734菌株液体发酵生物量与木质素降解酶活性A. Biomass; B. Lac; C. MnP; D. LiPFig.4 Biomass and ligninolytic enzyme activities of during the liquid fermentation of strain F1734
3 讨论与结论
白腐真菌对木质素的降解主要依赖于一些胞外酶,这些酶共同构成被称之为木质素降解酶系统,主要包括Lac、MnP和LiP等,它们各有分工又协同合作,为白腐真菌的生物降解能力提供基础[2]。根据这些木质素降解酶在木质素降解过程中扮演作用的不同,前人将白腐真菌分为三大类,即LiP-MnP类(LiP-MnP group)、MnP-Lac类(MnP-Lac group)和LiP-Lac类(LiP-Lac group)[14]。木质素降解酶系统研究最早也最为系统的是黄孢原毛平革菌(Phanerochaetechrysosporium),它能够分泌MnP和LiP,但不分泌Lac,属于LiP-MnP类;而红平菇(Pleurotusdjamor)可同时产生MnP和Lac,但不产生LiP,则属于MnP-Lac类[14, 15]。该研究前期以小脆柄菇F1734菌株开展产酶实验时发现,该菌株能够使愈创木酚平板变色,但不具有产漆酶活性,因而进一步开展了菌株鉴定、培养条件与液体发酵产木质素降解酶研究,分析其木质素降解酶系,为进一步开展该菌株木质素降解酶系统研究奠定基础。
小脆柄菇属(Psathyrella)真菌隶属于担子菌门(Basidomycota)伞菌纲(Agaricomycetes)伞菌目(Agaricales)脆柄菇科(Psathyrellaceae),最初由Fries于1874年定义,模式种为褐白小脆柄菇(Psathyrellagracilis)[5]。小脆柄菇属广泛分布于世界各地,在中国各地区均有报道,世界范围内至少存在400~600种[13]。小脆柄菇属真菌多发生于夏秋季节道旁、林缘、林中的腐木周围及草地、牧场等,可以食用,能用于木质素降解、制备香料等,具有一定的经济价值[16-18]。小脆柄菇通常具有湿润的菌盖,菌盖多呈圆锥形或钟型或扁半球形、薄,颜色多为浅黄色或褐色。菌柄较长,中空,弯曲状。孢子印迹呈褐色甚至黑色和较为脆弱的担子果等特点[5, 19]。由于小脆柄菇属的菌株具有较脆弱的担子和容易变色的湿润菌盖,所以利用形态学特征对其进行分类学鉴定具有较大的难度并且准确度不高。
近些年来,分子技术已广泛应用于对其的物种鉴定和系统发育学研究[20]。王月等报道,该属在中国26个省均有分布,包括51个种[5]。Yan等对中国东北的27个小脆柄菇属菌株进行研究发现了4个新种,分别是P.conica、P.jilinensis、P.mycenoides和P.subsingeri[21]。该研究通过形态学比较,发现F1734菌株子实体形态符合前人对白黄小脆柄菇(P.candolleana)形态描述[5, 13]。另外,基于ITS的系统发育树表明,F1734菌株与白黄小脆柄菇(EU622272.1)的相似性达到99%。因此,结合形态和分子鉴定,确定F1734菌株为白黄小脆柄菇。
对F1734菌株菌丝最适培养条件研究表明,该菌株最适碳源为麦芽糖,最适氮源为胰蛋白胨,最适C/N比为10/1,最适温度范围为25~30 ℃,最适pH值范围为7.0~9.0。尽管白黄小脆柄菇属于可食野生菌,其菌丝培养条件研究暂无相关报道,而前人对其相近属鬼伞属(Coprinus)培养条件研究较多。郝册等报道,分离自北京市怀柔区宝山镇的墨汁鬼伞(C.atramentarius)菌丝体生长的最适碳源为葡萄糖+玉米淀粉、最适氮源为蛋白胨、最适pH值为9[22]。朱玉兰等报道,分离自祁连山的毛头鬼伞菌(C.comatus)菌丝生长的最适碳源为蔗糖、最适氮源为酵母粉、最适温度为24~26 ℃、最适pH为7.0[23]。F1734菌株最适碳、氮源常见,最适温度、最适pH温和,有利于减少工业发酵条件下的菌丝培养的开发成本。
在利用马铃薯浸提物、蔗糖的液体发酵培养时,F1734菌株具有胞外MnP和LiP活性,而缺乏Lac活性,表明该菌株属于LiP-MnP类白腐真菌。傅恺等报道,白黄小脆柄菇进行液体深层发酵获得胞外漆酶,产量达到9100 IU/L[6]。张丽等报道,分离自广州地区亚热带阔叶林的白黄小脆柄菇发酵液中具有漆酶活性,在第3天达到高峰为31525 IU/L[24]。这表明,F1734菌株具有不同于这2个菌株的木质素降解酶特性。前人报道中,白腐真菌产Lac和MnP类型较多,而产LiP类型较少[15]。本研究中,菌株表现出较高的LiP和MnP活性,其中MnP活性是绒毛栓孔菌(Trametespubescens)的20倍左右[11]、是红平菇(P.djamor)的100倍[25],LiP活性是红平菇的20倍[26],显著高于前人研究结果。
综上,该研究通过对采集得到的菌种进行分离鉴定,获得一株白黄小脆柄,并确定了菌丝培养条件,明确该菌株属于LiP-MnP类白腐真菌。同时也是首次对白黄小脆柄菇中的木质素过氧化物酶和锰过氧化物酶进行了报道,为其进一步开发利用奠定基础。
