由蚕砂制备的碳量子点在不同激发、pH、金属离子、温度及极性环境下的荧光性质研究
2019-11-04黄彦捷连超周瑾艳黄梓宸康晓红黄振宇李小菁陈玲关妍
黄彦捷,连超,周瑾艳,黄梓宸,康晓红,黄振宇,李小菁,陈玲,关妍
1.广东省现代几何与力学计量技术重点实验室,广东省计量科学研究院,广州 510405
2北京交通大学理学院化学系,北京 100044
3北京大学化学与分子工程学院,北京 100871
1 引言
与众所周知并且已经商业化的量子点相比,碳量子点(Carbon dots,CDs)具有类似的特性,如发光亮度高、尺寸可调控,荧光发射波长可调、耐光漂白等。除此之外CDs中不含有毒元素,并且它们的使用不会给生态系统或有机体带来内在毒性的负担,因而是一种体内生物分析更为理想的材料。近年来,一系列性能优异的CDs见诸于报道1–3。迄今为止,CDs在能量转换与存储4、生物成像5,6、传感器7,8、生物探针9–11和各种其它领域都引起了极大的关注,并显示出巨大的应用潜力12。自2006年Sun和同事首次用激光消融法制备CDs13以来,许多研究都集中在亲水或疏水性CDs的合成方法上,目前已经提出了从自上而下14,15或自下而上16合成CDs的方法,前者基于从大的碳骨架上剥落下碳纳米颗粒的合成方法,后者则是以较小碳材料为碳源进行处理使其聚集成较大碳纳米颗粒的合成方法。具体的制备方法包括激光销蚀法,电化学法和弧光放电法等(自上而下),或化学氧化法,微波法,模版法,热分解法和反胶束法等(自下而上)12,17,18。
然而,大多数已报道的CDs合成路线需要以化学试剂作为碳来源,同时需要严苛的实验操作。近年来也有通过一些天然产物,如西瓜皮19、牛奶20、土豆21等制备CDs的报道,大大拓展了CDs的初始碳源。蚕砂是家蚕的干燥粪便,作为丝绸产业的副产物,具有广泛的原料来源。中医上认为性味甘温,入肝、脾、胃经,有燥湿、祛风、和胃化浊、活血定痛之功。民间用蚕砂作枕芯的填充物,有清肝明目之效。根据《中药大辞典》报道,蚕砂含有机物83.77%–90.44%,灰分9.56%–16.23%,总氮量1.91%–3.60%。含氮成分主要为尿嘧啶、二氢尿嘧啶等,还含有植物醇0.25%–0.29%,不皂化成分β-谷甾醇、胆甾醇、麦角甾醇和廿四醇、蛇麻脂醇、β-谷甾醇-β-葡萄糖甙等。蚕砂中含有的大量羟基、羧基化合物可作为制备CDs的理想起始材料,而其中含氮、硫化合物更是可以作为氮源及硫源为CDs增加一系列独特的性质。
本文报告了一种简单,低成本的水溶性CDs的制备方法,经微波处理的蚕砂可制备得到含氮、硫修饰的CDs,其具有粒径分布窄,水溶性好及荧光强度高等特点。进一步的,该CDs的荧光最大发射波长会随激发波长的增大或pH的增大而红移;最大荧光发射峰强度会随温度的升高而逐渐降低,一定范围内随着pH的减小而增加,随着金属离子(Cu2+、Al3+、Fe3+、Fe2+、Ag+、Ba2+、Ca2+、Cd2+、Hg2+、Mg2+、Mn2+、Ni2+、Pb2+、Zn2+)的加入而逐渐降低,并随着EDTA络离子的加入而逐渐回复,荧光强度的变化对铜离子的响应性质最为明显。与此同时,CDs在多种溶剂中均具有较好的溶解度,当换用不同极性的溶剂时,随着溶剂极性的增加,该CDs的荧光最大发射波长会逐渐红移。荧光性质随不同参量的变化为发展CDs作为多功能传感材料提供了多种可能及潜在的应用前景。
2 实验部分
2.1 试剂部分
蚕砂由家蚕正常饲喂桑叶获得;浓硫酸(GR,北化),B-R缓冲液采用硼酸,磷酸,乙酸及氢氧化钠(AR,J&K)按不同比例配置而成;HAc-NaAc缓冲液采用冰醋酸及醋酸钠(AR,J&K)按不同比例配置而成;HEPES缓冲液(索莱宝);乙二胺四乙酸(EDTA,GR,阿拉丁)。常见金属盐及溶剂均购自国药集团,AR。
2.2 仪器部分
使用美国FEI公司Tecnai F20场发射透射电镜观察CDs尺寸和形貌;使用美国Brook heaven公司ZetaPlus Potential Analyzers仪器采用动态光散射方法测量水合粒径;使用德国Elementar Analysensysteme GmbH公司Elemental Analyzer Vario EL元素分析仪(EA)测定CDs的元素组成;使用英国Kratos Analytical公司的X射线光电子能谱仪(XPS)测定CDs中的元素种类及价态信息;使用日本Rigaku公司的D/MAX-2500PC 18KW转靶X射线粉末衍射仪(XRD)测定CDs的晶型;使用美国Thermo Scientific公司的DXR2智能拉曼光谱仪测定CDs的拉曼光谱;使用美国Bruker公司FTTR Tensor 27红外光谱仪测定CDs的红外吸收光谱;使用日本Shimadzu公司UV3600 PLUS紫外可见近红外吸收光谱仪测定CDs的紫外可见吸收光谱;使用英国Horiba Jobin Yvon公司Nanolog FL3-2iHR红外荧光测试系统测定CDs的荧光激发光谱及发射光谱,配套积分球附件测定绝对发光量子产率,配套英国牛津公司OpstisDN2附件控制温度变化。
2.3 CDs的制备
研磨,过程中筛去正常饲喂桑叶获得的天然蚕砂中可能存在的枯叶、土粒等杂质。将0.5 g蚕砂与5 mL浓硫酸(浓硫酸中硫酸的质量分数为98%)混合后,置于25 mL微波反应釜中,加入磁子搅拌或是利用旋转微波反应器配套转盘,500 W功率下微波反应,3 min得到深黄色碳量子点溶液;过滤去除不溶性杂质,将得到的反应溶液置于透析袋(2000 Da)中进行透析,每30 min更换透析用的去离子水,共计10次,可得CDs水溶液。
将透析后的CDs冷冻干燥24 h,可得到棕黄色CDs粉末。或直接将透析后的CDs水溶液分散在10 mL缓冲液(B-R缓冲液,HAc-NaAc缓冲液或HEPES缓冲液)中,可得到棕黄色水溶性的CDs储备液。

图1 CDs的(a) XPS谱图,(b)傅里叶变换红外光谱Fig. 1 (a) XPS and (b) FTIR spectra of CDs.
3 结果与讨论
3.1 尺寸和组成
元素分析结果表明,制备的CDs中含碳59.84%,氮5.46%及硫2.32%,其中氮是从蚕砂中带来的,而硫可能是从蚕砂和浓硫酸中带来的。用XPS分析了CDs的元素组成(图1a),其中包含硫(约164 eV)、碳(约285 eV)、氮(约398.5 eV)和氧(约531 eV)。在XPS高分辨C 1s光谱中观察到4个峰(图S1a,Supporting Information),结合能分别为284.5、285.3、286.0和288.2 eV,这归因于sp2杂化C、C―S或C―N、C―O―C和C=O结构。在XPS高分辨N 1s光谱中(图S1b)在398.5和399.7 eV处有两个峰,分别归因于吡啶N和吡咯N结构。在XPS高分辨S 2p光谱中(图S1c)主要由以结合能为164.0和167.6 eV为中心的两个峰组成,表明硫存在两种化学环境。前一个峰可以被拆分成结合能为163.5和164.6 eV两个不同的组分,这与―C―S―键的2p3/2和2p1/2位置一致,这是由于它们的自旋-轨道耦合产生的。后一个峰可拆分成三个峰,结合能分别为167.6、168.7和169.5 eV,归因于―C―SO–x(x= 2,3, 4)结构,可能是硫酸盐或磺酸盐。在CDs的XRD谱图中(图S2a,Supporting Information),约在2θ=24.6°处具有一个较宽的峰,说明了该CDs主要是以无定型碳形式存在22,23,这可能是由于存在氮、硫和含氧基团导致。图1b为制备得到的CDs的红外光谱,分析得到的红外图谱中的峰:3296 cm-1归属为O―H键,2750–3000 cm-1的几个强峰归属为C―H或N―H键,1762及1695 cm-1归属为C=O键,1050 cm-1归属于C―O―C、―SO3―键的伸缩振动,1150–1550 cm-1归属于C―O、C―N及C―S键,400–650 cm-1处的峰为C―H的振动峰24。综上,红外数据显示所制得的碳量子点中可能含有羟基、氨基、羰基、磺酸基、酯基、醚键、碳氮键等基团。在碳纳米材料的拉曼光谱中,D带代表着缺陷程度,而G带则是源于sp2碳原子的E2g声子23,25。在CDs的拉曼光谱中,只有在大约1400 cm-1处观察到D带的出现(图S2b)。从CDs的透射电镜(图2a)中可知碳量子点的分布均匀,颗粒较小,粒径大约在3–4 nm左右。但由于铜网表面的碳膜与碳量子点的密度相似,导致衬度偏低,看起来颜色较浅,但是依然可以从电镜图中可以清晰观察得到。然而,CDs的高分辨透射电镜图像中并未显示任何清晰的晶格条纹,这表明其具有非晶态性质,是以无定型碳的形式存在,这与XRD结果相符合。利用动态光散射方法测得分散在水中的CDs粒径为4.86 nm(图2b),较透射电镜结果稍大,可能是结合了部分溶剂水分子所导致的。
3.2 随激发波长变化而变化的荧光性质
图3给出了微波法合成的CDs的紫外可见吸收光谱及不同激发波长下的荧光发射光谱,其紫外可见特征吸收峰较为明显,大约位于345 nm附近。对激发波长360–520 nm激发的荧光发射谱进一步细致性的测量,结果如图3a所示。随着激发波长从360 nm增加到520 nm,荧光强度先增大后减小,在激发波长为440 nm时,得到最大发射波长为548 nm。随着激发波长的增大,发射光谱也随之红移,且在400–700 nm范围内存在一个极具特征的宽峰,表明CDs表面有不同荧光发射基团相互影响。将所有激发波长下的发射光谱对最大激发波长(440 nm)下的发射光谱的最大强度作归一化处理,得到图3b。可看出随激发波长的增大,最大发射波长红移趋势更为明显。以最大发射波长λem,max对最大激发波长λex,max的变化拟合,可得如式(1)的变化关系。

式中λ0、A、B、C均为常数,当取值分别为530.59、333.82、1.25、50.63时,拟合效果最好R= 0.993。利用上述关系可以作为判别最大发射波长λem,max与最大激发波长λex,max二者的标准曲线,当测量得到上述CDs的一个最大发射波长时,即可推知其对应最大激发波长,反之亦然。

图2 (a) CDs的透射电镜图;(b)动态光散射测得的CDs的水合粒径分布Fig. 2 (a) TEM and (b) Hydrous particle diameter statistics of CDs.
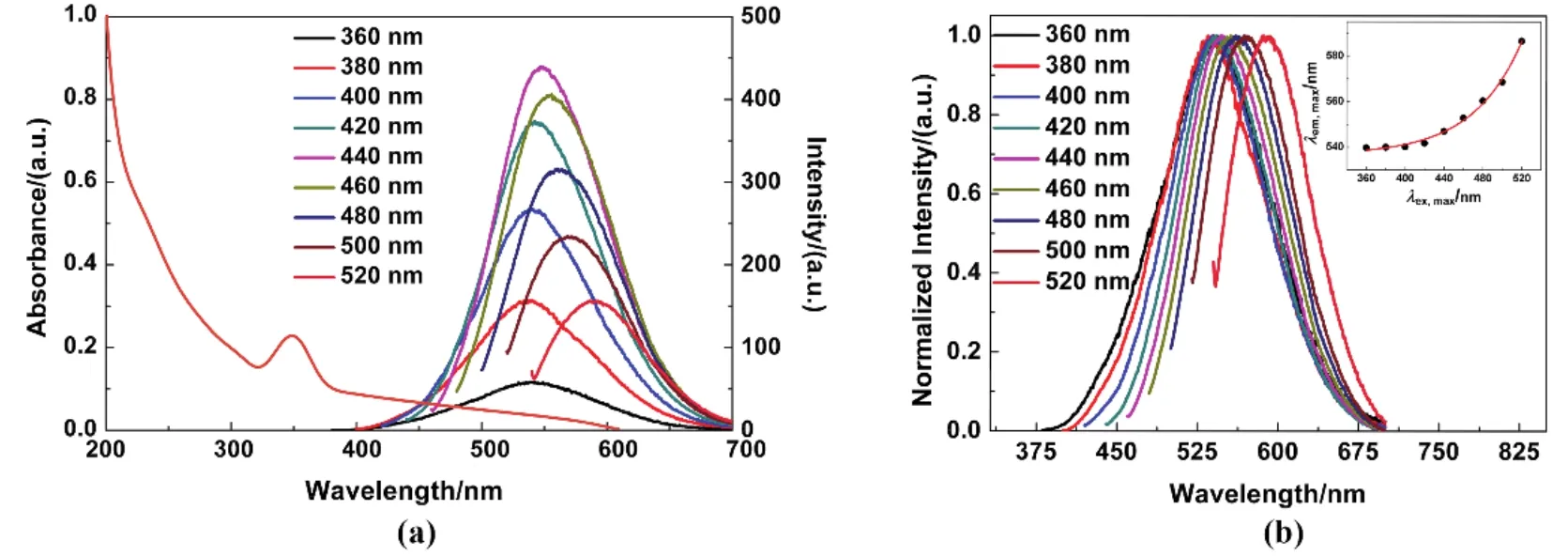
图3 碳量子点在pH = 7的B-R缓冲液中的荧光(a)紫外可见吸收光谱及发射光谱图;(b)归一化发射光谱(λex = 360,380, 400, 420, 440, 460, 480, 500, 520 nm),内插图为最大发射波长λem, max对最大激发波长λex, max的变化关系Fig. 3 (a) The UV-Vis absorbance and emission spectrum and (b) normalized emission spectrum of CDs in B-R buffer solutions (pH = 7; λex = 360, 380, 400, 420, 440, 460, 480, 500, 520nm. The inset shows the plot of λem, max versus λex, max).

图4 碳量子点的在不同缓冲液中的荧光(a)发射光谱图(内插图为不同pH下CDs的颜色变化);(b)归一化发射光谱;(λex = 440 nm,pH = 2.18, 3.59, 4.33, 5.56, 6.37, 7.63, 8.35, 9.25, 10.24);(c)最大发射波长λem, max对pH的变化关系;(d)不同pH下CDs发射光谱的色度变化Fig. 4 The emission spectrum of CDs in different pH B-R buffer solutions (The inset shows the color change of CDs versus pH); (b) Normalized emission spectrum of CDs. (λex = 440 nm, pH = 2.18, 3.59, 4.33, 5.56, 6.37, 7.63, 8.35, 9.25, 10.24).(c) The plot of λem, max versus pH; (d) CIE image of CDs.
3.3 随pH变化而变化的荧光性质
CDs在不同pH的缓冲液中表现出明显的颜色变化,随pH的增大棕黄色逐渐加深。在不同pH的B-R缓冲液中测得CDs的荧光发射谱的变化情况如图4a所示。在相同激发条件和浓度条件下,所得CDs的荧光强度随pH的升高而降低,并且CDs发射峰位置随pH的升高而红移(图4b)。更换缓冲体系后(如改用HAc-NaAc缓冲体系),荧光峰形并未发生明显变化(图S3,Supporting Information),荧光随pH的变化规律也没有发生变化,说明CDs荧光随pH的变化与缓冲体系的成分无关,而是主要由pH变化引起的。
联系红外图谱的相关数据,可以做出推断:由于所合成的CDs表面富含羧基、氨基、羟基、磺酸基和酯基等含氮、氧、硫的基团,容易与H+及OH-相互作用,因此其对pH的变化有一定的响应能力7。以最大发射波长λem,max对pH的变化拟合,可得如式(2)的变化关系。

式中A、B均为常数,当取值分别为2.79及535.73时,拟合效果最好R= 0.993 (图4c)。利用上述关系可以作为判别最大发射波长λem,max与pH二者的标准曲线,当已知任意一个CDs的最大发射波长时,即可其所处的环境的pH值,反之亦然。
将上述归一化发射光谱变化转换为色坐标,绘制于国际照明委员会(Commission Internationale de L’Eclairage,CIE)规定的色度图中(图4d)。由于色度图直观反应出色彩的变化,因此就可以通过肉眼或是相机识别色彩变化从而直接读取对应的pH值,成为一类光学“pH试纸”。
3.4 随金属离子浓度变化而变化的荧光性质
铜是人体必需的一种微量元素,广泛存在于人体内的所有器官与组织中,对于维持人的生命活动发挥着重要作用。目前,痕量铜的测定方法主要有原子吸收光谱法、萃取原子吸收光谱法、电化学分析法等。但不可避免的是,这几种方法往往都会受到其他金属离子的干扰。有文献曾报道可以将含有氮修饰的碳量子点用于Cu2+及其他金属离子的检验中26,27。

图5 制备的CDs在HEPES缓冲溶液中,λex = 440 nm时的(a)加入Cu2+荧光发射光谱(CCu = 2 × 10-4,4 × 10-4,6 × 10-4,8 × 10-4 mol·L-1);(b)加入 0.01 mol·L-1 EDTA 的荧光发射光谱(VEDTA = 0, 20, 40, 60, 80 μL);(c)Stern-Volmer猝灭关系;以及CDs在(d)HEPES缓冲溶液(pH = 7)及(e) B-R缓冲溶液(pH = 5.56)时的IF0/IF值Fig. 5 Fluorescence emission spectrum of the as-prepared CDs as function of Cu2+. 20 µL of the as-prepared CDs was added into 0.2 mol·L-1 HEPES buffer solutions (λex = 440 nm, CCu = 2 × 10-4,4 × 10-4,6 × 10-4,8 × 10-4 mol·L-1)(a) with increasing concentration of Cu2+ and (b) with different volume of 0.01 mol·L-1 EDTA (VEDTA = 0, 20, 40, 60, 80 µL);(c) The Stern-Volmer plot of CDs. The IF0/IF value in (d) HEPES (pH = 7) and (e) B-R buffer solutions (pH = 5.56).
利用蚕砂制备的CDs同样可应用于各种金属离子的检测中,以Cu2+的检测为例。随着铜离子的加入,CDs的荧光强度发生了显著的猝灭(图5a),推测是由于CDs结合后Cu2+吸附到颗粒表面,引起电子转移或CDs聚集,导致CDs荧光强度下降。随Cu2+浓度增加,荧光强度减弱。荧光淬灭的原因可能是Cu2+与碳量子点中N或O的螯合作用使它们间的距离更紧凑,并发生自淬灭。因此设计了竞争实验进行验证。在CDs与Cu2+的混合溶液中加入络合能力更强的配体EDTA将竞争性地与铜离子结合,从而引起Cu2+从CDs表面解离,与EDTA结合重新扩散到溶液中去,CDs的荧光则会回复。当往聚集体中加入强的络合配体EDTA后,实验结果证实了我们这一设想,CDs的荧光有所回复(图5b)。猝灭的过程通常可以用Stern-Volmer关系进行描述,即:

其中IF0和IF分别为无淬灭剂Cu2+和淬灭剂Cu2+存在时的荧光强度,KSV为Stern-Volmer淬灭常数,[Q]为淬灭剂Cu2+浓度。利用上式拟合Cu2+对CDs的猝灭关系,可得如图5c所示的线性关系。图中斜率KSV与淬灭速率和无淬灭剂时荧光分子的激发态寿命有关,当KSV取(0.798 ± 0.035) L·mol-1时,拟合效果最好,R= 0.993 (图5c)。该线性关系可以作为判别CDs荧光强度变化与铜离子浓度的标准曲线,利用荧光强度变化实现对铜离子浓度的准确测量。与此同时在相同浓度下,在HEPES缓冲溶液中(图5d)往CDs中加入其他常见的二价及三价金属离子,大部分不会引起CDs荧光的显著变化,体现了较好的选择性。
而在酸性B-R缓冲液(图5e)中,Fe2+、Co2+、Ni2+的存在均会对Cu2+的检测有一定的干扰,Fe3+及Al3+的干扰最大,这可能是由于碳量子点表面部分羧基结合Fe3+及Al3+所致,从另一方面也说明该CDs可用于对Ni2+、Fe3+、Al3+等的检测。上述结果说明,在HEPES缓冲溶液中(中性条件下),基于蚕砂制备的CDs可以高选择性地实现对Cu2+的检测,而在B-R缓冲液中(酸性条件下),该CDs可以在无其他离子干扰的情况下,分别实现对Cu2+、Fe3+、Al3+、Ni2+及Fe2+的检测。
3.5 随温度变化而变化的荧光性质
由于分散在水中,因而温度变化范围设定为20-70℃。在该温度范围内,CDs的荧光强度会随着温度的升高显著降低(图6a),但荧光峰并未放生明显的移动。上述现象可能是由于温度升高导致分子运动速度加快,CDs之间的碰撞概率增加,从而使得非辐射跃迁几率大大增加,从而降低了CDs的荧光效率引起的28,29。CDs的荧光强度IF与温度T之间满足如式(4)所示的线性关系:

图6 (a)制备的CDs在B-R缓冲溶液中λex = 440 nm时不同温度下荧光发射光谱;(b)荧光峰强度随温度的变化关系Fig. 6 (a) Fluorescence emission spectrum of the as-prepared CDs at different temperature in B-R buffer solutions (λex = 440 nm). (b) The plot of emission intensity versus temperature.

式中a、b均为常数,当斜率b和截距a分别取值为-2.3及321.3时,线性关系最好,R= 0.999。该线性关系可以作为判别CDs荧光强度变化与温度之间的标准曲线,利用荧光强度变化实现对温度的传感和监测。
3.6 随溶剂极性而变化的荧光性质
基于蚕砂制备的CDs不仅可以较好地分散在水中,当换用其他不同溶剂时,如N,N-二甲基甲酰胺(DMF)、丙酮、甲醇、乙醇、乙酸乙酯及乙腈时,CDs均可以较好地分散在其中。随着溶剂极性的增加,CDs的最大荧光发射波长随之红移(图7a)。这种溶剂效应可能是由溶剂附着或在CDs点表面形成不同的发射陷阱引起的30,31。这几种溶剂的极性经验参数及分散在其中CDs的最大荧光发射波长如表1所示。
CDs的荧光强度IF与溶剂极性经验常数ET之间满足如式(5)所示的线性关系:

式中a、b均为常数,当斜率b和截距a分别取值为0.67及506.3时,线性关系最好,R= 0.911 (图7b)。其中CDs在乙腈及DMF中最大发射波长位置偏离线性最为明显。该线性关系可以作为判别CDs荧光强度变化随溶剂极性变化的标准曲线,通过对比拟合得到的溶剂极性经验常数,可粗略判断CDs分散的溶剂极性。
与目前已报道的利用天然产物如蚕丝32,33、树叶34及西瓜皮19等制备得到的碳量子点相比,基于蚕砂制备的CDs虽然不具备明显的晶体结构,是以无定形碳的形式存在的,但其具有更为丰富的表面基团,使得其对于多种环境因素变化(pH、温度、离子浓度、溶剂极性等)均在较大的范围内具有优异的响应性质,且都具有一定的变化规律。该CDs荧光性质随多种不同环境因素的变化而变化的性质将为发展CDs作为多功能传感材料提供多种可能及潜在的应用前景。
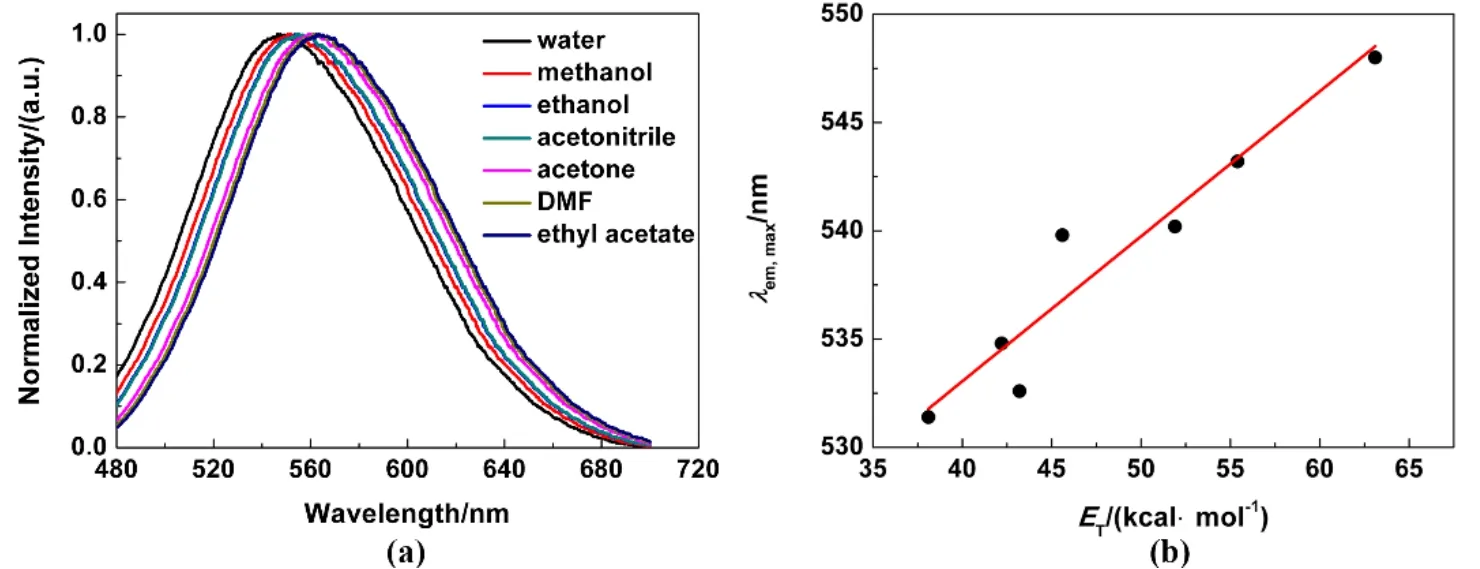
图7 (a)制备的CDs在不同极性溶剂下荧光发射光谱;(b)荧光发射峰强度随溶剂极性经验的变化关系Fig. 7 (a) Fluorescence emission spectrum of the as-prepared CDs in different solvents (λex = 440 nm).(b) The plot of emission intensities versus empirical parameters of solvent polarity ET.

表1 溶剂极性经验常数ET (30 °C)及分散在其中CDs的最大发射波长Table 1 Empirical parameters of solvent polarity ET (30 °C) and λem, max of CDs.
4 结论
综上,利用蚕砂作为初始原料,采用微波合成的方法制备得到了一种粒径分布均匀,发光性质优良,含氮、硫修饰的碳量子点材料。针对其荧光性质随激发波长、pH、金属离子浓度、温度及溶剂极性的变化,开发出一系列基于碳量子点的传感探针。
(1)碳量子点的荧光发射峰强度随激发波长的增加呈现先增大后减小的规律,荧光最大发射强度随激发波长的红移而逐渐红移,激发–发射波长之间呈现指数型变化关系。
(2)在pH为2.18–10.24范围内,碳量子点的荧光发射峰强度随pH增加而逐渐减小,荧光最大发射强度随pH的增加而逐渐红移,pH–发射波长之间呈现线性变化关系。
(3)碳量子点的荧光发射峰强度随金属离子浓度的增加而逐渐降低,中性条件下,碳量子点可以高选择性地实现对Cu2+的检测;在酸性条件下,碳量子点可以在无其他离子干扰的情况下,分别实现对Cu2+、Fe3+、Al3+、Ni2+及Fe2+的检测。金属离子浓度–荧光强度之间呈现Stern-Volmer型线性变化关系。
(4)碳量子点的荧光发射峰强度随温度的增加而逐渐降低,可能是由于分子热运动导致的非辐射跃迁过程所导致。温度–荧光强度之间呈现线性变化关系。
(5)碳量子点的荧光最大发射强度随所分散溶剂的极性增加而逐渐红移,荧光强度与溶剂极性经验常数ET之间呈现线性变化关系。
Supporting lnformation:available free of charge via the internet at http://www.whxb.pku.edu.cn.
