中国生物药CDMO/CMO展望和投资策略分析
2019-10-31■文/曹锋
■ 文 / 曹 锋
随着将来生物药研发的进一步提升,以及生物药价格的进一步下降,中国生物药CDMO/CMO将得到迅猛发展,未来具有较强研发能力的一体化生物药CDMO/CMO企业或能极大降低生产成本的生物药CMO企业将脱颖而出。
生物药发展拉动CDMO/CMO行业崛起
进入21世纪后,生物药开启了快速发展期。医疗健康领域服务商IQVIA分析报告显示,2014年至今,生物药的复合增长率超过12%,远高于小分子药物类的3.5%。2018年,全球生物药市场规模达4 428亿美元,对总药品市场的贡献近3成。全球销售额排名前10位的药品中,生物药占80%,单个药物的销售额都可以达到几十亿甚至200亿美元的销售规模。
说到生物药,不得不提的就是生物类似药。根据弗若斯特沙利文咨询公司报告,生物类似药将成为未来生物药市场增长的主要推动力。预计全球生物类似药市场2016年到2021年将超过50%的复合增长率,市场规模将达到366亿美元。
与化学仿制药相比,生物药和生物类似药的开发难度更高、生产工艺更为复杂、研发周期更长(8年到10年以上)、研发成本也更高(上亿美元)。因此,生物药的研发生产外包比化学仿制药将有更大的需求度,可以降低资金和时间成本。
早期合同加工外包(CMO)可能仅是作为简单的产能补充,如今CMO企业通过强化自身技术能力将业务由简单的“技术转移+定制生产”提升为“定制研发+定制生产”。这类强化版本的CMO公司被称为合同定制研发生产(CDMO)。CDMO有助于实现临床期药品由实验室向工厂车间转化,在药品上市后则能够降低制造成本,提升生产效率。因此,与传统CMO相比,CDMO与客户之间的合作更为持续和紧密,营利能力也更强。
近年来,国际上创新药研发企业的效率越来越低,成本攀升。为了降低成本,国际大型药企正在逐步减少自己的生产设施,将更多的产品转向外包服务合作,包括辉瑞、诺华、礼来等公司都已公布将逐步提高对CDMO和CMO的需求比例。
生物药CDMO/CMO市场分析
●市场规模不断扩大
全球生物药CDMO/CMO市场规模从2012年至2017年复合增速超过15%,高于全球医药研发服务的整体水平。未来,随着制药企业在生物制剂领域的持续投入,预计2018年至2021年全球生物药CDMO/CMO市场将按照复合年增值率19%的速度增长,以市场规模计算,2021年将达到200亿美元。此外,2016年全球生物药CDMO/CMO市场的渗透率为15.8%,而相对潜在生物药CDMO/CMO市场为529亿美元,表明其具有显著的增长空间。
中国生物药CDMO/CMO市场基数较小,但增长快,是全球增长最快的市场,远超全球生物药市场整体增长,并在未来有望继续保持强劲的增速。2012年,中国生物药CDMO/CMO市场由7亿元人民币增至2016年的21亿元人民币,复合年增长率为30.5%。预计到2021年,中国生物药制剂市场规模将达到92亿元人民币,2016年至2021年的复合年增长率为34.8%。目前,国内的CDMO/CMO市场主要是CDMO,即临床前研究和临床样品生产,商业化CMO占比很小。随着国内生物药及生物类似药的陆续上市,商业化CMO有望爆发式增长。

表1 化学仿制药、生物类似药、生物药的研发和生产对比
●订单源头增长强劲
生物药CDMO订单主要来源于研发阶段创新药、上市专利药和生物类似药等3种类型。
研发期创新药类订单可以为客户进行工艺路线的探索和优化,主要集中在临床阶段的药品生产服务。创新药研发是国际主流,国内趋势表现为CDMO助力创新药研发,代表企业药明生物早期项目订单年增速超过50%,后期订单数量同样保持着大比例的增速。
上市专利药类的CMO服务能够成为企业强有力的产能补给者,同时在行业降价和竞争对手产品压力下降低自己的生产风险和成本。抗体类药物是目前生物药最主要的品种,占比接近50%,未来会更高。近年来,抗体类新药迎来了审批高峰,2014年至今保持逐年增多的趋势。
生物类似药类是未来CDMO服务的重要方向,可以为企业缩短产品的上市年限并降低成本。虽然生物类似药还面临各国卫生医疗机构的监管、研发、生产、医保等问题,但是其优势也十分明显,可以为医生和患者提供更多的处方选择、缓解经济压力等。科睿唯安公司的数据显示,目前全球处于活跃状态的生物类似药共718个,其中上市121个,批准15个,注册阶段31个,III期临床72个,II期临床8个,I期临床75个,还有386个处于发现阶段。IQVIA公司的数据也显示,未来5年内,生物类似药有望为五大主要欧盟市场和美国市场的医疗卫生体系节约超过500亿欧元的费用。纵观全球生物类似物的研发,生物类似物已经进入收获期。
●政策助力CDMO/CMO行业发展
2018年5月,国家发展和改革委员会、工业和信息化部、国家卫生健康委员会和国家药品监督管理局联合发布《关于组织实施生物医药合同研发和生产服务平台建设专项的通知》,明确支持CDMO/CMO行业的发展,力争达到每年100个以上新药开发提供服务的能力,单个项目国家补助资金原则上为项目总投资的30%左右,金额不超过1亿元人民币。
2017年,药品上市许可持有人(MAH)制度正式落地施行。MAH制度的实施将使CDMO/CMO企业能承接更大范围的订单。从上海市公示的两批MAH试点品种名单来看,已申请的25个药品中有8个是与 CDMO/CMO企业合作的,充分反映出MAH制度提高了新药研发CDMO/CMO行业的订单数量。
生物药CDMO/CMO竞争格局
●商业模式
商业模式可以根据企业特色分成3种:一站式服务平台模式、上下游一体化模式和大规模生产模式。
一站式服务平台模式具有最完整的服务,特别对中小型生物制药公司将给予极大的赋能。其主要有2个优势:从CDMO企业角度看,与客户深度合作,可向同一客户提供更多产品服务,降低客户开发和维护成本;从客户角度看,产品临床开发至上市销售的生产只需要与单一供应商联系,效率更高。
上下游一体化模式指企业对上游的培养基、生物反应器,下游的层析介质、层析设备、膜材料及过滤系统等具有研发生产和销售能力。目前,这些材料主要还是依赖进口,价格高昂,使生物药的生产成本居高不下。设备国产化、原材料和耗材自主生产将极大地降低生产成本。另外,原材料、耗材等对外销售也能成为企业重要的销售收入来源。
大规模生产模式目前还是国际巨头的天下,国际巨头在设备、原材料、耗材、技术等方面差距不大,在此水平上的竞争优势就是产能。大规模的稳定生产可以大大降低生产成本,产生规模经济。国际巨头如龙沙集团、勃林格殷格翰、三星生物等都在大规模建设1.5万升、2万升的生产线。
生物药大规模生产模式目前还是国际巨头的天下,国际巨头在设备、原材料、耗材、技术等方面差距不大,在此水平上的竞争优势就是产能。大规模的稳定生产可以大大降低生产成本,产生规模经济。
●生物药CDMO是高壁垒行业
医药定制研发生产企业主要服务于创新药。关于创新药的研究、开发、生产及商业化应用均具有较高的门槛,这直接决定了医药定制研发生产服务行业的门槛,主要体现在以下方面。
(1)资金壁垒
生物药CDMO/CMO属于重资产行业,建立符合动态药品生产管理规范(cGMP)要求的设施的资本很高,前期需要大量资本投入。建设一座新的生物制剂厂房投资可能高达数亿美元,尤其是大规模不锈钢生物反应器。
(2)技术壁垒
生物药CDMO属于技术密集型行业,生产生物药的大分子的脆弱性及活细胞的敏感性,对生物制剂发现、开发和制造提出复杂的技术要求。此外,生物制剂分子体积大且复杂,会遇到制定相应测试方法以分析这些产品时进行质量控制的挑战。若无长时间、高成本的研发投入及技术储备,行业外企业很难真正进入该行业。
(3)人才壁垒
生物制药需要不断对工艺进行技术创新并产业化运营,如何聚集一支优秀的研发、生产以及项目管理的人才队伍是关键。我国乃至全球在生物医药大生产方面的高级管理人员都是稀缺的。
(4)客户壁垒
生物药CDMO企业基于以往业绩记录、行业信誉、产品质量、监管合规记录及知识产权保护能力获取客户订单,半途更换CDMO公司的成本很高。
(5)运营管理壁垒
生物药CDMO企业需要建立完善可靠的成本及效率控制、质量控制和EHS管理体系。由于生物药生产工艺复杂、成本高昂,质量控制体系严格,容错率低,其对成熟和完善运营管理体系要求较高。
●生物药CDMO行业集中度高
艾美仕市场研究公司(IMS)的数据显示,全球综合CDMO市场(生物药+小分子药)排名前5位的企业只占全球市场份额约10%,而生物药CDMO市场前7位的企业占市场份额的30%以上,且2018年的数据相比2017年有进一步提高。由此可见,生物药CDMO企业将更容易产生行业巨头,大体量、大规模化也是生物药CDMO企业竞争的未来趋势。
从市场份额看,龙沙集团是行业龙头企业,正准备在国内布局生物药CDMO。占市场份额第二的勃林格殷格翰公司总产能达24万升。2013年6月,勃林格殷格翰公司在上海启动了跨国药企在国内的首个基于哺乳动物细胞培养技术生产的生物制药基地建设,目前已有100升和500升规模临床样品生产以及2 000升一次性反应器临床样品和商业化生产能力。未来,勃林格殷格翰公司还将灵活增加2 000升一次性反应器和灌装设施以满足市场增长的需求。其客户包括百济神州、再鼎医药和北海康成等国内生物药研发行业领先者。
三星生物在生物药领域的布局有两家公司:Samsung Bioepis和Samsung Biologics,后者主营生物药CMO业务,总产能达到36.2万升,成为全球生物药CMO领域产能规模第一的企业。其订单主要以自己研发或合作的生物类似药产品为主,目前已有多个重磅级生物类似药产品获欧洲药品管理局(EMA)批准。
药明生物发展快速,已跃居行业第四。其在临床研发期药物的CDMO竞争实力已经毋庸置疑,但商业化订单只有1个,面对国内未来快速崛起的商业化CDMO竞争,未来发展如何将拭目以待。
●成本控制是生物药CDMO企业的竞争要素
以单抗药生产为例,生产设施一般可以分为细胞培养及纯化生产线和制剂灌装生产线。目前,主流的细胞培养工艺是流加式培养(Fed-batch),最大可线性放大至2万升,操作比较简单。其生产成本构成主要有设备、原材料、消耗品、劳动力等,其中反应器是设备成本的重心,而且规模越大越能体现成本优势。例如,2 000升生物反应器与1.5万升生物反应器相比,其尺寸增大7.5倍,但后者的购买价格仅是前者1.5倍左右,并且所需要的操作人员数基本不变,而大规模反应器单批次生产的成本单价则可以降至1/3。
除了设备成本外,大规模反应器主要的成本构成是原材料和消耗品。原材料包括无血清培养基、缓冲液、注射用水等,其中主要是无血清培养基,占比为90%以上。消耗品主要包括细胞培养瓶、层析介质、滤膜等,其中主要是蛋白A亲和层析介质,占比为80%以上。目前,原材料和耗材以进口为主,但国内相关企业的发展也十分迅速,未来有望实现国产替代,将显著降低大规模生产的材料成本。
●工艺技术的发展
除了在硬件上降低成本外,工艺技术优化提高产量也是提升效益的主要手段,如对宿主细胞改造提高表达量和上游优化等,但也有一定的局限性。当表达量达到一定程度,增加上游的表达水平对成本下降的贡献不大,除非高浓度的单抗料液可以使下游分离更为简单。因此,对于表达量的优化需要理性分析,更高表达量细胞株的购买是否有必要,或者高表达量的研发费用是否有相应的效益回报,都需要仔细权衡。此外,过高表达量可能会导致杂质增多,增加下游工艺处理难度。因此,当表达量提高会把成本控制的关键转移到下游过程时,优化下游过程将成为主要目标。
每个公司最终都会根据自己的表达系统和细胞培养过程以及其在研发中主要使用的单抗类型和子类来定制单抗下游平台的方法。已有安进制药、基因泰克、渤健、KBI等部分大型药企披露了其下游工艺平台。典型的精制工艺通常采用先阳离子交换层析(CEX)吸附模式,再根据需要采用疏水层析(HIC)的流穿模式去除高聚物,或采用阴离子交换层析(AEX)去除宿主蛋白残留(HCP)。
●未来可能的新兴生产工艺技术
连续生产是一种新兴技术,可以通过不间断的流程更快、更稳定、更经济、更安全地生产,可减少人工成本。连续生产还可以做到实时质量监控,随时撇下不达标的中间产品,从而让产品更可靠并减少浪费。连续生产可以实现设备小型化,高效利用厂房空间,大幅度缩小厂房的使用面积,减少固定资产的投资。连续生产还可以提高介质利用度,降低流动相及介质的使用量,从而降低生产成本。此外,连续生产规模易于调节,可大可小,方便适应不断变化的市场需求。这种操作灵活性同时减轻一些审批后的监管任务,也使得工艺更容易放大,减少传统工艺放大所面临的诸多验证和重复的问题。目前,药明生物在这一技术的应用上走得较前,未来可以期待,但在商业化生产应用上还面临许多监管的问题和技术的挑战。
在抗体的表达上除了通过哺乳动物细胞培养外,还可以在其他表达系统中产生,目前有转基因植物表达系统、大肠杆菌表达系统、酵母表达系统和微藻表达系统等。这些表达系统可以提高表达量,在其他领域已有应用,但在单抗药物上的生产运用只是处于尝试开发期,尚存较多不确定因素,仅仅在观望阶段。
层析步骤是限速步骤,尤其是遇到大批量生产的产品时,采用大体积的生物反应器进行高表达培养时,层析分离易受到载量限制。使用聚合物的选择性沉淀方案、双水相萃取(ATPS)等是目前尝试开发阶段的技术,但也只是技术早期探索阶段。
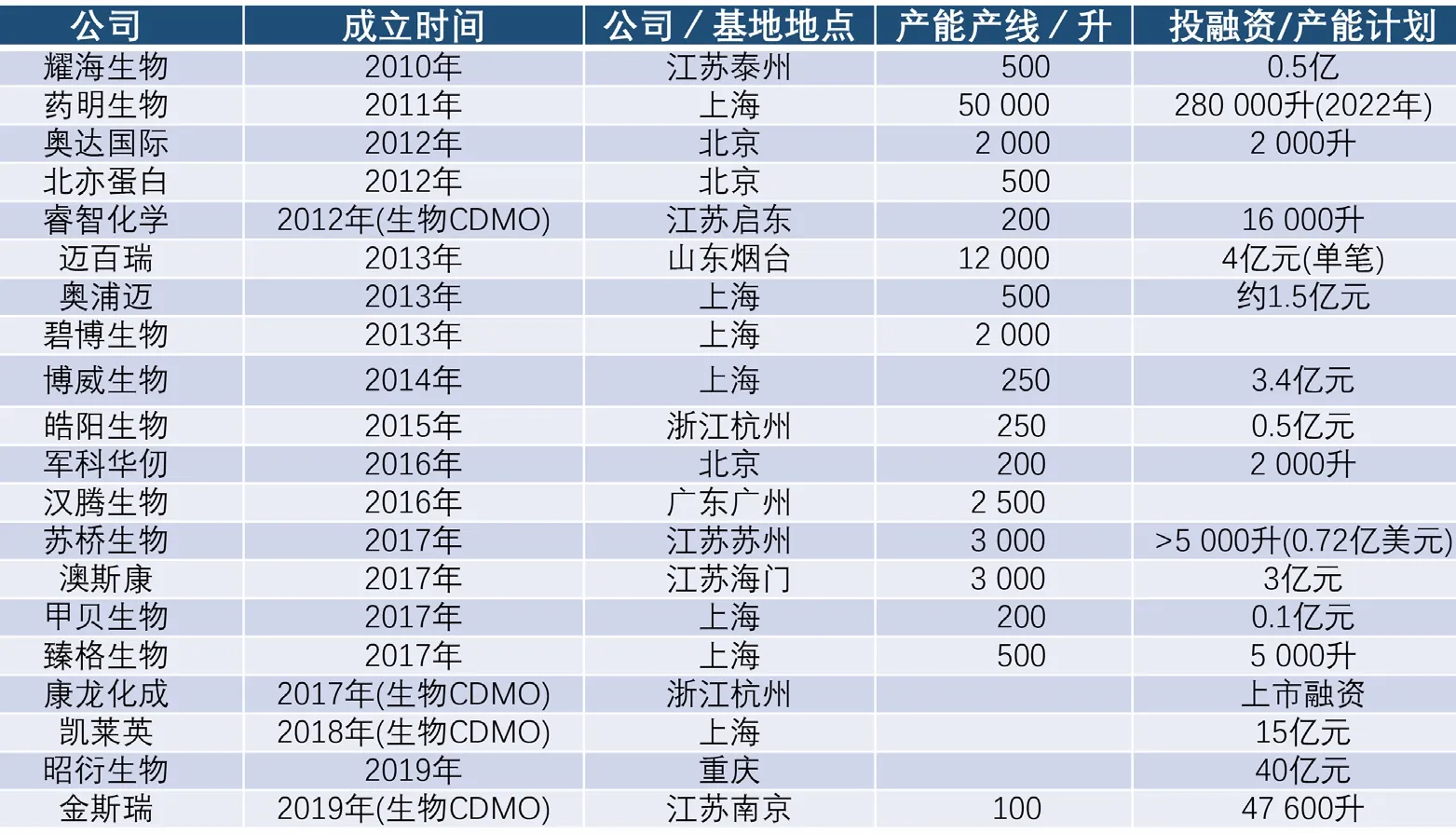
表2 我国部分CDMO企业
国内生物药CDMO投资分析
从需求的角度来看,生物药的发展趋势已毋庸置疑,但到底发展速度会多快,对于产能的需求会多大,这是推动生物药CDMO行业发展的最大动力。目前,讨论最多的生物药应该是抗体类药物,尤其是PD-1单抗药物。2019年上半年,君实生物和信达生物两家公司的PD-1单抗药物销售额均已超过3亿元人民币,这样的业绩完全超出了大多数主流预期。随着未来药物价格降低,即使从销售额上不一定能够看出足够的增长,其背后隐藏的对药物的使用量的增长必须要认清。从使用剂量来看,目前热销的PD-1单抗药物在使用剂量上都要显著高于以往的生物药。我们认为,未来对抗体类药物的需求量有可能会超出现在主流的乐观估计。
生物药的需求来自哪里,毫无疑问是患者。世界人口大国中国和印度都是发展中国家,如今,随着GDP的上升,人民收入的提高,对价格偏贵的单抗药物的需求才刚刚开始。再加上成本降低、市场竞争压价等降价行为,未来必将产生对生物药需求的暴增。以往提到化学仿制药CDMO的发展,肯定会提到由于人力成本等因素,产业由欧美向中国、印度转移。如今,生物药CDMO产业的人力成本优势并不明显,但龙沙集团、勃林格殷格翰等行业巨头纷纷开始在中国布局产能,三星生物等亚太公司产能疯狂扩张,究其原因不在于成本的降低,而是需求的强劲。
从供给的角度来看,目前国内真正做CDMO/CMO业务的专业公司有二三十家(我国部分CDMO企业见表3),如果与做新药的公司相比,无论是数量还是体量都还有很大的成长空间。国内公司中除了已在香港交易所上市的药明生物之外,还有许多已经具备一定规模和实力的后起之秀,如迈百瑞、澳斯康、苏桥生物等都获得了大额的融资,另外还有如碧博生物、甲贝生物等刚进入发展期的企业。生物药生产外包最看重质量和知识产权的保护等,这些由专业的外包公司做是最合适的。目前,国内现有的专业外包公司产能还不到10万升,虽有扩张计划,但依然是百家争鸣的情形。
我们认为,兼备一定研究能力和较强业务拓展能力,拥有2 000升及以下规模生物反应器,具备一体化服务以及接单能力的CDMO企业,将在未来5年中突围出来。企业具有1.5万升、2万升等大型生物反应器将大大降低成本,能接到国内重磅药物的单子,但同时需要具备国际接单能力。拥有国际企业经验的专业团队,具有更高质量管控能力和知识产权保护意识等CDMO最关键因素,可以提高客户黏性,从而形成壁垒。同时,具有人才自主培养能力将更有利于企业稳定发展。
