PCI术前Lp(a)、MAU蛋白水平与冠心病术后冠状动脉再狭窄的关系研究
2019-10-28
经皮冠状动脉介入术(percutaneous coronary intervention,PCI)因具有安全性高、创伤小、术后康复快等特征,已成为临床治疗冠心病(coronary heart disease,CHD)的重要措施,改善了病人的临床病症,但术后支架内再狭窄(in-stent restenosis,ISR)是影响支架长期使用的重要因素,也是影响PCI手术治疗效果的因素[1]。但术后诱发ISR的危险因素分析尚未明确,研究指出,PCI术后ISR与冠心病危险因素不同,该现象是较为复杂的生理病理过程,由多因素参与其中。炎症反应、细胞因子释放在动脉粥样硬化形成、PCI术后血管内皮损伤的作用已成为ISR研究热点[2]。为分析血清脂蛋白(a)[Lipoprotein(a),Lp(a)]、尿微量白蛋白(microablu-minuria,MAU)水平变化与冠心病PCI术后ISR的相关性,本研究对我院120例行PCI术的冠心病病人进行随访,以冠状动脉造影检测为标准,分析其在ISR发生中的作用。现报道如下。
1 资料与方法
1.1 临床资料 选取2016年4月—2017年4月我院接受PCI治疗的120例冠心病病人,随访12个月进行冠状动脉造影,失访4例,死亡4例。将再次发生冠状动脉狭窄的33例病人作为再狭窄组,将未再出现冠状动脉狭窄的79例病人作为对照组。再狭窄组:男20例,女13例;年龄52~79(62.1±9.5)岁;体质指数(BMI)为(24.2±1.8)kg/m2。对照组:男46例,女33例;年龄47~79(61.0±11.2)岁;BMI(24.0±2.1)kg/m2。两组年龄、性别、BMI等一般资料比较,差异均无统计学意义(P>0.05)。
1.2 纳入与排除标准
1.2.1 纳入标准 ①年龄≤79岁;②冠心病的诊断标准参考中华医学心血管病分会制定的《冠心病诊断与治疗指南》2014年版中的标准[3];③病人均在我院接受PCI治疗,术后接受随访;④冠状动脉再狭窄以冠状动脉造影检查结果作为标准[4],支架内再狭窄(距病变两端<5 mm,狭窄程度>50%),且需要对靶病变血管再次进行血运重建;⑤本研究获得病人知情及医学伦理委员会的批准。
1.2.2 排除标准 ①合并肺、肝、肾功能障碍;②合并凝血功能障碍性疾病;③首次置入支架为金属裸支架;④伴有恶性肿瘤或者具有放化疗史;⑤心肌病、心瓣膜病史。
1.3 冠状动脉造影检查方法 所有病人采用Jndkins冠状动脉造影,经右股动脉或桡动脉路径进行穿刺,选择多部位造影,以冠状动脉狭窄≥50%为阳性。由两名经验丰富的冠状动脉介入医师对造影结果进行详细分析。
1.4 观察指标 检测或收集两组病人PCI前的Lp(a)、MAU、血清总胆固醇(TC)、三酰甘油(TG)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)、空腹血糖(FPG)、血肌酐、尿酸、收缩压(SBP)、舒张压(DBP)、吸烟史、冠状动脉病变部位[左主干(LM);左前降支(LAD);左回旋支(LCX);右冠状动脉(RCA)]、支架直径、支架长度、规范用药情况。所有病人在行PCI前,于08:00抽取空腹肘静脉血3 mL,离心10 min,提取上清液,采用免疫比浊法检测Lp(a)水平,试剂盒购于宁波美康公司。所有病人在住院后第2天清晨取5~10 mL新鲜尿液,离心5 min,提取上层尿液,采用酶联免疫吸附法(ELISA)检测MAU水平,试剂盒由上海蓝基有限公司提供。采用德国罗氏Modular全自动生化分析仪,使用氧化酶法检测TC、TG、HDL-C、LDL-C、血肌酐、尿酸水平,试剂盒由北京博奥森生物技术有限公司提供。采用罗氏血糖仪测定FPG水平,试剂盒购于上海西唐生物科技有限公司。使用mindray IMEC8彩色超声多普勒超声测定仪(购自深圳迈瑞生物医疗电子股份有限公司)检测SBP、DBP水平。
2 结 果
2.1 两组临床资料比较 再狭窄组与对照组的TC、TG、HDL-C、FPG、血肌酐、尿酸、SBP、DBP、吸烟史、冠状动脉病变部位、支架直径、支架长度、规范用药情况比较,差异均无统计学意义(P>0.05);再狭窄组血清LDL-C水平高于对照组(P<0.05)。详见表1。
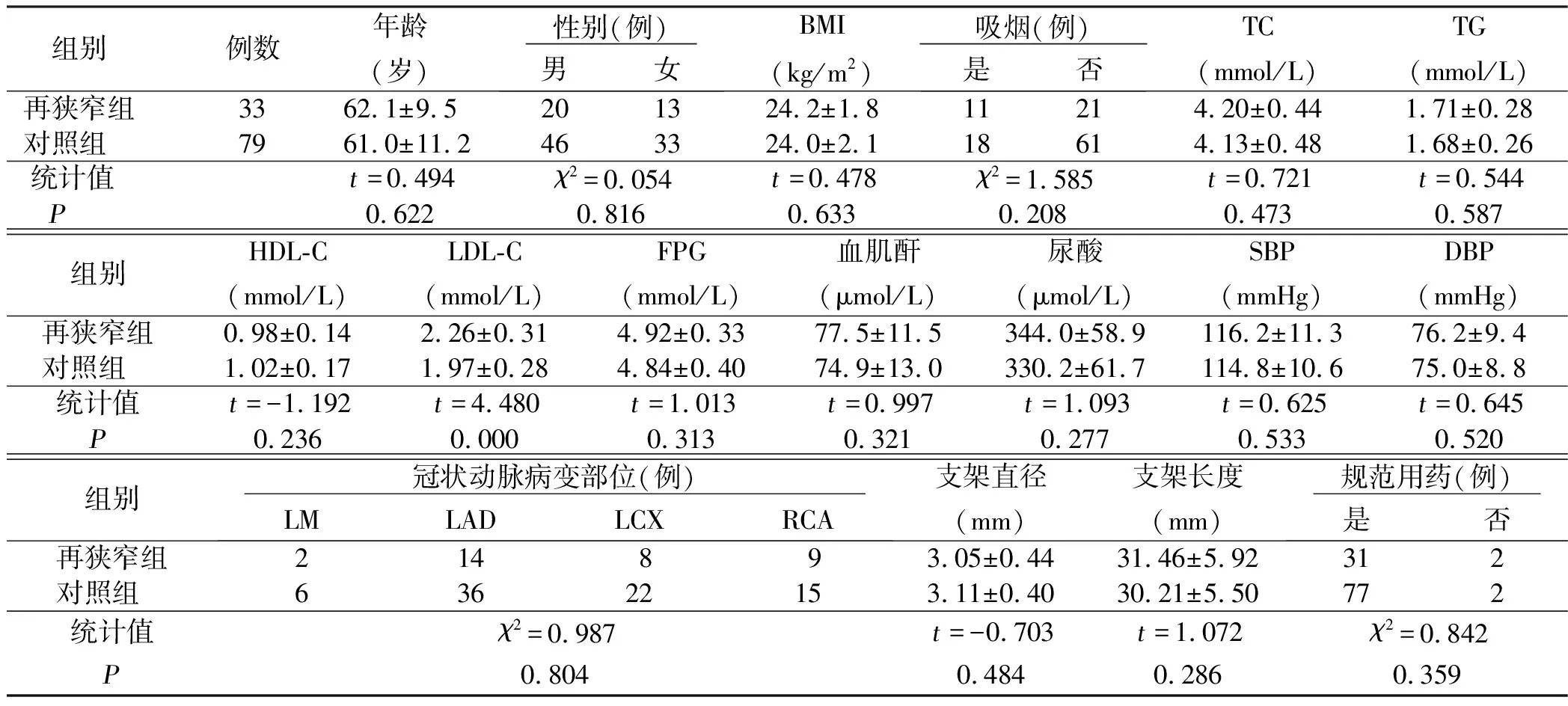
表1 两组一般资料比较
2.2 两组Lp(a)、MAU水平比较 再狭窄组Lp(a)、MAU水平高于对照组(P<0.05)。详见表2。
2.3 冠心病病人PCI术后再狭窄的影响因素 多因素Logistic回归分析结果显示:PCI术前Lp(a)、LDL-C、MAU水平升高是冠心病病人术后发生支架内再狭窄的独立危险因素(P<0.05)。详见表3。


组别例数Lp(a)MAU再狭窄组33208.5±33.662.09±10.56对照组 79143.7±17.243.11±8.73t值13.4769.847P <0.001<0.001

表3 Lp(a)、MAU水平与冠心病病人PCI术后再狭窄的关系
3 讨 论
冠心病作为临床常见的心血管疾病,常见于中老年人群,但目前流行病学显示,其发病呈现年轻化趋势[5]。PCI作为治疗冠心病最常用的血管重建方法,在提高治疗效果的同时也暴露了并发症,即ISR现象,已成为临床最为棘手的问题[6]。ISR是指冠心病病人在PCI术后植入支架的冠状动脉节段冠状动脉造影显示血管管腔内径狭窄≥50%,该疾病的发病过程较为复杂,目前,具体的分子生物学机制尚未明确阐明[7-8]。本研究结果显示,再狭窄组和对照组的TC、TG、HDL-C、FPG、血肌酐、尿酸、SBP、DBP、吸烟史、冠状动脉病变部位、支架直径、支架长度、规范用药情况比较,差异均无统计学意义(P>0.05),这说明以上因素不会对介入治疗病人ISR的形成产生影响。
LDL-C是动脉粥样硬化的始动因素,同时还会在免疫、炎症、氧化应激作用下损伤血管内皮细胞,加速血管狭窄,形成ISR[9-10]。本研究发现,再狭窄组病人的血清LDL-C水平高于对照组(P<0.05),这提示在PCI术后ISR形成中LDL-C发挥重要作用,促进冠状动脉再狭窄的发展。Lp(a)是一种脂蛋白大分子,富含胆固醇,是血管硬化性疾病的血清标志物,能够促进机体血栓形成,诱发动脉粥样硬化[11]。MAU是诊断糖尿病肾病的指标,随着临床对冠心病的研究,指出MAU是冠心病的危险因素之一[12]。本研究中再狭窄组的Lp(a)、MAU水平显著高于对照组(P<0.05),这提示Lp(a)、MAU参与了PCI术后ISR的形成。在PCI术后ISR形成中,其作用如下:①Lp(a)刺激血管内皮细胞、肝细胞分泌大量纤溶酶原抑制剂,引起脂质积聚,诱导血栓的形成,加速动脉粥样硬化的发展[13]。②Lp(a)与纤溶酶原的结构较为相似,竞争性抑制纤溶酶原激活,对其生理功能产生干扰,破坏纤溶系统平衡性,促进血栓形成。③Lp(a)可以激活生长因子(TGF-β)并转化,刺激细胞迁徙,使得血管平滑肌细胞迁徙至内膜,刺激其大量增殖,黏附在血管壁,产生动脉粥样斑块[14]。MAU是机体血管内皮功能障碍的重要标志物,冠心病病人PCI术后会出现神经-内分泌因素介导炎症反应,如血栓形成、血管内膜增生、血管重塑,损伤内膜,使得血管平滑肌细胞过度增殖、迁移,分泌大量的泡沫细胞与巨噬细胞源性泡沫细胞,演变成纤维脂肪病变,导致纤维斑块形成[15]。
为进一步明确冠心病PCI术后冠状动脉再狭窄的影响因素,本研究进行多因素Logistic回归分析,结果显示:PCI术前Lp(a)、LDL-C、MAU水平升高是冠心病病人术后发生支架内再狭窄的独立危险因素(P<0.05),这说明Lp(a)、LDL-C、MAU与PCI术后ISR形成具有密切联系,临床应对行PCI术病人检测以上3项指标,有助于预防术后ISR的发生,促进病人康复。本研究证实Lp(a)、MAU与ISR形成有密切联系,但Lp(a)、MAU与支架内再狭窄、靶病变再次血运重建的关系仍需进行多中心、大样本研究,获得理论支持。
综上所述,PCI术前病人的Lp(a)、MAU水平升高会增加冠心病病人术后发生支架内再狭窄的风险。
