丹参总酚酸滴丸的制备及质量评价
2019-10-24何银舟胡正明程建明
何银舟,胡正明,潘 旻,嵇 晶,程建明∗
(1.淮安市淮安医院,江苏 淮安 223001;2.南京中医药大学,江苏 南京 210023)
丹参为唇形科鼠尾草属多年生草本植物丹参Salvia miltiorrhiza Bge.的干燥根及根茎,是临床上较为常用的中药,在治疗心血管疾病、抗肿瘤、抗氧化等方面的应用日益广泛[1-3]。大量药理研究表明[4-6],丹参水溶性成分丹酚酸可用于心脑血管疾病的治疗,已成功研发出了注射用丹参多酚酸、多酚酸盐等相关制剂,临床疗效良好,目前以注射剂为主,虽然起效迅速,生物利用度较高,但也存在给药不方便、患者顺应性差的问题,同时直接入血,对生产工艺要求高,一旦出现质量问题将引起严重的不良反应,而且该类成分吸收消除快,无法维持长时间较高血药浓度,也导致相关注射剂只适合临床急救。目前,丹参总酚酸常用剂型主要有颗粒剂、片剂、脂质体、滴丸、磷脂复合物等,但由于该类成分大多不耐热,给相关生产工艺带来了难度。
滴丸是指将固体或液体药物与适当基质加热熔化混匀后,滴入不相混溶的冷凝液中,收缩冷凝而成的小丸状制剂[7-8],具有生产工艺简单、生物利用度高、起效迅速、稳定性好的特点,发展前景广阔。因此,本实验以丹酚酸中主要活性物质丹酚酸B、迷迭香酸为指标,对丹参总酚酸滴丸制备工艺和质量标准进行研究,以期为该类成分深入研究和相关制剂开发提供参考。
1 材料
1.1 仪器 滴丸机由南京中医药大学药学院中药药剂教研室提供;Waters E2695 高效液相色谱仪,配置Waters 2489 UV 检测器(美国Waters 公司);BT125D 型电子分析天平(德国赛多利斯公司);DW-2 型调温电热器(南通市通州申通电热器厂);FA2004 型电子分析天平(上海上平仪器有限公司);YP6002 型电子天平(上海光正医疗仪器有限公司);Unique-s15 型超纯水系统(北京佰亿新创科技有限公司)。
1.2 试药 丹参总酚酸中间体(自制,批号20170304)。液体石蜡、二甲基硅油(上海泰坦科技股份有限公司);聚乙二醇4000、聚乙二醇6000(无锡市亚泰联合化工有限公司,批号20170301)。丹酚酸 B(含有量98%,批号Y26O7H23683)、迷迭香酸对照品(含有量98%,批号P26A7F13802)(上海源叶生物科技有限公司)。毛细管(华西医科大学仪器厂);硅胶G 薄层板(青岛海洋化工有限公司)。甲醇(美国赛默飞世尔科技公司,批号LOT18055159)、乙腈(德国默克公司,AS1122-801),以及磷酸(批号D629033)、冰醋酸(批号E1702076)[阿拉丁试剂(上海)有限公司]均为色谱纯;乙酸乙酯(批号 14061411310 )、三氯化铁(批号14071210994)、铁氰化钾(批号15100210410)、盐酸(批号160912100825)(南京化学试剂有限公司);甲酸(批号10014128,国药集团化学试剂有限公司)。
2 方法与结果
2.1 滴丸制备工艺
2.1.1 冷却剂种类 固定药物与基质配比1∶5,取丹参总酚酸冻干粉1.5 g,加入混合基质7.5 g(PEG4000∶PEG6000=4∶1),65 ℃水浴熔融并搅拌混匀,80 ℃下分别滴入二甲基硅油、液体石蜡中,以滴丸下降速度、成型情况为指标考察冷却剂。结果,二甲基硅油处理时滴丸下降速度合适,丸形规则圆整;液体石蜡处理时滴丸下降速度过快,部分带有小尾巴,可能与其密度较小有关,故选择前者作为冷却剂。
2.1.2 基质配比 PEG4000 具有良好的分散力及较大的内聚力,符合滴丸对基质的要求,再加入一定比例黏度较大的PEG6000 以调整基质成型。两者按1∶1、2∶1、3∶1、4∶1、5∶1 比例混合熔融后滴入二甲基硅油中,制备空白滴丸,以易滴程度、空白滴丸成型情况为指标进行筛选,结果见表1。由表可知,随着PEG4000 比例增大滴速变快,不易控制;当 PEG4000、PEG6000 比例为3∶1 时,基质较易滴出,而且空白滴丸成型性较好,滴丸圆整,硬度适宜,故选择其作为基质。

表1 基质配比考察结果Tab.1 Results of matrix ratio investigation
2.1.3 药物与基质配比 滴丸中药物与基质的配比一般在1∶1~1∶10 范围内,但其过高时易导致滴丸成型困难,而过低时又会使载药量偏低,故在1∶1~1∶6 范围内进行考察,结果见表2。由表可知,1∶5 时效果最理想,故选择其作为药物与基质配比。

表2 药物与基质配比考察结果Tab.2 Results of drug-matrix ratio investigation
2.1.4 滴距、滴速 滴距过小时,液滴到达二甲基硅油中后来不及收缩,导致滴丸不圆整;滴距过大时,液滴容易呈扁形,或者因重力作用而被跌散生小丸[9],本实验筛选空白滴丸时发现,滴距为6 cm时滴丸圆整度较好。滴速过快时,滴丸连续下沉到冷却剂中,容易相互粘连,圆整度不佳;滴速过慢时,虽然滴丸圆整度好,成型性符合要求,但混合基质易凝固,导致滴口堵塞,并且容易增加丸重差异,从而影响滴丸质量,本实验在不影响成型效果、圆整度的情况下适度提高滴速,控制在60 滴/min。
2.1.5 料温 料温过低时,滴丸易出现拖尾现象,圆整度差;料温过高时,滴丸圆整度降低,若滴制过快则易粘连。本实验发现,混合基质在58 ℃时开始熔融,65 ℃时全部熔融,由于丹酚酸类成分高温不稳定,故选择65 ℃作为料温。
2.1.6 其他滴制条件 根据滴丸成型性和圆整度,确定冷却剂温度为上常温下低温,滴口内、外径为3、4.5 mm。
2.1.7 工艺验证 根据上述优化工艺参数,制备3 批滴丸(批号20170410、20170411、20170412),发现其丸形圆整,色泽均一,硬度较好,无拖尾、粘连现象,表明工艺稳定可行。
2.2 滴丸质量评价
2.2.1 HPLC 法测定丹酚酸B、迷迭香酸含有量
2.2.1.1 色谱条件 Waters XBridge C18色谱柱(4.6 mm×250 mm,5 μm);流动相乙腈(A)-1%醋酸(B),梯度洗脱,程序见表3;体积流量1.0 mL/min;检测波长280 nm;柱温30 ℃;进样量10 μL。
2.2.1.2 对照品溶液制备 精密称取丹酚酸B 对照品4.85 mg、迷迭香酸对照品3.80 mg,分别置于25、250 mL 棕色量瓶中,80%甲醇稀释,即得(190.12、14.90 μg/mL)。

表3 梯度洗脱程序Tab.3 Gradient elution programs
2.2.1.3 供试品溶液制备 取滴丸10 粒,置于100 mL 具塞锥形瓶中,精密称定质量,加入50 mL 80% 甲醇,超声(功率140 W、频率42 kHz)20 min,放冷,80% 甲醇补足减失的质量,滤过,即得。
2.2.1.4 专属性考察 取空白滴丸、含药滴丸适量,按“2.2.2.3”项下方法制备供试品溶液,在“2.2.2.1”项色谱条件下进样测定,结果见图1。由表可知,PEG4000、PEG6000 对测定无干扰,方法专属性良好。
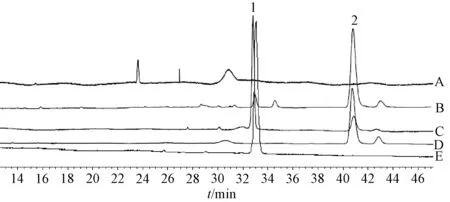
图1 各成分HPLC 色谱图Fig.1 HPLC chromatogram of various constituents
2.2.1.5 线性关系考察 精密量取190.12 μg/mL丹酚酸B 对照品溶液、14.90 μg/mL 迷迭香酸对照品溶液各1、2、4、6、8、10 mL,80% 甲醇定容至10 mL,在“2.2.2.1”项色谱条件下进样测定。以溶液质量浓度为横坐标(X),峰面积为纵坐标(Y)进行回归,得到丹酚酸B、迷迭香酸方程分别为Y=6 216.4X-1 019.6(R2=0.999 66)、Y=10 996X-153.46(R2=0.999 8),分别在19.01~190.12、1.49~14.90 μg/mL 范围内线性关系良好。
2.2.1.6 精密度试验 取152.10 μg/mL 丹酚酸B对照品溶液、8.94 μg/mL 迷迭香酸对照品溶液适量,在“2.2.2.1”项色谱条件下各进样测定6次,测得丹酚酸B、迷迭香酸峰面积RSD 分别为0.88%、1.62%,表明仪器精密度良好。
2.2.1.7 重复性试验 取同一批滴丸,按“2.2.2.3”项下方法制备6 份供试品溶液,在“2.2.2.1”项色谱条件下进样测定,测得丹酚酸B、迷迭香酸含有量RSD 分别为1.72%、1.17%,表明该方法重复性良好。
2.2.1.8 稳定性试验 取同一批滴丸,按“2.2.2.3”项下方法制备供试品溶液,在“2.2.2.1”项色谱条件下于0、3、6、9、12、24 h进样测定,测得丹酚酸B、迷迭香酸含有量RSD 分别为1.72%、1.17%,表明溶液在48 h 内稳定性良好。
2.2.1.9 加样回收率实验 分别取同一批滴丸25、100 粒,置于100 mL 具塞锥形瓶中,加入相当于滴丸中成分含有量80%、100%、120%的对照品后进行提取,取续滤液,在“2.2.2.1”项色谱条件下进样测定,计算回收率。结果,丹酚酸B、迷迭香酸平均加样回收率分别为 97.92%、96.58%,RSD 分别为2.45%、1.64%。
2.2.1.10 样品含有量测定 取3 批滴丸,按“2.2.2.3”项下方法制备供试品溶液,平行3 份,在“2.2.2.1”项色谱条件下进样测定,计算含有量,结果见表4。以平均值的-20% 为下限,初步确定丹酚酸B、迷迭香酸含有量分别不得低于5.45%、0.46%。
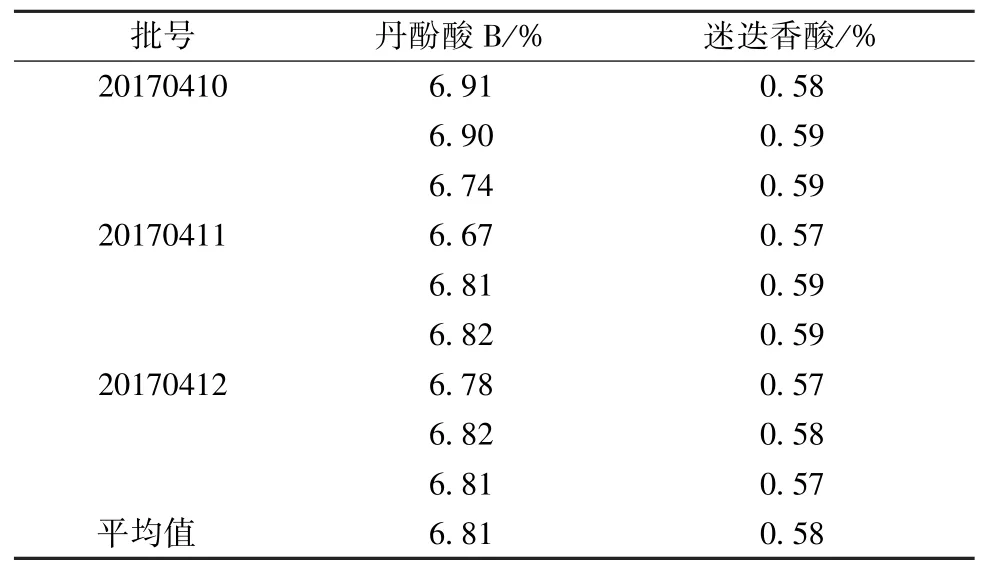
表4 各成分含有量测定结果(n=3)Tab.4 Results of content determination of various constituents(n=3)
2.2.2 TLC 法定性鉴别
2.2.2.1 供试品溶液制备 取滴丸15 丸,加水1 mL、稀盐酸2 滴,充分振摇,再加乙酸乙酯3 mL振摇1 min,离心2 min,上清液蒸干至2 mL,即得。
2.2.2.2 对照药材溶液制备 取丹参对照药材,按“2.2.2.1”项下方法制备,即得。
2.2.2.3 展开条件 硅胶G 薄层板;展开剂乙酸乙酯-水-甲酸(14∶2∶3)上层溶液;显色剂1%三氯化铁-1% 铁氰化钾(1∶1)溶液,临用时配制。
2.2.2.4 鉴别方法 取3 批滴丸,按“2.2.2.1”项下方法制备供试品溶液,按照2015 年版《中国药典》薄层色谱法(通则0502)试验,结果见图2。
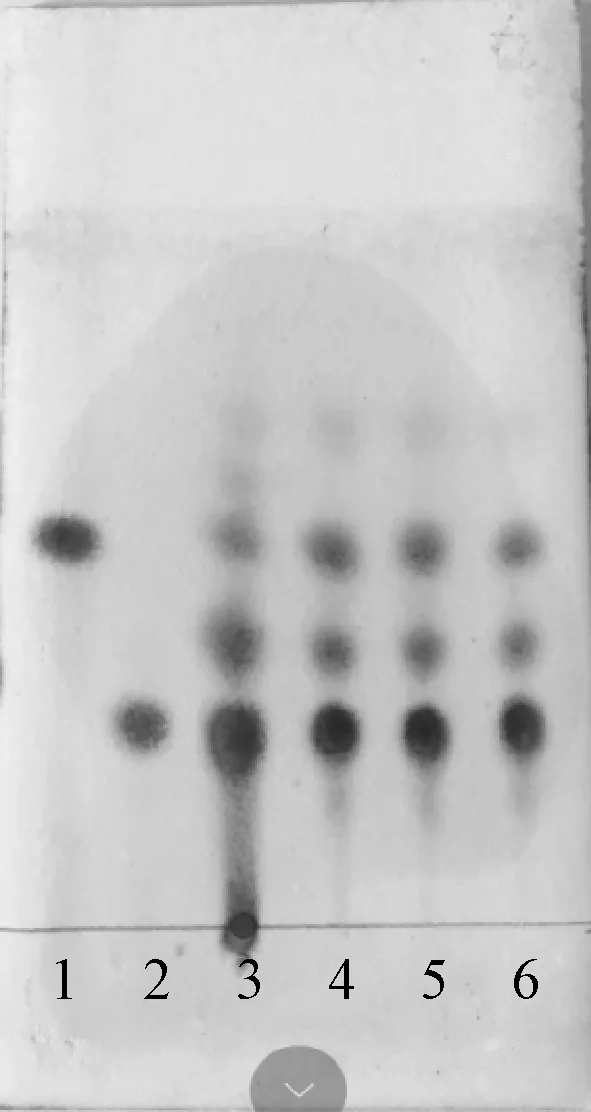
图2 各成分TLC 色谱图Fig.2 TLC chromatogram of various constituents
2.2.3 重量差异限度检查 精密称取滴丸20 粒,计算其总重和每粒丸重,根据2015 年版《中国药典》一部附录判断重量差异是否符合要求。结果,20 粒 滴 丸 丸 重 分 别 为25.56、25.51、25.43、25.57、25.48、25.48、25.43、25.49、25.51、25.54、25.39、25.55、25.62、25.58、25.53、25.53、25.61、25.47、25.45、25.51 mg,平 均25.51 mg<0.03 g,RSD 为0.24%。药典规定,重量差异限度应±15%,每粒滴丸丸重应在21.68~29.33 mg 范围内,超出标准限度的不得多于2 丸,不得有1 丸超出标准限度的1 倍,由此可知,本实验所制滴丸符合相关要求。
2.2.4 溶散时限检查 取6 粒滴丸于溶出仪的吊篮中,温度设定为37 ℃,发现所有滴丸在5 min内均完全溶解,符合2015 年版《中国药典》一部滴丸剂项下溶散时限不得超过30 min 的规定。
3 讨论
目前,丹酚酸类成分的缓控释制剂仍处于实验室阶段,未见市售产品。张丽红等[10]以大豆卵磷脂制备丹参总酚酸长循环脂质体,发现它可减缓丹酚酸在体内的消除,延长体内滞留时间,提高生物利用度;咸银库等[11]以丹参总酚酸为原料制备速释的口腔崩解片,可提高生物利用度;Jin 等[12]通过制备丹参总酚酸磷脂复合物,改善了脂溶性差的问题;此外,也有关于丹参总酚酸滴丸、胃滞留缓释片的报道[13-15],为相关制剂研究提供了参考。
本实验以滴丸成型性和圆整度为依据,考察了冷却剂、基质配比、药物与基质配比等影响滴丸成型工艺的因素,最终确定最优工艺为将丹参总酚酸冻干粉研细混匀备用,以PEG4000、PEG6000 为成型基质,按3∶1 比例混合,65 ℃水浴加热熔融,按药物与基质配比1∶5 分次加入冻干粉,搅拌均匀,在滴距6 cm,滴口内、外径3、4.5 mm,滴速60 滴/min 的条件下滴入二甲基硅油冷凝剂(上常温下低温)中,冷却,固化成丸,取出,滤纸吸干表面冷却剂,即得,所得滴丸外观圆整、硬度适宜,制备工艺合理可行。其中,丹酚酸B、迷迭香酸平均含有量分别为6.81%、0.58%,平均丸重为25.51 mg,重量差异限度、溶散时限均符合药典要求。由此可知,该工艺操作简单,生物利用度高,起效迅速,稳定性好,具有广阔的发展前景,可为丹参酚酸类成分研究和相关制剂开发提供参考。
