基于CT影像的肺叶分割技术研究进展
2019-10-22高磊段辉宏周韡鼎聂生东
高磊,段辉宏,周韡鼎,聂生东
上海理工大学医疗器械与食品学院,上海200093
前言
近年来,随着现代社会的快速发展,空气污染愈发严重,肺部疾病的发病率也在逐年升高。2017年《中国卫生和计划生育统计年鉴》显示[1],肺癌已经成为我国死亡率最高的恶性肿瘤疾病。为诊断和治疗肺部疾病,分析肺部组成结构进而探究肺部疾病的成因以及发展情况变得至关重要。
肺是人体重要的组织器官之一,主要分为5个功能相对独立的解剖结构—肺叶,其中肺裂是相邻肺叶间的物理边界。右肺包含3个肺叶,左肺由于与心脏相邻,其解剖结构受心脏影响体积较小,只有两个肺叶[2](图1)。
由于肺叶的功能相对独立且许多肺部疾病通常发生在单个肺叶中,例如肺气肿[3]、后发性肺结核[4]通常会影响上叶,而特发性肺纤维化通常与下叶相关[5],故肺叶的鉴别对肺部疾病的评估以及治疗起着重要的作用。其次肺叶内血管以及支气管树相对独立,因此肺叶边界的显示是众多肺部手术如肺叶减容手术的前提。

图1 肺部结构Fig.1 Lung structure
目前医生主要通过CT 图像对肺部疾病进行判别。如图2所示,CT 图像的优势在于能够较为清晰地显示肺部边界以及肺裂,但肺叶分割仍困难重重:首先受到部分容积效应以及患者运动的影响,肺裂可能会模糊不清,无法通过单一的阈值分割法对肺叶进行分割;其次肺裂附近的肺组织或肿瘤、肺气肿等也会影响肺叶分割的准确性。另外研究发现,CT图像中的肺裂通常不完整,相邻肺叶的肺实质可能发生融合[6]。
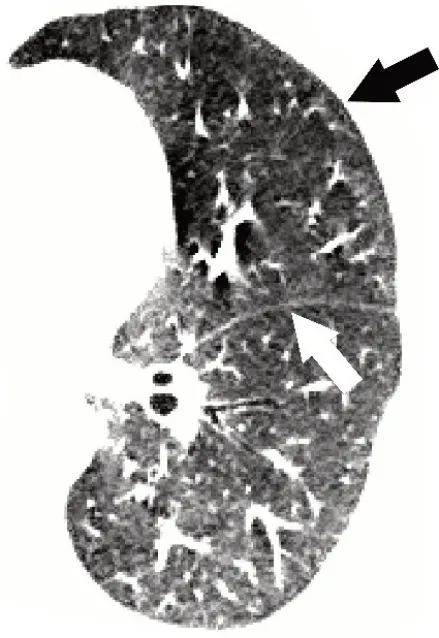
图2 CT图像中的肺裂(白色箭头)及肺边界(黑色箭头)Fig.2 Pulmonary fissure(white arrow)and lung boundary(black arrow)in CT image
为解决上述问题,专家学者将众多理论应用于肺叶分割领域,提出许多肺叶分割算法。近些年来机器学习也被应用于该领域,并取得较好的分割效果。目前肺叶分割算法的分割思路大致相同:①检测属于肺裂的像素点;②使用检测到的肺裂点生成肺裂表面,进而分割整个肺实质。本文总结了多年来国内外肺叶的分割方法,分别从上述两个步骤对其研究现状进行综述。
1 肺裂检测
肺裂是肺叶间天然的物理边界,目前常见的肺裂检测方法主要分为3 类:①基于肺裂结构特征的检测方法;②基于肺部解剖学知识的检测方法;③基于机器学习的检测方法。
1.1 基于肺裂结构特征的检测方法
考虑到二维空间内肺裂的结构特征,Kubo 等[7]利用VanderBurg线性算子对肺裂进行检测。但由于VanderBurg 线性算子无法检测到对比度不高的肺,Wang 等[8]首先利用基于sobel 算子的脊线图增强肺裂后,再对肺裂进行检测。
基于肺裂的三维结构特征,Wiemker等[9]利用结构张量以及三维hessian矩阵的特征值对肺裂进行检测。如图3所示,两种方法都能在无病变的肺中获取较好的检测效果,但噪声较多。通过结构特征直接检测肺裂通常需要在灵敏度和特异性之间进行取舍,灵敏度高的方法检测到的肺裂往往存在大量噪声,而特异性高的方法会错误地去除较大面积的肺裂,导致肺裂的检出率不高。因此研究人员一般将结构特征与解剖学知识相结合以提高肺裂的检测精度。

图3 文献[9]中的肺裂检测结果图Fig.3 Results of pulmonary fissure detection in literature[9]
1.2 基于肺部解剖学先验知识的检测方法
众多学者通常选择借助肺部解剖学的先验知识来辅助肺裂检测:通过肺部管道获取有关肺裂的位置信息或构建肺部模型。在借助肺部解剖信息的方法中应用最为广泛的为气管以及血管的解剖信息,如图4所示。
Kuhnigk 等[10]利用血管信息增强原始图像中肺裂后,使用三维的分水岭变换进行肺叶分割。但该算法需要手动选取种子点。为此Lassen 等[11]依据支气管与血管树彼此靠近的解剖学特性,通过气管树解剖描述自动选取了用于分水岭分割的种子点。Giuliani 等[12]同样利用了气管以及血管的解剖信息,但与Kuhnigk 等[10]和Lassen 等[11]使用分水岭算法不同,Giuliani等[12]将气管、血管的解剖信息结合成一个能量方程,通过图切割将能量方程最小化,从而得到最优分割。上述算法都需要对气管、血管进行分割,算法的复杂性较高,运算时间较长。为解决这一问题,Wei等[13]提出一种结合灰度信息、三维形状约束、气管以及血管树信息的自适应肺裂扫描算法。上述方法的优点在于可以在不分割血管与气管的情况下获取其解剖结构信息,减少算法的计算时间和复杂性。Firdouse 等[14]在文献[13]的基础上改用双树复杂小波变换对肺裂进行识别,提高肺裂检测的精度。Doel等[15]则提出一种结合肺裂增强滤波器、图像外观以及血管气管解剖信息的检测方法,这一方法在小血管穿过肺叶边界的情况下,会因为其他解剖信息的存在而得到补偿。

图4 血管树和气管树Fig.4 Vascular tree and trachea tree
基于肺部模型的方法中最典型的方法就是多图谱分割算法,Van Rikxoort 等[16]利用基于图谱的算法对肺裂位置进行检测。为提高检测算法的准确率,Van Rikxoort 等[16]还结合来自肺裂、肺部边界和气管树的信息来辅助图谱的注册。但基于图谱的方法同样存在一定的缺陷:首先需要有经验的医师花费大量的时间来获取图谱数据;其次如果没有图谱与正在处理的数据相似,则将导致分割效果不佳;最后图谱与处理图像进行配准的时间较长。为此Bragman等[17]提出建立一个不需要手工标记的简单肺裂模型。
解剖信息能够提供部分肺裂的位置信息,增加解剖学信息的使用可以提高肺裂检测的准确性。但解剖学信息可能存在错误,最小化解剖信息的依赖能够提高该方法的鲁棒性,但可能会忽略有价值的先验信息[18],因此单纯依靠解剖学信息不足以准确分割肺叶。
1.3 基于机器学习的检测方法
基于机器学习的肺叶分割方法是近几年来的研究重点之一,研究人员主要利用肺裂的结构和纹理特征来训练分类器或者神经网络,然后对CT图像中的肺裂区域进行识别。
传统的机器学习方法主要通过自学习算法,发现和挖掘数据潜在的规律,从而对未知的数据进行预测。Van Rikxoort等[19]首次提出利用基于机器学习的方法实现肺裂的检测。Van Rikxoort 等[19]基于CT图像提取57 个特征,然后通过浮动向前算法进行特征选择,最后选用K 最近邻(K-Nearest Neighbor,KNN)分类器对肺裂进行检测。
深度学习是机器学习研究中的一个新的领域,其目的在于建立模拟人脑进行分析学习的神经网络。Devaki 等[20]利用前馈后向传播神经网络[21]代替Van Rikxoort等[19]提出的KNN分类器获得了更好的肺裂检测结果。除了肺裂的结构特征,Wei等[22]和Neto等[23]分别利用灰度运行长度矩阵(Gray Level Run Length Matrix, GLRLM)以及局部二值模式(Local Binary Patterns,LBP)提取肺裂的纹理特征构建神经网络对肺裂进行检测。
卷积神经网络(Convolutional Neural Network,CNN)在医学图像的分割任务中表现突出。为了将该方法应用于肺叶分割领域,如图5所示,George等[24]将全层嵌套网络(Progressive Holistically-Nested Network,PHNN)架构[25]与随机游走(Random Walker,RW)算法结合,利用先验信息对肺叶进行分割。但上述的深度学习方法还需要RW算法进行后处理以获取肺叶分割结果。
基于机器学习的方法能够使得方法进行自主学习,并对各肺叶区域进行有效的区分。同时机器学习方法的算法复杂度较低,泛化能力较强,更能适应临床数据。
2 肺裂曲面生成
前文主要讲述肺裂检测方法,但部分容积效应、病理学改变或者患者移动都可能导致CT 图像中的肺裂不清晰,导致检测到的肺裂点无法形成连续的曲面,并产生虚假响应,因此实现肺叶分割,需要在去除噪声的基础上,利用检测到的肺裂点生成跨越整个肺容积的完整表面。目前能够保证获取完整边界表面的方法主要分为两种:直接生成肺裂曲面方法和间接生成肺裂曲面方法。直接生成肺裂曲面方法主要在去除噪声的基础上,对检测到的肺裂候选点进行插值以生成完整的肺裂表面。间接生成肺裂曲面方法将生成叶状边界作为分割算法的自然结果,例如基于图谱或分水岭方法。
2.1 直接生成法
直接生成肺裂曲面最重要的是去除噪声,为找到拟合肺裂表面的最佳方法,研究人员对众多曲面拟合算法进行了尝试。Pu 等[26]在获取肺裂点后,利用径向基函数(Radial Basis Function,RBF)以隐式函数的形式表示肺裂,这一方法能够使裂隙表面平滑地分割整个肺实质,从而获取完整的肺裂边界。Doel等[15]则采用平滑的B样条曲线穿过肺裂点,并以此来拟合推断肺裂边界。直接生成法的优势在于该方法独立于肺裂检测阶段,允许分别评估和比较各算法中这两个步骤的性能,从而允许混合不同方法达到最优的肺裂检测效果。
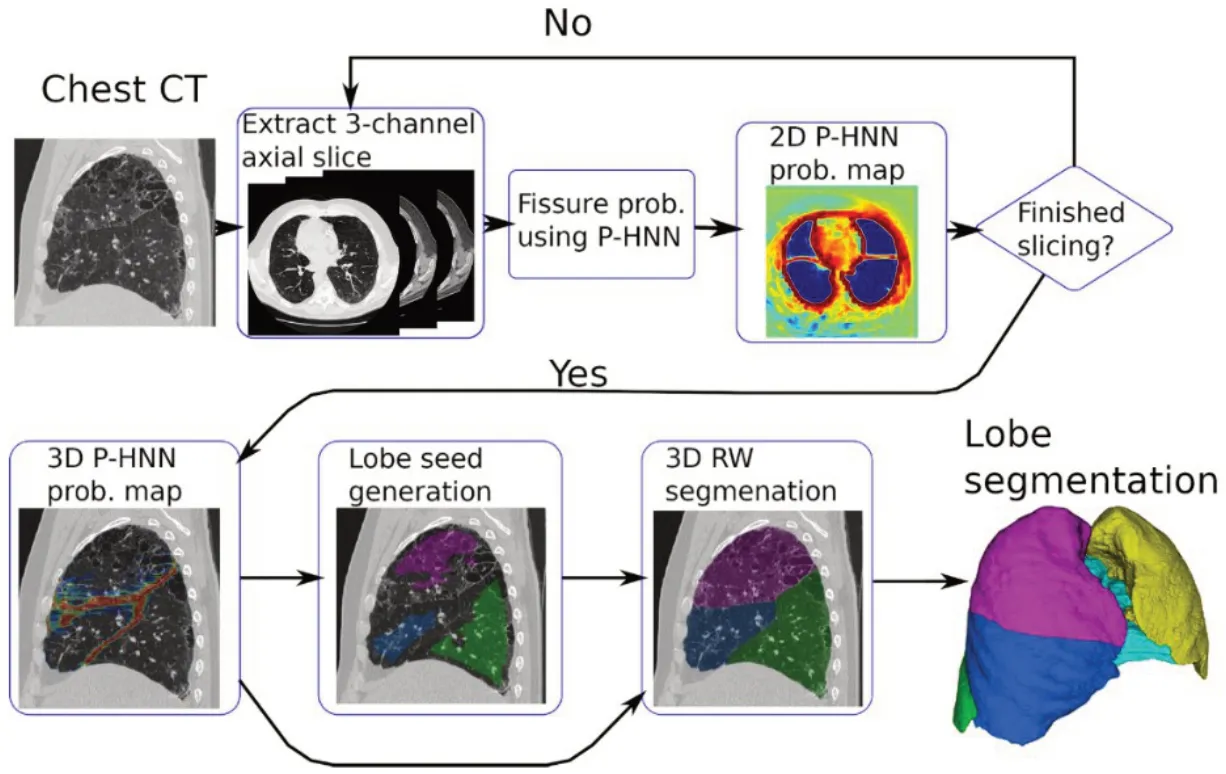
图5 文献[24]中基于P-HNN架构的肺叶分割算法流程Fig.5 Flow chart of lung lobe segmentation algorithm based on P-HNN architecture in literature[24]
2.2 间接生成法
与直接生成肺裂曲面的方法不同,对于某些肺裂分割方法,肺裂表面的生成隐含在方法中。如分水岭分割方法主要是在分水岭变换中推导出肺裂表面,这一分割过程最终会生成分割整个肺实质的连续表面[10-11]。基于图谱的方法也隐含地结合了肺裂表面的拟合,肺裂的曲率以及形状会受到配准方法中的正则化约束[16-17]。间接生成法将分割结果作为算法的自然结果,肺裂曲面的生成隐含在算法当中。该方法的优势在于运用算法同时进行了肺裂检测以及肺裂曲面生成步骤,降低算法复杂度。但由于间接生成法仅适用于本身算法,因此局限性较大。
3 总结与展望
本文从肺裂检测和肺裂曲面生成两个步骤出发,对国内外肺叶分割算法进行总结和归纳,为了能够更好地比较各类算法的特点,本文在表1中列举了部分具有代表性的肺叶分割算法进行了分析。
由表1可以看出,研究人员采用了几种不同类型的验证方法来评估自身的算法,从算法分割的肺叶边界到金标准(经验丰富的肺放射科医师手动描绘的肺叶边界)的肺裂边界平均距离(Average Mean Distance, AMD)和均方根距离(Root Mean Square,RMS)主要对算法分割结果的肺裂表面进行评价,而体积变异性、LOLA score 以及杰卡德相似系数则是对算法分割结果的肺叶体积重合率进行评价。其中LOLA score 为2011年举办的肺叶分割竞赛(https://lolall.grand-challenge.org/)中给出的评价指标,其与杰卡德相似系数都是计算自动分割的肺叶与金标准的重合体积比率,而体积变异性则计算自动分割的肺叶与金标准的非重合体积比率。由于不同的方法针对不同类型的数据集进行了测试,每个数据集可能存在不同的分割难点,即使使用相同的验证方法也不能直接比较方法的好坏,因此本文进行了方法学上的比较,而非定量比较分割结果。

表1 典型肺叶分割方法及其定量结果Tab.1 Summary and comparison of typical algorithms for lung lobe segmentation
通过对国内外肺叶分割方法的研究发现,单单依靠结构特征或者解剖学特征无法准确的分割肺叶,因此肺叶分割从刚开始的利用肺裂的结构特征向多种特征相结合的方向发展,分割算法的分割精度也得到了大幅度提升。同时通过总结发现,肺叶分割的关键在于肺裂位置信息的准确性,现有的肺叶分割算法都是基于肺裂的位置信息对肺叶进行分割,因此如何在获取尽可能多的肺裂位置信息的同时,保证位置信息的准确性成为了制约肺叶分割技术发展的瓶颈。
随着定量图像分析在肺部疾病评估和治疗计划中变得越来越普遍,需要从CT数据中进行精确的肺叶分割。这些方法需要对广泛的临床数据具有鲁棒性,然而现有的肺叶分割算法没有充分考虑到临床数据的多变性。如果要在临床实践中更广泛地使用肺叶分割算法,就必须评估图形分辨率、剂量和病理等因素的影响。
因此肺叶分割领域可以根据以下方向进行进一步的研究:(1)建立带有金标准分割的共享图像数据库,并规定统一的量化指标对实验结果进行评价。(2)研究肺裂的特征提取以及特征优化,提高方法的鲁棒性以及准确性,将机器学习进一步应用于肺叶分割领域。(3)评估临床数据中图形分辨率、剂量和病理等因素对肺叶分割算法的影响。
