右美托咪定在上肢骨折患者术后连续喙突旁臂丛神经阻滞镇痛中的应用
2019-10-16孙宗建吴水水李荣华李玲刘玲玲单士强
孙宗建, 吴水水, 李荣华, 李玲, 刘玲玲, 单士强
(沧州市中心医院麻醉科, 河北 沧州 061000)
上肢骨折发生率占骨折病例总数的4%~5%, 其主要的治疗手段为手术治疗。 疼痛是骨折术后最常见的症状, 镇痛不足会降低手术疗效, 影响患者恢复。 随着超声在麻醉领域的广泛应用, 臂丛神经阻滞的应用范围由术中区域阻滞扩展到术后镇痛, 因其具有局部用药、 全身不良反应率低等优点, 应用越来越广泛[1]。 有研究表明, 单纯超声引导下喙突旁入路连续臂丛神经阻滞可以有效的应用于上肢手术后镇痛[2]。 右美托咪定是具有高选择性α2肾上腺素能受体激动剂, 与α2、 α1受体结合的比例是1620 ∶1, 具有镇静、 镇痛、 抗焦虑及保持血流动力学稳定的药理作用。 研究表明, 右美托咪定复合罗哌卡因在关节镜肩袖修复术后自控肌间沟臂丛神经阻滞中产生有效镇痛、 镇静作用的同时减少全身并发症的发生率[3]。 本研究拟观察在上肢骨折切开复位内固定术患者术后连续喙突旁入路臂丛神经阻滞镇痛中, 使用右美托咪定的效果比较。
1 资料和方法
1.1 一般资料
本研究已获沧州市中心医院伦理委员会批准, 术前与患者或患者家属签署知情同意书。 选取我院2017-01/2018-01期间单侧上肢骨折择期行切开复位内固定术患者60例, 男女不限, 年龄18~60岁, ASA分级 Ⅰ 或 Ⅱ 级, 体质量指数(BMI)18~25 kg/m2, 按随机数字表法将患者分为右美托咪定+罗哌卡因组(D组,n=30)和罗哌卡因组(R组,n=30)。 两组患者术后镇痛使用连续喙突旁臂丛神经阻滞镇痛, 镇痛药物D组为0.2%罗哌卡因240 mL并加入右美托咪定2 μg/kg, R组为0.2%罗哌卡因240 mL。 患者均无相应药物过敏史, 无严重心、 脑血管系统疾病史, 无神经功能受损性疾病及糖尿病导致的周围神经病变, 凝血功能正常, 穿刺部位及周围无皮肤及软组织感染。 术前对患者进行视觉模拟评分(VAS)表的培训, 使其掌握不同刻度所代表的疼痛程度。
1.2 麻醉方法
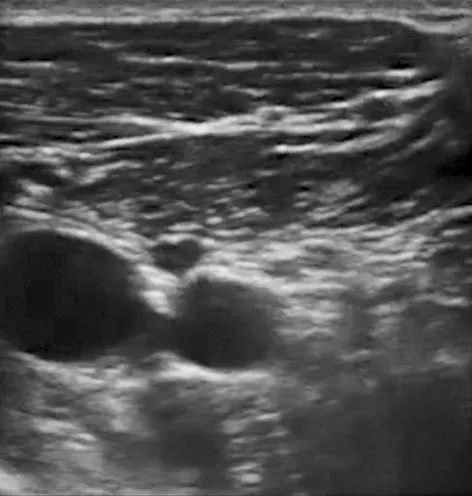
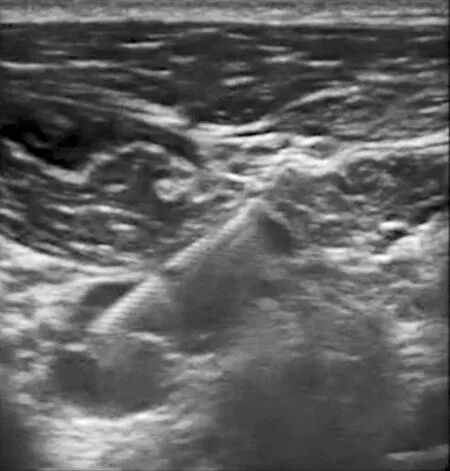
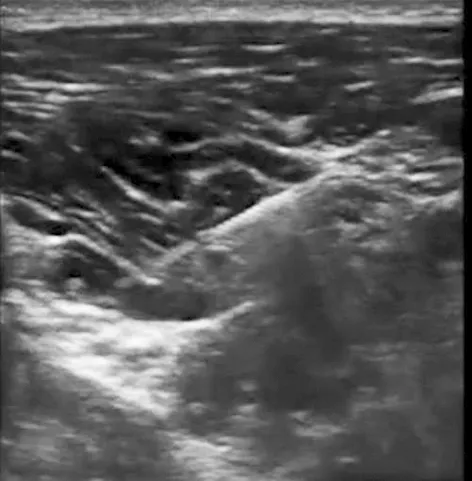
患者入手术室后行心电图(ECG)、 血压(BP)和脉搏血氧饱和度(SpO2)监测, 开放健侧上肢静脉通路, 静脉注射咪达唑仑0.03 mg/kg。 神经穿刺置管操作由同一麻醉医生完成。 根据文献描述的方法[4]行喙突旁臂丛神经阻滞置管术, 患者平躺仰卧位, 床头轻度抬高, 手臂贴于身侧, 头偏向对侧。 常规消毒, 高频线阵超声探头(SonoSite S-Nerve Ultrasound System, 美国)沿矢状面放置于三角肌胸大肌间沟下对臂丛神经丛进行定位(图1A)。 通过扫描以获得此处腋动脉短轴图像, 小幅度倾斜、 旋转探头, 寻找通常位于腋动脉周围3点、 6点及9点钟方向的高回声神经束。 此处臂丛神经后束附近一般无变异血管, 在探头上方(头侧)注射一局麻药皮丘, 用连续外周神经阻滞导管套件中18G、 长度90 mm穿刺针(Contiplex D, BRAUN, 德国)平面内进针, 进针方向由头端向尾向后, 针尖靠近腋动脉深部的臂丛神经后束, 调整穿刺针角度后注入0.5%盐酸利多卡因 (批号: C1810062, 山东华鲁制药有限公司)20 mL, 低回声局部麻醉药液性暗区自在腋动脉深部呈U型包绕在臂丛神经外侧束、 后束及内侧束周围, 同时药液向头侧及尾侧扩散(图1B-D)。
药液注射完毕后经穿刺针置入神经阻滞导管, 导管至少穿出针头3~5 cm, 回抽无血液后退针并固定, 术毕接电子镇痛泵。 阻滞完成后30 min内测定阻滞效果, 将神经阻滞不全患者排除。 两组患者均接受全身麻醉, 依次静脉注射枸橼酸芬太尼注射液2 μg/kg、 依托咪酯注射液0.3 mg/kg和顺苯磺酸阿曲库铵0.1 mg/kg诱导, 插入喉罩[Ambu Aura Once喉罩 Aura A/S(厦门)丹麦Ambu公司]后行机械通气。 静脉泵注盐酸瑞芬太尼, 吸入七氟醚维持全身麻醉, 维持肺泡气最低有效浓度(MAC)值在0.8左右、 脑电双频谱指数(BIS)在40~60之间。 术中根据肌松恢复情况和手术进程间断追加芬太尼及顺苯磺酸阿曲库铵, 保持BP、 心率(HR)稳定, 波动超过基础值的25%时通过调控麻醉深度, 应用盐酸麻黄碱6 mg、 尼卡地平0.2 mg或阿托品0.2 mg维持其稳定。 手术即将结束前30 min经静脉注射枸橼酸芬太尼0.1 mg镇痛、 甲磺酸托烷司琼注射液5 mg防止术后恶心呕吐。
A
B
C

D
A: 臂丛神经定位; B: 阻滞后束和内侧束; C: 阻滞外侧束; D: 药液包绕臂丛神经.
图1 超声引导下喙突旁臂丛神经阻滞
术毕患者意识恢复且满足拔管指征后拔除喉罩, 入麻醉恢复室(PACU)。 待患者完全苏醒后, 嘱其做手指分指动作及拇指屈伸运动, 检查有无手术操作所导致的尺、 桡神经损伤后行自控连续臂丛神经阻滞镇痛, 设定电子镇痛泵背景输注速率为5 mL/h, 患者自控镇痛(PCA)剂量为5 mL, 锁定时间为15 min, 术后持续镇痛48 h后专人拔出神经阻滞导管并撤除镇痛泵。
1.3 观察指标
记录神经阻滞导管置管时间(自穿刺操作开始至经导管注射局麻药结束止)和神经阻滞是否成功; 采用疼痛数字评分法(NRS)(0分为无痛, 10分为无法忍受的剧烈疼痛)评估神经阻滞导管置管时患者的疼痛程度, NRS评分>4分为中重度疼痛, 记录NRS评分>4分发生情况; 采用阻力评分法(无阻力为0分, 有阻力但可以推进使导管超出针尖3 cm为1分, 阻力使导管不能推出针尖为2分)评价神经阻滞导管置管时所遇到的阻力程度, 阻力评分>1分为高度置管阻力, 记录阻力评分>1的发生情况; 记录神经阻滞导管置管过程中神经异感和血管损伤等不良反应的发生情况。
记录患者术后4 h(T1)、 8 h(T2)、 12 h(T3)、 24 h(T4)和48 h(T5)静息状态下的VAS评分(0分无痛; 1~3分轻微疼痛; 4~7分中度疼痛; 8~10分重度疼痛); 记录患者术后24 h(T4)、 36 h(T5)和48 h(T6)患侧肢体运动时的NRS评分; 记录患者术后48 h内镇痛泵按压次数以及与导管相关的不良反应(如导管渗液、 堵塞、 移位、 脱出等)和局部麻醉药相关不良反应发生情况; 记录口服曲马多患者的数量以及首次服用时间、 剂量及次数; 记录患者术后头晕、 恶心呕吐、 皮肤瘙痒及呼吸抑制等不良反应的发生情况; 评价2组患者术后48 h对镇痛效果的满意度(9~10分为非常满意, 6~8分为基本满意, 4~5分为一般, 3分以下为不满意)。
1.4 统计学处理

2 结果
2.1 两组患者一般资料比较
两组患者性别、 年龄、 身高、 体质量、 ASA分级和手术时间比较, 差异均无统计学意义(P>0.05, 表1)。


组别n/(男/女)年龄/岁体质量/kg身高/cmASA分级/(Ⅰ/Ⅱ)手术时间/minR组17/1340±1466±9170±711/19159±12D组16/1439±1568±8169±812/18161±11
2.2 两组患者置管情况比较
两组患者神经阻滞导管置管时成功率均为100%, 置管情况各指标比较, 差异无统计学意义(P>0.05, 表2)。


组别置管 时间/s中重度疼痛发生率/%高度置管阻力发生率/%血管损伤发生率/%神经异感发生率/%R组149±820.020.03.316.6D组155±520.020.03.313.3
2.3 两组患者术后疼痛 VAS 评分比较
与R组相比较, D组术后各时点VAS评分降低(P<0.05, 表3)。
2.4 两组患者术后功能锻炼时的NRS评分比较
与R组比较, D组术后各时点功能锻炼时的NRS评分降低(P<0.05, 表4)
2.5 两组患者术后不良反应比较
与R组比较, D组患者术后头晕、 皮肤瘙痒、 恶心呕吐的发生率降低(P<0.05), 2组呼吸抑制发生率比较, 差异无统计学意义(P>0.05, 表5)。


组别T1T2T3T4T5T6R组4.6±0.84.5±0.84.2±0.64.1±0.84.2±0.74.0±0.8D组3.7±0.6a3.5±0.8a3.6±0.5a3.7±0.7a3.6±0.6a3.6±0.6a
aP<0.05vsR 组.

表4 两组患者不同时点功能煅炼时NRS评分比较 [n=30, n(%)]
aP<0.05vsR 组.

表5 两组患者术后不良反应比较(n=30, %)
aP<0.05vsR 组.
2.6 两组患者术后服用曲马多情况比较
D组患者48 h 内电子止痛泵的平均按压次数明显低于R组患者[0(1.25)次vs2(4)次]。 两组患者术后使用曲马多的人数、 首次时间及剂量比较, 差异均无统计学意义(P>0.05, 表6)。


组别首次服用曲马多时间/h48 h 内服用曲马多人数构成情况(使用/未使用)曲马多服用剂量/mgR组27±1012/18183±40D组28±1110/20166±57
2.7 两组患者术后满意度比较
术后48 h镇痛满意度 D组为90%, R组为70%, 差异有统计学意义(P<0.05, 表7)。
R组患者术后48 h内有2例发生导管渗液, 1例发生导管堵塞; D组患者未见神经阻滞导管和局部麻醉药相关不良反应发生。
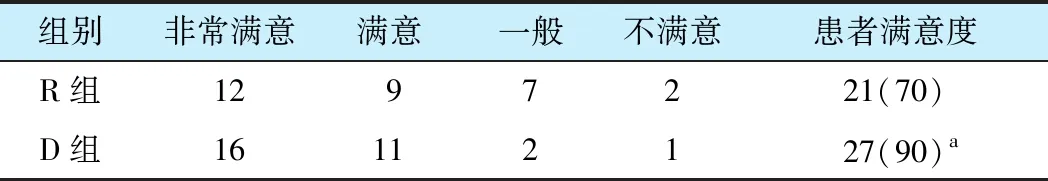
表7 两组患者术后满意度的比较[n=30, n(%)]
aP<0.05vsR 组.
3 讨论
上肢骨折后行切开复位内固定术对患肢造成的创伤大, 术后重度疼痛发生率高, 功能锻炼时剧烈疼痛导致患者术后活动量降低且影响康复。 术后患者自控静脉镇痛配药多使用阿片类镇痛药物, 患者易出现恶心呕吐、 皮肤瘙痒、 嗜睡、 意识障碍以及呼吸抑制等相关副作用。 研究显示, 不同穿刺入路的臂丛神经阻滞可安全、 有效的应用于上肢手术的术中及术后镇痛[5-6], 其中喙突旁入路连续臂丛神经阻滞镇痛效果好, 并发症少, 患者对术后镇痛效果的满意度高[2, 7]。 且局部麻醉药通过对交感神经的阻滞, 使血管扩张, 能够改善手术部位的微循环, 提高局部组织抗炎作用, 从而改善患者的预后。
本研究在神经阻滞导管置管成功后, 经导管注射1%利多卡因20 mL, 一方面是利用利多卡因麻醉强度大、 弥散作用强、 起效快的特点来测试神经阻滞的效果; 另一方面是由于上肢骨折切开复位内固定术中可能会导致神经损伤, 手术结束即刻需检查患肢运动功能, 排查手术原因可能造成的神经损伤, 利用利多卡因作用时间短的特点, 可以确保患者术毕配合检查。
临床上多采用0.2%盐酸罗哌卡因作连续神经阻滞镇痛[8-9]。 该药安全范围广、 不良反应少、 作用时间长、 对心血管系统影响小, 且具有运动与感觉分离的特点, 广泛应用于术后局部及区域阻滞镇痛。 右美托咪定对呼吸中枢的抑制作用轻微, 在吸入空气时, 健康成年志愿者静脉输注建议剂量10~15倍的右美托咪定的条件下, SpO2及动脉血二氧化碳分压能够维持在正常范围内[10]。 本研究中2组患者呼吸抑制发生率比较无统计学意义。 说明电子镇痛泵中加入2 μg/kg剂量的右美托咪定不会增加呼吸抑制发生率。
上肢骨折切开复位内固定术后24 h内患肢需要制动, 24 h后行功能锻炼。 本研究中D组患者术后4、 8、 12、 24、 36和48 h 的静息VAS 评分以及4、 36和48 h功能锻炼时的NRS评分均低于R 组, 说明右美托咪定复合盐酸罗哌卡因行连续神经阻滞镇痛较单独使用盐酸罗哌卡因镇痛能够进一步降低患者的疼痛评分。 另一方面, 术后48 h内, D组患者镇痛泵平均追加按压次数0(1.25)次, 明显低于R组患者的2(4)次, 说明D组的连续镇痛效果优于R组。 在额外口服曲马多的患者中, 48 h内2组患者首次服用时间、 服用人数、 服用剂量的比较, 差异均无统计学意义(P>0.05), 可能是因为2组患者术后追加按压镇痛泵后均能达到有效缓解疼痛的目的。
右美托咪定是高度选择性α2肾上腺素能受体激动剂, 其中枢镇静作用部位为颅内的蓝斑核。 以往的研究肯定了右美托咪定作为局部麻醉药辅助药在区域阻滞中所发挥的作用, 如增强局麻药镇痛作用[11]、 减少局麻药用量[12]及改善术后镇痛效果[13]等。 本研究中D组患者术后头晕、 皮肤瘙痒、 恶心呕吐的发生率降低也证明右美托咪定作为局部麻醉药辅助药的作用。 这可能与右美托咪定吸收入血后激活蓝斑核的受体, 阻止了部分促发恶心呕吐的相关递质的释放有关[14]。 但右美托咪定在外周区域神经阻滞中的作用机制尚没有定论, 有研究表明, 右美托咪定作为局部麻醉药辅助药物在外周神经周围可发挥一系列的作用起到增强镇痛的效果。 右美托咪定可能通过下调或抑制机体炎症因子的表达来发挥抗炎作用[15], 从而减轻术后炎性痛的发生和痛觉过敏。 Gaumann等[16]研究发现可乐定可增强盐酸利多卡因对神经C纤维动作电位产生的抑制作用, 提示右美托咪定有可能通过类似机制增强局部麻醉药的作用。 但右美托咪定增强盐酸罗哌卡因镇痛效果的作用机制有待于进一步研究。
综上所述, 右美托咪定复合罗哌卡因在上肢骨折患者切开复位内固定术后连续喙突旁臂丛神经阻滞镇痛中可以产生有效的镇痛、 镇静效果, 减少并发症的发生。
