深在性囊性胃炎1例报告*
2019-10-15王道明胡凯峰夏亚斌朱家胜卢林明
孔 琦 王道明 胡凯峰 夏亚斌 朱家胜 卢林明
(皖南医学院附属弋矶山医院胃肠一科,芜湖 244000)
深在性囊性胃炎(gastritis cystica profunda,GCP)又称为弥漫性囊性腺体畸形,临床上极为罕见。我科2015年7月收治1例,现将诊治过程报道如下。
1 临床资料
男,64岁。因无明显诱因出现食欲差,上腹部不适并进行性加重1个月于当地医院就诊。电子胃镜检查提示全胃多发息肉。予以抑酸、促胃肠蠕动等对症治疗后,上述症状无明显好转,2015年7月就诊于我院,以“胃多发息肉”收住消化内科。病程中患者无畏寒发热,无咳嗽、咳痰,无反酸、嗳气,无腹泻、便秘,无呕血、便血等,自诉最近2个月体重减轻7~8斤。查体:浅表淋巴结未及肿大,腹部平坦,未见胃肠型及蠕动波,腹部无压痛,无反跳痛及肌紧张,未扪及腹部包块。在消化内科行胃息肉切除术,胃镜插镜顺利,食道黏膜光滑、通畅,蠕动正常。贲门下方可见一1.2 cm×1.2 cm大小黏膜下隆起,表面光滑;胃底可见一1.0 cm×1.0 cm大小扁平黏膜下隆起;胃体可见一0.3 cm×0.3 cm大小息肉,以高频电凝灼除;胃角形态正常,黏膜光滑;胃窦可见2处0.5 cm×0.5 cm大小息肉样隆起,高频电圈套电切切除。幽门圆形,开闭自然,皱壁光滑柔软,桔红色,未见返流。球部黏膜光滑,未见充血、糜烂或溃疡,降部无异常(图1)。术后抑酸、止血、补液等对症治疗,因胃贲门部占位考虑间质瘤,建议手术,进一步在我科住院治疗。超声内镜见贲门下一隆起性病灶,表面光滑,超声探头于隆起病变处显示为一低回声病灶,约2.3 cm×2.0 cm大小,内部有分叶,起源于黏膜下层,内部无血管回声(图2),考虑贲门下隆起病变(平滑肌瘤可能)。实验室检查:AFP(-)、CEA(-)、CA19-9(-),其余各项血液指标均在正常范围。术中探查腹腔未见腹水,肝脏质地可,肝表面未扪及结节,肿瘤位于贲门下,直径约2.5 cm,质软,未侵及浆膜层,确定可切除后,为防止术后胃瘫、减少术后反流性食管炎发生,决定行开腹近端胃大部切除+幽门成形术[1],切除标本送病理检查。送检胃组织小弯长约4.5 cm,大弯长约11.0 cm,胃大小弯所附脂肪组织极少;贲门下小弯侧见一黏膜皱襞消失区,稍隆起,约3.0 cm×2.0 cm。显微镜下胃黏膜层变薄,腺体数目减少,腺上皮无明显异型性;黏膜及黏膜下层见大量呈囊性扩张的腺体,以幽门或十二指肠型腺体为主,少数为胃体型腺体,均分化良好;部分腺腔内可见黏液样分泌物;扩张腺体间可见纤维组织增生及血管扩张、充血,淋巴细胞、浆细胞、嗜酸性粒细胞浸润及淋巴滤泡形成,并见平滑肌包绕;组织学改变符合深在性囊性胃炎(图3)。术后密切随访3年,患者饮食正常,体重增加,无返酸、嗳气、饱胀不适等症状,胃镜及超声内镜检查吻合口通畅,胃内未发现复发病灶,见图4、5。
2 讨论
GCP临床罕见,病理特征改变类似于结肠的深在性囊性结肠炎,最初由Franzin等发现并命名。GCP的病因及发病机制不明,易与多种疾病如胃间质瘤、异位胰腺,淋巴瘤、平滑肌瘤等混淆,导致临床决断失误。因最初多发现于胃手术后胃肠吻合口部位,故推测其发病机制可能与手术对完整胃黏膜创伤引起的局部炎症反应、异物刺激黏膜腺体引起胃黏膜异位导致腺体增生有关[2]。近年来,随着消化内镜技术的不断发展,临床上GCP的检出率有所增加,这部分病人并无胃手术史,因此认为GCP可能与Kcne2基因缺失、EB病毒感染和幽门螺杆菌感染等的发生发展有密切关系[3~5]。大多数学者认为GCP是一种良性病变,但也有报道该病可与胃癌并发,发生率0.36%~3%,因此认为GCP可能也是一种癌前病变[6~8]。
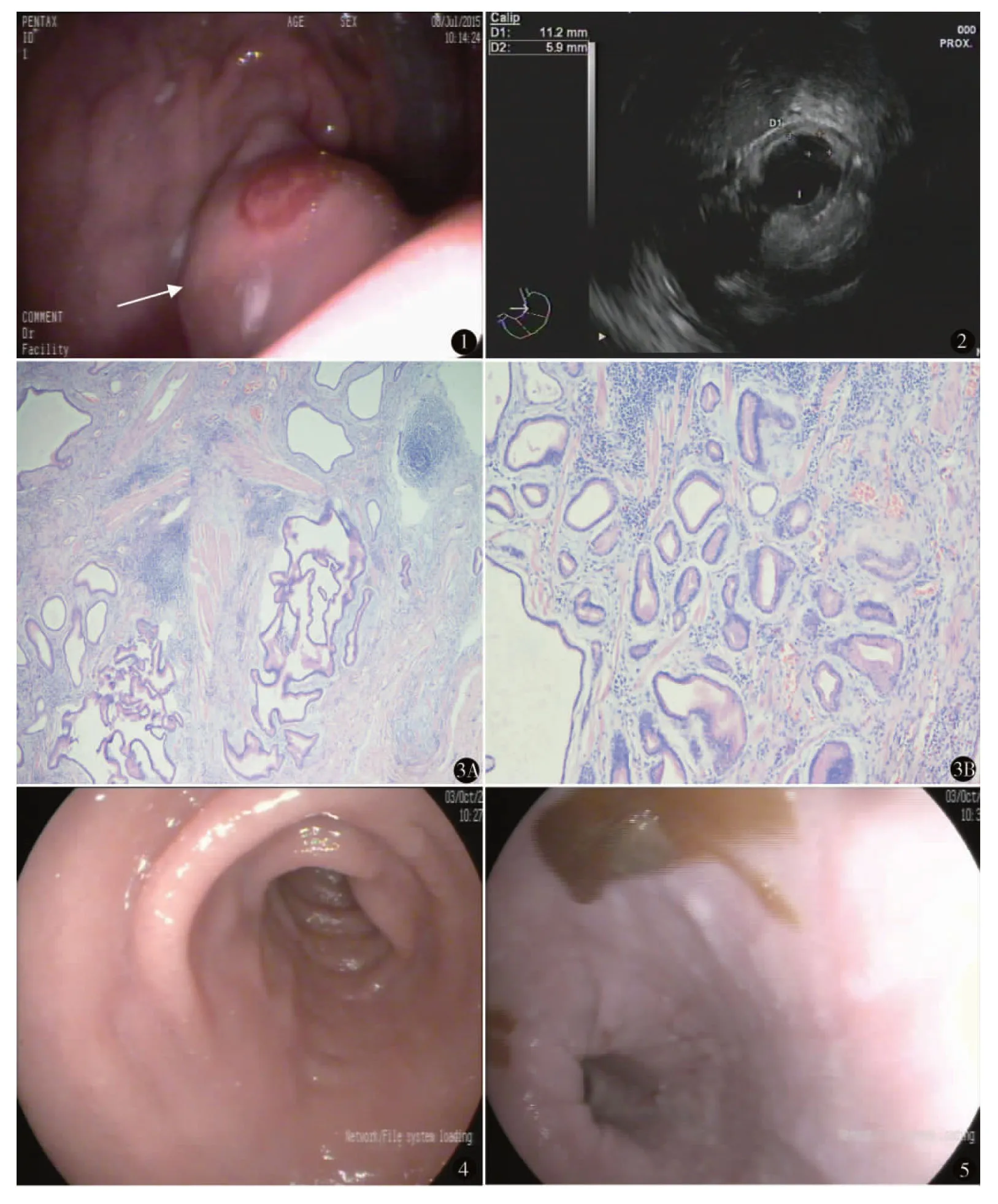
图1 胃镜示胃黏膜皱襞不规则增厚,贲门下方可见一1.2 cm×1.2 cm黏膜下隆起,表面光滑 图2 超声内镜示贲门下起源于黏膜下层隆起性低回声病灶,约2.3 cm×2.0cm大小,内部有分叶,无血管回声图3 胃黏膜层变薄,腺体数目减少,腺上皮无明显异型性;黏膜及黏膜下层见大量呈囊性扩张的腺体,分化良好(HE染色 A. ×40 B. ×100) 图4,5 术后复查胃镜,吻合口通畅,胃内未发现复发病灶
GCP的临床表现多样但缺乏特异性,多表现为程度不同的消化不良症状,如上腹胀痛不适、纳差、反酸等,部分病人伴有胃黏膜糜烂,上腹部疼痛较明显,并可有呕血、黑便等出血症状。本例就诊时主诉食欲减退、消瘦、上腹部不适并进行性加重,无呕血、黑便等出血症状,体检时腹部并无明显阳性体征。由于GCP临床表现缺乏特异性,血常规及生化等常规实验室检查并无明显异常表现,为临床正确诊断带来很大困难。上消化道造影可发现病变部位的充盈缺损,检出率与病变的大小有关。上腹部增强CT扫描可发现胃壁呈不规则增厚,部分病人黏膜隆起或为突向腔内的肿块,这些影像学表现对诊断并无特异性,容易误诊为胃癌、胃间质瘤、淋巴瘤等其他胃部疾病。胃镜和超声内镜检查对本病的诊断有一定的意义,胃镜检查镜下表现多样,朱博群等[8]将其典型表现分为黏膜病变型、息肉样隆起型、黏膜下隆起型、黏膜肥厚及皱襞粗大型四类,黏膜病变型又分为黏膜扁平隆起Ⅱa、黏膜扁平隆起伴轻度凹陷Ⅱa+Ⅱc、黏膜轻度凹陷Ⅱc三类,其中黏膜下隆起型为内镜下最常见表现,由于胃镜常规活检受限于取材表浅而少,局限于黏膜层,无法取得黏膜下病变部位组织,因而病理上难以做出准确诊断。超声内镜表现亦缺乏特异性,显示为无回声的囊腔或增厚的胃壁黏膜下层低回声区,还需与胃癌、胃间质瘤、胃淋巴瘤及胃囊肿等相鉴别。本例因胃多发息肉入院,内镜下表现为多发的息肉样隆起,术前经胃镜行息肉电灼切除,未行病理检查,因此,术前未能获得准确诊断。因贲门下隆起性病灶较大,超声内镜考虑平滑肌瘤可能,转入我科手术治疗,术后病理示黏膜及黏膜下层大量呈囊性扩张的腺体,分化良好,组织学改变符合GCP而确诊,故最终诊断尚需病理证实。
GCP的生物学行为虽表现为良性疾病,但术前获得正确诊断困难,部分病人可同时发生胃癌。朱博群等[9]报道GCP患者常合并早期胃癌,老年男性、既往远端胃切除史、病灶位于贲门、内镜表现为Ⅱa+Ⅱc型可能是GCP合并早期胃癌的高危因素,因此,GCP是否为一种癌前病变值得进一步研究证实。绝大部分患者因诊断为胃癌或间质瘤而施行胃大部切除术,术后病理证实为GCP,手术虽可以解除症状和根治疾病,但施行胃大部切除手术是否成为必须值得探讨,因此,如何进一步提高患者术前确诊率,避免过度治疗是一个需要解决的关键问题。我们体会虽然术前做到准确诊断GCP困难,但对于诊断不明患者可采用内镜黏膜下剥离术(endoscopic submucosal dissection,ESD)或内镜下黏膜切除术(endoscopic mucosal resection,EMR),既可以通过切除的标本获得准确诊断,又能够达到根治疾病的效果。Xu等[10]采用ESD和EMR治疗34例GCP,术后除1例出现迟发性出血外均无手术相关性并发症,术后随访1年未见复发。何志刚等[11]采用ESD治疗6例GCP, 随访1~3.5年均未见复发,获得满意的治疗效果。随着消化内镜技术的发展,ESD和EMR治疗GCP有可能成为取代传统手术方式的首选方法。
