维生素D及脂蛋白(a)和冠心病及其严重程度的关系
2019-10-10杨国康金红艳
杨国康 金红艳
(武汉科技大学附属汉阳医院心血管内科,湖北 武汉 430000)
冠状动脉粥样硬化性心脏病简称冠心病(CHD),是指冠状动脉粥样硬化使管腔狭窄或阻塞,和(或)功能性改变导致心肌缺血缺氧引起的心脏病。近年来,CHD发病率日益增高,且呈年轻化趋势,严重危害人类健康。鉴于目前传统的危险因素不能解释全部的CHD心血管事件,越来越多的研究致力于发现新的危险因素〔1〕。目前许多研究结果表示,维生素D〔25(OH)D〕缺乏可以增加心血管疾病的发病风险〔2~4〕。流行病学数据显示,血清25(OH)D不足或缺乏在各类人群中普遍存在,而在CHD患者中尤为显著〔5,6〕。低血清25(OH)D水平和CHD发病风险之间显著相关〔7,8〕。同样,亦有研究显示,血浆脂蛋白(Lp)(a)水平的升高是CHD的独立危险因素,且与冠脉粥样硬化的程度呈正相关〔9,10〕。因此,本研究旨在探讨25(OH)D及Lp(a)水平的交互作用与CHD及其病变程度之间的关系。
1 资料和方法
1.1一般临床资料 收集2016 年12月至 2017年12月武汉科技大学附属汉阳医院心血管科行经皮冠状动脉造影(CAG)的患者共472例,其中男312例,女160例。根据造影结果分为对照组和冠状动脉病变组,其中对照组81例,CHD组391例。排除标准:①心功能Ⅳ级、恶性肿瘤、肝肾功能不全、急慢性感染性疾病;②既往CHD介入治疗史;③近1月内使用过调节血脂类药物或其他可能影响脂质代谢的药物;④3个月内曾使用25(OH)D及相关制品。记录所有入选对象的一般情况,包括性别、年龄、身高、体重、高血压和糖尿病病史等情况。根据公式计算患者的体重指数(BMI)。
1.2血液生化指标及血清25(OH)D水平的测定 患者入院后次日清晨空腹采血5 ml,检测指标包括空腹血糖(FBG)、总胆固醇(TC)、三酰甘油(TG)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)、Lp(a)。应用罗氏Cobase601全自动电化学发光分析仪检测血清25(OH)D 水平(德国罗氏诊断有限公司试剂盒),操作步骤按说明书进行。
1.3CAG检查及评价 CAG采用Judkin法。成像设备采用美国GE Innova2100-IQ平板探测器血管造影系统,应用Seldinger穿刺技术,经桡动脉路径行左右CAG。CHD病变程度采用介于经皮冠状动脉介入治疗和心脏外科手术协同作用(SYNTAX)评分系统,分为轻度组(0~22分)、中度组(23~32分)和重度组(≥33分)。血管造影分析CHD导致直径≥1.5 mm血管狭窄≥50%的分别计分,并加在一起,根据SYNTAX评分算法生成累积SYNTAX评分〔11〕。
1.4统计学方法 采用SPSS17.0软件进行χ2检验或 Fishers 确切概率法、方差分析、非参数检验及Logistic回归分析。
2 结 果
2.1各组基本临床及生化指标比较 391例CHD患者,其中轻度组222例,中度组113例,重度组56例。四组在性别、吸烟史、HDL-C、Lp(a)、25(OH)D、SYNTAX评分方面差异有显著性意义(P<0.05)。随着CHD病变程度的加重,男性及有吸烟史的比例越来越大,HDL-C和25(OH)D水平降低,而Lp(a)和SYNTAX评分则随之升高。见表1。
表1 各组临床和生化指标比较
2.225(OH)D 水平及LP(a)水平与CHD的Logistic回归分析 以25(OH)D<20 ng/ml及25(OH)D≥20 ng/ml〔12〕分层分析,是否患有CHD(对照组为0,病变组为1)作因变量,Lp(a)水平为自变量(<30 mg/dl为0,≥30 mg/dl为1)〔13〕,同时纳入25(OH)D及Lp(a)的交互作用项,进行Logistic回归分析。结果显示若25(OH)D<20 ng/ml,Lp(a)水平与CHD不相关(P>0.05);若25(OH)D≥20 ng/ml,则Lp(a)水平与CHD独立相关,经年龄、性别、吸烟史、HDL-C等多因素校正后,仍有显著性意义(P=0.003)。同时25(OH)D及Lp(a)存在相乘的交互作用(P=0.032)。见表2。
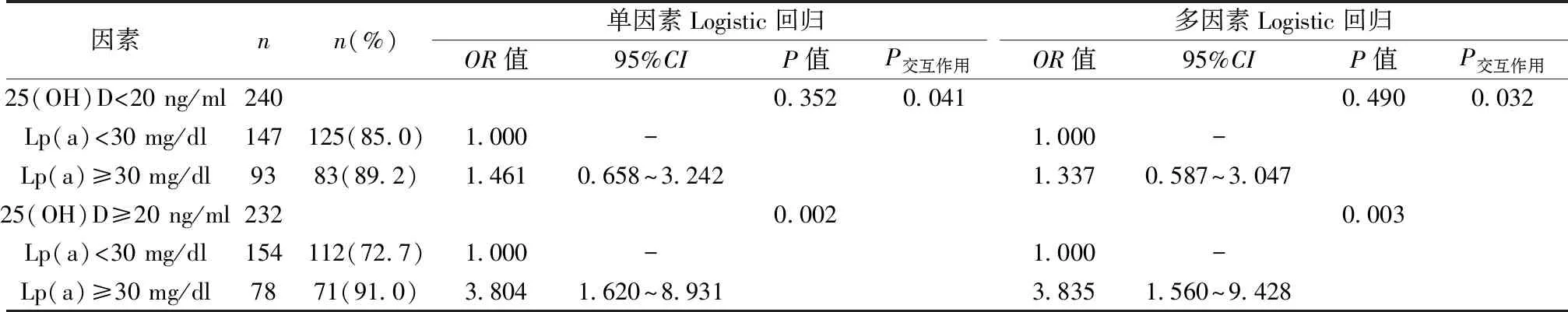
表2 25(OH)D及Lp(a)与CHD的Logistic回归分析
n(%)是否患有冠心病;多因素:经过年龄、性别、吸烟史、HDL-C校正
2.325(OH)D 水平及LP(a)水平与CHD病变程度Logistic回归分析 以25(OH)D<20 ng/ml及25(OH)D≥20 ng/ml分层分析,CHD病变程度(对照组及轻度组为0,中重度组为1)作因变量,Lp(a)水平为自变量(<30 mg/dl为0,≥30 mg/dl为1),同时纳入25(OH)D及Lp(a)的交互作用项,进行Logistic回归分析。结果显示无论25(OH)D水平如何,Lp(a)水平与CHD病变程度独立相关,经年龄、性别、吸烟史、HDL-C等多因素校正后,仍有显著性意义。同时25(OH)D及Lp(a)存在相乘的交互作用(P=0.024)。见表3。
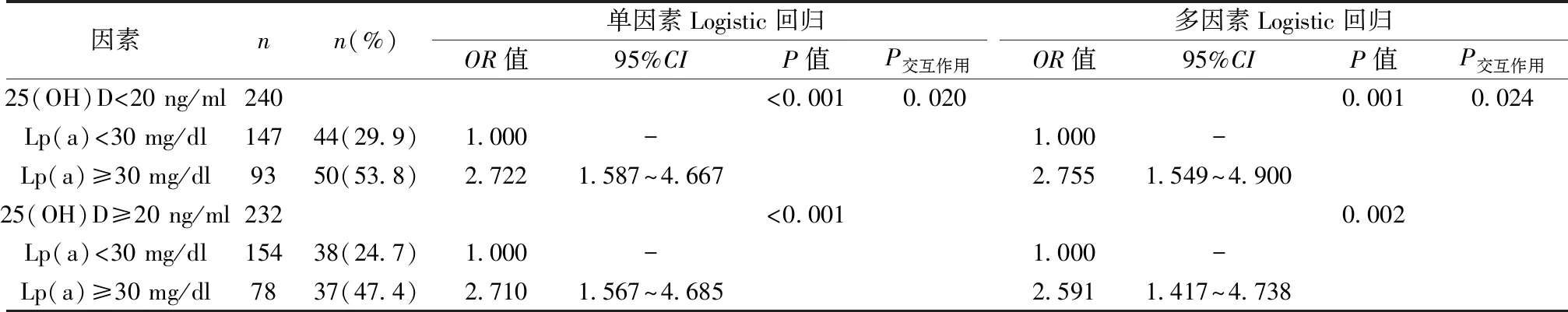
表3 25(OH)D及Lp(a)与CHD病变程度的Logistic回归分析
n(%)是冠脉病变中重度组(SYNTAX评分≥23);多因素:经过年龄、性别、吸烟史、HDL校正
2.425(OH)D及LP(a)相加的交互作用与CHD及病变程度的相关性分析 按照25(OH)D及LP(a)水平,将研究对象分为A组〔25(OH)D≥20 ng/ml,Lp(a)<30 ng/dl,n=154〕、B组〔25(OH)D≥20 ng/ml,Lp(a)≥30 mg/dl,n=78〕、C组〔25(OH)D<20 ng/ml,Lp(a)<30 ng/dl,n=147〕及D组〔25(OH)D<20 ng/ml,Lp(a)≥30 ng/ml,n=93〕。以A组为参考,其OR值(CHD风险)为1.00,经年龄、性别、吸烟史、HDL-C等多因素校正后,B、C、D三组的OR值(CHD风险)均显著性升高(P=0.003,OR=3.753,95%CI=1.556~9.056;P=0.036,OR=1.895,95%CI=1.044~3.441;P=0.012,OR=2.654,95%CI=1.234~5.707)。同样的,以A组为参考,其OR值(中重度CHD风险)为1.00,经年龄、性别、吸烟史、HDL-C等多因素校正后,B、C、D三组的OR值(中重度CHD风险)分别为(P=0.001,OR=2.626,95%CI=1.456~4.737;P=0.517,OR=1.187,95%CI=0.706~1.997;P<0.001,OR=3.274,95%CI=1.872~5.726),部分具有显著性意义。
3 讨 论
目前国际上较为普遍的评价25(OH)D状态的定义为:血清25(OH)D<20 ng/ml为25(OH)D缺乏,20~30 ng/ml为不足,>30 ng/ml为充足〔12,13〕。近些年来的研究发现25(OH)D不仅参与钙磷代谢,还与糖尿病、自身免疫性疾病、心血管疾病、肿瘤、感染性疾病等密切相关〔14〕。据一项Meta分析统计结果显示,血清25(OH)D水平在20~60 nmol/L范围内与心血管疾病的风险呈线性相关〔15〕。本研究结果表明25(OH)D水平高低与冠状动脉粥样硬化程度有关。然而,目前低水平25(OH)D如何影响冠状动脉粥样硬化过程,其内在机制尚不明确。研究表明,25(OH)D可能通过抗栓、抑制炎症〔16〕,调节内皮细胞功能〔17〕,调节胰岛素抵抗、参与血糖血脂调节〔18,19〕,调节肾素-血管紧张素-醛固酮系统(RAAS)〔20〕等方面参与冠状动脉硬化的过程。
Lp(a)由其特征性载脂蛋白(a)〔Apo(a)〕和LDL样颗粒包绕而成,其中Apo(a)通过二硫键与另一主要Apo B100 共价连接。人群中血清Lp(a)的浓度变异范围很大,有研究界定Lp(a)≥30 mg/dl为异常〔21〕。国外学者〔21〕研究亦认为当Lp(a)水平>30 mg/dl时,CHD的危险性增加1.75倍,当Lp(a)>50 mg/dl时,危险性可增加至2.3倍。此外,国内一项血脂与CHD的敏感度研究〔22〕显示,在诊断CHD价值方面,Lp(a)相对优于其他的各项血脂指标(Lp(a)>TG>LDL-C>TC>HDL>ApoB>ApoA)。还有国内外大量研究显示血浆Lp(a)水平与冠状动脉粥样硬化的严重程度亦有一定关系,同时也是急性心肌梗死的强有力的预测因子〔23〕。然而,由于Lp(a)浓度在不同种族人群中差异极大,因此尚有研究指出CHD为非西方人群及高加索人群预测CHD的独立危险因素〔24〕。本研究中亦得出相似结论,发现Lp(a)与CHD发病风险及其严重程度独立相关。本研究结果说明对于非25(OH)D缺乏的人群而言,Lp(a)水平的异常可能更容易导致CHD的发病,尚需要进一步研究证实。
既往的研究对评估低25(OH)D水平对CHD患者病变程度的影响有待商榷。一项对CAG人群的研究表明,低25(OH)D水平和冠脉严重狭窄之间存在的相互作用〔25〕。而另一项研究发现低25(OH)D水平和冠脉严重狭窄无明显关联〔26〕。以往对冠状动脉严重程度采用Gensini评分进行评估,但Gensini评分并不能完全反映冠状动脉病变的复杂性,因为Gensini评分没有考虑如分叉、钙化、病变长度和弯曲度相关的因素。SYNTAX评分是一种新的根据冠状动脉病变解剖特点进行危险分层的积分系统,根据病变位置、严重程度、分叉、钙化等解剖特点定量评价冠脉病变的复杂程度,以期作为手术方式选择及预测复发率和死亡率的判断手段。本研究存在显著性的相乘的交互作用,提示25(OH)D水平和Lp(a)之间的交互作用可能对CHD的患病风险及其冠脉病变程度有着重要的影响。
本研究结果提示可能25(OH)D及LP(a)相加的交互作用与CHD及病变程度之间存在相关性。目前在体外研究中,25(OH)D已被发现可以调节高血糖介导的M1/M2巨噬细胞极化过程,抑制M2巨噬细胞的胆固醇形成,增强TC外流〔27,28〕。在动物试验中〔29〕,25(OH)D可以通过增强的CYP27A1激活控制胆固醇外流及巨噬细胞极化,从而对抗高TC模型猪的动脉粥样硬化过程。目前已知LP(a)是TC的组成成分,同样也有研究发现对于2型糖尿病的患者,提高25(OH)D水平有利于降低血清LP(a)的水平〔30〕。综合以上研究发现,25(OH)D缺乏和LP(a)均有引起动脉粥样硬化形成的作用,或许可以解释本研究中25(OH)D和Lp(a)在CHD中的交互作用。
