二尖瓣置换术中术后左心室后壁破裂的影响因素
2019-09-27何剑成邢朝阳
何剑成,邢朝阳,郑 涛,赵 帆,姚 蓉
1)广元市第一人民医院重症医学科四川广元628000 2)四川大学华西医院急诊科成都610000
我国风湿性心脏瓣膜病多发,二尖瓣置换(mitral valve replacement,MVR)为其主要治疗方法。目前我国MVR开展的绝对数量远多于国外[1-2]。接受MVR的患者心功能一般较差,病情较严重,病死率高[3-4]。左心室后壁破裂为一种MVR术中及术后罕见的并发症,目前仅有少数病例报道,但即便在大规模心脏中心该并发症也时有发生。该并发症抢救成功率低,常危及患者生命,国内学者刘进平等[5]认为该症重在预防,及早判断,一旦发生,经积极探查、修补裂伤,可挽救部分患者生命。因此分析MVR术中术后左心室后壁破裂发生的危险因素,探寻相应的预防措施已成为重症医学科的共识[6-8]。本文回顾性分析了2012年9月至2018年9月在我院行MVR的520例患者的资料,分析术中术后左心室后壁破裂发生情况及其危险因素,结果报道如下。
1 临床资料
1.1 一般资料 520例患者心脏彩超均提示二尖瓣增厚,交界粘连,主动脉瓣增厚,开放受限;CT显示二尖瓣瓣叶明显增厚,主动脉瓣叶增厚;均诊断为重度二尖瓣狭窄伴持续房颤,接受MVR;患者临床资料完整,且均能配合完成本次研究。其中男291例,女229例;年龄43~72岁;美国纽约心脏病学会(NYHA)心功能分级Ⅱ级383例,Ⅲ级53例,Ⅳ级84例;既往有风湿性瓣膜病355例,高血压9例,高血脂4例,脑梗死5例。520例中共10例发生左心室后壁破裂。
1.2 MVR手术方法 术中采用静吸复合麻醉,行胸部正中切口,体外循环直视停跳后,主动脉根部顺行灌注4℃血液停跳液以保护心肌。经房间沟左心房切口或房间隔切口显露二尖瓣并病变二尖瓣。若瓣环强度差则以间断带垫片褥式缝合固定人工瓣,否则予以2-0聚丙烯线连接缝合。患者均保留二尖瓣腱索。
1.3 观察指标 收集的资料信息包括性别、年龄、风湿性心脏病史、营养不良、贫血状况、心包积液、心房纤颤、术前窦性心律、感染性心内膜炎、瓣膜假体选择(瓣膜假体型号与患者情况不匹配等为假体选择不当)、NYHA心功能分级、左室射血分数(LVEF)、左室舒张末期内径(LVEDD)、左心房内径(LAD)、左心室容量负荷、左室后壁厚度、体外循环时间、心肌致密化不全(NVM)、正性肌力药物(β-受体阻滞剂或ACEI类药物)使用等情况。左心室容量负荷过重标准:主动脉瓣关闭不全时,主动脉瓣反流导致左心室前负荷(容量负荷)增加。
1.4 统计学处理 采用SPSS19.0处理数据,发生和未发生左心室后壁破裂患者年龄的比较采用两独立样本的t检验,其他分析指标的比较采取校正χ2检验,采用Poisson回归分析筛选左心室后壁破裂发生的影响因素,检验水准α=0.05。
2 结果
2.1 左心室后壁破裂发生情况 520例中共3例于术中、7例于术后发生左心室后壁破裂,发生率为1.92%(10/520)。1例术中发生早期破裂,经体外循环心室内修补存活;另9例均于院内死亡。
2.2 MVR术中术后左心室后壁破裂的影响因素分析 发生和未发生左心室后壁破裂患者各项指标的比较见表1。其中 NYHA分级、LVEF、LVEDD、LAD、左室后壁厚度、体外循环时间分组依据参照文献[9]。表1显示,破裂组女性、贫血、瓣膜假体选择不当、NYHA分级Ⅲ~Ⅳ级、LVEF<50%、LVEDD>80 mm、LAD>60 mm、左心室容量负荷过重、左室后壁厚度≥10 mm患者比例和年龄大于未破裂组,而有风湿性心脏病史、有心包积液、体外循环时间<140 min、未使用正性肌力药物的患者比例小于未破裂组。
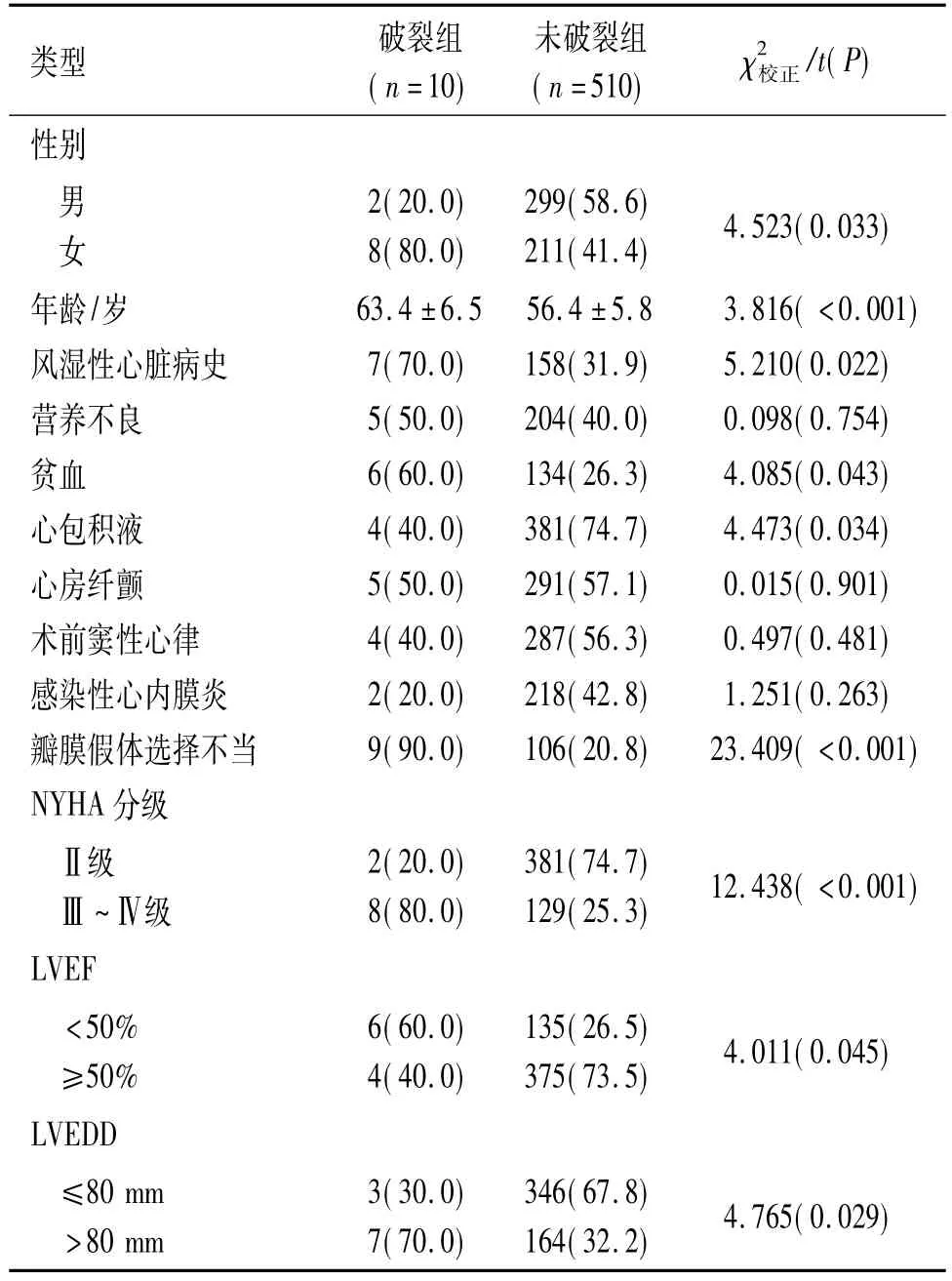
表1 2组各指标的比较 例(%)
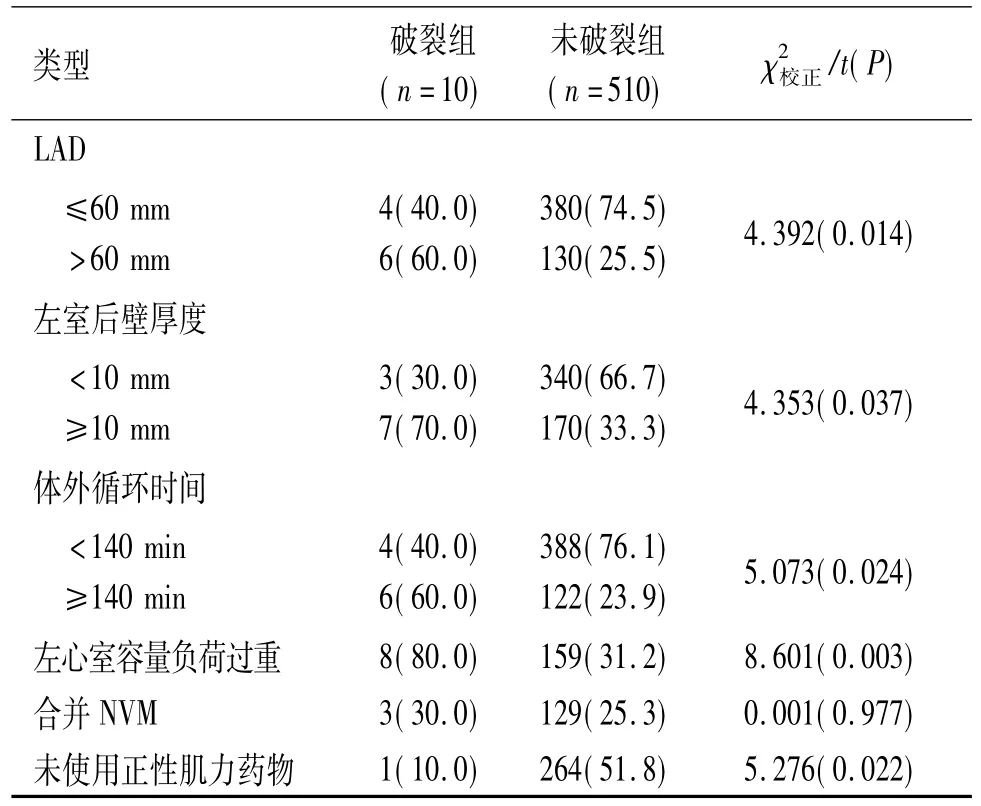
续表1
以是否发生左心室后壁破裂为因变量(破裂为1,未破裂为0),以上述两组差异有统计学意义的指标为自变量,构建Poisson回归模型。结果(表2)显示,年龄、贫血、瓣膜假体选择不当、有风湿性心脏病史、NYHA心功能分级Ⅲ ~Ⅳ级、LVEF<50%、LVEDD>80 mm、左室后壁厚度≥10 mm为MVR术中术后发生左心室后壁破裂的危险因素,而体外循环时间<140 min、未使用正性肌力药物为保护因素。
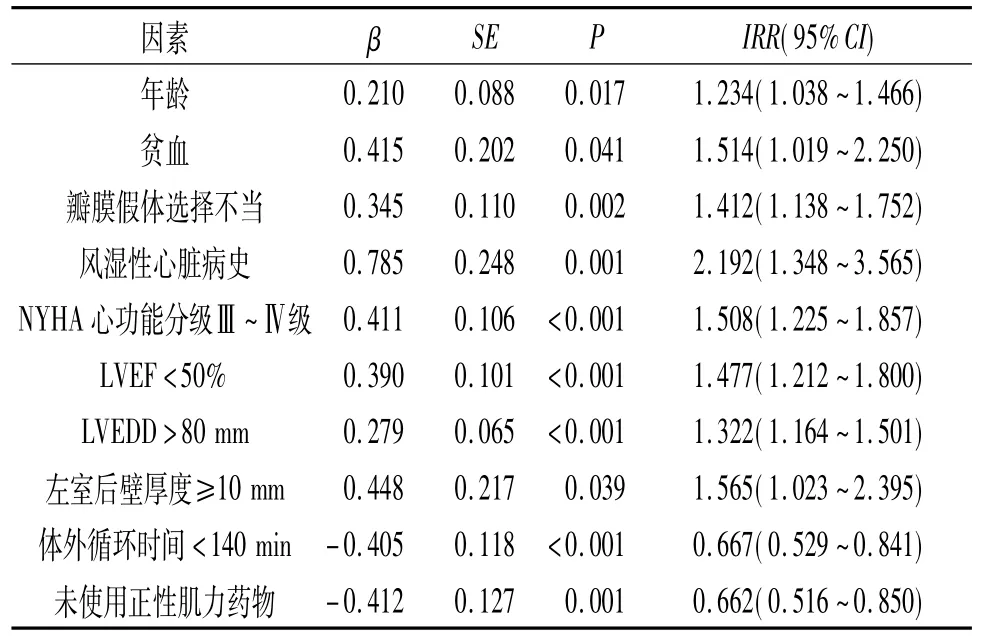
表2 Poisson回归分析结果
3 讨论
左心室后壁破裂是MVR术中术后发生的高致死性并发症,其治疗难度大,效果差。本研究回顾性分析了520例MVR患者的资料,左心室后壁破裂发生率为1.92%,与陈长城等[10]报道的发生率 0.36%(27/7 495)相比略高(P<0.001);本组病死率为90.00%,与陈长城等[10]报道的 96.3%(26/27)相比,差异并无统计学意义(P=0.473)。
本研究对MVR术中术后左心室后壁破裂与未破裂患者的资料进行了对比,并应用Poisson回归筛选危险因素。结果显示,高龄、贫血、瓣膜假体选择不当、有风湿性心脏病史、NYHA心功能分级Ⅲ~Ⅳ级、LVEF<50%、LVEDD>80 mm、左室后壁厚度≥10 mm为其危险因素。年龄大、有贫血症状及风湿性心脏病史的患者,心肌水肿严重,瓣膜增厚、钙化发生率高,腱索挛缩,在置入瓣膜时缝线可能损伤左室心肌。NYHA心功能分级Ⅲ ~Ⅳ级、LVEF<50%、LVEDD>80 mm预示患者心功能较差,术中心脏暴露欠佳,加上此类患者术中与术后对麻醉、药物、吸入性操作的各种应激反应能力差,钝性分离过度牵拉或抬高心尖均会导致左心室后壁破裂。左室后壁厚度≥10 mm预示心肌肥厚及心脏扩大,机体心肌发生线粒体溶解、高能磷酸键降低及心肌纤维化,从而增加了患者左心室后壁破裂的风险[9,11]。瓣膜假体选择不当、手术操作机械损伤如反复搬动心脏、左心引流及心内吸引的不合理应用等也可能造成左心室后壁破裂。因此,为避免患者心功能恶化,应在术前积极调整心功能,若调整后症状有所改善说明有一定数量的心肌细胞存活,仍有手术机会。同时在术中应科学显露二尖瓣、保留二尖瓣后叶与腱索,减少手术风险。
本研究发现体外循环时间<140 min、不使用正性肌力药物可减小MVR术中术后发生左心室后壁破裂的风险。体外循环时间短既可以保证心脏得到适度的按摩,又不会因时间过长或用力过大而引起左心室后壁破裂,同时也能避免剪断腱索时视线不良而划伤左心室后壁[12]。正性肌力药物(β-受体阻滞剂、ACEI类)主要影响患者血压。尽管本研究结果显示不使用正性肌力药物可减小MVR术中术后发生左心室后壁破裂的风险,但我们还是建议术后在不影响血压的情况下可使用小剂量卡托普利等ACEI类药物,对于合并快心室率患者同时可考虑应用β-受体阻滞剂。ACEI类药物不仅能减轻心脏前后负荷,还可防止心肌进一步恶化,逆转心肌与血管重构,而β-受体阻滞剂则能调节心肌细胞上β-受体密度与数量,使心肌细胞对正性肌力药物敏感性增强,继而改善心功能[13]。
