六溴环十二烷(HBCD)对H4细胞和SK-N-AS细胞脱碘酶2和3表达的影响
2019-09-16郝小吉尚小娜于海华么建萍韩璐刘晓晖李亚晨邵静
郝小吉,尚小娜,3,于海华,么建萍,韩璐,刘晓晖,李亚晨,#,邵静,*
1. 大连医科大学公共卫生学院,大连市血液病重点实验室,辽宁省造血干细胞移植医学中心,辽宁省造血干细胞移植临床转化医学研究重点实验室,大连 116044 2. 大连市妇幼保健院,大连 116033 3. 康龙化成(北京)新药技术股份有限公司,北京 100176
六溴环十二烷(hexabromocyclododecane, HBCD)是一种高溴含量的脂环族添加型阻燃剂,与多溴联苯醚(PBDEs)均属于溴系阻燃剂(BFRs),作为PBDEs替代物被广泛使用,同样应用于电子、电器、化工、交通、建材、纺织、石油和采矿等领域。与PBDEs类似,HBCD易于从产品中游离、释放到环境介质中,具有持久性和蓄积性,从而成为一种新型环境有机污染物[1-2]。有研究认为,HBCD可能与PBDEs形成复合污染体系,二者共同作用,对人类健康造成潜在危害[3]。
HBCD毒性作用主要表现为肝脏损伤[4]、内分泌干扰[5-6]和神经毒性[7]等方面。尤其,处于脑发育期的婴幼儿及儿童是HBCD及HBCD/PBDEs复合污染物暴露的高风险人群。HBCD诱导的发育神经毒性效应主要来源于神经发育时期[8]。研究表明,HBCD引起发育神经毒性的机制可能与2个因素有关:(1)引起脑局部神经细胞损伤,而直接影响神经系统发育;(2)通过影响脑局部甲状腺激素水平,间接影响神经发育水平,但二者的联系机制尚不清楚。
机体不同组织细胞对甲状腺激素的生理需求不同,需要对来自循环的甲状腺激素在局部细胞中进行调节,使组织局部甲状腺激素并不完全依赖外周循环水平。组织中脱碘酶(deiodinase, Dio)对此起着关键作用。Dio是一组含硒蛋白酶,分三型(Dio1、Dio2和Dio3),各自以独特的脱碘方式调节其所分布组织细胞内甲状腺激素(thyroxine, TH)的生物活性。Dio2功能是通过外环脱碘在细胞内将四碘甲状腺原氨酸(tetraiodothyronine, T4)转化为活性三碘甲状腺原氨酸(triiodothyronine, T3),并通过特异的T3受体发挥生物功能,在机体生长发育中起重要作用,是哺乳动物胚胎中主要的脱碘酶[9];在脑组织中,Dio2主要分布于神经胶质细胞中[10-11]。Dio3主要分布于神经元细胞,特别是胎脑、1月龄以内的婴儿皮肤、胎盘和胎儿肠组织中,是通过内环脱碘将细胞外T4和T3分别转化为无活性的反三碘甲状腺原氨酸(reverse triiodothyronine, rT3)和二碘甲状腺原氨酸(diiodothyronine, T2),调节组织细胞内T3水平,避免发育中的胎儿和胎儿组织暴露于高浓度活性甲状腺激素中[11-12]。Dio1具有内、外环脱碘的双重活性,可在外周组织中清除rT3,并介导血清T3生成[13-14]。
作为环境有机污染物神经毒性研究的一部分,本研究以人脑神经母细胞瘤细胞(SK-N-AS)和人神经胶质瘤细胞(H4)作为体外生物模型,初步探讨HBCD对2种神经细胞的细胞毒性,以及对2种脱碘酶在不同细胞中表达特征的影响,明确Dio2和Dio3在HBCD诱导神经毒性中的作用,以期探索孕期HBCD暴露是否通过影响胚胎脑局部脱碘酶表达、调控局部甲状腺激素水平,进而导致子代神经系统发育损伤。
1 材料与方法(Materials and methods)
1.1 试剂与材料
HBCD(纯度95%,美国Sigma公司),胎牛血清(Gibco公司,北美),DMEM低糖、高糖培养基(Hyclone公司,美国),兔抗人多克隆抗体Dio2、Dio3及BDNF脑源生长因子ELISA试剂盒(Abcom公司,美国),Dio2和Dio3基因引物、RNA提取及反应试剂盒PrimeScriptTMRT reagent Kit、SYBR®Premix Ex TaqTM( TaKaRa公司,日本),BCA蛋白浓度测定试剂盒、预染彩色蛋白分子量Maker、RIPA裂解液、四甲基乙二胺(TEMED)等(碧云天生物技术有限公司,北京),HRP标记的羊抗兔二抗(Proteintech公司,美国),ECL检测试剂盒(南京凯基生物科技发展有限公司),氯仿、乙醇和异丙醇等均为分析纯,分别购自天津市科密欧化学试剂有限公司和天津市化学试剂一厂。SK-N-AS、H4细胞来自美国ATCC细胞库。
1.2 仪器
细胞培养箱(Thermo 3111,赛默飞世尔科技(中国)有限公司),354型多功能酶标仪(Thermo公司,美国),CKX41型倒置相差荧光显微镜(Olympus公司,日本),电泳系统(EPS-300,上海天能),梯度PCR仪(T100TM Thermal Cycler,美国Bio-RAD公司),实时PCR系统(Takara Thermal Cycler Dice TP800,宝生物公司),高速冷冻离心机(HERMLE公司,德国),化学发光凝胶成像系统(UVP公司,美国),Biodropsis超微量核酸分析仪(BD-1000,北京五洲东方科技发展有限公司)。
1.3 样品采集及指标检测
1.3.1 细胞的复苏及培养
将冻存的SK-N-AS、H4细胞复苏,SK-N-AS用DMEM低糖培养基,H4用DMEM高糖培养基培养,其中各加入10%的胎牛血清及1%的青-链霉素双抗,将细胞放置于37 ℃、5% CO2培养箱中,待细胞融合将近80%时,用0.25%胰酶消化为细胞传代,培养过程中及时换液,保证细胞生长状态良好。
1.3.2 MTT检测细胞存活率
收集对数生长期的细胞,调整细胞悬液浓度为8×104个·mL-1,铺于96孔板底100 μL·孔-1,设置5个复孔。置37 ℃、5% CO2培养箱中培养8~24 h,弃清液;加入不同浓度HBCD(0、1、3、9 μmol·L-1),100 μL·孔-1,置37 ℃、5% CO2培养箱染毒24 h,弃清液;每孔加100 μL新鲜配制的MTT应用液,继续置37 ℃、5% CO2培养箱中2 h,弃清液;每孔加100 μL二甲基亚砜(DMSO),置37 ℃、5% CO2培养箱中1 h,使结晶物充分溶解。用酶标仪于波长595 nm测定各孔OD值,计算细胞在不同浓度下的存活率。保证实验条件的稳定性,结果重复3次以上。
1.3.3 实时荧光定量PCR(qRT-PCR)检测脱碘酶Dio2和Dio3基因表达
取生长对数期的SK-N-AS、H4细胞,分别用0、1、3和9 μmol·L-1HBCD处理24 h,用TransZol Up试剂盒提取总RNA,超微量核酸分析仪分析RNA的纯度,保证无污染及降解。Dio2、Dio3以及GAPDH基因引物序列见表1。将1 μg的总RNA逆转录成cDNA,按照PrimeScriptTMRT reagent Kit的说明操作,具体反应步骤如下:首先去除基因组DNA(表2),再进行反转录(表3),然后按照SYBR®Premix Ex TaqTM试剂盒说明,构建qRT-PCR的反应体系(表4)。反应在八联管中进行,置于PCR仪上进行实时荧光定量反应。PCR反应条件为:预变性95 ℃、30 s;95 ℃、3 s,60 ℃、30 s,循环40次;95 ℃、15 s,60 ℃、30 s,95 ℃、15 s;每次实验均设置阴性对照,检验引物质量。观察目的基因的扩增曲线及溶解曲线,需满足特异性及灵敏性的要求,以GAPDH的表达量对结果进行标准化,实验重复3次以上。
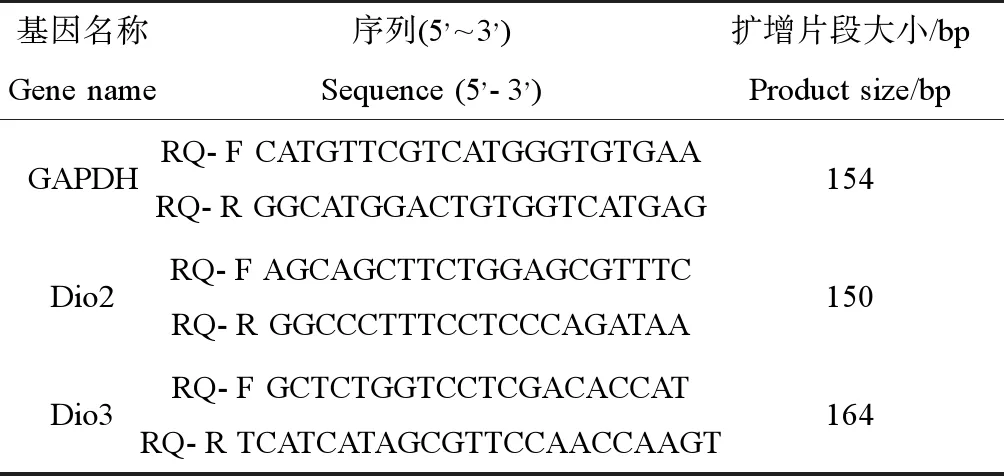
表1 引物GAPDH、Dio2、Dio3的基本参数Table 1 Parameters of GAPDH, Dio2, Dio3 genes

表2 去除基因组DNA反应Table 2 Reaction for eliminating the genomic DNA
1.3.4 Western Blot检测Dio2和Dio3蛋白表达
取生长对数期的SK-N-AS、H4细胞,调整细胞浓度为2×105个·mL-1,铺于10 cm的培养皿中,分别用0、1、3、9 μmol·L-1HBCD处理24 h。(1)提取总蛋白及定量保存:用RIPA裂解液提取总蛋白,用BCA蛋白浓度测定试剂盒对蛋白定量,用蛋白变性剂及煮沸的方法使蛋白变性。(2)电泳分离蛋白及免疫印迹:按表5分别配制12%分离胶和5%浓缩胶,上40 μg的蛋白样品。电泳条件为恒压100 V、90 min;根据预染彩色蛋白分子量Maker,切取所需的蛋白凝胶,采用槽式湿转法将蛋白转移至PVDF膜上,转膜条件为恒流220 mA、90 min。(3)封闭:5%脱脂奶粉封闭2 h。(4)孵育一抗:用1%的脱脂奶按1:400、1:200和1:1 000的比例分别稀释Dio2、Dio3和β-actin抗体,4 ℃孵育过夜。(5)孵育二抗:取一抗孵育的PVDF膜,摇床上TBST洗膜3×10 min,用1%的脱脂奶按1:2 000、1:3 000分别稀释HRP标记的二抗,室温孵育2 h。(6)显影:用TBST洗膜3×10 min,按ECL检测试剂盒用UVP化学发光凝胶成像系统检测蛋白的相对表达量。

表3 反转录反应Table 3 Reaction for reverse transcription

表4 qRT-PCR反应体系Table 4 qRT-PCR reaction
1.3.5 HBCD对H4细胞BDNF分泌的影响
星形胶质细胞(例如H4)分泌的生长因子包含纤维细胞生长因子(bFGF)、内皮生长因子(EGF)、IL-6和BDNF等,不仅影响星形胶质细胞的生长状态,还影响神经元细胞的分裂、分化和迁移、树突和轴突的生长及突触的生成等。其中,BDNF是一种促进受损伤的神经元再生及分化的营养因子,在正常大脑中,介导胶质细胞与神经元细胞之间的相互影响。本实验通过检测HBCD对H4细胞分泌BDNF水平的影响,即细胞上清液中BDNF含量,可初步了解在神经元和胶质细胞共培养体系中或体内生理条件下,HBCD对2种细胞相互作用的改变。
具体方法:细胞经0、1、3和9 μmol·L-1HBCD处理24 h后,收集细胞存活率实验中结果稳定且有意义的细胞上清液,保存于-80 ℃,用于检测BDNF含量,上清经2 000 r·min-1去除细胞碎片,按照ELISA试剂盒的说明进行实验,每个染毒浓度设置3个复孔,每次实验均制作标准曲线,准确计算上清中BDNF的含量。
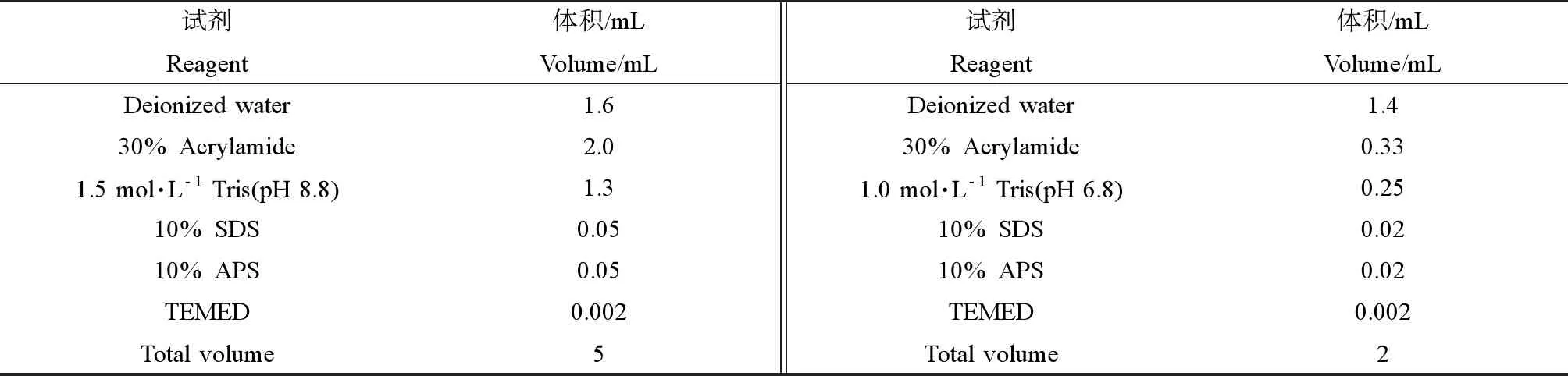
表5 分离胶(12%)和浓缩胶(5%)的配制Table 5 Preparation of separation gel (12%) and stacking gel (5%)
注:SDS表示十二烷基硫酸钠,APS表示过硫酸铵,TEMED表示N,N,N',N'-四甲基乙二胺。
Note: SDS stands for sodium dodecyl sulfate; APS stands for ammonium persulfate; TEMED stands for N,N,N',N'-tetramethylethylenediamine.
1.4 统计分析
结果表示为均值±标准差(Mean±SD),用Graph Prism 7.0进行统计分析和制图。用单因素方差分析(ANOVA test)进行组间比较,方差不齐则用Dunnett’s T3直接进行多重比较。*表示,与对照组比较差异具有统计学意义(P<0.05)。
2 结果(Results)
2.1 HBCD对SK-N-AS细胞生存率及脱碘酶表达的影响
2.1.1 细胞生存率
人神经元细胞SK-N-AS细胞分别暴露于0、1、3和9 μmol·L-1HBCD 24 h,以MTT法检测细胞活力,发现其存活率下降,并具有一定剂量依赖性。由图1可知,与对照组比较,1、3和9 μmol·L-1HBCD染毒组细胞存活率分别为对照组的89%、76%和53%,其中3和9 μmol·L-1HBCD染毒组具有统计学意义(P<0.05)。
2.1.2 Dio3基因和蛋白表达
脑局部神经元主要表达Dio3,因此,本研究考察HBCD对SK-N-AS细胞中Dio3基因和蛋白表达的影响。细胞暴露于0、1、3和9 μmol·L-1HBCD 24 h后,用qRT-PCR法分析SK-N-AS中Dio3基因表达水平,由图2可知,低剂量HBCD使Dio3表达略有下降,而高剂量(9 μmol·L-1)则引起Dio3表达显著上调(P<0.05)。
WesternBlot分析Dio3蛋白表达水平。由图3可知,Dio3的蛋白表达水平变化与基因基本相似,低剂量组略有下降趋势,而9 μmol·L-1组则明显上调(P<0.05)。
2.2 HBCD对H4细胞生存率、脱碘酶表达和BDNF分泌的影响
2.2.1 细胞生存率
人神经胶质细胞H4细胞分别暴露于0、1、3和9 μmol·L-1HBCD 24 h,以MTT法检测细胞活力。与SK-N-AS细胞相似,H4细胞存活率下降,并具有一定剂量依赖性。由图4可知,与对照组比较,1、3和9 μmol·L-1HBCD染毒组细胞存活率分别为对照组的~80%、69%和60%,其中3和9 μmol·L-1HBCD染毒组具有统计学意义(P<0.05)。

图2 HBCD对SK-N-AS细胞Dio3基因表达的影响Fig. 2 Effect of HBCD on Dio3 gene expression in SK-N-AS cells

图3 HBCD对SK-N-AS细胞Dio3蛋白表达的影响Fig. 3 Effect of HBCD on Dio3 protein expression in SK-N-AS cells

图4 HBCD对H4细胞存活率的影响Fig. 4 Effect of HBCD on cell viability of H4 cells
2.2.2 Dio2基因和蛋白表达
脑局部神经胶质细胞主要表达Dio2,本研究考察HBCD对H4细胞中Dio2基因和蛋白表达的影响。细胞暴露于0、1、3和9 μmol·L-1HBCD 24 h,用qRT-PCR法分析H4细胞中Dio2基因表达变化。由图5可知,HBCD引起基因表达下调,且具有剂量依赖性,其中,3和9 μmol·L-1组有统计学意义(P<0.05)。
Western Blot分析H4细胞中Dio2蛋白表达水平。由图6可知,HBCD对Dio2蛋白表达的影响与对基因表达影响一致,亦可引起蛋白表达下调,且具有剂量依赖性,其中,3和9 μmol·L-1组有统计学意义(P<0.05)。
2.2.3 对BDNF分泌的影响
H4细胞暴露于0、1、3和9 μmol·L-1HBCD 24 h,ELISA分析细胞外BDNF蛋白含量,由图7可知,HBCD暴露可致H4细胞分泌的BDNF蛋白明显减少,其中,3和9 μmol·L-1HBCD组与对照组相比有统计学意义(P<0.05)。
3 讨论(Discussion)
环境有机污染物对甲状腺激素水平影响已成为发育神经毒性研究的重点之一,甲状腺激素对脑发育的影响逐渐受到重视。甲状腺激素水平的相对稳态主要是靠下丘脑-腺垂体-甲状腺轴(HPT轴)调控。HPT轴是一个复杂的甲状腺激素(TH)代谢和作用调节网络,TH受体、脱碘酶、甲状腺素转运蛋白(TTR)和钠碘转运体被认为是重要的功能基因参与TH合成、运输、代谢和发挥生物活性[15],并且可能是暴露于环境污染物的生物体甲状腺破坏的敏感分子生物标志物[16-17]。

图5 HBCD对H4细胞Dio2基因表达的影响Fig. 5 Effect of HBCD on Dio2 gene expression in H4 cells

图6 HBCD对H4细胞Dio2蛋白表达的影响Fig. 6 Effect of HBCD on Dio2 protein expression in H4 cells
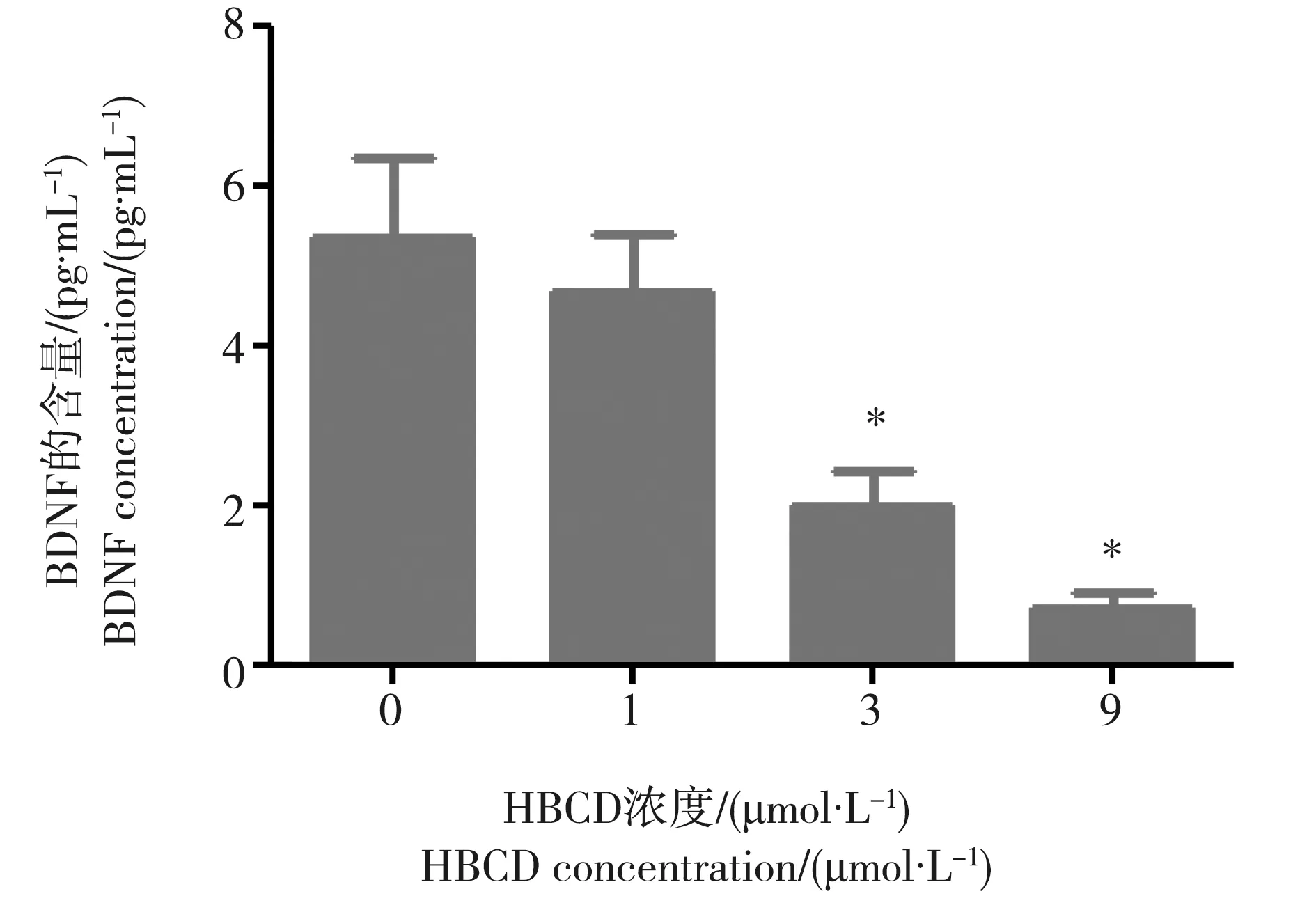
图7 HBCD对H4细胞BDNF分泌的影响Fig. 7 Effect of HBCD on BDNF secretion in H4 cells
HBCD与PBDEs均具有内分泌干扰作用,其中,孕期PBDEs对甲状腺激素的干扰作用,已在动物实验研究中得到证实,主要表现为血液中T4浓度降低。脱碘酶是甲状腺激素代谢中最重要的转化酶,对维持机体甲状腺激素水平起着决定作用。脱碘酶不仅参与甲状腺激素的合成与活化,而且对甲状腺功能具有重要的调节作用。组织中脱碘酶对来自循环的甲状腺激素在局部细胞中的调节起着关键作用。笔者课题组的前期研究发现,孕哺期BDE 209暴露能够影响出生后子代甲状腺激素脱碘酶基因的表达,同时伴有学习记忆能力下降[18]。由于HBCD与PBDEs和甲状腺激素结构不相似,因此,HBCD被认为具有较低干扰甲状腺轴的可能性。然而,最近研究表明,HBCD与PBDEs一样可干扰生物体内甲状腺稳态[5,19],从而影响机体生长发育,特别是脑的正常发育。
研究证实,HBCD暴露能够影响脱碘酶的活性和基因表达,从而干扰生物体内甲状腺稳态。Palace等[20]研究发现,虹鳟鱼用含HBCD饲料喂养32 d后,肝脏Ⅱ型外环脱碘酶活性显著升高,而虹鳟鱼幼鱼经HBCD暴露后,血浆游离三碘甲状腺原氨酸(free triiodothyronine, FT3)和游离甲状腺素(free tetraiodothyronine, FT4)水平改变,14 d后肝微粒体T4外环脱碘酶(T4ORD)活性未受到影响,但56 d后T4外环脱碘酶活性显著降低。刘园园等[21]研究发现,脑发育期大鼠,经HBCD暴露后,血清中总甲状腺素(total tetraiodothyronine, TT4)、总三碘甲状腺原氨酸(total triiodothyronine, TT3)、FT4、FT3浓度随着暴露剂量增大呈现先升高后下降的趋势,并且肝脏D1活性及基因表达水平和脑D2活性及基因表达水平均呈下降趋势。García等[22]研究发现,循环T3和T4通过改变Ⅱ型脱碘酶活性影响脱碘作用的速度。此外,HBCD暴露可通过增强葡萄糖苷酸化来提高甲状腺激素的分泌[23],通过增强组织结合能力[24]或增强脱碘和消除作用[21]提高甲状腺激素从循环中的摄取,这些都能影响循环甲状腺激素的水平,继而影响脱碘酶活性。这些研究显示了HBCD对甲状腺激素代谢过程影响的复杂性。HBCD暴露是直接影响脱碘酶转录或翻译,还是通过改变外周甲状腺激素水平间接影响脱碘酶尚不能确定。本研究中,笔者调查了HBCD对H4人脑神经胶质瘤细胞Ⅱ型脱碘酶(Dio2)和SK-N-AS人神经母细胞瘤细胞Ⅲ型脱碘酶(Dio3)表达的影响,结果显示,HBCD以剂量依赖方式降低H4细胞和SK-N-AS细胞生存率,引起H4细胞Dio2蛋白和基因表达下调,而致SK-N-AS细胞Dio3蛋白和基因表达上调。这些结果提示,HBCD可能通过抑制Dio2的表达,减少脑细胞内由T4向T3的转化,而通过增加Dio3的表达,将细胞外T4和T3分别转化为无活性的rT3和T2,从而使脑局部T3水平降低,影响脑发育。为明确HBCD对脱碘酶表达的影响是否对局部T3、T4水平有干扰作用,本研究试图检测SK-N-AS和H4这2种细胞上清液中T3、T4和rT3含量,但由于体外表达和分泌量很低,检测结果非常不稳定,笔者课题组未来将在体内研究中探讨HBCD对脱碘酶以及T3、T4的毒理学效应。
另外,值得注意的是,本研究发现,HBCD对SK-N-AS中Dio3表达具有浓度效应,在低浓度下致Dio3表达略有下降,尽管未见统计学意义,而在高浓度下则致Dio3表达显著增高。Dio3是细胞表面受体,环境有机污染物在低浓度下对其RNA或蛋白表达影响不明显,但可能通过氧化应激、经由其他生物分子而改变Dio3结构和功能,从而影响局部甲状腺激素水平[25-27]。而在高浓度下,环境有机毒物可能通过甲基化或microRNA调控Dio3表达,影响局部组织甲状腺激素水平,从而可能引起神经系统损伤[28]。
神经营养因子如脑源性神经营养因子(BDNF)在TH介导的脑发育中起关键作用[29]。在脑发育中,BDNF广泛涉及神经元增殖和分化[30],特别是BDNF促进神经突迁移和伸长[31]。此外,小鼠BDNF基因缺失显示的脑发育异常类似于甲状腺功能减退的动物[32]。BDNF表达在甲状腺机能减退的小鼠中也受到抑制[33]。Ibhazehiebo等[34]报道BDNF能缓解HBCD引起的甲状腺激素诱导的颗粒细胞轴突延长抑制。因此,本研究初步探讨HBCD对H4细胞BDNF分泌的影响,结果显示,HBCD可以降低H4细胞BDNF的分泌,而BDNF降低,很可能加剧HBCD对神经元的损伤,或阻碍神经元的修复和再生过程。笔者课题组今后将在SK-N-AS和H4这2种细胞共培养体系以及在体内研究中,进一步探讨BDNF和其他生长因子在HBCD神经毒性中的作用。
综上,本研究结果表明,HBCD暴露可能通过影响胚胎脑局部脱碘酶表达、调控局部甲状腺激素水平,影响BDNF的分泌,导致子代神经发育异常。下一步将进行动物实验,研究孕期HBCD暴露对胚胎脑局部脱碘酶表达的影响及甲状腺激素水平的调控,以阐明HBCD引起子代神经发育毒性的机制。
