例说培养学生新情境下氧化还原反应方程式的书写思路
2019-09-11熊心强
熊心强
(成都高新三岔中学,四川 成都 641418)
化学是一门以化学方程式为载体的自然学科,通过学习化学方程式来掌握物质的结构及其性质,反过来知道物质的结构和性质以及物质间反应的现象,我们可以推断出物质之间反应的化学方程式。要学会新情境下氧化还原反应方程式的书写思路,我们可以先依次学会化学方程式的配平、氧化还原反应方程式的配平、缺项氧化还原反应方程式的配平,在学会在特定化学环境下判断出反应物和生成物、写出部分反应物和部分生成物、利用物质的性质现象判断出其余的反应物和生成物、利用氧化还原反应方程式的特征将其配平。
一、化学方程式的配平
(一)利用原子守恒配平
【典例分析】 配平下列化学方程式
【针对练习1】配平下列化学方程式
(二)利用化合价升降相等和原子守恒相结合给氧化还原反应方程式配平
【典例分析】配平下列化学方程式
【针对练习2】配平下列化学方程式
(三)利用化合价升降相等和原子守恒以及电荷守恒相结合给氧化还原反应缺项离子方程式配平
配平步骤
【典例分析】配平下列化学方程式
【针对练习3】
二、新情境下方程式的书写
常见氧化剂、还原剂在各自条件下分别对应的还原产物和氧化产物
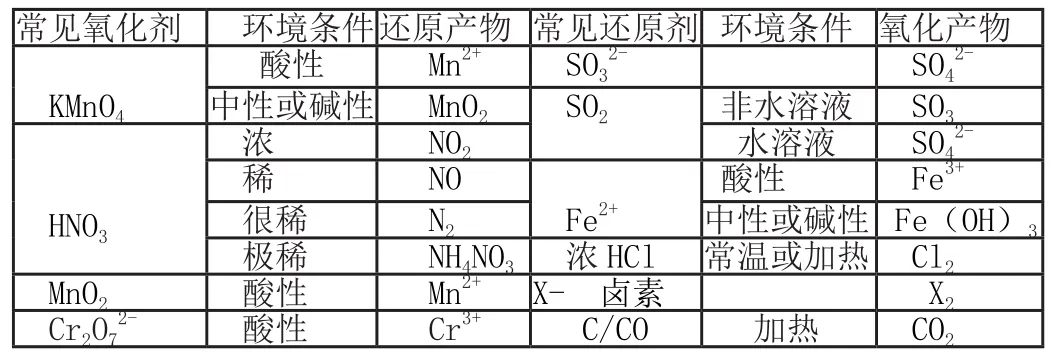
常见氧化剂 环境条件还原产物 常见还原剂 环境条件 氧化产物KMnO4酸性 Mn2+ SO32- SO42-中性或碱性 MnO2 SO2 非水溶液 SO3 HNO3浓 NO2 水溶液 SO42-稀 NO Fe2+酸性 Fe3+很稀 N2 中性或碱性 Fe(OH)3极稀 NH4NO3 浓HCl 常温或加热 Cl2 MnO2 酸性 Mn2+ X- 卤素 X2 Cr2O7 2- 酸性 Cr3+ C/CO 加热 CO2

碱性 H2O Na2O2 OH- 中性或酸性 H+Fe3+ 酸性 Fe2+ Fe 弱氧化剂 Fe2+X2 卤素 X- 强氧化剂 Fe3+HClO或ClO- Cl-H+ H2 H2O2 酸性 H2O NH3 加热 N2或 NO中性或碱性H2O或OH- H2C2O4 酸性 CO2浓H2SO4 加热 SO2 H2
【典例分析】
(1) 向FeSO4和硫酸混合溶液中加入NaClO溶液,反应的离子方程式为:
(2) 向FeSO4溶液中加入NaClO溶液,反应的离子方程式为:
(3) 向NaClO和NaOH溶液中滴入FeSO4溶液,反应的离子方程式为:
【考点练习】
(2017年新课标1卷27).(4)+6价铬的化合物毒性较大,常用NaHSO3将废液中的Cr2O72-还原成Cr3+,反应的离子方程式为。
三、结束语
新情境下氧化还原反应方程式的书写是考查学生的化学综合能力,要提升学生的这种综合的能力,必须抓好氧化还原反应方程式配平和缺项氧化还原反应方程式配平的基础,学生还应对常见物质结构及其性质的掌握要牢固。
