98例格林巴利综合征患者寡克隆区带电泳分析
2019-09-10王利娟陈柯霖李斯文谷愉愉刘淑静康熙雄张国军
王利娟,刘 杰,陈柯霖,李斯文,谷愉愉,刘淑静,周 金,康熙雄,张国军△
(1.首都医科大学附属北京天坛医院检验科,北京 100070;2.北京市免疫试剂临床工程技术研究中心,北京 100070)
格林巴利综合征(GBS)是一种周围神经炎性脱髓鞘疾病,病因尚未阐明,目前普遍认为它是由病原微生物先驱感染而诱发的自身免疫性脱髓鞘性疾病[1-2],由于髓鞘脱失体内形成抗原,激活B淋巴细胞和浆细胞,导致克隆株浆细胞异常增生,合成的免疫球蛋白在电泳时形成几条比较狭窄且不均匀的不连续条带,即寡克隆区带[3],仅在脑脊液中存在特异性寡克隆区带,提示中枢神经系统内存在体液免疫反应,是判定鞘内IgG合成的定性指标[4-5]。目前普遍认为寡克隆区带电泳是多发性硬化的可靠诊断指标,而关于其在GBS中的特点及诊断意义研究较少,本研究总结了近些年来首都医科大学附属北京天坛医院住院确诊的GBS患者寡克隆区带电泳结果,旨在探讨寡克隆区带电泳在GBS中的分布特点及诊断意义。
1 资料与方法
1.1一般资料 根据美国国家神经学疾病与中风研究院1990年修订的GBS诊断标准[6],纳入2013-2019年于首都医科大学附属北京天坛医院就诊的98例GBS患者,并收集血清和脑脊液,其中患者男65例,女33例; ≤50岁56例,>50岁42例;按病程分为急性组68例,慢性组30例。
GBS急慢性判断标准[7]:急性GBS病程达到峰值的时间常<2周(不超过4周),单向性病程;慢性GBS病程达到峰值通常在8周以上,进行性、波动性病程,通过临床表现、脑脊液蛋白及常规电生理检查综合判断。
1.2仪器与试剂 法国Sebia HYDRASYS蛋白电泳仪以及其配套试剂。
1.3方法 收集患者肘静脉血5 mL,通过离心分离血清标本,同时行常规腰椎穿刺,留取脑脊液2 mL,离心后取上清液进行实验。使用法国Sebia Hydrasys蛋白电泳仪,通过琼脂糖凝胶等电聚焦电泳检测寡克隆区带,判断标准为出现2条或2条以上分开的、较狭窄、不均一、不连续的条带即为阳性,其中OB(CSF)+代表脑脊液中阳性条带,OB(S)+代表血清中阳性条带,SOB(CSF)+代表仅见于脑脊液而未见血清中的条带,提示有鞘内合成;临床常见结果组合有4种类型,见表1。

表1 寡克隆区带电泳临床常见结果组合
注:+表示阳性;-表示阴性
1.4统计学处理 采用SPSS20.0统计软件进行数据分析,计数资料以[n(%)]表示,采用χ2检验,以P<0.05表示差异有统计学意义。
2 结 果
2.1GBS患者寡克隆区带电泳检测结果 OB(CSF)阳性37例(37.8%),OB(S)阳性33例(33.7%),二者阳性率接近,而SOB(CSF)及全阳的阳性率较低,其中SOB(CSF)阳性7例(7.1%),全阳阳性3例(3.1%)。98例GBS患者寡克隆区带电泳结果见表2。

表2 98例GBS患者寡克隆区带电泳检测结果
注:全阳表示OB(CSF)、OB(CSF)、SOB(CSF)三者均可见阳性条带
2.2不同性别GBS患者寡克隆区带电泳检测结果 男性患者OB(CSF)、OB(S)、SOB(CSF)、全阳的阳性率分别为40.0%、35.4%、2.7%、1.5%,女患者OB(CSF)、OB(S)、SOB(CSF)、全阳的阳性率分别为3.3%、30.3%、9.1%、6.1%,男女性别以上指标比较,差异均无统计学意义(P>0.05)。见表3。
2.3GBS患者急慢性组间寡克隆区带电泳结果比较 急性患者OB(CSF)、OB(S)、SOB(CSF)、全阳的阳性率分别为35.3%、32.4%、5.9%、2.9%,慢性患者OB(CSF)、OB(S)、SOB(CSF)、全阳的阳性率分别为43.3%、36.7%、10.0%、3.3%,急性患者以上指标比较,差异均无统计学意义(P>0.05)。 见表4。

表3 不同性别GBS患者寡克隆区带电泳检测结果比较[n(%)]
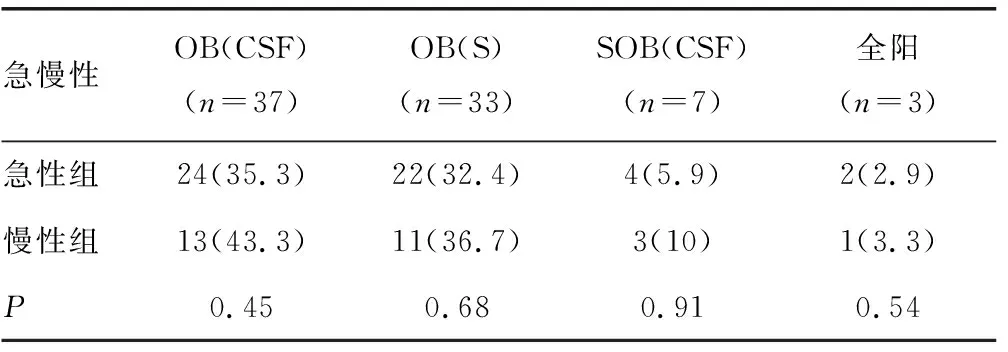
表4 急慢性组间寡克隆区带电泳检测结果比较[n(%)]
2.4不同年龄GBS患者寡克隆区带电泳检测结果 不同年龄段OB(CSF)、OB(S)阳性率趋势基本一致,随着年龄的增长呈上升趋势,而SOB(CSF)、全阳两组呈波动性。按照年龄≤50及>50分为2组,>50岁年龄组OB(CSF)、OB(S)的阳性率(52.4%、50.0%)明显高于≤50岁年龄组(26.8%、21.4%),差异有统计学意义(P<0.05)。见表5、图1。

表5 不同年龄患者寡克隆区带电泳检测结果比较[n(%)]

图1 不同年龄GBS患者寡克隆区带电泳检测结果
3 讨 论
1942年有研究者首先用电泳法发现多发性硬化患者脑脊液球蛋白增加,并于1971年证实为寡克隆区带[8]。目前公认脑脊液中特异性寡克隆IgG区带是诊断多发性硬化的常规检查[9-10],并于2010修订版McDonald多发性硬化诊断标准中作为重要的实验室附加依据[11]。寡克隆区带作为多发性硬化常见的免疫学异常表现,是影像学检查不可代替的辅助检查,并可以协助判断多发性硬化的严重程度、疾病进程及是否处于活动期。而目前关于寡克隆区带在GBS中的分布特点及诊断价值研究较少。刘业松等[12]、于素贞等[13]、张旭等[14]、李义召等[15]研究提示,GBS组寡克隆区带的阳性率分别为76.7%、57%、38.9%、70.0%,显著高于对照组,且在中枢神经系统内有免疫球蛋白的异常合成,存在免疫功能异常。
本研究回顾性分析了2013-2019年98例确诊为GBS患者的寡克隆区带电泳阳性情况,并从不同方面进行分组比较。GBS中脑脊液寡克隆区带阳性率为37.8%,与以往的文献报道基本一致,部分的差别可能是由于检测方法的灵敏度不同引起。本研究分别对OB(CSF)、OB(S)、SOB(CSF)及三者全阳结果从不同性别、年龄、急慢性间进行统计分析,结果显示性别、急慢性间差异无统计学意义;>50年龄组OB(CSF)、OB(S)的阳性率(52.4%、50.0%)明显高于≤50年龄组(26.8%、21.4%),差异有统计学意义;而SOB(CSF)及全阳在不同年龄间差异无统计学意义,提示>50年龄组OB(CSF)阳性率高的原因是由于血清中蛋白的渗透,并不全是鞘内合成,可能是由于老年人的血脑屏蔽功能较年轻人较差[16]。
4 结 论
GBS患者中枢神经系统内有免疫球蛋白的异常合成,且存在免疫功能异常,对GBS的辅助诊断有一定意义。GBS患者>50岁年龄组脑脊液及血清寡克隆区带阳性率高,而脑脊液中特异性寡克隆区带的阳性率较低,提示>50岁年龄组脑脊液寡克隆区带阳性部分是由于血清中的蛋白渗透,并不全是鞘内合成,可能与老年人的血脑屏蔽功能较年轻人较差有一定关系。因此,临床诊断应考虑年龄造成的影响。
