牛蒡子标准汤剂质量评价体系的建立
2019-09-10张肖建张岩岩高晗孙福仁李军山李振江
张肖建 张岩岩 高晗 孙福仁 李军山 李振江





摘要:為了提高牛蒡子标准汤剂的质量标准,制备了15批牛蒡子标准汤剂,通过对牛蒡苷含量及指纹图谱的研究,建立了牛蒡子标准汤剂的质量评价体系。第一煎加入8倍水,浸泡30 min,煎煮20 min;第二煎加入6倍水,煎煮15 min,经浓缩、干燥后制得标准汤剂,应用HPLC法测定牛蒡子标准汤剂中牛蒡苷的含量及指纹图谱。结果显示:15 批牛蒡子标准汤剂中牛蒡苷的转移率为21.3%~33.3%,平均转移率为27.3%,出膏率为7.1%~11.3%,平均出膏率为9.4%;通过中药指纹图谱相似度评价系统,确定了11 个共有峰,通过对照品指认出了5个色谱峰,分别为绿原酸、咖啡酸、3,5-O-二咖啡酰基奎宁酸、牛蒡苷、牛蒡苷元。所建立的评价体系,牛蒡子标准汤剂制备规范,样品质量稳定,指纹图谱相似度大于0.94,对提高牛蒡子配方颗粒的质量标准具有一定的参考价值。
关键词:医药工程;牛蒡子;标准汤剂;牛蒡苷;出膏率;指纹图谱
中图分类号:R284.1 文献标志码:A doi: 10.7535/hbgykj.2019yx01009
ZHANG Xiaojian,ZHANG Yanyan,GAO Han,et al.Establishment of quality evaluation system for standard decoction of Arctii fructus[J].Hebei Journal of Industrial Science and Technology,2019,36(1):47-52.Establishment of quality evaluation system for
standard decoction of Arctii fructus
ZHANG Xiaojian1, ZHANG Yanyan1, GAO Han1, SUN Furen1, LI Junshan1,2, LI Zhenjiang1
(1.Shineway Pharmaceutical Group Limited,Shijiazhuang, Hebei 051430, China;2.TCM Formula Granule Engineering Technology Research Center of Hebei, Shijiazhuang, Hebei 050091, China)
Abstract:In order to improve the quality standard of standard decoction of Arctii fructus, 15 batches of Arctii fructus standard decoction is prepared. The quality evaluation system of Arctii fructus standard decoction is established by studying the content of Arctii fructus glycoside and its fingerprint. Firstly, 8 times of water is added, then soaking for 30 minutes and frying for 20 minutes. Secondly, 6 times of water is added, then frying for 15 minutes. The standard decoction of Arctii fructus is prepared by using standardization method of concentration and drying, and the content of Arctiin and the fingerprint in the standard decoction are determined by HPLC. The results show that the transfer rate of Arctiin in the 15 batches of standard decoction is 21.3%~33.3%,and the average transfer rate is 27.3%. The extractum is 7.1%~11.3%, and the average ointment rate is 9.4%. The fingerprints are determined by similarity evaluation system of Chinese herbal medicine fingerprints. Five of the 11 common peaks representing chlorogenic acid, caffeic acid, 3,5-O-dicaffeoylquinic acid, arctiin and arctigenin are identified. In this study, preparation of Arctii fructus standard decoction meets the specifications, sample quality is stable, and fingerprint similarity is greater than 0.94. It has certain reference value for improving the quality standard of Arctii fructus formula granules.
Keywords:pharmaceutical engineering; Arctii fructus; standard decoction; arctiin; ointment rate; fingerprint
牛蒡子始载于《本草图经》,为菊科牛蒡Arctium lappa L.的干燥成熟果实[1],性寒,味苦,归肺、胃经,具有疏风散热、利咽解毒、宣肺透疹的功效。其在中国广泛分布,主产于东北、华北、西南地区,目前在重庆的潼南、西阳、江津等地均有大面积的种植基地。甘肃是牛蒡子的主产地,产量占全国的50%~60%[2-3]。近年来,科研人员关于牛蒡子化学活性成分方面的研究取得了重要进展,许多重要的药理和生理活性被发现,如抗衰老活性、抗肿瘤活性、降血压、降血糖,以及对急慢性肾炎等方面的作用。
第1期张肖建,等:牛蒡子标准汤剂质量评价体系的建立河北工业科技第36卷中药配方颗粒是由现代工艺制备的供临床配伍使用的颗粒,近几年产量增长迅速。目前,牛蒡子配方颗粒没有统一的质量标准,相关报道也较少。笔者依照《中药配方颗粒管理办法》(征求意见稿)和《中药配方颗粒质量控制与标准制定要求》(征求意见稿),收集了几个不同产地的牛蒡子药材,通過制备标准汤剂及建立检测方法,测定了牛蒡子标准汤剂中牛蒡苷的含量并计算了转移率,同时,对15批牛蒡子标准汤剂进行了HPLC指纹图谱的研究,以期为牛蒡子配方颗粒的质量控制提供依据[4-6]。
1材料
1.1主要仪器
Shunliu-12N型冷冻干燥机,南京顺流仪器有限公司提供;DHG-9140A型热风循环鼓风干燥箱,上海精宏实验设备有限公司、太仓精宏仪器设备有限公司提供;LC-20A高效液相色谱仪,岛津仪器设备有限公司提供;Agilent Zorbax Eclipes C18色谱柱(250 mm×4.6 mm 5 μm);AE 240 型电子分析天平,瑞士Mettler-Toledo公司提供;KH-3200 E超声波清洗器,江苏昆山禾创超声仪器有限公司提供。
1.2试药
牛蒡苷标准品(批号为110819-201812),绿原酸标准品(批号为110753-201716),3,5-O-二咖啡酰基奎宁酸标准品(批号为111782-201706),咖啡酸标准品(批号为110885-201703),均购自中国食品药品检定研究院;牛蒡苷元标准品(批号为HA010075198),购自宝鸡市辰光生物科技有限公司;甲醇、乙腈,色谱纯;其他试剂均为分析纯。
1.3样品
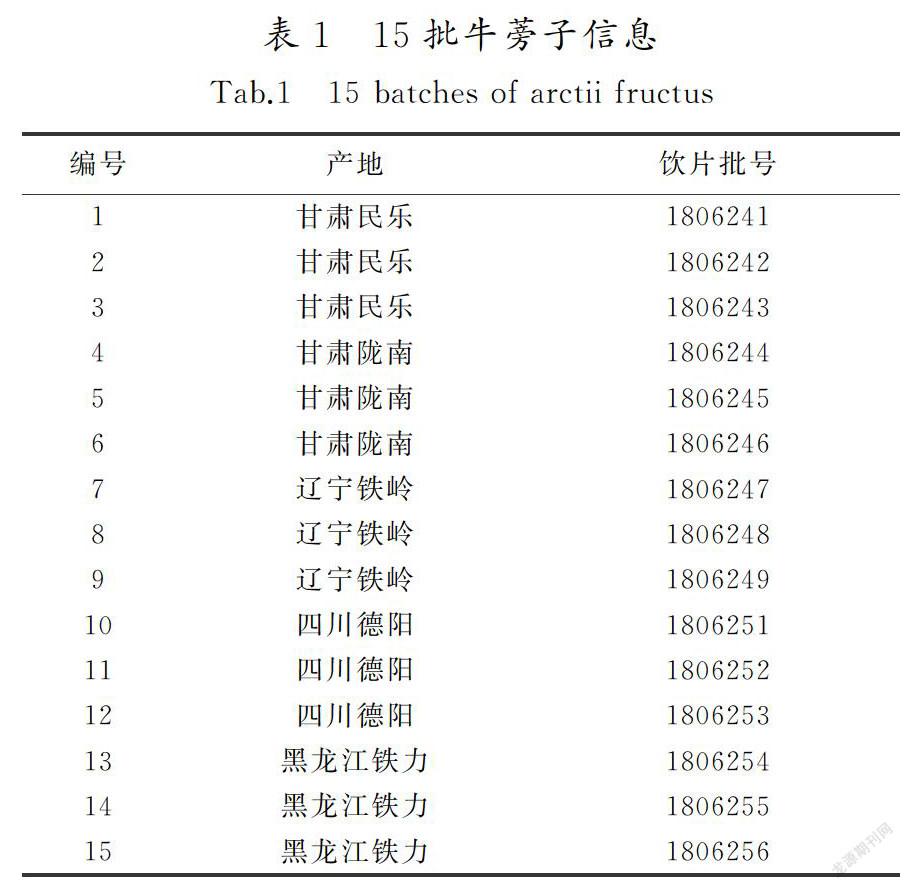
采集了5个产地的15批牛蒡子药材,按2015年版《中华人民共和国药典》规定制成饮片,具体来源见表1。
2方法与结果
2.1牛蒡子标准汤剂的制备
称取饮片100 g,加水煎煮2次。第一煎加水800 mL,浸泡30 min,沸腾后煎煮20 min;第二煎加水600 mL,沸腾后煎煮15 min。合并煎液,用48 μm(300目)筛网趁热过滤。将滤液迅速冷却,用旋转蒸发器(65 ℃,-0. 09 MPa)浓缩至适当相对密度的流浸膏,经冷冻干燥,制备成标准汤剂干燥粉末[7-10]。
2.2牛蒡子及标准汤剂中牛蒡苷含量的测定
2.2.1色谱条件
色谱柱为Agilent Zorbax Eclipes C18(250 mm×4.6 mm,5 μm),流动相为甲醇-水(二者体积比为40∶60),检测波长为280 nm。按牛蒡苷峰计算,理论塔板数不低于1 500。
2.2.2参照物溶液的制备
取牛蒡苷参照物,精密称定,加甲醇溶解,制成每1 mL含0.5 mg的参照物溶液,即得。
2.2.3供试品溶液的制备
1)牛蒡子饮片供试品溶液取牛蒡子饮片粉末(过3号筛),精密称定0.5 g,置于50 mL容量瓶中,加入甲醇约45 mL,超声(功率150 W,频率20 kHz)20 min,放冷,加甲醇至刻度,摇匀,过滤,取续滤液,即得。
2)牛蒡子标准汤剂供试品溶液取牛蒡子标准汤剂干膏粉,研细,精密称定0.2 g,置于具塞锥形瓶中,精密加入50 mL甲醇,密塞,称重,超声提取20 min(功率为150 W,频率为20 kHz)后,室温放置,用甲醇补足失重,摇匀,过滤,取续滤液,即得[11-14]。
2.2.4线性关系考察
精密称取牛蒡苷参照物62.51 mg,置于25 mL容量瓶中,加甲醇溶解定容至刻度,作为牛蒡苷参照物储备液。分别精密量取储备液0.5,1.0,2.0,5.0,10.0 mL,置于25 mL容量瓶中,用甲醇定容。分别精密吸取10 μL不同质量浓度的参照物溶液,注入高效液相色谱仪,测定相应峰面积。以参照物质量浓度X为横坐标,测定的峰面积Y为纵坐标,绘制标准曲线。结果表明:在0.048~2.393 μg/mL范围内,牛蒡苷线性关系良好,回归方程为Y=420 783X+15 251,r=0.999 9。
2.2.5精密度实验
取牛蒡子标准汤剂供试品溶液,连续进样6次,测定牛蒡苷的峰面积,计算药材中牛蒡苷的含量,测得样品中牛蒡苷峰面积的RSD值为0.30%,说明仪器精密、准确。
2.2.6稳定性实验
另取相同供试品溶液,分别在0,2,4,6,8,10 h时注入高效液相色谱仪中测定含量,计算药材中牛蒡苷色谱峰面积的RSD值为0.44%,说明供试品溶液在10 h内较稳定。
2.2.7重复性实验
取牛蒡子标准汤剂冻干粉样品,依照2.2.3方法制备6份,按上述色谱条件测定,计算样品中牛蒡苷含量。结果表明,6份样品中牛蒡苷含量的RSD值为0.79%,表明该方法的重复性良好。
2.2.8加样回收实验
分别称取含量已知的牛蒡子标准汤剂冻干粉6份,每份精密称定0.1 g。按样品含量的100%加入牛蒡苷参照物,按供试品溶液的制备方法进行制备,依照2.2.1项色谱条件测定,计算各样品的加样回收率,结果见表2。6份样品的加样回收率均在95%以上,RSD值为0.81%,表明供试品制备方法的回收率良好。
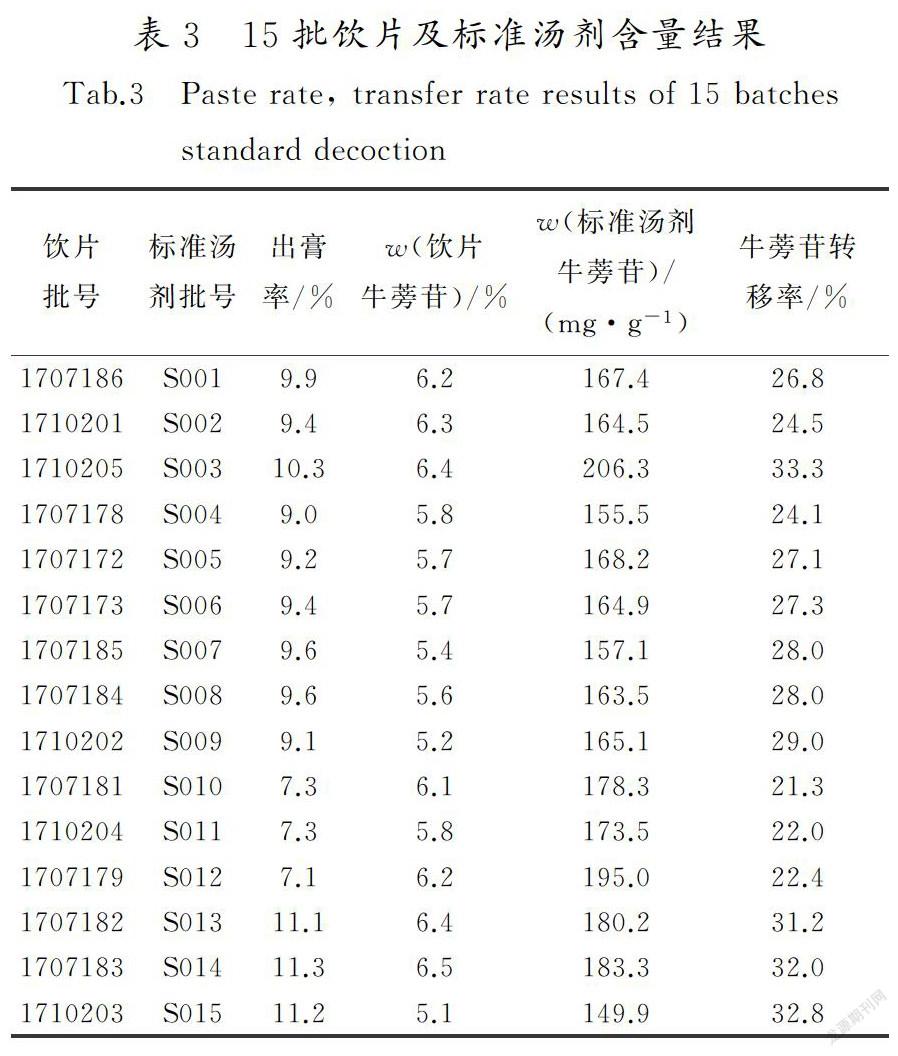
按照上述含量测定方法,测定15批牛蒡子饮片、牛蒡子标准汤剂的含量,结果见表3。
2.3出膏率及牛蒡苷含量转移率计算
根据冻干得到干膏粉量,计算各批牛蒡子标准汤剂的出膏率;根据膏粉和饮片中牛蒡苷含量,计算各批标准汤剂的含量转移率,结果见表3。
结果显示,15 批牛蒡子标准汤剂出膏率范围为7.1%~11.3%,出膏率平均值为9.4%,标准偏差为14.2%;牛蒡苷转移率为21.3%~33.3%,平均转移率为27.3%,标准偏差为14.3%。
3牛蒡子标准汤剂指纹图谱的测定
3.1色谱条件
色谱柱为Agilent C18 (250 mm×4.6 mm,5 μm),以乙腈(A)-0.2%(体积分数)磷酸水溶液(B)为流动相,进行梯度洗脱,检测波长为250 nm,流速为1.0 mL/min,柱温为30 ℃,进样量10 μL[14-16],流動相洗脱梯度条件见表4。
精密称定牛蒡苷、牛蒡苷元、绿原酸、3,5-O-二咖啡酰基奎宁酸、咖啡酸对照品,加甲醇制成每1 mL含0.50 mg牛蒡苷、0.10 mg牛蒡苷元、0.30 mg绿原酸、0.03 mg咖啡酸、0.07 mg 3,5-O-二咖啡酰基奎宁酸的混合对照品溶液,即得。
3.3供试品溶液的制备
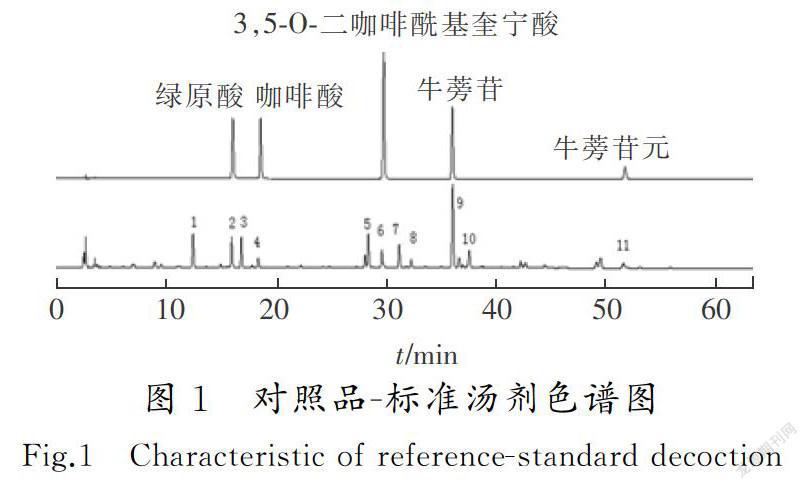
取牛蒡子冻干粉研细,精密称定0.2 g,置于具塞锥形瓶中,精密量取甲醇25 mL,加入锥形瓶中,称重,超声处理30 min(250 W,40 kHz)。取出,室温放置,称重,用甲醇补足减失的质量,摇匀,过滤(过0.45 μm膜),取续滤液,即得。色谱图见图1。
3.4方法学考察
3.4.1精密度考察
取同一供试品溶液,连续进样6次,以牛蒡苷峰为参比峰,计算其他主要色谱峰的相对保留时间(RRT)及相对峰面积(RPA)。结果显示,RRT的RSD值为0.41%,RPA的RSD值为1.3%,相似度为l.00,说明仪器的精密度良好。
3.4.2稳定性考察
精密吸取同一供试品溶液,按3.1项色谱条件,分别在0,2,4,6,8,10 h时进行测定,记录色谱图。以牛蒡苷为参比峰,计算其他各共有峰的相对保留时间和相对峰面积。结果显示,RRT的RSD值为0.21%,RPA的RSD值为3.1%,相似度为1.00。说明在10 h内,供试品溶液稳定。
3.4.3重复性考察
取标准汤剂冻干粉样品,制备6份,按3.1项色谱条件测定,记录色谱图。以牛蒡苷为参比峰,计算其他各主要色谱峰的RRT及RPA。结果显示,RRT的RSD值为0.42%,RPA的RSD值为1.9%,相似度为1.00,说明该方法的重复性良好。
3.5样品检测与分析
取15批牛蒡子标准汤剂粉末,根据3.3项所述方法制备供试品溶液,依照3.1项色谱条件进行测定,记录样品色谱图。将得到的15批供试品色谱图导入中药色谱指纹图谱相似度评价系统软件(2012版)中,通过对各样品中色谱峰的匹配,生成15批牛蒡子标准汤剂的对照图谱,确定牛蒡子标准汤剂11个共有峰,见图2。其中,以牛蒡苷峰为参照峰,计算11个共有色谱峰的相对峰面积及相对保留时间,见表5和表6。经计算,15批牛蒡子标准汤剂相似度均在0.94以上,见表7。
4讨论
1)牛蒡苷作为牛蒡子饮片的指标成分,是评价牛蒡子饮片质量的重要指标。牛蒡子标准汤剂由牛蒡子饮片经提取、浓缩、干燥而制成,其质量评价应以牛蒡苷为指标成分。结果显示,15批牛蒡子标准汤剂中牛蒡苷含量的转移率为21.3%~33.3%。
2)通过实验考察了3种溶液(乙腈-0.1%磷酸水溶液、乙腈-水、乙腈-0.2%磷酸水溶液)、3个流速(0.8,1.0,1.2 mL/min)、3个柱温条件(25,30,35 ℃)对反应的影响。结果显示,在乙腈-0.1%磷酸水溶液、1.0 mL/min及25 ℃柱温条件下所得到的指纹图谱基线稳定、分离度较好,可选用该条件作为牛蒡子标准汤剂指纹图谱检测的最优条件。应用中药指纹图谱相似度评价软件检测可知,15批牛蒡子标准汤剂冻干粉的相似度均大于0.94。
3)中药标准汤剂对于研究配方颗粒具有重要的指导作用,本文根据《中药配方颗粒质量控制与标准制定要求》(征求意见稿),制备了15批牛蒡子标准汤剂,通过对牛蒡苷含量及指纹图谱的研究,建立了牛蒡子标准汤剂的质量标准,对提高牛蒡子配方颗粒的质量标准具有一定的参考价值。有关牛蒡子饮片、标准汤剂、配方颗粒三者之间各成分的变化规律,以及各成分变化所引起的药理作用还需今后作进一步的研究。
参考文献/References:
[1]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2015.
[2]徐国钧.中国药材学[M].北京:中国医药科技出版社,1996.
[3]南京中医药大学.中药大辞典[M].上海:上海科学技术出版社,2006.
[4]毕葳,雷海民,何远景,等.不同产地牛蒡子药材质量评价[J].中国中医药信息杂志,2005,12(4):47-48.
BI Wei,LEI Haimin,HE Yuanjing, et al. Quality evaluation of Arctium lappa in various market[J]. Chinese Journal of Information on Traditional Chinese Medicine,2005,12(4):47-48.
[5]MARUTA Y, KAWABATA J. Antioxidative caffeoylquinic acid derivatives in the roots of burdock (Arctium lappa L.) [J]. J Agric Food Chem, 1995,43(10):2592-2595.
[6]刘启迪.牛蒡子炮制工艺及质量标准研究[D].南京:南京中医药大学,2014.
LIU Qidi.Study on Processing Technology and Quality Standards of Arctii Fructus[D].Nanjing:Nanjing University of Chinese Medicine,2014.
[7]李军山,聂丽建,冀艳花,等.白鲜皮饮片标准汤剂质量评价体系构建[J].河北工业科技,2018,35(5):370-376.
LI Junshan,NIE Lijian,JI Yanhua, et al.Establishment of quality evaluation system of standard decoction of Dictamni Cortex pieces[J].Hebei Journal of Industrial Science and Technology, 2018,35(5): 370-376.
[8]陳士林,刘安,朱广伟,等.中药饮片标准汤剂研究策略[J].中国中药杂志,2016,41(8):1367-1375.
CHEN Shilin,LIU An, ZHU Guangwei, et al.Research strategies in standard decoction of medicinal slices[J]. Chinese Journal of Traditional Chinese Medicine, 2016,41(8):1367-1375.
[9]朱广伟,李西文,陈士林.白芍饮片标准汤剂质量标准研究[J].世界中医药,2016,11(5):753-757.
ZHU Guangwei,LI Xiwen,CHEN Shilin. Quality standard research on standard decoction of paeonialactiflora[J]. World Chinese Medicine, 2016,11(5):753-757.
[10]林伟雄,乐智勇,车海燕,等.甘草饮片标准汤剂的研究[J].中国中药杂志,2017,42(3):6-11.
LIN Weixiong,LE Zhiyong,CHE Haiyan, et al.Research on Glycyrrhizeae Radix standard decoction[J]. Chinese Journal of Traditional Chinese Medicine, 2017,42(3):6-11.
[11]LIU H,ZHANG Y,SUN Y,et al. Determination of the major constituents in fruit of Arctium lappa L. by matrix solid-phase dispersion extraction coupled with HPLC separation and fluorescence detection[J]. J Chromatogr B, 2010, 878(28): 2707-2711.
[12]杨申明,王振吉,徐成东,等.重齿鳞毛蕨中总黄酮的含量测定[J].河北工业科技,2014,31(1):48-52.
YANG Shenming,WANG Zhenji,XU Chengdong, et al.Content determination of total flavonoids in Dryopteris juxtaposita[J].Hebei Journal of Industrial Science and Technology,2014,31(1):48-52.
[13]姚小丽,郝亮,陈秀红.熊果苷及其中间体的含量测定[J].河北工业科技,2012,29(4):228-231.
YAO Xiaoli,HAO Liang,CHEN Xiuhong.Content determination of arbutin and its intermediate[J]. Hebei Journal of Industrial Science and Technology,2012,29(4):228-231.
[14]TENG H, CHOI Y H. Optimization of ultrasonic-assisted extraction of bioactive alkaloid compounds from rhizome coptidis (Coptis Chinensis Franch.) using response surface methodology[J].Food Chem,2014,142:299-305.
[15]张肖建,霍保军,李军山,等.葛根水煎剂和配方颗粒HPLC指纹图谱相关性研究[J].河北工业科技,2018,35(3):226-230.
ZHANG Xiaojian, HUO Baojun, LI Junshan , et al.Correlation of fingerprint of puerariae water decoction and formula granules by HPLC [J].Hebei Journal of Industrial Science and Technology, 2018,35(3): 226-230.
[16]宾婕, 施建莲, 胡珊珊,等.不同产地牛蒡子的指纹图谱研究[J]. 药物资讯, 2017, 6(5): 121-126.
BIN Jie,SHI Jianlian,HU Shanshan,et al.Identification of Arctium lappa L. from different cultivation places by HPLC fingerprint[J]. Pharmacy Information, 2017, 6(5): 121-126.第36卷第1期河北工业科技Vol.36,No.1
