结肠癌及其分型的靶分子修饰递送药物的研究进展
2019-09-10杨波张艳君彭海生郑沛育
杨波 张艳君 彭海生 郑沛育
摘 要 目的:为结肠癌靶向治疗药物的研发提供参考。方法:以“结肠癌”“靶分子”“分型”“靶向机制”“修饰递送药物”“Colon cancer”“Target molecule”“Typing”“Targeting mechanism”“Modified delivery drug”等为关键词,在中国知网、万方数据、PubMed等数据库中组合检索2001年7月-2018年6月发表的相关文献,筛选出能够准确靶向至结肠癌细胞的靶分子,并针对不同类型的结肠癌患者的靶向药物及其靶向特征的研究进展进行综述。结果与结论:共检索到相关文献255篇,其中有效文献54篇。目前,国内外学者研究和应用较多的结肠癌靶分子包括透明质酸、叶酸、小麦胚芽凝集素、核酸适配体、Affibody分子、单克隆抗体、多肽、microRNA等。为了能够更加精准地对结肠癌进行靶向,可以运用逆转录定量聚合酶链反应或者免疫组化法分析候选的生物标志物,将结肠癌分为杯状型、肠上皮细胞型、干细胞型、炎症型以及过渡扩增型CS-TA、CR-TA等6种类型,在研究结肠癌靶向药物时根据结肠癌不同分型选择其靶点及靶分子进行研发。目前,临床上已出现的靶向药物仍然因为对不同的结肠癌患者缺乏选择性使其应用受到限制。虽然可将结肠癌患者分型并据此给予不同的靶向药能够达到事半功倍的效果,但是目前这个分型方法还没有应用到临床上,并且此分型方法也由于样本量的限制,还不够完善。因此,关于结肠癌的分型以及针对不同分型的靶向药物还有必要继续深入研究。
关键词 结肠癌;靶分子;分型;靶向机制;靶向特征;结肠癌
结肠癌在全球女性中的发病率高居第2位,在男性中居于第3位。结肠癌在西方国家中的发病率更高,在我国的发病率也在逐年提高[1]。有证据表明,结肠癌是由于饮食问题引起了肠道菌群紊乱,进而导致致癌基因和抑癌基因的改变,并最终导致结肠黏膜上皮发生恶性病变[2]。结肠癌按Dukes’分期可分为A、B、C、D期,一般因初期症状不明显,确诊时患者通常已经到了中晚期。尽管结肠癌患者可以进行局部结肠切除手术,但仍有25%~40%的B~C期患者会复发,因此结肠癌患者常需在术后进行辅助化疗[3]。然而采用常规化疗药物时,常因药物对于结肠癌部位的选择性不足而导致一系列的不良反应(ADR),如中性粒细胞减少、贫血、腹泻、胃肠道毒性、黏膜炎、恶心呕吐、血液系统疾病和肝脏毒性等,从而降低患者的治疗依从性,严重影响其生存质量和生存期[4]。
近年来,国内外学者为了避免抗肿瘤藥物靶向性不佳导致的正常细胞损伤,提高药物靶向至肿瘤部位的准确度,对结肠癌靶向药物进行了大量的研究。结果发现,一些靶分子不仅能帮助药物准确靶向至结肠癌部位,还能用于结肠癌诊疗过程中的成像示踪等[5];而为了能够更加精准地对结肠癌进行靶向,可将结肠癌分为不同类型从而有针对性地进行精准靶向[6]。笔者以“结肠癌”“靶分子”“分型”“靶向机制”“修饰递送药物”“Colon cancer”“Target molecule”“Typing”“Targeting mechanism”“Modified delivery drug”等为关键词,在中国知网、万方数据、PubMed等数据库中组合检索2001年7月-2018年6月发表的相关文献。结果,共检索到相关文献255篇,其中有效文献54篇。本研究以此筛选出能够准确靶向至结肠癌肿瘤部位的靶分子,并针对用于不同类型的结肠癌患者的靶向药物及其靶向特征的研究进展进行综述,旨在为结肠癌靶向治疗药物的研发提供参考。
1 结肠癌靶分子
将靶分子通过制剂或者化学合成的方式连接在治疗结肠癌的药物上,可实现将化疗药物靶向至结肠癌细胞的效果。因此,目前对于结肠癌靶向药物的研究主要集中在可以与结肠癌细胞上的受体特异性结合的靶分子上。研发过程中选择能够准确靶向至细胞的靶分子是至关重要的,目前应用较多的靶分子包括透明质酸(HA)、叶酸(FA)、小麦胚芽凝集素(WGA)、核酸适配体、亲和体(Affibody)分子、单克隆抗体、多肽、微RNA(microRNA)等。
1.1 HA
HA是细胞外基质的主要成分,为非硫酸化、无支链的糖胺聚糖,由重复的二糖单元D-葡萄糖醛酸和N-乙酰基-D-葡糖胺组成[7]。HA能特异性地识别结肠癌细胞上过表达的CD44受体(CD44是一种多结构、多功能的细胞表面分子,多存在于结肠癌细胞上,在结肠癌的发展和转移中发挥重要作用[8]),而CD44在结肠癌细胞外结构域上有HA结合位点,因此可作为HA的主要细胞表面受体[9]。目前,有很多研究人员将HA修饰在纳米粒上,从而靶向至结肠癌中过表达的CD44受体,进一步靶向性治疗结肠癌。例如,Zhu C等[10]运用HA与生育酚琥珀酸(TOS)通过二硫键连接制成智能纳米胶束,可以准确地将紫杉醇靶向至CD44受体,抑制原位结肠癌及转移的肿瘤细胞的生长;Liu K等[11]制备了负载有5-氟尿嘧啶(5-FU)缀合HA的二氧化硅纳米粒以靶向至结肠癌细胞,通过CD44介导的内吞作用使5-FU的吸收增多,使得抗肿瘤效力显著增强。HA除了具有CD44受体介导的结肠靶向特性之外,还可以特异性地识别透明质酸酶(HAase)。Zhang M等[12]使用了负载盐酸多柔比星的介孔二氧化硅纳米粒(MSN)来靶向至HAase,在将脱硫生物素植入MSN表面后,制成了链霉抗生素蛋白复合物,其中脱硫生物素可以和肿瘤组织中的标志物唾液酸特异性结合,而HA的修饰可使纳米粒在表达HAase的癌细胞中定位释放药物。
1.2 FA
FA由蝶啶、对氨基苯甲酸和L-谷氨酸组成,是B族维生素的一种,其可通过载体蛋白或在叶酸受体(FR)介导的内吞作用下进入细胞[13]。FR有两种膜结合亚型,分别为α型和β型,其中FR-α与肿瘤细胞的增殖、迁移和侵袭密切相关[14]。近年来,FR-α已成为潜在的癌症治疗靶点。白细胞介素12(IL-12)具有很强的抗肿瘤活性,但是由于具有严重的全身毒性,其临床使用受到了限制。Luo M等[15]制备了经FA修饰的包裹IL-12的脂质体,通过对该脂质体的体内外考察发现,该脂质体能够显著抑制肿瘤的生长,且原位结肠癌模型小鼠主要脏器的形态和功能仍完好,说明经过FA修饰,能够将IL-12靶向至结肠癌肿瘤区域,发挥其特异性抑制肿瘤生长的作用。
1.3 WGA
WGA是由两个相同亚基组成的蛋白质,分子量为36 kDa,其每个亚基都包含4个同源结构域[16]。WGA可以特异性地快速识别和结合结肠癌细胞上过表达的N-乙酰葡糖胺,通过受体介导的内吞作用导致细胞内化。Wang C等[17]将负载紫杉醇的聚乳酸-羟基乙酸共聚物(PLGA)纳米粒与WGA结合,结果,结合WGA的纳米粒具有更强的抗结肠癌细胞增殖活性,表明WGA可将药物靶向至结肠癌的肿瘤细胞。
1.4 核酸适配体
核酸适配体是一种能够特异性识别靶分子的短链或单链DNA[18],具有体积小、非免疫原性和毒性较小等优势[19]。目前针对结肠癌已开发出许多不同的核酸适配体。结肠癌细胞上皮黏附分子(EpCAM)是一种跨膜糖蛋白,可在多种癌症甚至癌症干细胞中过度表达,并与多种癌细胞增殖、迁移和侵袭有关[20]。Xie X 等[21]开发出了一种特异性识别EpCAM的核酸适配体,并将其修饰在MSN上,用于负载阿霉素以治疗结肠癌。这种纳米粒可以选择性地靶向至EpCAM,从而使药物集中在肿瘤部位。不同的核酸适配体可以靶向至结肠癌肿瘤的不同位置。5TR1适配体能够准确地靶向至黏蛋白(MUC)1糖型,并被癌细胞摄取[22-23];而MUC1是一种细胞表面相关糖蛋白,能够通过O-糖基化对其进行大量修饰,在多种上皮癌细胞(如乳腺癌、结肠癌等)中均存在异常表达的情况。基于此,用5TR1适配体偶联的超顺磁氧化铁纳米粒可通过准确地识别MUC1,从而靶向至结肠癌细胞,进而进行成像示踪[5]。
1.5 Affibody分子
Affibody分子是一类新的亲和配体,是由58个氨基酸残基组成,其相对分子量小,结构稳定性高,可以耐受化学修饰,不仅能特异性地结合细胞表面的Fc受体,而且具有很强的亲和力[24]。ZEGFR:1907是一个新开发的靶向至表皮生长因子受体(EGFR)的Affibody分子。EGFR是一种跨膜受体,具有细胞外配体结合位点和内部酪氨酸激酶结构域,通常在结肠癌细胞中呈过表达,且约60%~80%的结肠癌患者都存在EGFR表达或上调[25-26]。肿瘤中EGFR的表达与药物治疗和放疗的副作用有关,可能预示着预后不良[27]。有研究显示,ZEGFR:1907联合外部辐射可将药物靶向至结肠癌细胞,显著降低肿瘤细胞的存活率[28]。
1.6 单克隆抗体
单克隆抗体是由单一B细胞克隆产生的高度均一、仅针对某一特定抗原表位的抗體,因其可以靶向至特定抗原而受到广泛的应用。如小鼠单克隆抗体17.1A可以特异性地识别结肠癌上皮细胞抗原EpCAM。有研究运用17.1A与光敏剂二氢卟吩e6制备光敏免疫偶联物,该偶联物可以识别结肠癌细胞上的特异性靶点,准确发挥光敏剂对肿瘤细胞的杀伤作用[29]。利用单克隆抗体还可以制备免疫脂质体(即通过表面连接单克隆抗体而起到靶向作用的脂质体)。Koning GA等[30]将抗癌药物氟尿脱氧核苷包裹在脂质体中,并在脂质体表面偶联上与结肠癌细胞CC531特异性结合的单克隆抗体,结果发现这种免疫脂质体对CC531具有很强的抑制作用。Cho YS等[31]合成了二氧化硅涂层和有机染料结合的氧化铁纳米粒(MFSN),通过检测细胞和组织中的荧光物质,并运用磁共振表征磁性,实现了成像示踪。为了提高示踪的准确性,将能够特异性靶向至结肠癌细胞EGFR的西妥昔单抗(西妥昔单抗是一种嵌合型免疫球蛋白G1单克隆抗体,可靶向至EGFR细胞外结构域,并可高亲和力结合EGFR,竞争性抑制EGFR与配体结合,抑制EGFR活化[32])连接在纳米粒上,结果显示,MFSN能够被多种细胞摄取,且有效地靶向至肿瘤细胞,可通过成像示踪和定量检测来反映EGFR阳性肿瘤细胞的生长状况。
1.7 多肽
多肽是α-氨基酸以肽键连接在一起而形成的化合物,是蛋白质水解的中间产物,一般由10~100个氨基酸分子脱水缩合而成。目前已发现多种多肽结合可导致细胞周期阻滞或诱导细胞凋亡。多肽可靶向至肿瘤细胞的特定靶点,因此常被设计作为靶分子以抑制肿瘤细胞的增殖[33]。现已有专利研制出靶向至结肠癌细胞过表达MUC2的多肽,可特异性地与MUC2进行结合,从而诱导细胞凋亡[34]。
1.8 microRNA
microRNA是一类非编码RNA内源性小分子,其能够通过结合靶向至mRNA的30个非翻译区中的互补序列来沉默蛋白质编码基因,从而抑制细胞生长[35-36]。能够靶向至结肠癌细胞的microRNA有很多。例如,有研究表明,microRNA-320a能直接靶向至结肠癌细胞中过表达的β-连环蛋白,从而抑制结肠癌细胞的无限增殖[37]。Nie J 等[38]研究发现,microRNA-365可通过靶向G1/S特异性周期蛋白D1(Cyclin D1)和Bcl-2抑制结肠癌细胞的生长并促进其凋亡。
2 不同类型结肠癌的靶向特征
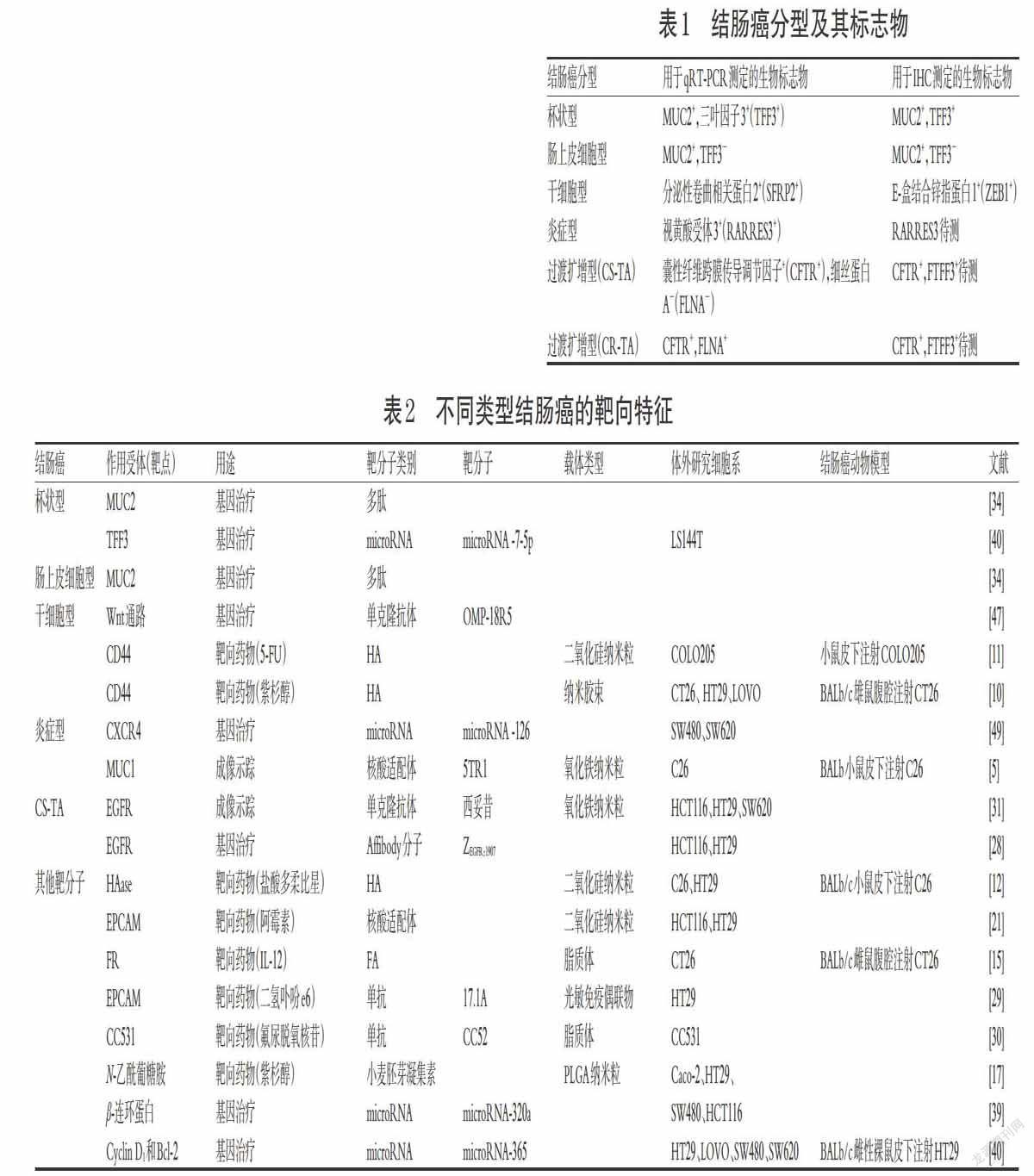
为了能够更加精准地对结肠癌进行靶向,可以运用逆转录定量聚合酶链反应(qRT-PCR)或者免疫组化法(IHC)分析候选的生物标志物,将结肠癌肿瘤分类。目前已有研究把不同的结肠癌患者分为6型[6](表1),在研究结肠癌靶向药物时可根据结肠癌的不同分型选择其靶点及靶分子进行研发(表2),从而进行分类靶向,以提高靶向的准确性。
2.1 杯状型与肠上皮细胞型
杯状型结肠癌患者无病生存期长,临床化疗一般优先使用伊立替康等药物。在基础研究中可使用HT29和LS1747等细胞系模拟杯状型结肠癌模型,这种类型具有杯状特异性MUC2和TFF3 mRNA高表达的特点[39]。MUC2和TFF3主要存在于肠上皮的黏液层,并与杯状细胞一起分布于大肠和小肠[39]。MUC2是一种糖基化黏蛋白,由串连而不规则的重复序列组成,富含作为寡糖链潜在附着位点的丝氨酸和苏氨酸。目前已有专利研发出靶向MUC2蛋白的多肽[33]。TFF3是一种三叶因子,在肠黏膜的创面修复和愈合中起着重要的作用,已有研究证实microRNA-7-5p能够靶向至TFF3并调节结肠癌细胞的增殖[40]。但目前还没有专门靶向至MUC2和TFF3的制剂形式,可考虑利用多肽或microRNA-7-5p与伊立替康等结合制备成口服吸收的纳米粒,以靶向至杯状型结肠癌组织。
而肠上皮细胞型结肠癌特点为MUC2特异性基因的高表达,较少表达TFF3。因此,肠上皮细胞型结肠癌患者应服用针对MUC2基因高表达制备的靶向药物,从而使药物精准靶向至MUC2,减小对正常组织的伤害。
2.2 干細胞型
干细胞型结肠癌患者无病生存期短,伊立替康为该型患者的一线化疗药物。现有研究表明,可运用SW48、HCT8、SW620、HCT116、COLO320等细胞系模拟干细胞型结肠癌模型进行体外试验[6]。干细胞型结肠癌不仅具有高表达细胞外因子(Wnt)信号传导与干细胞、肌上皮基因、间充质基因的特点,还存在着低表达分化标志物的情况。CD44受体在结肠癌干细胞中也具有高表达[41]。与正常干细胞类似,结肠癌干细胞具有对称的细胞分裂无限自我更新的能力,并通过不对称分裂产生子代细胞[42-43]。因为结肠癌干细胞不进行终末分化,所以会产生无限增殖的后代,这个过程直接促进了实体瘤的形成[44]。Wnt信号通路是细胞增殖分化、胚胎和器官发育的关键调控环节和信号转导途径之一[45],在多种恶性肿瘤的生长过程中Wnt途径都被异常激活,证明了其与癌症的相关性。Wnt信号通路包括Wnt/β-连环蛋白、Wnt/Ca2+、Wnt/细胞极性通路等,其中Wnt/β-连环蛋白的生物信号就是卷曲受体[46]。Gurney A等[47]运用单克隆抗体OMP-18R5通过识别卷曲蛋白7与卷曲受体结合,并阻断Wnt信号传导,结果表明,该抗体能够选择性地抑制一系列Wnt/β-连环蛋白信号通路高表达肿瘤的生长。若将该单克隆抗体或者靶向CD44受体的靶分子HA与伊立替康等化疗药物结合,可能对干细胞型结肠癌有较好的治疗效果。
2.3 炎症型
炎症型结肠癌以趋化因子和干扰素(IFN)相关基因及MUC1的相对高表达为特征[48]。趋化因子是一种小细胞因子样肽,分子量为7~15 kDa,与其受体共同协调白细胞在稳态和炎症条件下的迁移。Li Z 等[49]发现,microRNA-126可以通过靶向趋化因子受体4(CXCR4),抑制结肠癌细胞的侵袭和迁移。IFN是反映炎症状况的一个指标,与炎症反应密切相关,根据受体特异性和序列同源性可分为Ⅰ型和Ⅱ型:Ⅰ型IFN由多种IFN-α、IFN-β、IFN-ω和IFN-τ亚型组成,这些亚型结构相似,并可与常见的异二聚体受体结合;Ⅱ型IFN主要是由IFN-γ亚型组成[50]。但是目前尚未见针对IFN及IFN亚型的靶向药物或靶分子的研究。
2.4 过渡扩增型
过渡扩增型结肠癌分为CS-TA和CR-TA两类。CS-TA类结肠癌患者无病生存期长,可过表达EGFR配体表皮调节素和双调蛋白,所以使用靶向EGFR的西妥昔单抗进行治疗可以获得很好的疗效。针对CS-TA类结肠癌的体外研究可使用NCL-H508、SW1116等细胞系[6]。而CR-TA类结肠癌患者无病生存时间短,具有FLNA高表达和对细胞间质上皮转化因子(cMET)抑制剂比较敏感的特点。体外研究CR-TA型结肠癌时可使用LS1034、SW948等细胞系[6]。近期有研究表明,敲除FLNA基因的细胞对抗肿瘤药物多西紫杉醇更加敏感[51]。癌细胞缺乏FLNA,易出现DNA损伤、G2/M期阻滞以及磷酸化组蛋白H2AX增加,进而促进细胞凋亡[52-53];FLNA还与血管内皮生长因子A共同参与了肿瘤血管生成[54]。但是目前靶向至FLNA受体的靶分子研究较少,尚未寻找到适宜的靶分子与cMET抑制剂结合以制备CR-TA靶向药物。
3 展望
随着结肠癌患者人数的逐年上升,病死率居高不下,再加上化疗药物缺乏选择性,在杀死癌细胞的同时也会杀死正常细胞,对患者的身体造成了极大的损害,因此准确靶向至结肠癌细胞的药物及靶分子的研发迫在眉睫。结肠癌靶分子在选择性识别结肠癌细胞受体上起着非常重要的作用。故寻找对结肠癌细胞更加敏感的靶分子从而提高药物的选择性,成为了结肠癌治疗的关键。目前,临床上已经出现了可以靶向至结肠癌细胞的药物,但仍然因为其对不同的结肠癌患者缺乏选择性使其应用受到限制。虽然将结肠癌患者分型并据此给予不同的靶向药能够达到事半功倍的效果,但是目前这个分型方法还没有应用到临床上,并且此分型方法也由于样本量的限制,还不够完善。为此,关于结肠癌的分型以及针对不同分型的靶向药物还有必要继续深入研究。近年来,国内外科研工作者将靶向结肠癌细胞的靶分子与化疗药物结合在一起,大大提高了靶向结肠癌药物的有效性和安全性。相信随着科研工作的进一步发展,一定会早日研发出准确有效靶向至各型结肠癌的药物。
参考文献
[ 1 ] JEMAL A,BRAY F,CENTER MM,et al. Global cancer statistics[J]. CA Cancer Clin,2011,61(2):69-90.
[ 2 ] O’KEEFE,STEPHEN JD. Diet,microorganisms and their metabolites,and colon cancer[J]. Nat Rev Gastroenterol Hepatol,2016,13(12):691-706.
[ 3 ] LEE GH,MALIETZIS G,ASKARI A,et al. Is right-sided colon cancer different to left-sided colorectal cancer:a systematic review[J]. Eur J Surg Oncol,2015,41(3):300- 308.
[ 4 ] BANERJEE A,PATHAK S,VIMALA DS,et al. Strategies for targeted drug delivery in treatment of colon cancer:current trends and future perspectives[J]. Drug Discov Today,2017,22(8):1224-1232.
[ 5 ] JALALIAN SH,TAGHDISI SM,SHAHIDI HN,et al. Ep- irubicin loaded super paramagnetic iron oxide nanoparticle-aptamer bioconjugate for combined colon cancer therapy and imaging in vivo[J]. Europ J Pharm Sci,2013,50(2):191-197.
[ 6 ] SADANANDAM A,LYSSIOTIS CA,HOMICSKO K, et al. A colorectal cancer classification system that associates cellular phenotype and responses to therapy[J]. Nat Med,2013,19(5):619-625.
[ 7 ] LEE JY. Hyaluronan:a multifunctional,megadalton,stea- lth molecule[J]. Curr Opin Cell Biol,2000,12(5):581- 586.
[ 8 ] ZÖLLER M. CD44:can a cancer-initiating cell profit from an abundantly expressed molecule? [J]. Nat Rev Cancer,2011,11(4):254-267.
[ 9 ] TOOLE BP. Hyaluronan in morphogenesis[J]. Semin Cell Dev Biol,2001,12(2):79-87.
[10] ZHU C,ZHANG H,LI W,et al. Suppress orthotopic colon cancer and its through exact targeting and highly selective drug release by a smart nanomicelle[J]. Biomaterials,2018. DOI:10.1016/j.biomaterials.2018.0.1.043.
[11] LIU K,WANG ZQ,WANG SJ,et al. Hyaluronic acid- tagged silica nanoparticles in colon cancer therapy:therapeutic efficacy evaluation[J]. Int J Nanomed,2015,10(1):6445-6454.
[12] ZHANG M,XU C,WEN L,et al. A hyaluronidase responsive nanoparticle-based drug delivery system for targeting colon cancer cells[J]. Cancer Res,2016,76(24):7208- 7218.
[13] ANTONY AC. Folate receptors[J]. Annu Rev Nutr,1996,16(16):501-521.
[14] SIU MKY,KONG DSH,YAN CH,et al. Paradoxical impact of two folate receptors,FR-α and RFC,in ovarian cancer:effect on cell proliferation,invasion and clinical outcome[J]. PLoS One,2012. DOI:10.1371/journal.pone. 0047201.
[15] LUO M,LIANG X,LUO ST,et al. Folate-modified lipoplexes delivering the interleukin-12 gene for targeting colon cancer immunogene therapy[J]. J Biomed Nanotechnol,2015,11(11):2011-2023.
[16] LEHR CM. Lectin-mediated drug delivery:the second generation of bioadhesives[J]. J Control Release,2000,65(1/2):19-29.
[17] WANG C,HO PC,LIM LY. Wheat germ agglutinin-conjugated PLGA nanoparticles for enhanced intracellular delivery of paclitaxel to colon cancer cells[J]. Inter J Pharm,2010,400(1/2):201-210.
[18] PEI X,ZHANG J,LIU J. Clinical applications of nucleic acid aptamers in cancer[J]. Mol Clin Oncol,2014,2(3):341-348.
[19] ZHOU B,WANG B. Pegaptanib for the treatment of age- related macular degeneration[J]. Exp Eye Res,2006,83(3):615-619.
[20] SUBRAMANIAN N,KANWAR JR,KANWAR RK,et al. EpCAM aptamer-siRNA chimera targets and regress epithelial cancer[J]. PLoS One,2015. DOI:10.1371/journal.pone.0132407.
[21] XIE X,LI F,ZHANG H,et al. EpCAM aptamer-functionalized mesoporous silica nanoparticles for efficient colon cancer cell-targeted drug delivery[J]. Europ J Pharm Sci,2016. DOI:10.1016/j.ejps.2015.12.014.
[22] RAY P,WHITE RR. Aptamers for targeted drug delivery[J]. Pharmaceuticals,2010,3(6):1761-1778.
[23] FERREIRA CSM,CHEUNG MC,MISSAILIDIS S,et al. Phototoxic aptamers selectively enter and kill epithelial cancer cells[J]. Nucleic Acids Res,2009,37(3):866-876.
[24] 张磊,鲁莹,钟延强. Affibody分子:一類具有高度亲和力的新配体[J]. 国际药学研究杂志,2012,39(2):127-131.
[25] SPANO JP. Impact of EGFR expression on colorectal cancer patient prognosis and survival[J]. Ann Oncol,2005,16(1):102-108.
[26] PORĘBSKA I,HARŁOZIŃSKA A,BOJAROWSKI T. Expression of the tyrosine kinase activity growth factor receptors(EGFR,ERB B2,ERB B3)in colorectal adenocarcinomas and adenomas[J]. Tumor Biol,2000,21(2):105-115.
[27] LIANG K,ANG KK,MILAS L,et al. The epidermal growth factor receptor mediates radioresistance[J]. Int J Radiat Oncol Biol Phys,2003,57(1):246-254.
[28] SARA HS,DIANA S,JOHAN L,et al. The effect of a dimeric Affibody molecule(ZEGFR:1907)2 targeting EGFR in combination with radiation in colon cancer cell lines[J]. Int J Oncol,2012,40(1):176-184.
[29] GOVERNATORE MD,HAMBLIN MR,PICCININI EE,et al. Targeted photodestruction of human colon cancer cells using charged 17.1A chlorin(e6)immunoconjugates[J]. Br J Cancer,2000,82(1):56-64.
[30] KONING GA,KAMPS JAAM,SCHERPHOF GL. Efficient intracellular delivery of 5-fluorodeoxyuridine into colon cancer cells by targeted immunoliposomes[J]. Cancer Detect Prev,2002,26(4):299-307.
[31] CHO YS,YOON TJ,JANG ES,et al. Cetuximab-conjugated magneto-fluorescent silica nanoparticles for in vivo colon cancer targeting and imaging[J]. Cancer Letters,2010,299(1):63-71.
[32] THOMAS SM,GRANDIS JR. Pharmacokinetic and pharmacodynamic properties of EGFR inhibitors under clinical investigation[J]. Cancer Treat Rev,2004,30(3):255- 268.
[33] GENE LB,AISHA ND,DRAZEN R. Targeting a c-Myc inhibitory polypeptide to specific intracellular compartments using cell penetrating peptides[J]. J Control Release,2009,135(1):2-10.
[34] MARTEYN B,COIC YM,BALEUX F,et al. Polypeptides targeting glycosylated MUC2 proteins,methods of synthesis,their nucleic acids and uses thereof:U.S. Patent Application 10/138,280[P]. 2018-11-27.
[35] BARTEL DP. MicroRNAs:target recognition and regulatory functions[J]. Cell,2009,136(2):215-233.
[36] BARTEL DP. MicroRNAs:genomics,biogenesis,mechanism,and function[J]. Cell,2004,116(2):281-297.
[37] SUN JY,HUANG Y,LI JP,et al. MicroRNA-320a suppresses human colon cancer cell proliferation by directly targeting β-catenin[J]. Biochem Biophys Res Commun,2012,420(4):787-792.
[38] NIE J,LIU L,ZHENG W,et al. MicroRNA-365,down- regulated in colon cancer,inhibits cell cycle progression and promotes apoptosis of colon cancer cells by probably targeting Cyclin D1 and Bcl-2[J]. Carcinogenesis,2012,33(1):220-225.
[39] PODOLSKY DK,GERKEN G,EYKING A,et al. Colitis-associated variant of TLR2 causes impaired mucosal repair because of TFF3 deficiency[J]. Gastroenterology,2009,137(1):209-220.
[40] GUO J,XU L,TENG X,et al. MicroRNA-7-5p regulates the proliferation and migration of intestinal epithelial cells by targeting trefoil factor 3 via inhibiting the phosphoinositide 3-kinase/aktsignalling pathway[J]. Int J Mol Med,2017,40(5):1435-1443.
[41] YAN Y,ZUO X,WEI D. Concise review:emerging role of CD44 in cancer stem cells:a promising biomarker and therapeutic target[J]. Stem Cells Transl Med,2015,4(9):1033-1043.
[42] REYA T,MORRISON SJ,CLARKE MF,et al. Stem cells,cancer,and cancer stem cells.[J]. Nature,2001,414(6859):105-111.
[43] VISVADER JE,LINDEMAN GJ. Cancer stem cells in solid tumours:accumulating evidence and unresolved questions[J]. Nat Rev Cancer,2008,8(10):755-768.
[44] CURTIN JC,LORENZI MV. Drug discovery approaches to target Wnt signaling in cancer stem cells[J]. Oncotarget,2010,1(7):563.
[45] TAPIA-ROJAS C,INESTROSA NC. Loss of canonical Wnt signaling is involved in the pathogenesis of Alzheimer’s disease[J]. Neural Regen Res,2018,13(10):35-40
[46] 劉艳玲,李方兵,赵曦. Wnt信号通路在成骨细胞中的作用:成骨还是破骨?[J].中国组织工程研究,2014,18(33):5366-5371.
[47] GURNEY A,AXELROD F,BOND CJ,et al. Wnt pathway inhibition via the targeting of Frizzled receptors results in decreased growth and tumorigenicity of human tumors[J]. Proc Natl Acad Sci,2012,109(29):11717- 11722.
[48] CASCIO S,FAYLO J,XUE J,et al. Abstract 4153:abnormal expression of MUC1 mucin on colon epithelia stimulates production of pro-inflammatory cytokines promoting colitis-associated colon cancer in a murine model[J]. Cancer Res,2016. DOI:10.1158/1538-7445.AM2016-4153.
[49] LI Z,LI N,WU M,et al. Expression of miR-126 suppresses migration and invasion of colon cancer cells by targeting CXCR4[J]. Mol Cell Biochem,2013,381(1/2):233- 242.
[50] SCHRODER K,HERTZOG PJ,RAVASI T,et al. Interferon-γ:an overview of signals,mechanisms and functions[J]. J Leukoc Biol,2004,75(2):163-189.
[51] ZHAO P,MA W,HU Z,et al. Filamin A(FLNA)modulates chemosensitivity to docetaxel in triple-negative breast cancer through the MAPK/ERK pathway[J]. Tumor Biol,2015,37(4):5107-5115.
[52] MENG X,YUAN Y,MAESTAS A,et al. Recovery from DNA damage-induced G2 Arrest requires actin-binding protein filamin-a/actin-binding protein 280[J]. J Biol Chem,2004,279(7):6098-6105.
[53] YUE J,WANG Q,LU H,et al. The cytoskeleton protein filamin-A is required for an efficient recombinational DNA double strand break repair[J]. Cancer Res,2009,69(20):7978-7985.
[54] URAMOTO H,LEVENT MA,HANAGIRI T. A positive relationship between filamin and vegf in patients with lung cancer[J]. Anticancer Res,2010,30(10):3939-3944.
(收稿日期:2019-04-15 修回日期:2019-08-14)
(编辑:孙 冰)
