胆南星发酵制品与混合蒸制品的鉴别研究
2019-09-10陈云陈劲松郁红礼吴皓王卫程梓烨单雪莲蔡宝昌
陈云 陈劲松 郁红礼 吴皓 王卫 程梓烨 单雪莲 蔡宝昌
摘要 目的:以豬胆汁及天南星、制天南星为原料分别制备发酵制胆南星及混合蒸制胆南星,以胆汁酸类成分为指标,建立以猪胆汁为炮制辅料的胆南星2种炮制品的薄层鉴别及HPLC-ELSD特征图谱。方法:采用硅胶G薄层板,以石油醚:丙酮:冰醋酸(11∶ 8∶ 0.8)为展开剂,10%硫酸乙醇溶液为显色剂,建立薄层色谱鉴别方法。采用Agilent Eclipse XDB C18(4.6 mm×250 mm,5 μm)色谱柱,以乙腈与0.1%冰醋酸水为流动相进行梯度洗脱,流速为1 mL/min,柱温为30 ℃,ELSD:漂移管温度为105 ℃,氮气流量为2.5 mL/min,建立胆南星HPLC-ELSD特征图谱鉴别方法。结果:TLC和HPLC-ELSD图谱均显示发酵制胆南星可检测到游离型胆汁酸类成分猪胆酸(HCA)、猪去氧胆酸(HDCA)和鹅去氧胆酸(CDCA)3个特征成分,而混合蒸制胆南星中未检测出;混合蒸制胆南星可检测到结合型胆汁酸类成分甘氨猪去氧胆酸(GHDCA)和甘氨鹅去氧胆酸(GCDCA)2个特征成分,而发酵制胆南星中未检测出。结论:所建胆汁酸类成分的薄层色谱鉴别法(TLC)和高效液相色谱-蒸发光散射法(HPLC-ELSD)均可有效鉴别胆南星的发酵制品和混合蒸制品,为胆南星质量控制提供依据。
关键词 胆南星;胆汁酸类成分;薄层色谱鉴别;HPLC-ELSD特征图谱;炮制;发酵;蒸制
Study on Identification of Fermentation Products and Mixed Steamed Products of Arisaema Cum Bile
Chen Yun1,Yu Hongli1,2,3,Wu Hao1,2,3,Chen Jinsong4,Wang Wei1,Cheng Ziye1,Shan Xuelian1,Cai Baochang1,2,3
(1 Pharmacology College of Nanjing University of Chinese Medicine,Nanjing 210023,China; 2 Jiangsu Key Laboratory of Chinese Medicine Processing,Nanjing 210023,China; 3 Engineering Center of State Ministry of Education for Standardization of Chinese Medicine Processing,Nanjing 210023,China; 4 Sichuan Qianyuan traditional Chinese Medicine Decoction Co.,Ltd.Guanghan 618304,China)
Abstract Objective: Using pig bile and Arisaematis Rhizome and Arisaematis Rhizoma Preparatum as raw materials,the fermenting and mixed evaporating of arisaema cum bile were prepared respectively,and the bile acids were used as the index.To establish thin layer identification and HPLC-ELSD characteristic map of 2 processed products from porcine bile.Methods Silica gel G thin layer plate was applied,and petroleum ether:acetone:glacial acetic acid (11∶ 8∶ 0.8) were used as developing agent and 10% sulfuric acid ethanol solution as chromogenic agent,a TLC identification method was established.An Agilent Eclipse XDB C18 (4.6 mm×250 mm,5 μm) column was used,with acetonitrile and 0.1% glacial acetic acid water as mobile phase for gradient elution.The flow rate was 1 mL/min,at 30 ℃ and ELSD:drift tube at 105 ℃.The identification method of HPLC-ELSD characteristic map of arisaema cum bile was established by nitrogen flow rate of 2.5 mL/min. Results: TLC and HPLC-ELSD spectra showed that three characteristic components of free hyocholic acid (HCA),hyodeoxycholic acid (HDCA) and chenodeoxycholic acid (CDCA),could be detected in fermented arisaema cum bile,but not in mixed evaporation.Two characteristic components of conjugated bile acids,(GHDCA) and (GCDCA),could be detected by mixed evaporation of arisaema cum bile,but not in the fermentation of arisaema cum bile. Conclusion: TLC and HPLC-ELSD can be used to identify the fermented and mixed distilled products of arisaema cum bile which can provide the basis for the quality control of arisaema cum bile.
Key Words Arisaema cum bile; Bile acid components; TLC identification; HPLC-ELSD characteristic map; Processing; Fermentation; Steaming
中图分类号:R282.5 文献标识码:A doi: 10.3969/j.issn.1673-7202.2019.02.006
《中华人民共和国药典》2015版收载胆南星(Arisaema cum bile)制法为制天南星的细粉与牛、羊或猪胆汁经加工而成,或为生天南星细粉与牛、羊或猪胆汁经发酵加工而成[1]。具有清热化痰,息风定惊的功效,临床上多用于小儿百日咳、癫痫病、中风等疾病的治疗[1]。通过查阅全国及各省市炮制规范,胆南星的炮制方法主要有发酵法和混合蒸制法2种。全国各地2种炮制方法的炮制工艺差异较大,并且炮制辅料胆汁用量也存在很大差异。本课题组前期以猪胆汁为原料,按照《全国中药炮制规范》(1988版) 中胆南星项下2种炮制方法自制胆南星,通过对胆南星2种炮制品炮制前后的成分分析,发现胆汁酸类成分发生明显变化[2-3]。由于胆南星的原药材为天南星或制天南星,天南星味苦,辛温,为有毒中药[4-7],胆南星为其炮制品之一,用胆汁炮制后的2种胆南星炮制品均可达到减毒存效的作用[8-11],且胆汁具有调节免疫力、镇静安神的功效,胆汁中的膽汁酸类成分被认为是其主要药效成分[12-14]。因此,本文以胆南星2种炮制品中所含胆汁酸类成分为指标性成分,采用薄层色谱鉴别法(TLC)和高效液相色谱-蒸发光散射法(HPLC-ELSD)对胆南星2种炮制品中胆汁酸类成分进行分析鉴别。建立切实可行、操作简单的鉴别方法,为胆南星的质量控制提供依据。
1 仪器与试药
1.1 仪器 BP211D电子天平(德国Sartorius公司);HH-2数显恒温水浴锅 (上海维诚仪器有限公司);Milli-Q纯水仪(南京耀灵生物科技有限公司);打粉机(天津市泰斯特仪器有限公司);四号筛网(江苏南京市雄晨筛网厂);超声仪(昆山市超声仪器有限公司)。ZF7三用紫外分析仪(上海康华生化仪器制造有限公司);DB-2型不锈钢电热板(江苏金坛市金城园胜实验仪器厂)。Waters 2695型高效液相色谱仪(美国Waters公司),配Waters 2996型ELSD 2000ES(美国Alltech公司)检测器,Empower色谱工作站;移液管;容量瓶;注射器;0.45 μm微孔滤膜(天津津腾实验设备有限公司);圆底烧瓶。
1.2 试剂 乙醇(分析纯,批号170308076K)、冰醋酸(分析纯,批号151009910E)均购自南京化学试剂有限公司;石油醚(分析纯,批号20160818)购自国药集团化学试剂有限公司;丙酮(分析纯,批号Lot.No.20180105)、硫酸(分析纯,批号Lot.No.20161026)均购自上海凌峰化学试剂有限公司;水为超纯水;胆汁购自南京市栖霞区农贸市场的新鲜猪胆囊,经纱布过滤,去除絮状物,于-20 ℃保存,备用。
对照品:猪胆酸(Hyocholic Acid,HCA,大于98%)购自甄准生物科技有限公司;猪去氧胆酸(Hyodeoxycholic Acid,HDCA,大于98%)、鹅去氧胆酸(Chenodeoxycholic Acid,CDCA,大于98%)、甘氨猪去氧胆(Glycohyodeoxycholic Acid,GHDCA,大于97%)、甘氨鹅去氧胆酸(Glycochenodeoxycholic Acid,GCDCA,大于97%)均购自上海源叶生物科技有限公司。
1.3 分析样品 天南星药材由四川仟源中药饮片有限公司提供,经南京中医药大学陈建伟教授鉴定为天南星科植物天南星( Arisaematis rhizoma)的干燥块茎;制天南星(Arisaematis rhizoma preparatum )采用生天南星按照《中华人民共和国药典》2015年版制天南星项下的炮制方法自制。
2 方法与结果
2.1 胆南星样品制备 发酵法:按照《全国中药炮制规范-1988》:取生天南星粉末,加入净胆汁(天南星:胆汁=1∶ 4),搅拌拌匀,放温暖处,发酵7~15 d后,再连续蒸或隔水炖9昼夜,每2 h搅拌1次,除去腥臭气。至呈黑色浸膏状,口尝无麻味为度,取出,晾干。再蒸软,趁热制成小块。
混合蒸制法:按照《全国中药炮制规范-1988》:取生天南星粉末,加入净胆汁(天南星:胆汁=1∶ 4)拌匀,蒸60 min至透,取出放凉,制成小块,干燥。
2.2 胆南星中胆汁酸类成分的薄层色谱鉴别
2.2.1 薄层色谱条件 按照2015年版《中华人民共和国药典》第4部(通则0502)项下薄层色谱法操作,吸取上述对照品溶液和供试品溶液各5 μL,分别点于同一硅胶G薄层板上,以石油醚:丙酮:冰醋酸(11∶ 8∶ 0.8)为展开剂展开,取出,晾干,喷以10%硫酸乙醇溶液,在105 ℃加热至斑点显色清晰,置紫外灯下(365 nm)检视。在胆南星供试品色谱中,在与对照品色谱相应位置显相同颜色的斑点,结果见图1。
2.2.2 对照品溶液的制备 取猪胆酸(HCA)、猪去氧胆酸(HDCA)、鹅去氧胆酸(CDCA)、甘氨猪去氧胆酸(GHDCA)和甘氨鹅去氧胆酸(GCDCA)对照品适量,精密称定,加80%乙醇分别制成每1 mL含猪胆酸0.44 mg、猪去氧胆酸1.894 mg、鹅去氧胆酸1.026 mg、甘氨猪去氧胆酸1.108 mg、甘氨鹅去氧胆酸1.048 mg的溶液,即得。
2.2.3 供试品溶液的制备 取胆南星粉末(过四号筛)约0.5 g,精密称定,置于圆底烧瓶中,加80%乙醇20 mL,加热回流30 min,放冷,过滤,滤渣再加80%乙醇20 mL继续回流30 min,放冷,过滤,合并2次滤液,转移至50 mL容量瓶中,加80%乙醇定容至刻度。
3 胆汁酸类成分的HPLC特征图谱鉴别
3.1 色谱条件 色谱柱为Agilent Eclipse XDB C18(4.6 mm×250 mm,5 μm);流速:1.0 mL/min;柱温30 ℃;进样量:10 μL;流动相:乙腈(A)-0.1%乙酸(B);梯度洗脱程序:0~2 min,25% ~33%乙腈;2~20 min,33% ~62%乙腈;20~25 min,62% ~25%乙腈;25~26 min,25% ~25%乙腈。
ELSD条件:载气流速2.5 mL/min,漂移管温度:105 ℃。
3.2 对照品溶液的制备 同“2.2.2”项下方法。
3.3 供试品溶液的制备 同“2.2.3”项下方法。
3.4 样品测定法 分别精密吸取对照提取物溶液与供试品溶液各10 μL,注人液相色谱仪,测定,记录色谱图,即得。
3.5 精密度实验 取自制发酵胆南星和自制混合蒸制胆南星粉末(过四号筛),按照上述供试品溶液制备方法,制备供试品溶液,按照上述检测方法进行测定,重复进样6次,记录色谱图,各共有峰保留时间与峰面积的 RSD 值均小于5.0%,表明仪器精密度良好,符合特征图谱研究要求。
3.6 重复性实验 取同一批取自制发酵胆南星和自制混合蒸制胆南星粉末(过四号筛),按照上述供试品溶液制备方法,重复制备供试品溶液6份。分别进行检测,结果色谱图中各共有峰保留时间与峰面积的 RSD 值均小于5.0%,表明重复性良好,符合特征图谱研究要求。
3.7 稳定性实验 取自制发酵胆南星和自制混合蒸制胆南星粉末(过四号筛),按照上述供试品溶液制备方法,制备供试品溶液,按照上述检测方法分别在0 h、2 h、4 h、8 h、16 h、24 h进行检测,记录各色谱峰的各共有峰保留时间与峰面积的 RSD 值均小于5.0%,表明24 h内供试品溶液稳定性较好,符合特征图谱研究要求。
3.8 胆南星胆汁酸类成分特征图谱的建立
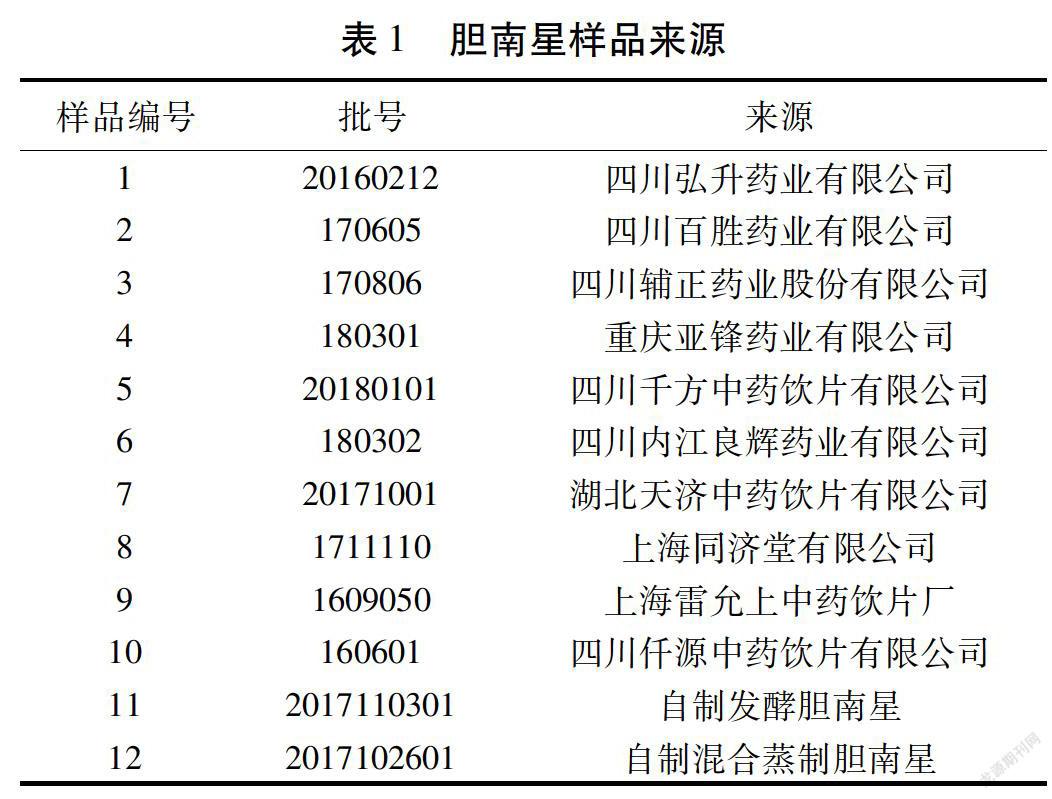
结果表明,胆南星的发酵制品与混合蒸制品中所含胆汁酸类成分差异较大,因此,对胆南星的发酵制品与混合蒸制品分别建立胆汁酸类成分HPLC特征图谱,结果见图2。通过各厂家胆南星与自制发酵胆南星和自制混合蒸制胆南星比较,发现四川千方、四川辅正、四川弘升、四川仟源4个厂家的胆南星样品与发酵制胆南星的特征成分相一致,经国家药典委员会“中药色谱指纹图谱相似度评价系统A版软件”(2012版),自动匹配分析,标定5共有峰,其中峰3、4、5与对照品对照,分别定性为游离型胆汁酸类成分猪胆酸(HCA)、猪去氧胆酸(HDCA)、鹅去氧胆酸(CDCA),结果见图2-A。上海同济堂、内江良辉、上海雷允上、四川百胜、重庆亚峰、湖北天济六个厂家的胆南星样品与混合蒸制胆南星的特征成分相一致,经自行匹配,标定6个共有峰,其中峰2、3与对照品对照,分别定性为结合型胆汁酸类成分甘氨猪去氧胆酸(GHDCA)、甘氨鹅去氧胆酸(GCDCA),结果见图2-B。
因此,在胆南星发酵制品中可检测到游离型胆汁酸类成分猪胆酸(HCA)、猪去氧胆酸(HDCA)和鹅去氧胆酸(CDCA)3个特征峰,而在胆南星混合蒸制品中检测不到;在胆南星混合蒸制品中可检测到结合型胆汁酸类成分甘氨猪去氧胆酸(GHDCA)和甘氨鹅去氧胆酸(GCDCA)2个特征峰,而在胆南星发酵制品中未检测到相应特征峰。见图2。
4 讨论
胆南星是批准文号管理的饮片。根据市场调研发现,现有生产胆南星的厂家使用的胆南星主要以猪胆汁为辅料。本文以猪胆汁中胆汁酸类成分作为胆南星鉴别的指标性成分,为胆南星质量控制提供坚实基础。
本文以自制发酵胆南星和自制混合蒸制胆南星与胆汁酸类成分的混合对照品对照,TCL及HPLC法均显示发酵法胆南星中可检出游离型胆汁酸类成分猪胆酸(HCA)、猪去氧胆酸(HDCA)、鹅去氧胆酸(CDCA)成分,混合蒸制胆南星中可检出结合型胆汁酸类成分甘氨猪去氧胆酸(GHDCA)、甘氨鹅去氧胆酸(GCDCA)。因此,以胆汁酸类成分作为胆南星的指标性成分,分别建立胆汁酸类成分的薄层鉴别和HPLC特征图谱,可有效鉴别并区分市售胆南星的2种炮制品,并控制胆南星质量。研究发现市售胆南星中有厂家中的胆汁酸类成分含量极低,几乎检不出,此原因可能与厂家在炮制过程中所加胆汁的量及炮制工艺有关[15-16],本文建议《中华人民共和国药典》中胆南星制备方法中规定辅料胆汁的用量及增加胆南星胆汁酸类成分的鉴别。
本文前期实验对环己烷:乙酸乙酯:冰醋酸(8∶ 8∶ 0.8)、石油醚:丙酮:冰醋酸(11∶ 8∶ 0.8)、正己烷:乙酸乙酯:冰醋酸:甲醇(20∶ 25∶ 2∶ 0.8)这3种不同的展开剂体系[17-18],结果表明石油醚:丙酮:冰醋酸(11∶ 8∶ 0.8)的展开效果较好,Rf值适中;分别以10%硫酸乙醇溶液和香草醛2种为显色剂,结果显示2种显色剂均能使游离型胆汁酸类各成分在紫外荧光下斑点更清晰;对不同批号薄层板和不同厂家薄层板进行了重现性考察,结果在与对照品色谱相应的位置上,均显示相同颜色的斑点,显示不同批号和不同厂家的薄层板重现性较好;分别考察了高温(40 ℃)和低温(4 ℃)的展开效果,结果显示高低温的分离效果相近,受到温度的影响较小,在高低温度均可鉴别;通过以硫酸與水不同比例调节湿度,分别考察了高湿(88%)和低湿(18%)的展开效果,结果表明,低湿的分离效果较好,高湿湿的环境含水量大,导致Rf值整体偏高,影响分离效果。因此,在鉴别时需要控制湿度,不能过高。
本文前期实验考察了不同的流动相体系(甲醇-水、乙腈-水、乙腈-0.1%甲酸水、乙腈-0.1%乙酸水)的分析条件,根据色谱图比较分析显示,乙腈-0.1%乙酸水体系的梯度洗脱均可使所有成分达到有效分离,故选择乙腈-0.1%乙酸水体系进行梯度洗脱。本文对不同流动相梯度体系进行比较,通过色谱图比较,最终确定了在胆汁酸类各指标成分分离度好且分析时间适中的梯度体系。
参考文献
[1] 国家药典委员会.中华人民共和国药典[S].一部.北京:中国医药科技出版社,2015:261.
[2]李瑶.胆南星炮制前后成分变化及质量标准研究[D].南京:南京中医药大学,2018.
[3]陈云,郁红礼,吴皓,等.发酵对胆南星中胆汁酸类成分的影响及胆南星中3种游离胆汁酸含量测定研究[J].中国中药杂志,2018,43(22):4457-4461.
[4]吴仪洛.本草从新[M].上海:上海科学技术出版社,1958:100.
[5]太平惠民和剂局.太平惠民和剂局方[M].北京:人民卫生出版社,1985:18.
[6] 曾世荣.活幼心书[M].北京:中国书店,1985:46.
[7]成都中医学院.中药炮制学[M].上海:上海科学技术出版社,1980:142.
[8]刘养清,刘二保.动物胆汁理化特性及药用[M].北京:化学工业出版社,2002:74-92.
[9]石岩,耿颖,郑天骄,等.猪胆粉HPLC-ELSD全轮廓谱图主要胆汁酸测定及化学计量学分析[J].药物分析杂志,2017,37(2):283.
[10] 杨伟鹏,王怡薇,王彦礼,等.不同胆汁炮制方法对天南星解毒存效作用的实验研究[J].中国实验方剂学杂志,2009,15(12):33-35.
[11]赫炎,王孝涛.胆南星不同炮制品的药效和毒性实验研究[J].中药材,1997,20(9):459-461.
[12]游元元,万德光.动物胆汁药用研究进展[J].贵阳中医学院学报,2007,29(4):58-61.
[13]石岩,耿颖,郑天骄,等.猪胆粉HPLC-ELSD全轮廓谱图主要胆汁酸测定及化学计量学分析[J].药物分析杂志,2017,37(2):283.
[14]鄢海燕,邹纯才.四种动物胆粉中胆酸类成分分析及药理作用比较[J].皖南医学院学报,2012,31(4):274-277.
[15]赵启苗,单国顺,陈江宁,等.胆南星质量评价方法初探[J].中国实验方剂学杂志,2017,23(6):28-31.
[16]黎量,李欣逸,艾莉.胆南星炮制及质量标准研究进展与思考[J].中药与临床,2015,6(3):7-9.
[17]姚志昂,郭力,周娟,等.三十一批膽南星的对比研究[J].成都中医药大学学报,2011,34(3):57-59.
[18]贲永光,李康,李坤平,等.胆南星的薄层色谱鉴别[J].广东药学院学报,2009,25(2):160-161.
