血清淀粉样蛋白A与急性脑梗死关系的Meta分析
2019-09-05郑文惠李北辰
郑文惠,李 倩,张 磊,李北辰,方 瑗
2019年《Lancet Neurology》杂志发布了2016全球疾病负担研究( Global Burden of Disease Study,GBD)关于卒中的分析数据,结果显示:2016年卒中是全球第二大死亡原因(550万),全球卒中患病人数为8010万,2016年新增卒中病例1370万;在所有卒中的患病人数中,84.4%为缺血性卒中,东亚的卒中年龄标化发病率最高,特别是中国(354/10万人年)[1]。但是目前脑卒中的预后评估尚缺乏良好的生物学指标。血清淀粉样蛋白A(serum amyloid protein A,SAA)是一种急性时相反应蛋白[2],可通过改变高密度脂蛋白的功能,影响胆固醇的转运和清除,进而引起脂质沉积,加速动脉硬化进程和动脉粥样硬化性血管疾病的发生[3]。前期研究显示SAA可以作为评估和预测冠心病病情和严重程度的敏感标志物[4],但在急性脑梗死的研究中尚无明确定论。为了探讨SAA与急性脑梗死的关系及其临床意义,本文荟萃有关SAA与急性脑梗死的文献进行Meta分析。
1 方 法
1.1 文献纳入标准 (1)研究类型:队列研究;(2)研究人群:急性脑梗死组符合急性脑梗死的诊断标准,并且经头部CT和(或)头部MR确诊;(3)文献数据完整:提供了或通过数据可计算淀粉样蛋白A的均值及标准差。
1.2 文献排除标准 (1)完全重复发表或者同一数据发表;(2)资料和统计所需数据不全;(3)实验设计、操作实施过程有误或者存在重大缺陷。
1.3 文献检索 计算机检索PubMed、Cochrane Library、中国期刊全文数据库(China National Knowledge Infrastructure,CNKI)、中国生物医学文献数据库(CBM),检索时限均为从建库至2019年4月,语种限制为中文或英文,中文检索词为“卒中”或“脑梗死”和“淀粉样蛋白A”;英文检索词为“stroke”OR“ischemic stroke”和“serum amyloid protein A”。同时,追溯纳入文献的参考文献,避免漏查尚未公开发表的文献。
1.4 资料提取和文献偏倚风险评价 (1)资料提取和文献偏倚风险评价由2名研究者完成,如有分歧讨论决定。以EndNote X7 软件管理文献,筛选可能符合纳入标准的文献并阅读全文进行判断,合并整理后建立文献数据库,提取文献基本信息:第一作者、发表时间、国家。(2)研究对象基本特征:年龄、性别、病例来源时间和样本量。(3)各实验室指标结果:均数及标准差。以 Newcastle-Ottawa Scale (NOS)[5]量表评估纳入文献的偏倚风险,包括纳入文献对象的选择(4分)、可比性(2分)、暴露(3分)3 个方面,≥7分为低度偏倚风险;6分为中度偏倚风险;≤5分为高度偏倚风险。
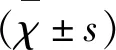
2 结 果
2.1 文献检索结果 共检索到322篇文献,10项队列研究[6~15]纳入本文进行Meta分析,共1054例急性脑梗死患者。纳入文献基本情况(见表1)。文献检索流程及结果(见图1)。
2.2 文献质量评价 采用非随机研究偏倚风险评估方法(NOS)对纳入研究的方法学质量进行评估。NOS包括研究对象选择(4个条目,4分)、组间可比性(1个条目,2分)和结果测量(3个条目,3分),总共 9 分,6分及以上为高质量文献。如遇分歧则讨论解决,必要时根据第三意见进行商议,最后达成一致性意见。质量评价结果(见表1)。
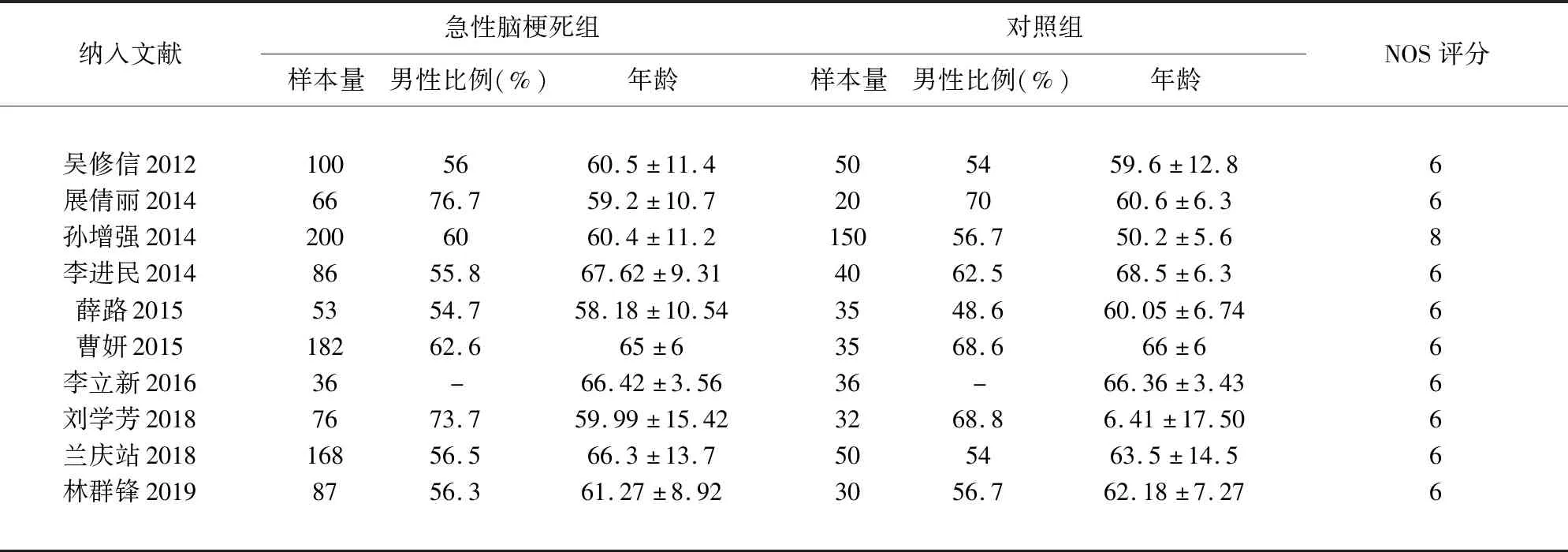
表1 纳入文献基本信息
2.3 Meta分析结果 急性脑梗死组与健康组血清淀粉样蛋白A水平比较,共纳入10篇文献包括1470名受试者对血清SAA水平进行了比较,异质性检验结果 I2=100%,P<0.00001,提示存在统计学异质性,故采用随机效应模型。合并效应量结果:(MD=14.86,95%CI=12.09~17.63,P<0.00001),显示急性脑梗死组血清SAA水平高于健康组具有统计学意义(见图2)。共3篇文献在患者入院后行美国国立卫生研究院卒中量表评分(National Institute of Health stroke scale,NIHSS)进行脑卒中严重程度评定。其中重度神经功能缺损和中度神经功能缺损的血清SAA水平的Meta分析显示重度神经功能缺损组的血清SAA水平高于中度组,具有统计学意义(MD=1.17,95%CI=0.32~2.03,P=0.007),其中中度神经功能缺损和轻度神经功能缺损的血清SAA水平的Meta分析显示中度神经功能缺损组的血清SAA水平高于轻度组,具有统计学意义(MD=0.60,95%CI=0.12~1.08,P=0.02)(见图3、图4)。
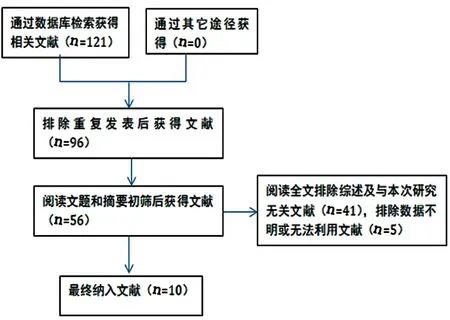
图1 文献筛选流程及结果
3 讨 论
通过分析可以得出结论:急性脑梗死患者SSA的水平明显高于正常健康人,而且SSA的水平跟脑卒中严重程度呈正相关。结论由纳入的研究进行分析得出,共10项给出了观察组和对照组的血清淀粉样蛋白A的水平,均为前瞻性研究,且以均值和标准差的形式给出,从而提取连续性数据进行分析,通过NOS量表对文献质量进行评估,所有研究均在5分以上。但是上述研究均来自国内文献,对国外数据库搜索后得到相关文献数量很少,且没有符合纳入标准的文献,所以结论适用范围有限,对研究的最终结果,我们应该谨慎对待。
SAA主要由肝脏分泌产生,可分为急性期SAA和结构型SAA,急性期SAA包括SAA1和SAA2在炎性急性反应期分泌显著增加,结构型SAA不参与急性炎症反应含量基本保持不变[16]。一项大规模前瞻性研究[17],对28263例健康绝经期女性进行随访结果显示,SAA是动脉粥样硬化相关心血管事件的预测因素,并且大量研究发现SAA在动脉粥样硬化损伤时表达增加[18~20]。动脉粥样硬化是一个复杂的动态过程,斑块内脂质随着时间的推移逐渐累积并被纤维帽覆盖,在致炎性物质(如氧化的脂质或炎性因子)的刺激下发生炎症反应;在触发因素(应激、血压升高或神经因素)的协调作用下发生斑块破裂或糜烂,动脉粥样硬化与脑梗死的发病密切相关。SAA与脑梗死的关系,其可能机制包括以下几个方面:(1) SAA通过替换高密度脂蛋白胆固醇(high-density lipoprotein,HDL)中的载脂蛋白A-I(Apo A-I),并与HDL形成新的颗粒,从而失去对卵磷脂胆固醇酰基转移酶(LCAT)的激活作用,最终影响胆固醇的逆向转运[3]。进一步研究显示,SAA对Apo A-I的替换及HDL/SAA复合物的形成,是HDL与肝细胞的亲和力减低,而HDL/SAA复合物与巨噬细胞的亲和力比单纯HDL提升3~4倍,这些脂质进入巨噬细胞促使其转为泡沫细胞,进一步促进动脉粥样硬化[21]。(2)SAA被发现在急性和慢性炎症中均有表达,能促进单核细胞/巨噬细胞的趋化和黏附,增加动脉粥样硬化斑块的炎性浸润[22],还具有促进多种炎性因子的表达及对炎症相关信号通路的激活作用[23~25]。(3)SAA通过诱导基质金属蛋白酶的表达,加速纤维帽中细胞外基质的降解,导致纤维帽破裂,进一步造成粥样斑块破裂,进一步导致斑块不稳定性增加[6]。虽然大量研究显示SAA是形成动脉粥样硬化的重要原因,但是目前也存在争议,近期国外一项研究,通过观察亚临床颈动脉粥样硬化的长期病死率,进行12 y的随访发现病死组的血清淀粉样蛋白A的水平高于存活组,但是排除了超敏C反应蛋白的混杂因素后,我们发现这一统计学意义就丢失了,进一步说明可能SAA与动脉粥样硬化可能并没有直接的因果关系,也许只是机体炎症状态的标志物[26]。这也引发了我们对急性期脑梗死血清淀粉样蛋白A升高的意义的思考,血清淀粉样蛋白A的升高仅仅是一种炎性状态的标志物?还是急性脑梗死发展过程中的一个积极参与者?如果它参与了急性脑梗死的发生,又是通过什么样的途径和靶点实现的?目前的研究还不能够充分解释,后期需要进一步的高质量的研究去说明,以期对急性脑梗死的预防和治疗发挥用处。
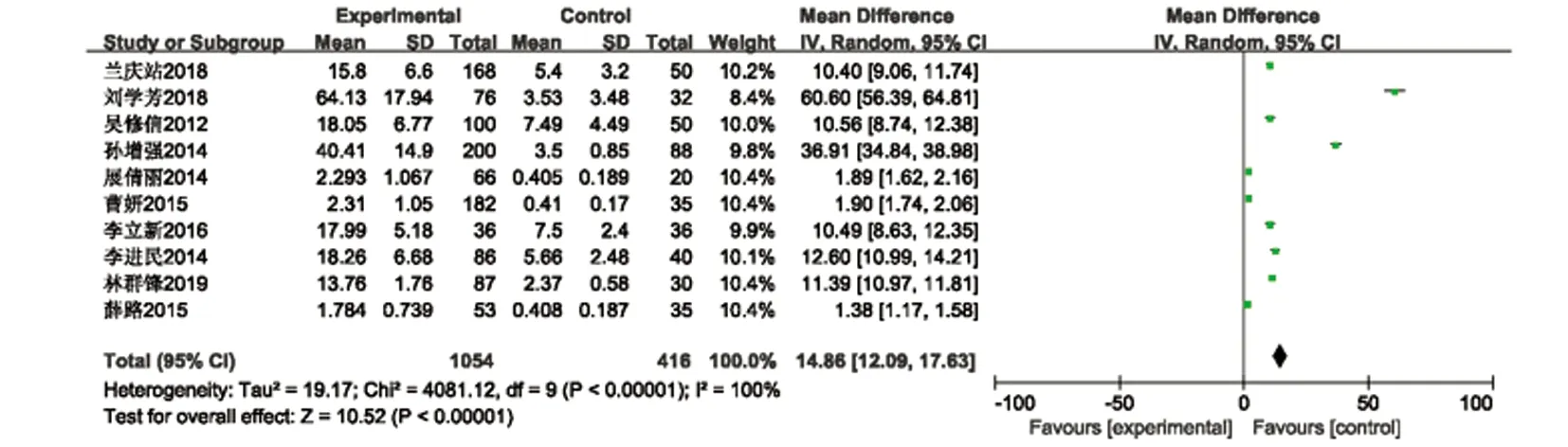
图2 急性脑梗死组与对照组组淀粉样蛋白A水平的Meta分析
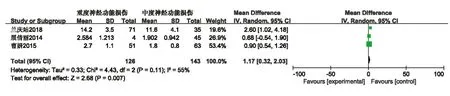
图3 重度神经功能损伤和中度神经功能损伤组淀粉样蛋白A水平的Meta分析
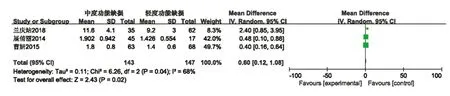
图4 中度神经功能损伤和轻度神经功能损伤组淀粉样蛋白A水平的Meta分析
