非医疗用品辐照加工剂量设定方法研究
2019-09-03陈志云杨绍雨
陈志云,杨绍雨,马 琴
(南京喜悦科技股份有限公司,江苏 南京 211316)
辐照加工作为核技术利用的一个重要分支,具有非常广泛的用途,大致可分为微生物控制和非微生物控制两大类。非微生物控制的辐照加工包括辐照改性、农残降解、白酒陈化等[1]。对于微生物控制分为灭菌和杀菌,灭菌就是完全杀灭微生物,无菌保证水平达到10-6以上,如医疗用品的灭菌、无特定病原体(SPF)实验动物饲料的灭菌等;而杀菌则是对食品、药品、化妆品等的微生物控制,达到延长货架期、降低微生物危害的目的[2-3]。对于医疗用品的辐照灭菌,辐照剂量设定按照ISO11137-2[4]有明确的方法。然而,对于非医疗用品的辐照杀菌并没有明确的剂量设定标准方法。以食品辐照为例,无论是强制性的通用标准[5],还是某一特定食品的工艺控制推荐标准,如熟畜禽肉类辐照杀菌工艺标准GB/T 18526.5[6],均没有涉及到辐照的剂量设定方法,仅给出了辐照的最高和最低剂量限值及微生物控制限值等要求。虽然研究表明,10 kGy剂量的辐照对于食品和药品的药理、毒理影响可以不用检测,甚至可超过10 kGy剂量辐照[7],但是高剂量辐照会对食品营养物质产生不良影响,因此对于辐照杀菌,应该坚持合理可行尽量低的原则[5,8]。合理设定辐照剂量一直是辐照加工行业研究的重点之一[9-12]。在标准方法缺失的情况下,当前非医疗用品辐照加工需求剂量通行的做法是由客户给出,辐照中心负责满足需求剂量即可[13],但作为产品生产厂家,负有产品安全的主体责任,对辐照技术不熟悉,无法合理设定剂量。
针对上述问题,本文在前人工作的基础上,结合生产实践,开展非医疗用品辐照的剂量设定方法研究,以某一种袋装食品的辐照杀菌为例,介绍剂量设定过程。采用微生物辐照杀灭理论与辐照杀菌实践相结合的方法,给出一种非医疗用品辐照杀菌剂量设定的可行方法,拟为非医疗用品辐照杀菌剂量设定提供参考。
1 实验材料及仪器
1.1 实验样品
袋装样品,真空袋装,每袋重量100 g,共60袋。
1.2 主要试剂
平板计数琼脂、氯化钠:250 g/瓶,上海盛思化学科技有限公司。
1.3 主要仪器设备
γ辐照装置:BFT-IV,北京比尼公司;净化操作台:SW-CJ-2G,上海苏净实业有限公司;卧式压力灭菌锅:YX600W,上海三申医疗器械有限公司;生化培养箱:SPX-150B-Z,上海博讯实业有限公司医疗设备厂。
2 实验方法
2.1 产品初始污染菌测定
2.1.1食品初始污染菌测定 参照GB 4789.1-2016标准方法进行测定。
2.1.2初始污染菌检测 (1) 样品制备:称取样品25 g移置225 mL无菌生理盐水中,充分摇匀制成1∶10供试液。(2) 供试液制备:用无菌吸管或微量移液器吸取1∶10 样品匀液1 mL,沿管壁缓慢注于盛有9 mL 稀释液的无菌试管中,反复吹打使其混合均匀,制成 1∶100的样品匀液。(3) 梯度稀释:根据对样品污染状况的估计,选择2~3个适宜稀释度样品匀液(液体样品可包括原液),在进行10倍递增稀释时,吸取1 mL 样品匀液于无菌平皿内,每个稀释度做两个平皿。(4) 空白对照:分别吸取1 mL空白稀释液加入两个无菌平皿内,及时将冷却至46 ℃的平板计数琼脂培养基(可放置于(46±1) ℃恒温水浴箱中保温)倾注平皿,每皿约20 mL,并转动平皿使其混合均匀。(5) 培养:待琼脂凝固后,将平板翻转,培养箱(36±1) ℃培养(48±2) h,水产品(30±1) ℃培养(72±3) h。(6) 菌落计数:用放大镜或菌落计数器,记录稀释倍数和相应的菌落数量。菌落计数以菌落形成单位(colony-formingunits, CFU)表示。选取菌落数在30~300 CFU之间,以最接近30~300 CFU的稀释级平均数乘以稀释倍数报告。如果稀释级平均菌落数均无菌生长或最低稀释级平均菌落数小于1时,应报告菌落数<10 CFU/g。
2.2 产品菌落耐辐照实验
该产品要求辐照后微生物含量为1 CFU/g以下,根据初始污染菌含量,结合辐照经验,设定0、1、2、3、4、5、6 kGy剂量为辐照实验剂量,考虑工作量和实际工业辐照过程的可操作性,每种辐照剂量取10个样品,同时辐照并检测辐照后污染菌,取平均值,首次出现一组全部无菌的剂量即作为最高辐照剂量值。
3 结果与讨论
3.1 菌落总数
辐照前样品菌落总数列于表1。 从表1可见,同一批产品的初始污染菌较为接近,在其他产品中也有类似情况。
不同剂量辐照后样品菌落总数列于表2。由表2中数据可知,10个样本经5 kGy辐照后检测无菌,因此5 kGy作为辐照实验的最高剂量。
3.2 理论分析和多项式拟合数值处理
根据辐照灭菌的基本理论和假设,初始含菌量为N0的任何一种微生物,吸收剂量D后剩余含菌量N的关系为:
(1)
式中,D10为微生物减少90%所需要的剂量,kGy。对于实际产品,其所含的菌往往有多种,可根据不同辐照抗性微生物的含量确定上述关系[1],如ISO11137-2中给出的标准抗性分布(SDR)列于表3。

表1 辐照前样品菌落总数Table 1 Total numbers of colony of Samples before irradiation
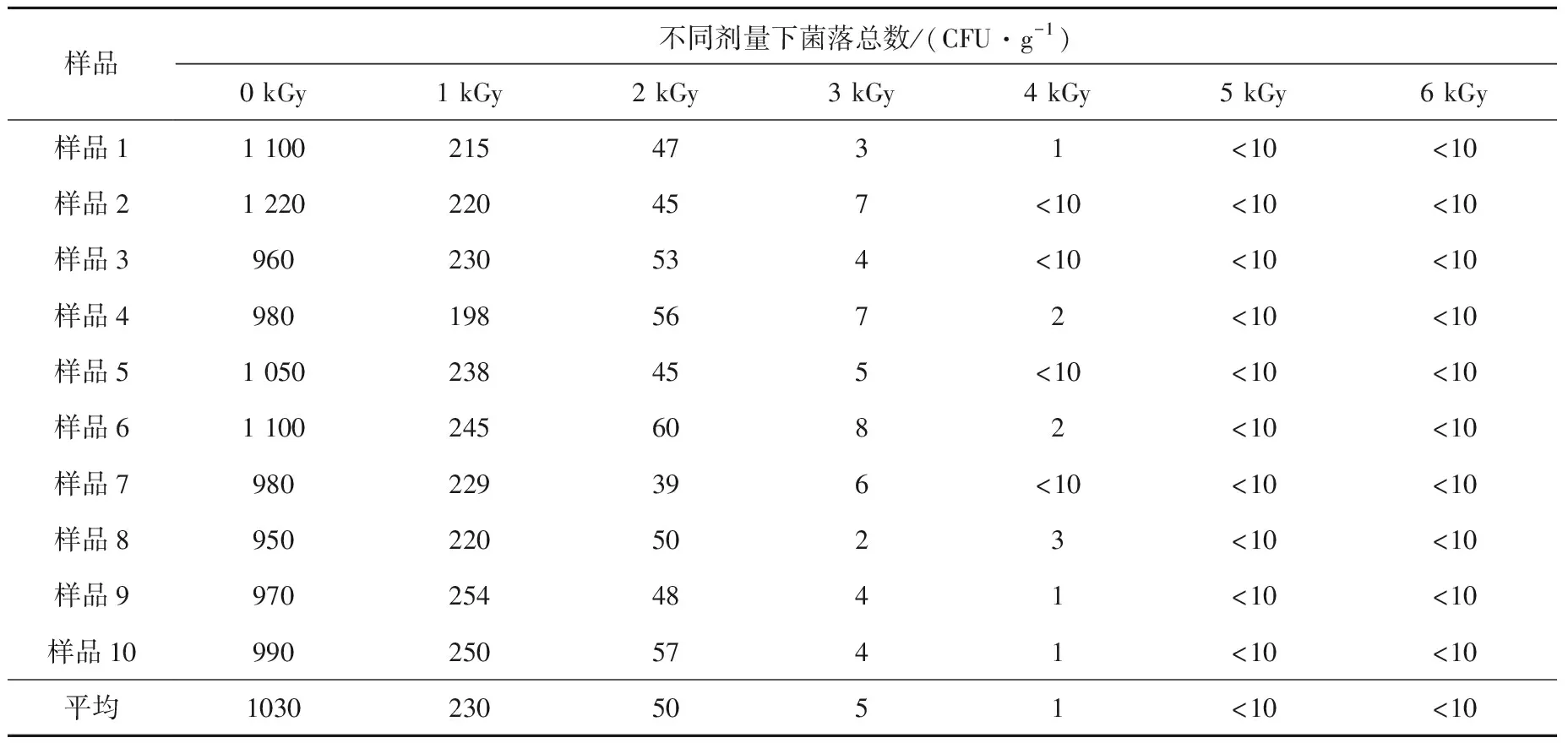
表2 不同剂量辐照后样品菌落总数Table 2 Total numbers of colony of samples after irradiation by different dose
注:菌落总数<10 CFU·g-1为实验室微生物表达方式,实际值为0。

表3 标准抗性分布Table 3 Standard distribution of resistance
假定p(i)为第i种微生物的比例,D10(i)为第i种微生物的D10值,由公式(1)可得到混合菌群的关系式:
(2)
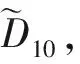
(3)
即,
(4)
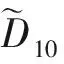
合,结果示于图1。
由图1结果可见,3次和4次多项式拟合结果较好,而5次和6次多项式拟合在剩余微生物接近0的附近发生了错误趋势,说明不能采用5次以上的多项式进行拟合,与文献[11]的结论不同。究其原因可能是文献[11]的剂量范围设定较大,而本文研究的食品药品辐照中,剂量范围要小很多,因此在剂量测量精度范围内,阶梯辐照的取点较少。较少的取点可大大减少设定剂量的工作量,对于辐照加工的实用性具有意义。
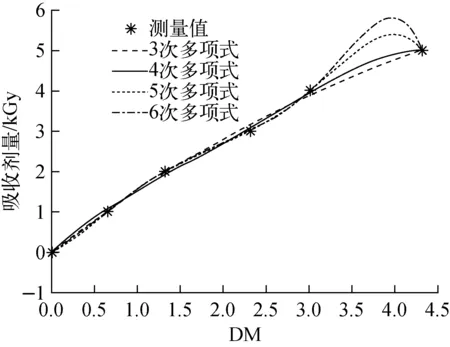
图1 DM-D多项式拟合Fig.1 DM-D Polynomial fitting
3次、4次多项式拟合所得的系数列于表4。根据拟合上述3次和4次多项式,该产品从平均1 030 CFU/g辐照降至1 CFU/g所需的剂量分别为3.88 kGy和3.94 kGy。
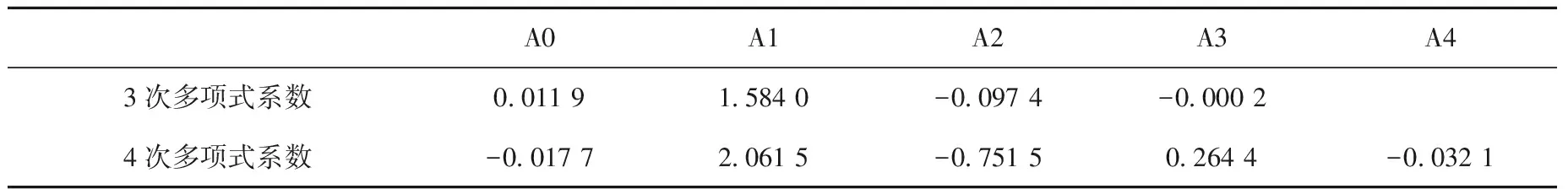
表4 多项式拟合系数Table 4 Coefficient of Polynomial fitting
根据ISO11137标准给出的微生物标准抗性分布,由表3和公式(2)可以得出微生物含量从1 030 CFU/g降至1 CFU/g以下需要的辐照剂量为5.33 kGy。可见根据拟合所得剂量比按照标准抗性所得剂量要降低约1.4 kGy。
该产品不同时期四个批次的产品,取样品根据拟合参数设定的辐照剂量,照射后的微生物检测结果列于表5,辐照剂量设定采用4次多项式拟合系数,由表5数据可见,辐照后产品菌落总数全部符合要求。
在辐照加工的实践过程中,对生产厂家没有指定辐照剂量的情况下,采用文中所述方法,都取得了较好的效果。任一产品初始污染菌的情况会每季度监测至少一次,对于可能导致初始污染菌发生较大变化的因素,如生产厂家的原料来源有重大变化,也会要求生产厂家说明情况,开展针对性监测。通过这种定期监测和针对性监测,可有效保证对微生物污染水平的掌握,同时积累该产品的污染菌数据库,对于超出原拟合参数范围的情况,则进行辐照实验并重新拟合关系式。
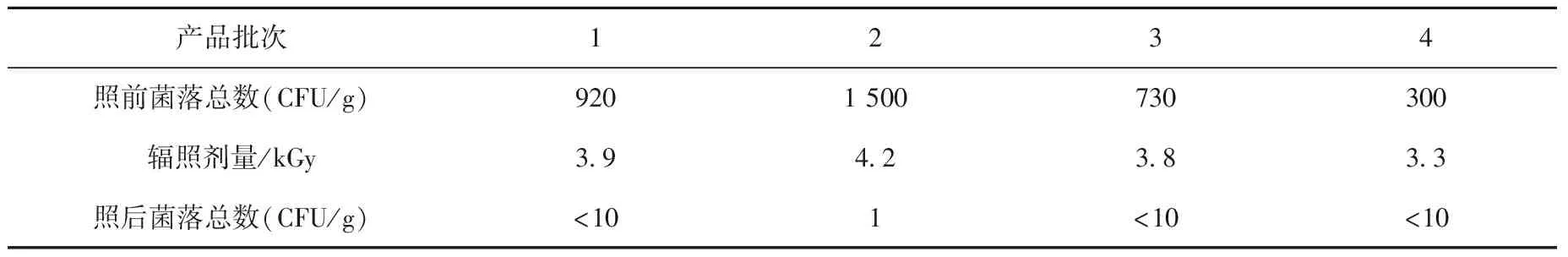
表5 辐照验证结果Table 5 Results of irradiation Test
4 结论
本文所述方法经辐照实践证明可达到灭菌要求并且可有效降低辐照剂量。多项式拟合确定辐照剂量的方法对于多菌种的情况是一种较好的方法,但拟合次数需要根据实际情况而定,对于食品等非医疗用品杀菌的辐照加工应采用3次或者4次多项式拟合。和医疗用品辐照标准ISO11137-2中的SDR抗性相比,在实践中发现食品、药品中微生物的抗性普遍比SDR小,采用SDR作为辐照抗性,偏保守。
