基于“学习进阶”的初中化学教学设计
2019-08-27梁荣君
梁荣君

摘要: 针对教学实践中的问题,结合学习进阶基本要素进行教学设计;按能力层面设定宏观、微观和符号三个认知层面进阶维度;通过对各层级进阶水平、预估目标和评估方式的阐述,分析学习进阶路径图,得出学习是螺旋上升的过程。在这过程中促成核心知识的落实和进阶目标的达成。
关键词: 学习进阶; 化学方程式; 质量守恒定律; 教学设计; 初中化学 文章编号: 10056629(2019)6004407 中图分类号: G6338 文献标识码: B
提高每一个学生的科学素养是科学课程的核心理念[1]。纵观初中科学的知识体系,浙教版《科学》八年级下册第三章第3节“化学方程式”包括“质量守恒定律”、“化学方程式”和“依据化学方程式进行计算”。在“质量守恒定律”部分注重宏观实验现象和微观本质分析,而“化学方程式”和“依据化学方程式进行计算”这两个部分以符号作为化学语言,融合宏观、微观层面,开始从符号表征的角度去认识化学反应过程,因此这节内容是初中化学中的核心知识内容。
然而,在教学实践中却存在一些問题,主要体现在以下几个方面: (1)教学开始时忽略学生已有知识;(2)为了使质量守恒定律的得出具有普遍性,多个实验的呈现缺乏逻辑性,缺少个体到系统思想的渗透和全部反应到具体反应的思维转变;(3)在质量守恒定律内容表述上缺乏完整性;(4)在深化质量守恒定律过渡到化学方程式的书写过程中,对于微观本质的探讨缺乏连贯性,没有将宏观现象和微观本质进行有效融合;(5)依据化学方程式进行计算的教学中,缺乏对宏观、微观和符号三重表征有效整合的理解,将计算过程作为孤立和模式化的过程,导致学生在处理相关问题时缺乏自主和灵活应用能力。
学习进阶是对学生在各学段学习同一主题的概念时所遵循的连贯的、典型的学习路径的描述,一般呈现为围绕核心概念展开的一系列由简单到复杂、相互关联的概念序列[2]。学习进阶基本要素包括进阶起点、进阶终点、进阶维度、多个相互关联的成就水平和各水平预期表现及其评估。其中进阶终点又称为进阶目标;多个相互关联的成就水平表现为进阶起点和各进阶维度内的各层级进阶水平;各水平的预期表现是指在达成较低层级进阶水平后,处于某一层级进阶水平时的应有表现,也可以称为某一进阶水平对应的预估目标。
1 进阶起点分析
进阶起点是指学生在学习新的知识时已有的知识。
在七年级上册第四章已学习过物理变化和化学变化,通过实验和生活中的现象,学生基本上能区分这两种变化。在宏观层面已形成了化学变化和物理变化的根本区别在于有无新物质产生。在八年级下册第三章第一节也已学习过用文字表达式来表示化学反应的过程,学生已基本具备用文字表达式来表示常见化学反应的能力。
在八年级下册第二章中学习了组成物质的元素、表示元素的符号、表示物质的符号等,已形成通过宏观组成、微观构成和符号表征三个维度进行认知的途径。结合这些知识对物理变化中的微观本质作出解释,物质由分子等微粒构成,多个分子等微粒的质量之和表现为宏观物质的质量。既然物理变化中分子种类和数量不变,那么宏观物质的质量也不变,即物理变化的过程中,所有物质的质量保持不变,那么化学变化中各物质总质量如何变化?从物质能量观角度而言,在化学变化中能量会发生变化,那么总质量是否会发生变化?
2 进阶目标确定
当将学习进阶应用到较长时段时,进阶目标表现为课程目标。当将学习进阶应用于一节内容教学时,进阶目标则表现为课程标准中对应内容的目标和教学目标,因此进阶目标是基于《初中科学课程标准》[3]、《科学教学参考书》[4]中关于实验探究和该节内容的相关要求进行确定。
3 进阶维度设定
进阶维度是学习进阶的内容维度[5]。内容可以是知识也可以是能力。将学习进阶应用到“化学方程式”一节内容时,知识层面的核心概念包括质量守恒定律、化学方程式的书写以及化学方程式的应用;能力层面则表现为从宏观、微观和符号不同的视角去认知化学反应的过程。知识和能力有一定的对应关系。
一般地,都以知识内容作为进阶维度和各层级进阶水平划分的依据。但由于化学最重要的特征是利用宏观、微观和符号三重表征知识,同时在上述进阶起点分析中已知学生已形成从宏观、微观和符号三个视角去认知具体的物质,因此在本节内容的教学中,进阶维度设定为宏观认知层面、微观认知层面和符号认知层面。教学设计过程是在具体进阶维度中按照认知特点分为若干层级的进阶水平逐级进阶的过程。由于进阶维度的设定是基于能力层面的,因此各层级进阶水平的设定也是与能力水平相对应的阶段。
4 各维度进阶水平及其预估目标和具体评估方式阐述
4.1 宏观认知层面
这一维度对应的知识内容主要包括利用实验得出质量守恒定律的完整表述的过程。按照教学进程将这一维度分成四个层级的进阶水平。
4.1.1 层级11: 定性感知阶段
这一阶段是教学的起始阶段,从具体的化学反应入手,感知化学反应中的质量变化问题。教师展示“木头燃烧后留下灰烬”和“铁钉生锈后外表附有厚厚的铁锈”两组实验并设问: “这两组图片展示的是什么变化过程?其反应物分别是什么?质量如何变化?”。学生通过问题的思考和回答能辨别常见的化学反应并对反应物及其质量的变化有了定性的感知。
教师追问: “反应物的质量减少了,那生成物的质量呢?反应前后的总质量呢?”“用什么实验方法能准确比较出化学反应前后物质的质量变化情况?”此时,教师引导学生通过实验的方法测定化学反应前后物质的质量变化情况。
4.1.2 层级12: 间接定性比较阶段
在层级1进阶水平的基础上,学生设计简单的实验方案测定实验“木头燃烧后留下灰烬”中参加反应物的质量变化。通过先测定反应物和生成物的质量,反应物是木头和氧气,生成物是灰烬和二氧化碳气体。但氧气和二氧化碳的质量比较难测定,因此遵循实验可操作原则重新选择具体的化学反应。最后确定氢氧化钠溶液和硫酸铜溶液反应、过氧化氢制取氧气、白磷燃烧三个实验作为具体化学反应进行探究。
利用如图1所示装置,反应前将锥形瓶和滴管置于天平左盘,调节天平平衡,将滴管内的氢氧化钠溶液滴入锥形瓶内,使两种液体混合,观察到产生了蓝色沉淀确定已经发生化学反应,再次观察天平是否平衡,判断反应前后质量变化情况。由于该实验通过天平是否平衡来确定总质量是否改变,不涉及具体的“量”,因此这一实验涉及的实验方法为间接定性比较的方法。
由于该实验中不会有气体进入或离开反应系统,是封闭型化学反应。实验过程中封闭型化学反应无需密封实验装置即可对反应前后的质量进行比较。过氧化氢制取氧气和红磷燃烧的实验中有气体进入或离开反应系统,是开放型化学反应。开放型化学反应利用上述实验装置探究反应前后质量变化情况时应对锥形瓶进行密封。在过氧化氢制取氧气的实验中由于气体的产生会使瓶内气压增大,可能会导致瓶塞冲出,造成实验误差并具有危险性。因此,對于封闭型化学反应利用该实验装置比较化学反应前后质量的变化是准确的,而对于开放型化学反应则会有较大的误差。
4.1.3 层级13: 实验修正并向定量测定转变阶段
过氧化氢制取氧气的实验中由于气压增大导致瓶塞冲出,可逐步对实验装置进行修正减少误差,具体修正过程如图2所示。经过修正发现活塞处摩擦不可避免,因此对实验装置进行修改: 利用精确的电子秤变间接定性比较为直接定量测定。直接定量测定的操作步骤为,首先分别称出反应容器和反应物总质量及集气瓶的质量,然后打开分液漏斗的阀门,通过排水法收集氧气,最后重新称出反应容器和剩余反应物总质量及收集满气体集气瓶的质量,进行数据分析比较。
根据具体的化学反应,通过对实验中误差和不足的分析,有针对性地对实验装置逐步进行修正,促进学生分析和自主思考能力的提升,是发展宏观辨识能力的体现。
4.1.4 层级14: 思维突破阶段
通过上述各进阶水平的达成,学生已经知道在化学反应中,反应前后物质的总质量不变的结论,但对于定律中“参与化学变化”这一难点还未突破。于是采用思维探究的方式,通过教师与学生的双边思维活动进行难点突破。
以红磷燃烧的实验为例,在通过实验得出了红磷燃烧前后质量不变之后,设置问题: “红磷燃烧的实验中是不是所有的物质都发生了反应?”“是不是可以认为发生反应的物质和生成的物质的质量相等?如何证明?”。通过对一系列问题的思考以及教师的指引和讲解,得知若反应物全部反应了,那么生成物增加的质量一定和反应物减少的质量相等;若反应物部分反应了,由于未反应物质的质量不变,那么生成物增加的质量也应和反应物减少的质量相等。于是就可以确定质量守恒定律的适用范围应是“在化学反应中,参加化学反应的各物质”。这一维度中各层级进阶水平、预估目标和具体评估方式如表1所示。
这一进阶维度对应的知识内容为质量守恒定律微观本质的解释及其理解,表现为三个层级的进阶水平。
4.2.1 层级21: 宏观向微观认知过渡阶段
此时已经确定质量守恒定律的内容及其适用范围。根据进阶起点,已经知道化学反应的实质在宏观层面是产生新物质,从微观层面而言是分子变成原子,原子重新组合成分子的过程。化学反应前后物质的总质量保持不变是宏观现象,由于物质由微观粒子构成,因此可以通过微观认知视角对宏观现象进行解释。
如图3是红磷燃烧微观示意图,让学生进行思考与讨论: 红磷燃烧前后磷原子和氧原子的数目在反应前后分别为多少个?如何变化?可得出化学反应的过程是原子重新组合成分子的过程,这一过程分子种类一定改变,而原子的种类和数目则不变。如图4是过氧化氢制氧气微观模型图,让学生思考化学反应前后微观粒子的变化情况。通过思考从微观角度突破质量守恒定律中关于“参与化学变化”这一难点。
4.2.2 层级22: 微观向宏观认知反馈阶段
质量守恒定律实质上是对质量变化规律的文字表述,从实验角度证明这一规律是宏观表征的体现,而对其进行微观解释则是微观表征的体现,因此在理解微观本质的基础上,更要知道微观和宏观表征的对应之处。依据进阶起点物质由元素组成,元素是指质子数相同的一类原子的总称,因此物质从宏观角度而言由元素组成,从微观角度而言由分子或原子构成。结合图3和图4进行思考,在红磷燃烧和过氧化氢制取氧气的实验中,反应物和生成物分别由哪些元素组成?在化学反应前后元素种类和生成物质量发生怎样的改变?
4.2.3 层级23: 微观和宏观认知融合阶段 认识化学反应的过程是“宏观微观宏观”的过程,因此对于质量守恒定律的进一步理解应体现在宏观和微观认知视角的相互融合上。结合具体实验,通过分析建立学生认知转变图(如图5所示),体现学生从“物质改变”到“元素守恒”这一宏观认知的提升。
因此,化学反应中的“变化”,从实验这一宏观现象出发表现为反应物及其状态等实验现象的变化得出物质种类的变化;其微观本质则是分子变成原子,原子重新组合形成新的分子,导致“守恒”这一结果的出现;宏观表征为质量不变和元素守恒,微观表征为原子种类和数目的不变。通过双重认知视角的融合,学生充分理解了质量守恒定律中的变化和守恒的辩证关系,也是平衡思想和变化观念的具体表现,更体现了微观探析能力。这一维度中各层级进阶水平、预估目标和具体评估方式如表2所示。
4.3 符号认知层面
化学符号是化学语言,也是化学学科特有的一种表征方式,学生从宏观和微观视角认知化学反应后,在建立模型的基础上,通过符号对物质进行表征是必然结果,因此化学反应过程也应体现在符号认知层面上,这一维度对应的知识内容是化学方程式及其应用,其进阶水平表现为四个层级。
4.3.1 层级31: 符号定性表征反应阶段 化学反应的文字表达式是对化学反应过程的定性表达。结合表示物质的化学式,让学生写出“红磷燃烧”、“过氧化氢制取氧气”的化学表达式。
4.3.2 层级32: 符号定量表征反应阶段
质量守恒定律是对化学反应过程的定量描述。在学生能写出表达式的基础上,结合质量守恒定律将表达式转化为定量表达是必然结果。
由于宏观物质和符号是对应的,再结合微观层面各层级进阶水平的达成,在化学式前填上合适的计量数可以达到表征反应前后原子数量相等的目的,因此让学生尝试在“红磷燃烧”的化学表达式中的化学式前面填上合适的计量数使表达式满足质量守恒定律。这一过程称为配平,此时将表达式中的“→”改为“”,再在符号上方添加反应条件,该表达式更名为化学方程式。学生完成“过氧化氢制取氧气”的化学方程式,结合学生书写情况,确定书写化学方程式的具体步骤和书写原则。
4.3.3 层级33: 宏微结合理解符号阶段
在熟练掌握化学方程式的书写后,在回顾化学式意义的基础上,尝试回答化学方程式的意义。以红磷燃烧的化学方程式为例,定性宏观层面表示反应物是红磷和氧气,生成物是五氧化二磷,反应条件为点燃;定量微觀层面表示4个磷原子和5个氧分子结合变为2个五氧化二磷分子,此时提示学生将具体的数量关系转变为比例关系,即在这一化学反应中磷原子、氧气分子和五氧化二磷分子之比为4∶5∶2;再以化学式对应的相对原子质量或相对分子质量引导学生得出这一化学反应中磷原子、氧气分子和五氧化二磷分子的相对分子质量之比为31∶40∶71;最后引导学生理解从宏观定量层面而言,这一化学反应中各物质的质量之比为31∶40∶71。
上述具体例子说明,实现从宏观定性→微观定量→微观比例关系→宏观比例关系→宏观定量的转变,宏观和微观相结合达到了理解化学方程式的目的。
4.3.4 层级34: 三重表征初步整合阶段
用符号将化学反应的宏观和微观表征进行有效整合,是“三重表征”的体现,也是从三个视角去认知反应的过程。
学习知识是为了解决实际问题。在生产和科学研究中,对于化学反应常常要分析清楚各物质间的质量关系。如选取例题“实验室用分解过氧化氢的方法制取氧气。现要制得2克氧气,需要多少克过氧化氢?”结合例子讲解确定根据化学方程式计算的步骤。依据化学方程式进行计算是实际应用的一种方式,具体体现在对化学方程式的理解上。其他更多的实际问题要求学生在了解三重表征的基础上,从三个认知视角去解决。如:
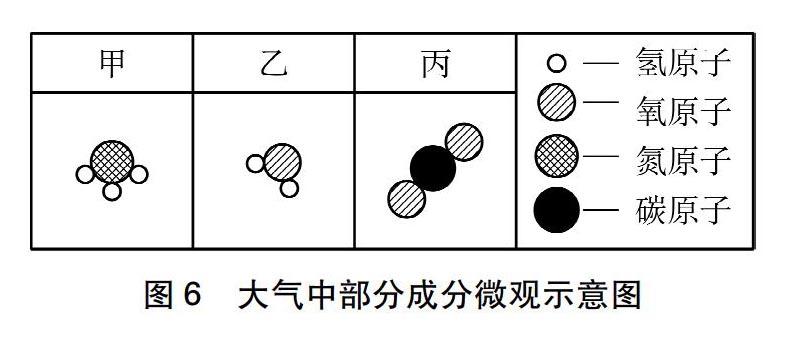
地球大气演化经历了原始大气、次生大气和现代大气三个阶段,次生大气中部分成分的微观示意图如图6所示,一定条件下,3.4g甲物质和4.8g氧气恰好完全反应,生成5.4g乙物质和另一种物质X,下列判断不正确的是( )。
A物质甲的化学式是NH3
B物质X的质量为2.8g
C 物质X中含两种元素
D 该反应的化学方程式中物质X与O2的化学计量数之比为2∶3[6]
在求解这一题目的时候学生要懂得灵活地选择认知视角和表征方式,A选项是微观和符号表征的结合;B选项则要通过对微观模型和宏观质量关系得出宏观结果,是微观和宏观表征的结合;C选项则是符号和微观表征的结合;D选项则是宏观、微观和符号三重表征整合的结果。
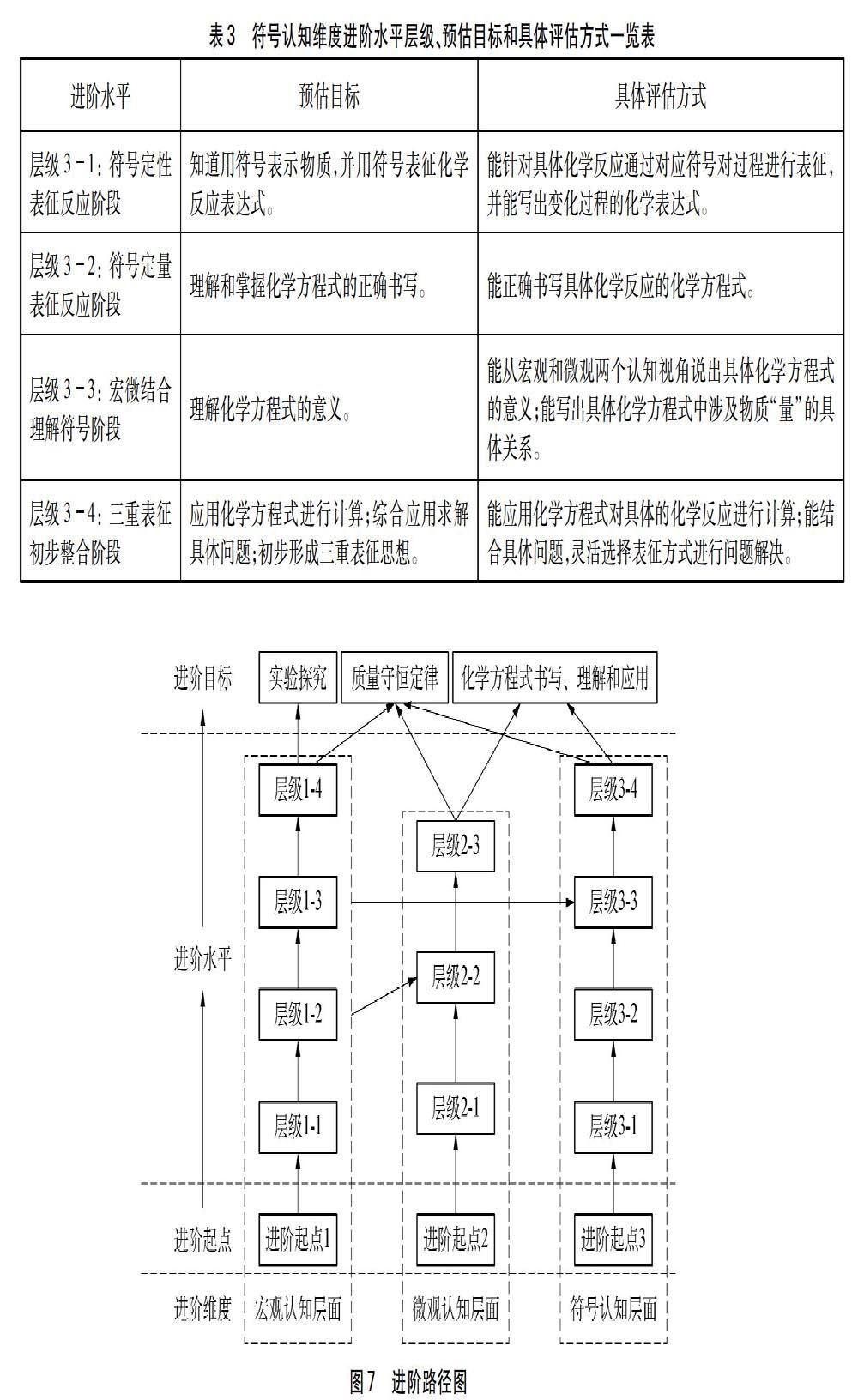
因此,在具体的问题中学生应懂得选择合适的认知视角和表征方式去解决实际问题,这就要求学生需形成“三重表征”的思想,从而达成进阶目标。这一维度中各层级进阶水平、预估目标和具体评估方式如表3所示。
5 进阶路径图及其说明
综上,“化学方程式”具体学习进阶路径如图7所示。
在教学的进程中,各进阶维度所达成的各层级进阶水平是独立的,较低层级进阶水平是较高层级进阶水平的基础,随着每个层级进阶水平的达成促成进阶目标的达成。具体的进阶目标落脚于具体的知识,这体现在进阶路径图的纵向进程上,可以认为各进阶维度之间是并列的关系。但进阶维度的某些层级进阶水平与其他维度的某些层级进阶水平是关联的,如层级22(微观向宏观认知反馈阶段)即以层级21(宏观向微观认知过渡阶段)为基础,也涉及到宏观认知层面这一维度;再如层级34(三重表征初步整合阶段)的达成即涉及同维度低层级进阶水平的达成,也涉及到宏观和微观认知层面这两个进阶维度等等,这体现在进阶路径图的横向进程上,可以认为各进阶维度之间是交叉关系的;然而作为化学知识特有的三种表征方式,从学生的认知角度而言,首先接触的是宏观认知层面及其相关表征,再深入到微观认知层面及其相关表征,最后通过构建模型建立符号去认识化学知识并进行相关表征,可以认为各进阶维度之间是递进关系的。因此,学生学习的过程是通过进阶路径图中各层级进阶水平的达成螺旋上升的过程。
总之,“化学方程式”作为初中科学中核心的化学知识,也是学生定量认知化学变化的开始,在整个知识体系的构建中起着重要的作用。另者,就学习进阶而言,进阶目标的达成是本节教学的终点,也是新的教学的进阶起点,如宏观辨识与微观探析能力、“三重表征”思想、守恒观的初步形成等等均要通过更高一级的学习再逐级进阶。
参考文献:
[1][3] 中华人民共和国教育部制定. 义务教育科学课程标准[S]. 北京: 北京师范大学出版社, 2012: 5, 14, 33.
[2] 刘晟, 刘恩山. 学习进阶: 关注认知发展和生活经验[J]. 教育学报. 2012, (4): 81.
[4] 朱清时. 科学教学参考书(八年级下册)[M]. 杭州: 浙江教育出版社, 2014: 80.
[5] 杨云霞. 学习进阶的研究现状[J]. 科教导刊, 2018, (8): 3.
[6] 陈继清. 质量守恒定律考点例谈[J]. 中学化学, 2017, (2): 21.
