电感耦合等离子体质谱法测定高钙片中铅、砷、铬和镉含量的不确定度评定
2019-08-27闫顺华王秀霞严娅沙拉麦提艾力
闫顺华,王秀霞,严娅,沙拉麦提·艾力
(新疆维吾尔自治区食品药品检验所,新疆 乌鲁木齐 830004)
随着经济的发展,人们对保健食品的需求日益增加,补钙类保健食品原料多以海产动物鲜骨、水产贝壳等构成,由于动物的饮食及海洋污染等原因,导致此类产品摄取、沉积重金属较多,原材料的污染导致了其产品的重金属元素超标,这些有毒有害元素被人体摄取后,会和体内蛋白质结合,影响人体正常代谢,最终伤害神经、肝、肾等组织。测量不确定度是目前国际上普遍接受和推荐使用的定量说明检测结果质量的参数,能够客观地评价检测结果的准确性和可靠性。在保健食品国家风险监测任务中,铅、砷、汞是日常检测指标,铬、镉检测的相对较少。本试验采用电感耦合等离子体质谱法同时测定铅、砷、铬、镉4 种元素,能够极大的提高检验效率,并依据JJF 1135-2005《化学分析测量不确定度评定》[1]和JJF 1059.1-2012《测量不确定度评定与表示》[2],按照国家新颁布的GB 5009.268-2016《食品安全国家标准食品中多元素的测定》[3]中的电感耦合等离子体质谱法(inductively couple plasma mass spectrometer,ICP-MS),分析检测过程中影响不确定度的因素,并对不确定度进行评估,如实反映检测结果的置信度和准确度[4-8],为保健食品国家安全性评价提供有力的技术支撑。
1 材料与方法
1.1 主要仪器与试剂
ICAP Q 型电感耦合等离子体质谱仪(ICP-MS):Thermo Fisher Scientific 公司;Mettler Toledo AE240 型万分之一分析天平:梅特勒-托利多仪器(上海)有限公司;Multiwave PRO 型微波消解仪:奥地利安东帕公司;DTK-型控温电热板:湖南金蓉园仪器设备有限公司;所用玻璃量器均为A 级。
ICP-MS 分析用多元素标准溶液:100 μg/mL,国家有色金属及电子材料分析测试中心;硝酸:优级纯,德国Merck 公司。
高钙片:国家认监委提供的能力验证样品。
1.2 标准溶液的配制
1.2.1 标准储备液的配制
用1 mL 单标线吸量管准确吸取1.0 mL ICP-MS分析用多元素标准溶液于10 mL 容量瓶中,用3%的硝酸定容至刻度,得到浓度为10 μg/mL 的混合标准储备液。
1.2.2 标准中间液的配制
用1 mL 单标线吸量管准确吸取1.0 mL 混合标准储备液至100 mL 容量瓶中,用3%的硝酸定容至刻度,摇匀,得到浓度为100 ng/mL 的混合标准中间液。
1.2.3 标准工作液的配制
分别移取 0.50、1.00、2.00、3.00、4.00 mL 和 5.00 mL标准中间液至6 个10 mL 容量瓶中,用3%的硝酸定容至刻度,摇匀,得到质量浓度为 5.0、10.0、20.0、30.0、40.0 ng/mL 和50.0 ng/mL 的混合标准工作溶液系列。
1.3 样品前处理
称取0.25 g(精确至0.000 1 g)高钙片样品于微波消解管内,加硝酸6.0 mL 浸泡过液;加2.0 mL 过氧化氢,然后将其放在微波消解仪中按微波消解程序(见表1)进行消解,直至消化液呈无色透明,冷却后取出,缓慢打开罐盖排气,用少量水冲洗内盖,将消解管放在控温电热板上于160 ℃加热2 h 进行赶酸。放冷,用滴管将试样消化液洗入25 mL 容量瓶中,用超纯水少量多次洗涤消解管,洗液合并于容量瓶中并定容至刻度,混匀备用,同时做试剂空白。

表1 微波消解程序Table 1 Microwave digestion program
1.4 加标样品制备
平行称取6 份阴性钙片样品,每份0.25 g(精确至0.000 1 g)置于25 mL 具塞磨口离心管中,分别加入35 μL 10 μg/mL 的混合标准中间液,其余步骤同1.3样品前处理。
1.5 ICP-MS工作条件
射频功率:1.55 kW;采样深度:10 mm;等离子气流量:15.0 L/min;载气流速:0.8 L/min;雾化室温度:2 ℃;氦碰撞模式:泵速 40 r/min;测量点数/峰:3;数据采样模式:跳峰采集;重复次数:3。测定时选取的同位素为208Pb、75As、52Cr、111Cd,同时选用209Bi、72Ge、115In 作为内标元素,并让系统自动进行匹配待测元素,以监控和校正信号的漂移,有效消除基体性干扰。
1.6 数学模型
标准工作溶液系列经ICP-MS 分析,以待测元素的浓度(ng/mL)为横坐标,离子强度响应值(cps)为纵坐标绘制标准曲线。待测样品用同样的方法分析后,将样品的离子强度响应值代入标准曲线,计算得到样品中各元素的浓度。计算公式为:

式中:X 为样品中待测元素的含量,mg/kg;c 为样品中待测元素的浓度,ng/mL;V 为样品消化后的定容体积,mL;m 为样品的称取质量,g。
1.7 不确定度的来源分析
从样品的检测过程,分析不确定度的来源,用图1所示的因果图表示如下。
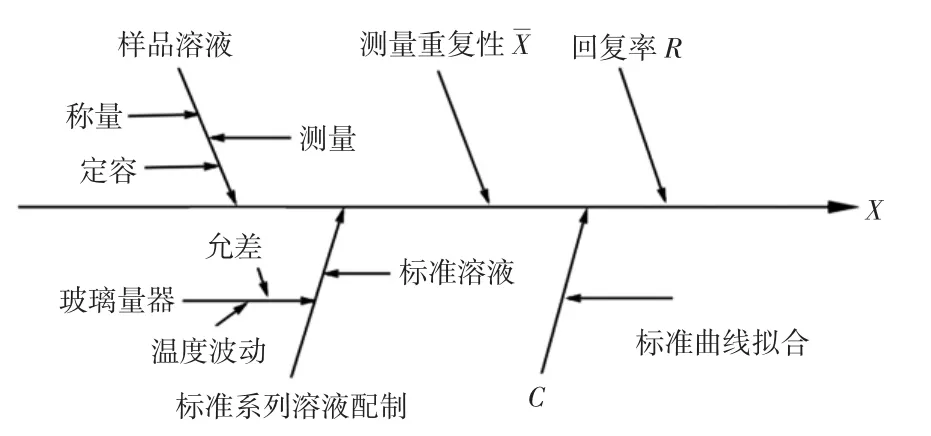
图1 ICP-MS 测定高钙片中Pb、As、Cr 和Cd 含量的不确定来源因果图Fig.1 Uncertainty sources for determination of Pb,As,Cr and Cd in high calcium tablets with ICP-MS
2 结果与分析
2.1 样品溶液制备及测量过程引入的不确定度分量
2.1.1 样品称量引入的相对标准不确定度u(rW样)
查万分之一天平的检定证书,在10 mg≤m≤50 g 的称量范围内,其最大允许误差为0.5 mg(即0.000 5 g),假定为均匀分布实际称取样品质量的平均值则:

相对标准不确定度为:

2.1.2 样品溶液定容引入的相对标准不确定度ur(W样)
25 mL 容量瓶(A 级)的不确定度主要由容量允差及温度影响引入。查JJG196-2006《常用玻璃量器检定规程》[9]得,A 级 25 mL 容量瓶的允差为±0.03 mL,按均匀分布估算,则:

实验室温度为25 ℃,容量瓶校准时温度为20 ℃,由于液体的体积膨胀明显大于容量瓶的体积膨胀,可只考虑液体的体积膨胀,认为供试液的体积膨胀系数与水近似,水的体积膨胀系数为0.000 21 ℃-1,因此产生体积变化的半宽为:25 mL×0.000 21 ℃-1×5 ℃=0.026 3 mL,假设体积变化为均匀分布,则:

2.1.3 ICP-MS 引入的相对标准不确定度ur(E)
查所使用ICP-MS 的校准证书,该仪器的测量重复性即相对标准偏差(relative standard deviation ,RSD)为1.1%,按均匀分布,则ICP-MS 引入的相对标准不确定度为:

按1.3 样品前处理方法,平行制备10 份待测样品溶液,测量数据及计算结果见表2。

表2 样品溶液测量数据Table 2 Results for the determination of samples

续表2 样品溶液测量数据Continue table 2 Results for the determination of samples
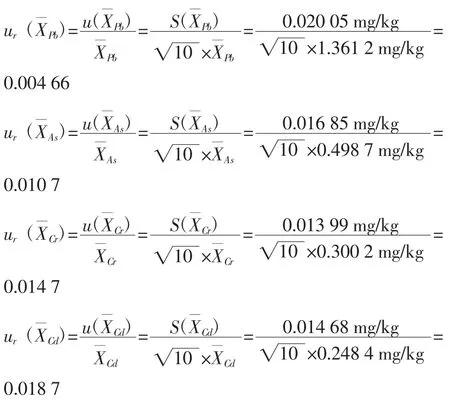
2.1.5 方法回收率引入的相对标准不确定度ur(R)
由于待测样品在前处理过程中受样品性质和基质效应等的影响,会引起样品中的待测元素不能100%的进入测定液中,该过程引入的不确定度可以通过加标回收试验进行评估[10-12]。对1.4 制备的加标样品进行测定,将平均回收率、标准偏差S(R)结果分别代入公式计算回收率引入的相对标准不确定度。根据统计学t 方法检验,按公式计算,判断偏差是否显著。计算结果均见表3。
当置信度为95%,n-1=5,查t 值临界值分布表,发现Pb、Cr 和Cd 的t 值均大于双边临界值t(0.05,5)=2.571,回收率与100%具有显著性,回收率需要带入公式(1)修正这3 种元素的测量结果。

表3 加标回收率结果Table 3 Results of recovery
2.2 标准物质溶液引入的不确定度分量
2.2.1 标准物质引入的相对标准不确定度u(rP对)
查多元素标准溶液证书,知其扩展不确定为1.4 μg/mL,按均匀分布考虑,则标准溶液引入的标准不确定度为:

相对标准不确定度为:

2.2.2 标准溶液配制过程使用玻璃量器引入的相对标准不确定度ur(V对)
标准溶液配制过程中,用1 mL 和5 mL 刻度吸管分别移取 0.5 mL 和 4 mL 液体各 1 次,使用 1、2、3 mL和5 mL 单标线吸量管各1 次,100 mL 容量瓶1 次,10 mL 容量瓶6 次。根据JJG196-2006《常用玻璃量器检定规程》要求,按照均匀分布处理,则玻璃器具及温度波动引入的不确定度如表4所示。
单标线吸量管则标准溶液配制过程中所使用的玻璃量器引入的相对标准不确定度为:


表4 标准系列溶液配制过程玻璃量器引入的不确定度Table 4 Relative standard uncertainty from working glass container in standard solution preparation
2.2.3 标准曲线拟合引入的不确定度ur(C)
用ICP-MS 分别对标准工作溶液系列进行测定,每个浓度重复测定2 次,对测定数据进行拟合得到形式Ai=aCi+b 的线性回归方程,其中Ai为强度响应值,Ci为相对应的浓度值,a 为拟合曲线的斜率,b 为截距。4 种元素的线性回归方程分别为Pb:A = 84 862.428 1C + 153 605.751 3,R2= 0.997 6;As:A = 6 611.580 7C + 7 345.714 7,R2= 0.999 4;Cr:A= 52 099.537 6C + 36 986.609 5,R2= 0.999 6;Cd:A = 76 274.748 7C+55 348.730 5,R2=0.996 7。标准工作溶液系列测定数据如表5所示。

表5 标准曲线数据Table 5 Results of standard curves
根据表2测得的样品溶液中 Pb、As、Cr 和 Cd 质量浓度的平均值,计算由标准曲线拟合产生的标准不确定度为:

式中:SR 为标准溶液响应强度值残差的标准差,根据稀释所得的系列标准溶液浓度C,利用标准曲线求得响应强度值的理论值Ai,计算实际测得的响应强度值 A实i的残差 A实i-Ai=A实i-(aCi+b),则SR=为标准溶液测定次数,n=2×6=12;a 为拟合曲线的斜率;P 为样品溶液的重复测定次数,P=10;C实i为标准工作溶液系列的实测质量浓度,ng/mL;为标准工作溶液系列质量浓度的平均值为测得的样品溶液质量浓度的平均值,ng/mL。将相关数据代入公式(2),计算标准曲线引入的相对标准不确定如表6所示。
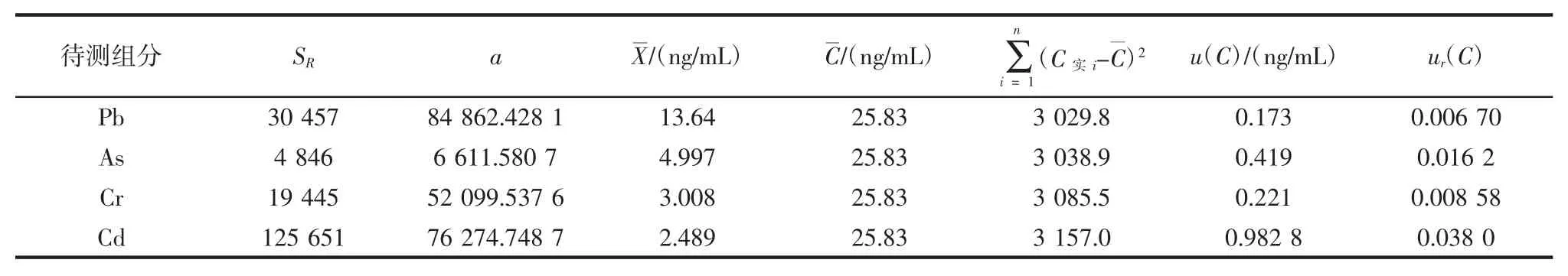
表6 标准曲线拟合引入的相对标准不确定度Table 6 Relative standard uncertainty from standard curve fitting
2.3 不确定度的合成
2.3.1 相对标准不确定度的合成
4 种元素的相对不确定分量见表7。

表7 各不确定度分量Table 7 The uncertainty values
2.3.2 扩展不确定度及结果表示
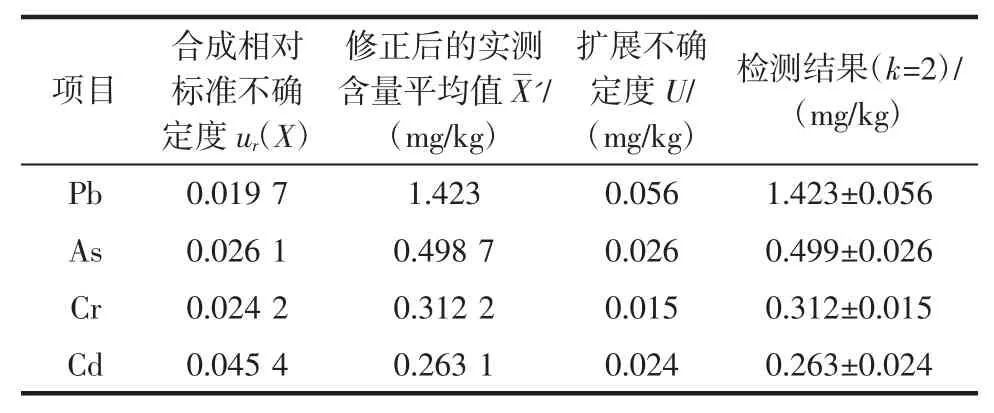
表8 不确定度评定结果Table 8 The uncertainty values
3 结论
试验过程中,称量、提取、仪器测定等过程均会引入不确定度。通过分析发现,标准溶液配制、标准曲线拟合、测量重复性对不确定度的贡献比较大。本试验中的元素测定属于痕量分析,可以通过选择合适的消解程序及赶酸条件、当仪器的灵敏度发生变化时要及时进行标准曲线的校正、保证样品溶液和标准溶液的基体匹配、不断提高检测人员的操作水平和熟练程度等途径降低方法的不确定度,保证测定结果的准确性[13-15]。
