响应面法优化党参多糖硒酸酯的制备工艺
2019-08-27舒畅夏洁袁帅张西锋鄢又玉
舒畅,夏洁,袁帅,张西锋,鄢又玉
(武汉轻工大学生物与制药工程学院,湖北武汉430023)
党参是我国经常使用的传统补益中药之一,又名中灵草、防风党参、黄参等。《中国药典》2015版(一部)中规定其为桔梗科植物党参、川党参或素花党参的干燥根部[1]。近年来,许多研究工作者对党参进行了深入探究,发现它在增强机体免疫力、调理肠胃运动、抗溃疡、降血压、抗缺氧、延缓衰老、抗辐射等方面有较好的治疗效果。党参除了作为药用药材利用之外,还可以作为保健药材,现多用于食疗方面[2]。近几年来,许多研究者对党参的化学成分进行了研究,发现党参所含的化学成分种类繁多[3],主要包括糖类、生物碱类、三萜类、黄酮类、甾体类等多种化合物,其中主要有效成分是党参多糖。党参多糖和其他的植物多糖一样,都具备一定的药理作用,主要有调节机体免疫力、促进造血机能、抗缺氧、调节血糖和血脂代谢、抗氧化等功能[4-5]。
硒元素是一种动植物生命活动所需的微量元素,其主要存在于酶中,例如谷胱甘肽过氧化物酶、硫氧还蛋白还原酶和甲酸脱氢酶[6]。据相关数据统计,全球大约有10亿人可能患有硒摄入不足,并且一些疾病与硒的缺乏有关,如病毒性疾病,心血管硬化,癌症和糖尿病等[7-9]。硒元素主要有无机硒和有机硒两种存在形式[10],相比于无机硒,有机硒的生物利用度相对较高,因为它比较容易在人体消化道中被吸收,并在人体尿液中排泄。目前无机硒有亚硒酸钠和硒酸钠,有机硒主要以硒多糖和硒蛋白的形式存在,无机硒具有蓄积性毒性,而有机硒的毒副作用小,可以更好地发挥硒元素的作用。而天然有机硒多糖在植物和微生物中含量较低,这就使得以硒多糖为主要补硒剂的研究显得更加重要。
多糖硒是由硒元素和多糖经过硒氧键结合在一起的化合物[11]。硒元素具有抗氧化、抗病毒和抗癌等活性,多糖也具有增强机体免疫力、促进造血功能、抗溃疡等作用。这就使多糖硒更好地拥有两者的生理和药理功能,在治疗机体一些疾病时,能更好地发挥其生物活性,达到治疗效果。多糖硒为有机硒化合物,是目前效果优良的补硒剂和免疫反应调节剂之一。党参作为我国传统的补益中药,种植面积广,多糖又是其主要成分且含量高,易制备多糖提取物,使得党参多糖硒的研究越来越具有开发前景。
响应面(response surface methodology,RSM)[12]是一种找到最佳模型的现代统计手段,可以为最佳工艺的探寻提供技术支持。本课题通过响应面法优化合成党参多糖硒酸酯(Codonopsis pilosula polysaccharide selenate,CPPS)的最佳合成工艺,对其进行了结构表征及体外抗氧化活性考察,为硒资源和传统中药的深度开发与利用提供了理论依据。
1 材料与方法
1.1 材料试剂与仪器
党参多糖(Codonopsispilosulapolysaccharide,CPP):武汉轻工大学生物与制药工程学院制药实验室自制,纯度90%以上;硒粉标准品(纯度>99.99%):河南华宇化工原料有限公司;亚硒酸钠、邻苯二胺、正丁醇、三氯乙烷、氨水、无水碳酸钠、无水硫酸钠、抗坏血酸、氯化钡、硫酸、硝酸、甲苯等(均为分析纯):国药集团化学试剂有限公司。
硒储备液(1.0 mg/mL):准确称量50.0 mg硒,置于烧杯中,加入 3 mL混酸(H2SO4∶HNO3=1∶2,体积比),反应至澄清,用蒸馏水定容至50 mL,备用;硒对照品溶液(4 μg/mL):用移液管准确移取1.0 mL硒储备液用蒸馏水定容到250 mL。CPPS样品溶液的配制:分别配制 1.0、2.0、4.0、8.0、10.0 mg/mL 的水溶液备用。
数显恒温水浴搅拌锅(SHJ-6):金坛市亿能实验仪器厂;紫外-可见光分光光度计(Lambda25):美国PerkenElmer公司;pH 计(STARTER 2100):奥豪斯仪器(上海)有限公司;真空干燥箱(DZF-6020):上海新苗医疗器材制造有限公司;低速大容量离心机(TDL-5):上海安亭科学仪器厂;旋转蒸发器(RE52-A):上海亚荣生化仪器厂。
1.2 方法
1.2.1 CPPS的制备
参照文献,采用HNO3-NaSeO3法合成CPPS[13-15]。称取一定质量的CPP粉末置于圆底烧瓶中,加入一定体积分数的稀HNO350 mL,搅拌均匀使多糖全部溶解。加入适量的Na2SeO3和BaCl2。70℃水浴5 h。反应结束后,冷却至25℃,依次加无水Na2CO3调节pH值至 6~7,适量无水 Na2SO4去除 Ba2+,并于 6 000 r/min 转速离心5 min以去除沉淀。将上层清液装入截留分子量3 500 Da的透析袋中,25℃流水透析24 h,然后用超纯水透析清洗12 h。取少量透析液于烧杯中,加入一定量抗坏血酸观察颜色,当溶液无红色时停止透析处理。将透析溶液与3倍体积95%乙醇溶液混合,置于锥形瓶中密封,于4℃冰箱中醇沉12 h后10 000 r/min离心10 min后得到沉淀,即为CPPS。25℃真空干燥24 h后研磨粉碎,即得CPPS粉末。
1.2.2 CPPS中硒含量的测定及硒标准曲线的建立
采用邻苯二胺法[16]测定硒含量。准确称量20.0 mg的CPPS固体,置于50 mL烧杯中,然后加入3 mL混酸,置于95℃水浴锅中消化2 h至澄清后冷却至25℃。另外精密吸取1.1中硒对照品溶液(4 μg/mL)0、1.0、2.0、3.0、4.0、6.0、8.0、10.0、12.0 mL,分别依次加入 25 mL蒸馏水,然后用氨水调节pH值至2,再加入1%的邻苯二胺水溶液2 mL,摇匀,置于具塞锥形瓶中,避光反应2 h,随后转入分液漏斗中,加入9.5 mL甲苯,摇匀,静置萃取分层,取甲苯层定容至10 mL,再从中吸取1 mL稀释1倍,于334 nm测定吸光度。计算CPPS中硒的含量,并作出硒标准曲线[15]。
1.2.3 CPPS合成单因素试验
参照1.2.1方法,设计CCP与Na2SeO3的质量比(X1:1 ∶0.6、1 ∶0.8、1 ∶1.0、1 ∶1.2、1 ∶1.4)、HNO3体积分数(X2:0.2%、0.4%、0.6%、0.8%、1.0%)、反应温度(X3:50、60、70、80、90 ℃)及反应时间(X4:1、3、5、7、9 h)4 个单因素试验,分别找出各单因素最佳反应条件。
1.2.4 响应面优化试验设计
在1.2.3单因素试验的基础上,固定反应时间为5 h,进一步优化3个单因素对CPPS合成的影响,采用三因素三水平的Box-Behnken方法进行设计,并通过Design-Expert 8.0.6.1软件进行数据处理。
1.2.5 CPP和CPPS的结构表征
参照1.2.2中测量CPPS中Se含量的方法,精密称取20 mg CPP和CPPS进行消化,最后在200 nm~600 nm波长范围内进行全波段紫外扫描。采用傅立叶变换红外光谱仪,分别取适量CPP和CPPS粉末与适量KBr混合压片,在4 000 cm-1~500 cm-1范围内进行红外光谱扫描,得到CPP和CPPS红外光谱图。
1.2.6 Fe2+清除能力测定
参考Que等[17]抗氧化活性测定方法,将40 μL 5 mmol FeCl2溶液,80 μL 5 mmol菲啰嗪溶液和 1.08 mL蒸馏水与400 μL 1.1中不同浓度的CPPS样品溶液混合,于 562 nm 处测吸光度。清除率/%=[1-(A1-A2)/A0]×100,式中:A0(蒸馏水代替样品)为对照组吸光度;A1为样品吸光度;A2(蒸馏水代替FeCl2溶液)为样品的本底吸光度。每个样品重复测定3次,结果带入计算清除率后取平均值。
1.2.7 超氧阴离子自由基清除能力测定
参考张越锋等[18]超氧阴离子自由基清除能力测定方法:取1.1中各浓度CPPS溶液300 μL于试管中,加入 Tris-HCl缓冲溶液 900 μL,再加 90 μL 7 mmol/L 的邻苯三酚溶液显色,再加入300 μL 10mol/L盐酸溶液,于 25 ℃反应 20 min。清除率/%=[1-(A1-A2)/A0]×100。(A0用水代替样品;A1为样品吸光度;A2用非极性溶剂无水乙醇替换显色溶液邻苯三酚)于420 nm波长处依次测定吸光度值。每个样品重复测定3次,结果带入计算后取平均值。
2 结果与分析
2.1 硒标准曲线的建立
参照1.2.2设计测定结果,以硒浓度(X,μg/mL)对吸光度(Y)进行线性回归,可知在 0~4.8 μg/mL 浓度范围内,吸光度与硒浓度呈线性关系:Y=0.146 7X+0.006 3(R2=0.999 2)。
2.2 单因素试验
按照1.2.3中单因素设计进行试验,结果如图1所示。
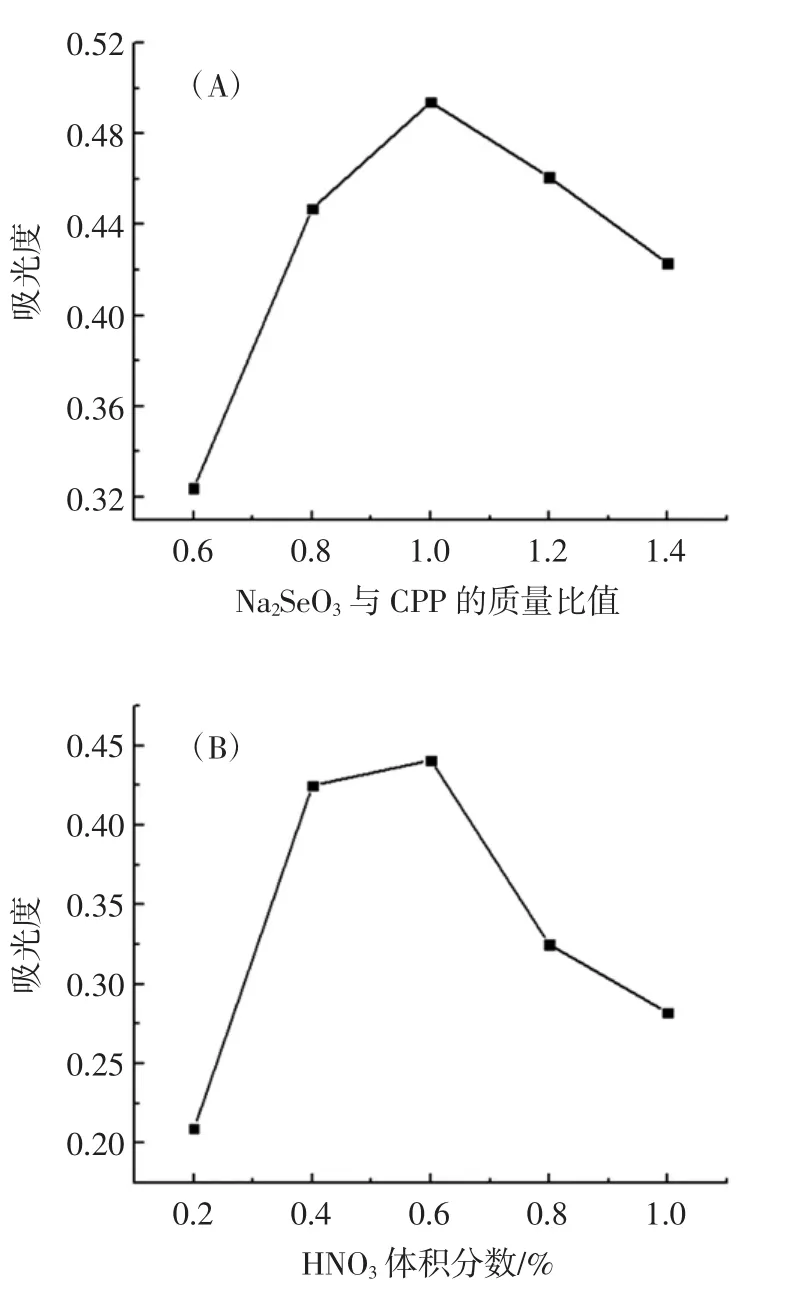
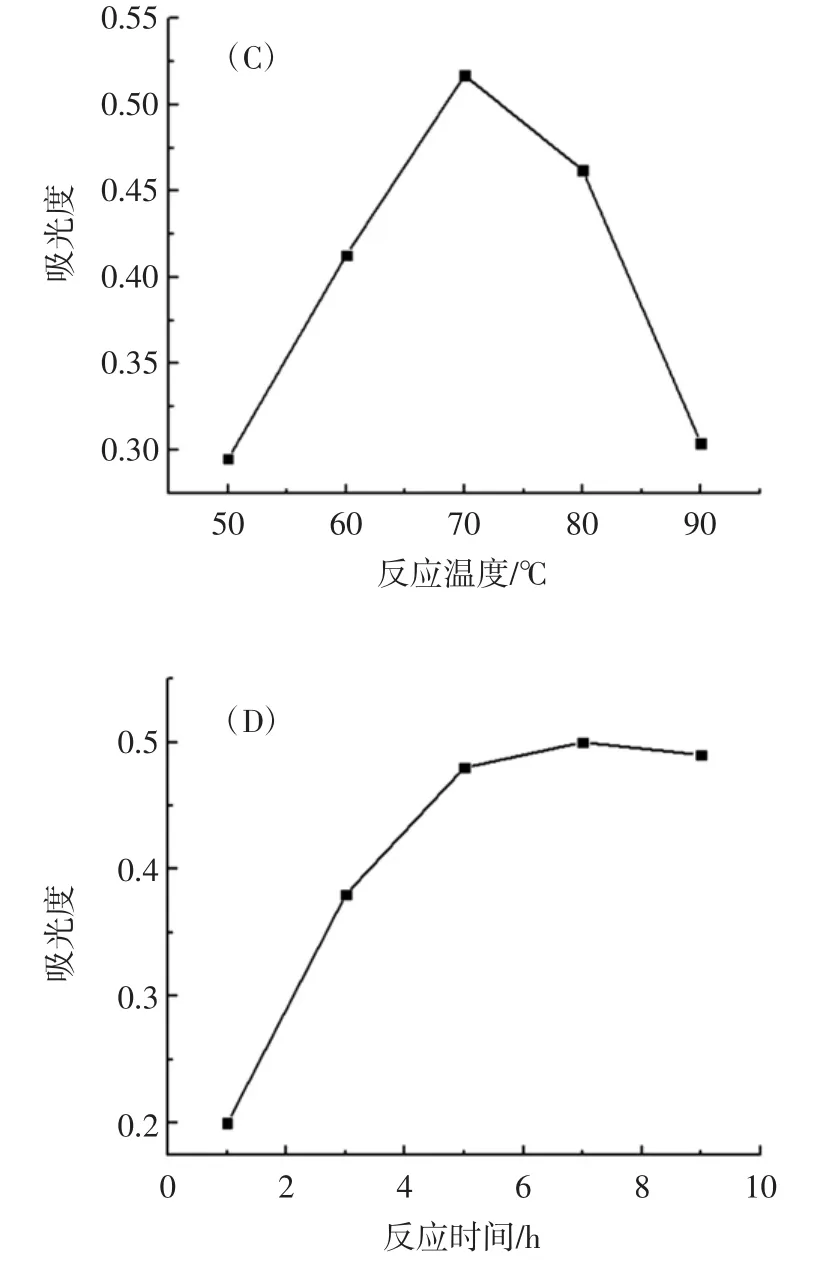
图1 Na2SeO3与CPP的质量比值、HNO3体积分数、反应温度及反应时间对CPPS合成的影响Fig.1 Effect of the ratio of Na2SeO3to CPP,the volume fraction of HNO3,reaction temperature and reaction time on the synthesis of CPPS
由图1(A)可知,随着Na2SeO3与CPP的质量比值的增加,吸光度先升后降,在Na2SeO3与CPP的质量比值为1.0时达最大,所以最佳质量比值选1.0;由图1(B)可知,随着HNO3体积分数的增加,吸光度先上升后下降,在HNO3体积分数为0.6%时最大,在HNO3体积分数大于0.6%时吸光度降低可能是反应体系酸性太大,导致多糖的结构被破坏从而阻碍多糖硒的合成,故HNO3最佳体积分数选择0.6%;由图1(C)可知,反应温度对合成的影响较大,随着温度的升高,吸光度值先上升后下降,后降低可能是因为温度过高破坏了多糖的结构,部分多糖丧失了活性导致合成多糖硒效率降低,所以最佳温度选为70℃;由图1(D)可知,随着反应时间的增加,吸光度先上升后趋于平稳,反应5 h后吸光度增加不明显,为了节省时间成本以及后续可能的工业化扩大生产着想,故最佳反应时间选择5 h。
2.3 响应面优化试验设计
根据2.2单因素试验结果,进行三因素三水平的Box-behnken试验设计,如表1所示。
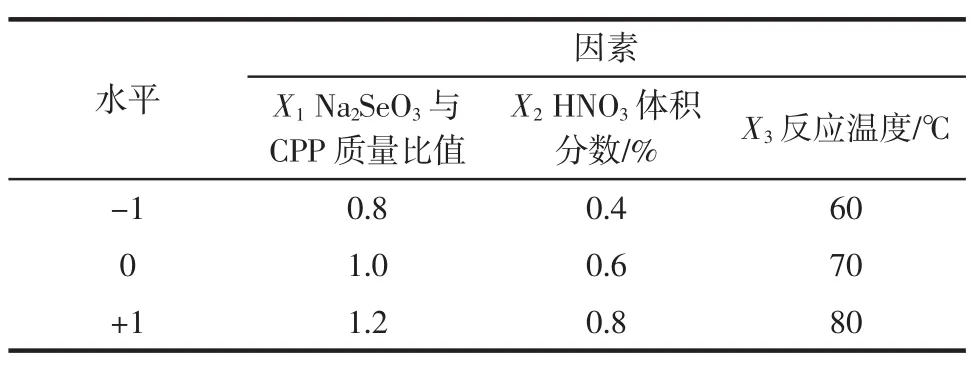
表1 Box-behnken设计因素水平及编码值Table 1 Design factor level and code value
2.4 响应面优化试验
2.4.1 CPPS合成工艺响应面试验结果
参照2.3设计,得到响应面试验结果如表2所示。

表2 Box-Behnken试验设计及结果Table 2 Design and results of Box-Benhnken experiment
以吸光度为响应值,利用Design-Expert 8.0.6.1软件,将表2中试验数据进行统计分析,得到二次多项式回归方程:Y=-3.542 88+1.162 50X1+1.406 87X2+0.083 013X3-0.1X1X2+0.006 5X1X3+0.000 125X2X3-0.765 62X12-1.059 37X22-0.000 628 750X32,并对此设计的模型进行方差分析,结果见表3。
根据表3可知,不显著的有X1X2和X2X3,显著的有X1,其余都是极显著作用。试验所建立的模型(P<0.001)为极显著,失拟项(P=0.685 3>0.05)为不显著,所建立的响应面模型用来优化CPPS制备的最佳工艺条件是可行的。信噪比=36.028比较高,这个数据可以证明该模型可预测试验结果,而校正判定系数R2Adj=0.989 9,表示可以利用此模型来预测98.99%的响应值。判定系数R2=0.995 6,说明此模型拟合程度良好,可以利用模型来分析和预测制备的CPPS的吸光度值,R2Pred=0.974 9与R2=0.995 6的值相差不大说明该响应面方程无需做进一步优化。
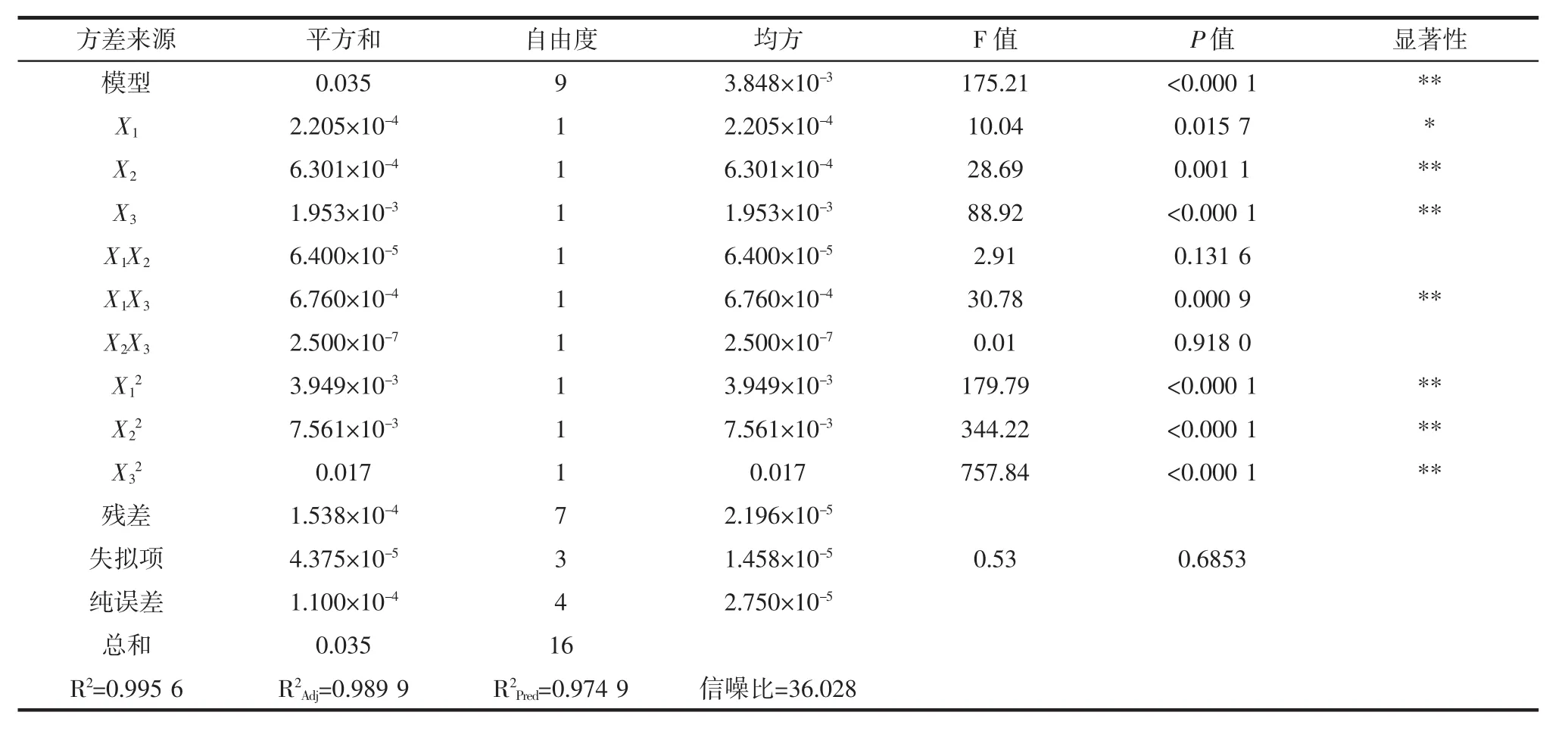
表3 回归模型的方差分析Table 3 Analysis of variance for items of regression equation
2.4.2 CPPS合成工艺响应面图分析与对比
根据2.4.1所得回归方程,考察拟合响应面的形状,绘制响应面图及等高线图,结果见图2所示。

图2 CPPS中硒吸光度响应面及等高线图Fig.2 Response surface plot and contour plot of Se absorbance of CPPS
各因素的交互作用可以通过图2中响应面图的陡峭程度和等高线图的疏密程度来直观的表现出来。由图2(A)可以看出HNO3体积分数的响应面相对陡峭,等高线较密集,Na2SeO3与CPP的质量比值的响应面较平缓,等高线较稀疏,说明HNO3体积分数对CPPS制备的影响比Na2SeO3与CPP的质量比值更显著。同理,由图2(B)可以看出反应温度的响应面相对陡峭,等高线较密集,Na2SeO3与CPP的质量比的响应面较平缓,等高线较稀疏,说明反应温度对CPPS制备的影响比Na2SeO3与CPP的质量比值更显著。由图2(C)可以看出温度的响应面相对陡峭,等高线较密集,HNO3体积分数的响应面较平缓,等高线较稀疏,说明温度对CPPS制备的影响比HNO3体积分数更显著。上述结论与2.3.1中单因素显著性分析结论完全吻合。由图2(A~C)可以看出,响应面和等高线存在极值,响应面的最高点也就是等高线中的最小椭圆的中心点[19]。通过观察等高线图中中心椭圆的情况可以了解两两交互作用的影响强弱:中心椭圆越接近圆形,两两交互作用相对越弱,越偏离圆形,交互作用越强。根据结论由图2(A~C)等高线图判断可知:Na2SeO3与CPP的质量比值和反应温度即X1X3的交互作用最强,Na2SeO3与CPP的质量比值和HNO3体积分数即X1X2的交互作用适中,HNO3体积分数和反应温度即X2X3的交互作用最弱,这一结论也与表3方差分析结果相吻合。
2.4.3 最佳提取工艺验证
通过响应面软件优化得到的最佳制备工艺条件为:Na2SeO3与党参多糖的质量比为1.02,HNO3体积分数为0.62%,反应温度为71.35℃,此时的理论吸光度值为0.449。为验证该试验模型的可靠性,按照上述最佳方案进行5组平行试验。实际合成条件取Na2SeO3与CPP的质量比值为1,HNO3体积分数为0.6%,反应温度为 70 ℃,吸光度值为:0.448、0.457、0.462、0.458、0.454,平均吸光度值为0.456,相对误差为1.56%,说明此模型可靠性较高,可以用来优化CPPS制备的工艺条件。此时CPPS中硒含量为3.06 mg/g,CPP中未检测到硒。据报道,天然富硒土壤种植的党参硒多糖中硒含量高达0.886 mg/kg[20],本文合成的CPPS中硒的含量远高于天然CPP,也高于陈文霞等[21]合成的硒化纹党参多糖中硒含量(1.07 mg/g),但远低于刘宽辉等[22]合成的硒化党参多糖中硒含量(11.86 mg/g)。认为因CPP的纯度、CPPS合成的条件及硒的检测方式不一,CPPS中硒含量的高低并不具备可比性,因此通过此指标比较硒化工艺的优劣也并不科学,后期可在一定的限制条件下展开进一步研究。
2.5 CPPS结构表征
2.5.1 紫外光谱分析
为了验证CPP硒化成功,分别对CPP及CPPS做了紫外全波段扫描,具体参见图3。

图3CPP和CPPS的紫外扫描光谱Fig.3 Ultraviolet scanning spectrum of CPP and CPPS
由图3 CPP与CPPS的紫外扫描图谱对比可知,在300 nm~400 nm波长范围内CPP没有明显的吸收峰;而CPPS在334 nm处有一个强吸收峰,这与高义霞等[23]报道的硒在334 nm产生的最大吸收峰位吻合,表明合成的CPPS中含有硒元素。
2.5.2 红外光谱分析
为了便于观察与比较,对CPP与CPPS的红外谱图沿着纵轴进行了平移处理,结果如图4所示。

图4CPP和CPPS红外光谱Fig.4 IR spectroscopy of CPP and CPPS
由图4可知,CPP具有典型的多糖特征吸收峰(3 417.4、2 935.2、1 627.7、1 430.9、1 145.5、662.19、602.17cm-1)。3417.4 cm-1处出现的宽峰为多糖O-H的伸缩振动峰,2935.2cm-1为多糖C-H伸缩振动吸收峰,1 627.7 cm-1为多糖羰基C=O伸缩振动峰,1 430.9 cm-1为多糖羰基C-O伸缩振动峰、1 145.5 cm-1为多糖羟基O-H弯曲振动峰,662.19 cm-1为多糖C-H弯曲振动峰、602.17 cm-1为多糖C-O-C振动吸收峰。CPPS中多糖的特征吸收峰依然明显(3 374.9、2 931.4、1 631.5、1 415.5、1 091.5、937.28、871.71、821.56、651.85、600.28 cm-1),与未修饰的CPP基本相同,只是某些官能团特征峰的峰形略有改变,峰位出现了略微的红移与蓝移。说明CPP与Na2SeO3反应后结构没有发生大的变化,保持了CPP原有的性质。不同的是,CPPS红外光谱相对CPP而言,在937.28、871.71、821.56 cm-1处多出了3个明显的特征吸收峰,分别依次归属为Se=O、C-Se、Se-O伸缩振动峰,证明Na2SeO3已经与CPP 结合成酯[15,23-24]。
2.6 CPPS的抗氧化分析
2.6.1 Fe2+清除能力测定
金属离子(如Fe2+和Cu2+)在自由基的氧化中起催化作用。金属离子被螯合后失去其催化能力,可减缓自由基的产生。因此,测定样品的金属离子螯合能力是测定其抗氧化性能的常用评价方法。CPPS对Fe2+螯合能力如图5所示。
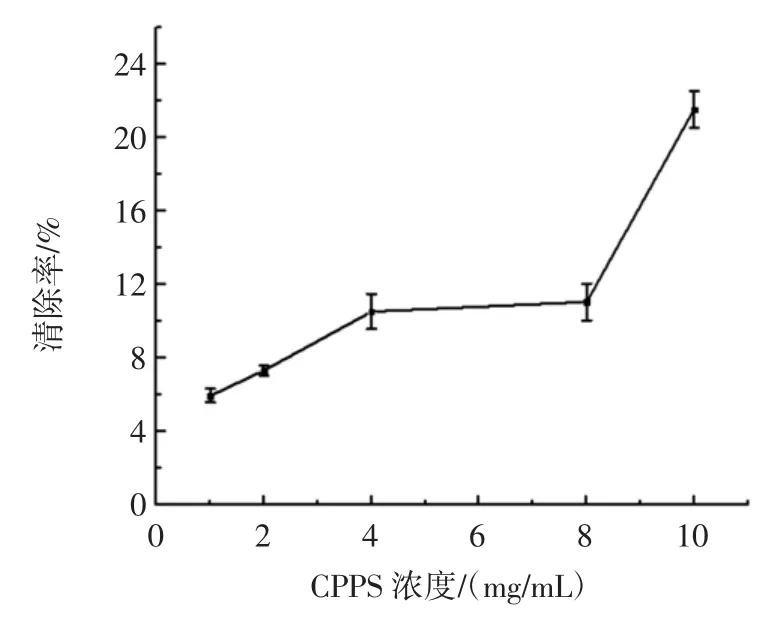
图5 CPPS对Fe2+的清除能力Fig.5 Scavenging effects of CCPS on Fe2+
由图5可知,随着CPPS浓度的增加,其清除率先缓慢后急剧升高,当浓度为10 mg/mL时达到相对最大清除率21.62%,后续因CPPS溶解性及浓度过大导致溶液黏度过大等问题,没法再增加浓度继续试验,故在0~10 mg/mL浓度范围内,CPPS对Fe2+有一定的清除效果。
2.6.2 CPPS对超氧阴离子自由基清除能力测定
CPPS对超氧阴离子自由基的清除率如图6所示。
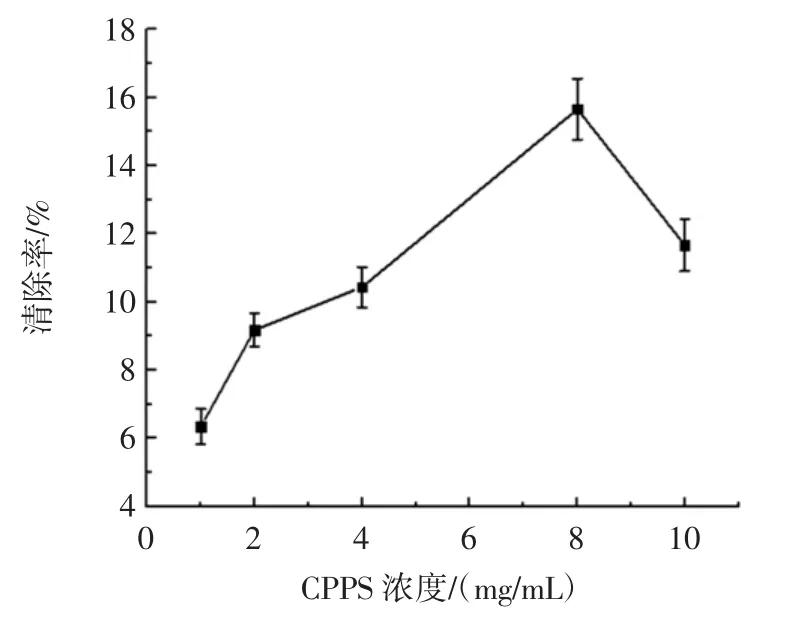
图6 多糖硒对超氧阴离子自由基的清除能力Fig.6 Scavenging effects of CCPS on superoxide radical
由图6可知,CPPS对超氧阴离子自由基清除能力随着其浓度的增加而增加,当CPPS浓度达到8 mg/mL时达到相对最大清除率16.67%,但随着CPPS浓度的继续增加,清除率逐渐降低,这可能是因为CPPS浓度增加引起粘度增加抑制了其抗氧化活性,即在0~8 mg/mL浓度范围内,CPPS对超氧阴离子自由基具有一定的清除作用。这些结果表明CPPS可以作为潜在的抗氧化剂后续继续探索。
3 结论
选用CPP为材料,通过单因素考察,得出合成党CPPS的最佳单因素条件为:温度为70℃,HNO3体积分数为0.6%,Na2SeO3与CPP的质量比值为1.0。进一步运用响应面软件Design-Expert优化合成工艺,得出CPPS合成最佳的条件为:温度为70℃,HNO3体积分数为0.6%,Na2SeO3与CPP的质量比为值1。经过对CPPS的紫外及红外结构表征,表明CPPS合成成功,硒在CPPS中以Se=o形式存在。同时对CPPS进行了抗氧化研究,结果表明CPPS对Fe2+以及超氧阴离子自由基具有一定的清除能力。
