2种免疫方法测定尿微量白蛋白的对比研究
2019-08-21徐羽中王金虹刘香萍
徐羽中,王金虹,刘香萍
(南方医科大学附属深圳市宝安区人民医院检验科,广东深圳 518101)
0 引言
尿微量白蛋白(UMA)是尿中难以用常规定量定性方法检出的清蛋白。正常人的肾小球滤过膜具有电子和分子筛双重屏障,可以阻挡带负电且分子量大的白蛋白。倘若滤过膜遭到破坏,白蛋白将漏出,当浓度超出肾小管的重吸收阈值,会出现微量白蛋白尿或白蛋白尿。
UMA水平是高血压肾病的早期标志[1],可以早期诊断肾病、评估糖尿病患者肾并发症的危险度、监测妊娠诱发性高血压的肾损伤,同时也可以提示其他疾病,如狼疮性肾病、泌尿系统感染、心衰等。
迄今为止,UMA的检测方法主要有放射免疫法、时间分辨荧光法、免疫比浊法和乳胶增强免疫比浊法,而如何保证不同检测方法结果之间的可比性是临床应用中的难题。目前,研究UMA检测方法的文献有单方法的临床应用与评价,如ELISA法[2]、免疫散射比浊法等;也有双方法的可比性研究[3],如干化学法和免疫透射比浊法、化学发光免疫测定法和免疫放射法等的比较。本文就深圳市某三甲医院检验科的免疫荧光定量法和免疫散射比浊法进行比对试验和偏差估计。此次研究包括重复性试验和方法比较试验,目的在于检测2种方法的精确度和准确度,评估部分性能指标,了解医院开展相应临床检测项目的可行性,并判断2种检测方法的结果在临床应用上的可比性和相关性。
1 材料与方法
1.1 仪器与试剂
免疫散射比浊法测定UMA采用该医院检验科生化室BECKMAN COULTER AU5800全自动生化分析仪(以下简称“AU5800生化仪”),试剂盒由BECKMAN COULTER公司提供,批号为2298;免疫荧光定量法测定UMA采用门诊检验科i-CHROMA Reader免疫荧光分析仪,试剂盒由韩国巴迪泰公司提供,批号为MANDC13C。
1.2 样本来源
样本均为生化室测ACR值(UMA/肌酐)的患者的晨尿,重复性试验需3个浓度分别为低(L1)、中(L2)、高(L3)水平的样本,其样本浓度(首次在AU5800生化仪测量的浓度)分别为 6.6、24.4、192.9 mg/L;方法比较试验需40个样本(均在该项目线性范围内:0~200 mg/L),其中 30个在参考范围内(0~20mg/L),10个大于参考范围(20~200mg/L)。
1.3 检测方法
1.3.1 免疫散射比浊法
测定前清洗保养AU5800生化仪,并进行质控、校准,要求质控结果在允许误差范围±2SD之内。
1.3.2 免疫荧光定量法
将10 μl尿液加入缓冲液,充分混匀,将75 μl混匀后的样本加入反应板的加样孔中,室温下放置12 min,由i-CHROMA Reader免疫荧光分析仪读取结果。
1.4 可比性研究方法
1.4.1 重复性试验
将L1、L2、L3 3个水平的尿液样本分装储存,分别用2种方法每日检测4次,连续测5 d,记录数据,计算各方法所测结果的批内均值、批内标准差和变异系数[4]。计算公式如下:
批内均值=每轮测定值均值之和(∑X)/测定轮数(m)

其中,S2i为各轮测定值的方差。
变异系数=批内标准差/批内均值×100%
1.4.2 方法对比试验
40个样本用2种方法各测定2次(正序、倒序),设免疫散射比浊法测定结果为x值,免疫荧光定量法测定结果为y值。40个样本则有80对x和y的结果,检查测定结果中有无离群值;根据直线回归分析法作统计处理,求出回归方程y=a+bx及相关系数R2,计算免疫荧光定量法的系统误差(SE),与不同医学决定水平(Xc)的允许总误差(TEa)作比较,对可否接受免疫荧光定量法的系统误差作出判断[5]。
2 结果
2.1 重复性试验
各方法L1、L2、L3 3个浓度水平的样本的重复测定结果及初步计算见表1。
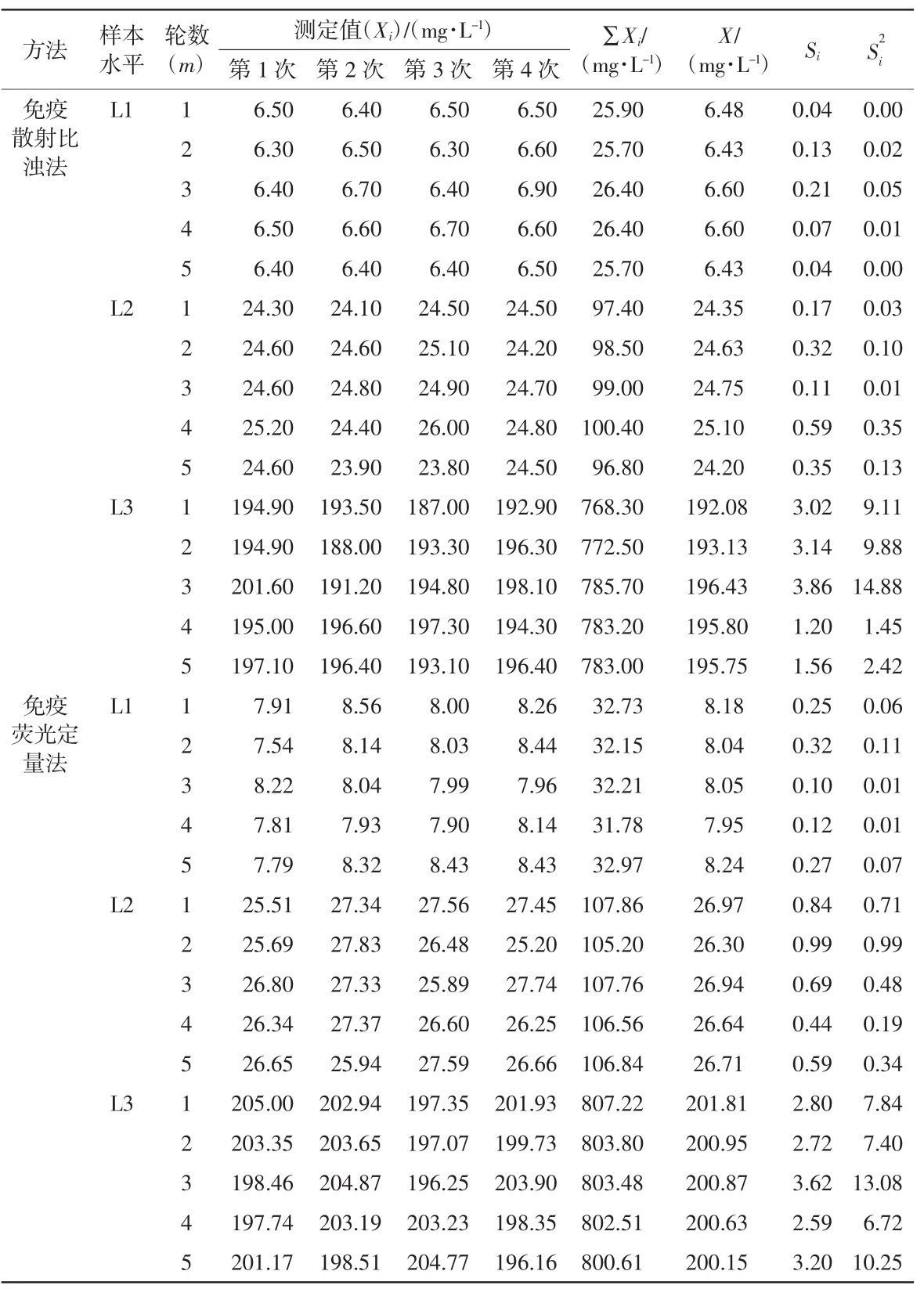
表1 免疫散射比浊法和免疫荧光定量法的精密度结果
检查离群值:检验20次测定结果的离群值,20个样本属于小样本,故采用Grubbs检验,其统计公式为Gn=|Xd-X¯|/s,式中X¯为包括离群值在内的测定值的均值,s为包括离群值在内的测定值的标准差,Xd为离群值。分别计算各个样本的Gn值,结果见表2。

表2 免疫散射比浊法和免疫荧光定量法的Grubbs检验结果
查阅Grubbs检验临界值Gn参考表可知,测定次数为20次时,显著性水平为0.05的Gn值为2.557,显著性水平为0.01的Gn值为2.884。
根据表2可知,免疫散射比浊法的L1水平第3轮第4次的测定结果大于2.557,L2水平第4轮第3次测定的结果大于2.557,故均舍弃;免疫荧光定量法的检测结果没有离群值。
剔除离群值后,计算各样本的批内均值、批内标准差和变异系数,计算结果见表3。
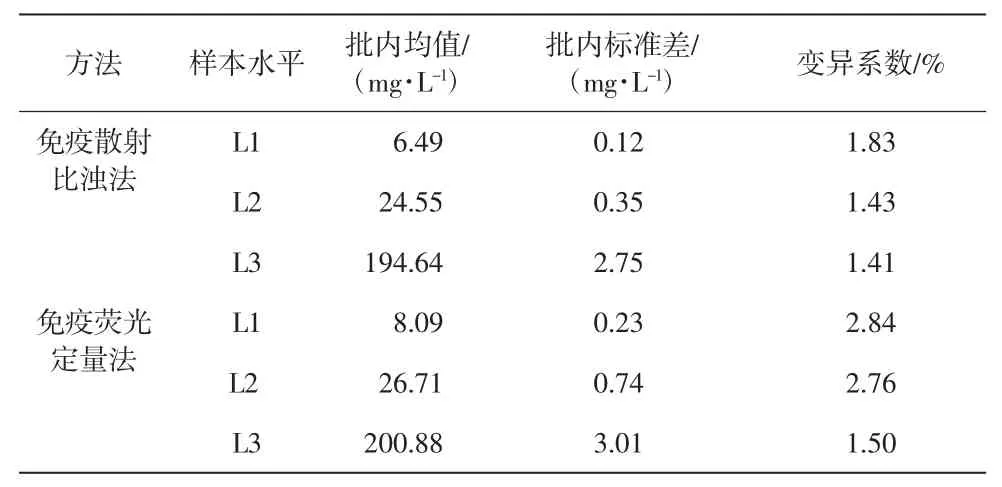
表3 免疫散射比浊法和免疫荧光定量法测定结果的批内均值、批内标准差和变异系数
批内不精密度的判断限是1/4TEa,根据卫生部临床检验中心室间质量评价标准,尿中清蛋白的TEa是30%,即判断限为7.5%。
由表3可知,免疫散射比浊法各样本检测值的变异系数分别为1.83%、1.43%、1.41%,免疫荧光定量法各样本检测值的变异系数分别为2.84%、2.76%、1.50%,均<7.5%,故可接受免疫散射比浊法和免疫荧光定量法的不精密度。
2.2 方法对比试验
2.2.1 方法对比试验的结果数据
40个样本(30个样本的浓度为0~20 mg/L,10个样本的浓度为>20 mg/L)采用2种检测方法各测定2次(正序、倒序),得到双份结果,详见表4。
2.2.2 双份检测数据的离群值
方法内的离群值检查:分别计算每个样本重复测定差值的绝对值及其均值,以4倍平均绝对差值作为2种方法重复测定绝对差值的可接受限。计算可得,免疫散射比浊法的可接受限为1.36,离群值个数为0;免疫荧光定量法的可接受限为3.45,第34号样本所测结果的差值为3.59,是离群值,舍弃。
方法间的离群值检查:计算单样本2种方法检测结果的差值的绝对值,得到80个差值绝对值的均值,以该均值的4倍为判断限,即为8.30。因此,第37号样本计算所得的差值的绝对值为10.02,为离群值,舍弃[6]。
2.2.3 绘制散点图、线性回归及相关分析
剔除离群值后2种方法的测定均值见表5。
用Microsoft Excel软件将剔除离群值后的数据制作成散点图,以x轴代表免疫散射比浊法的测定均值,y轴代表免疫荧光定量法的测定均值,添加趋势线,得出线性相关方程y=a+bx及相关系数R2,散点图如图1所示。
该线性方程为y=1.025 5x+1.247 9,R2=0.999 5。因此恒定系统误差的大小为1.247 9,即截距a;比例系统误差的大小为1.025 5,即斜率b。计算免疫荧光定量法测定UMA的SE,公式为SE=|(a+bXc)-Xc|,而UMA的Xc为20 mg/L,计算得到SE为1.757 9 mg/L。从卫生部临床检验中心室间质量评价标准查得UMA的TEa为30%,本次试验提高标准,将允许误差缩小为20%。方法比较试验一般以1/2TEa作为评价标准,计算可得本次实验UMA的允许误差为2 mg/L。因 SE<1/2TEa,且R2≥0.95,故以免疫散射比浊法为参考方法,可以接受免疫荧光定量法的总系统误差。

表4 免疫散射比浊法和免疫荧光定量法的双向测定结果

表5 免疫散射比浊法和免疫荧光定量法的测定均值

图1 免疫荧光定量法均值与免疫散射比浊法均值散点图
3 讨论
UMA是肾功能损害的临床重要指示物之一。与尿蛋白相比,UMA的检测敏感性和可靠性更佳,对狼疮肾炎早期损伤[7]和糖尿病肾病的早期诊断价值更佳[8-9]。UMA可作为高血压肾病的早期标志[10],在早期阶段UMA水平升高,经严格治疗可好转,从而延迟蛋白尿及高血压肾病的发展[11];同时它也可作为产后诱发肾损伤[12],类风湿性关节炎患者活动性、泌尿系统感染、亚临床心血管调节功能等的评价指标[13]。
检测方法的性能指标可通过精密度评价、线性评价、干扰试验、回收试验、方法对比试验、基质效应评价等方法进行评估,本文就UMA的2种检测方法的部分性能指标进行分析。重复性试验的操作规程参考美国国家临床实验室标准化委员会(National Committee for Clinical Laboratory Standards,NCCLS)的EP15-A文件,测定精密度;方法比较试验参考美国临床实验室改进修正案(Clinical Laboratory Improvement Amendments,CLIA)的 EP9-A2文件(2002年),测定总系统误差。对于重复性试验,免疫散射比浊法3个浓度水平的变异系数分别为1.83%、1.43%和1.41%,免疫荧光定量法分别为2.84%、2.76%和1.50%,由此可知,免疫散射比浊法测定UMA的结果精密度优于免疫荧光定量法。根据卫生部临床检验中心室间质量评价标准,尿白蛋白的总允许误差是30%,批内不精密度的判断限是1/4TEa,即为7.5%,2种方法各样本检测值的变异系数均<7.5%,故可接受免疫散射比浊法和免疫荧光定量法的不精密度。
由于我院免疫散射比浊法参加并通过了卫生部室间质评,故以免疫散射比浊法为参考方法。利用直线回归分析法可得该线性方程为y=1.025 5x+1.247 9,R2=0.999 5。参考微量白蛋白的Xc值(20mg/L),算得免疫荧光定量法测定UMA的SE为1.757 9 mg/L,小于1/2TEa,即2 mg/L。故以免疫散射比浊法为参考方法,免疫荧光定量法测定UMA的方法可以被接受。
综上所述,免疫散射比浊法和免疫荧光定量法对于人晨尿中UMA的检测结果精密度良好,免疫散射比浊法为大多研究认可的灵敏度、准确度俱佳的方法,以此为参考方法,免疫荧光定量法的总系统误差可以被接受,故UMA的2种检测方法均可采用。但由于免疫荧光定量法检测UMA过程简便、成本较低,且相对于因批量上机而检测速度受限的免疫散射比浊法用时更短,可满足门诊30 min内需发送报告的需求。考虑到荧光定量法稀释样本和计量读数时间过程中容易产生误差,精密度不如免疫散射比浊法等特点,对于住院患者,特别是糖尿病患者、高血压患者及病情与该指标相关的患者,监测该指标时建议采用免疫散射比浊法。
