国产CalliSpheres载药微球DEB-TACE治疗无法手术肝癌的临床价值
2019-08-19王忠刘启榆杨伟周西范丹丹
王忠 刘启榆 杨伟 周西 范丹丹
肝癌在全球患病率均较高,5年生存率约10%~15%,我国每年死于该病的患者超过40万,部分患者因错过手术时机,仅能采取保守治疗[1]。经导管动脉化疗栓塞(TACE)是常用的保守治疗方式,它能促进肿瘤坏死,达到治疗目的,然而,临床关于TACE化疗药物选择、栓塞剂尺寸等仍有争议[2]。近年来,载药微球TACE(DEB-TACE)在肝癌治疗中被应用,它可对化疗药物栓塞球事先进行加载,从而使其与肿瘤接触时间延长,并降低药物毒性,控制进入血液系统内的药物浓度[3]。为了进一步了解该方案在肝癌中的应用价值,本研究纳入90例无法手术的肝癌病例进行研究,现报道如下。
资料与方法
一、一般资料
选取我院2016年1月—2017年1月收治的无法手术肝癌患者90例,所有患者均给予经导管动脉化疗栓塞(TACE)治疗。根据随机数字表法分成对照组(45例)、观察组(45例)。对照组男23例,女22例,年龄46~78岁,平均(65.72±11.69)岁;肿瘤直径3~8 cm,平均(5.46±1.74)cm;肿瘤个数:多发12例、单发33例;Child-Pugh肝功能分级:A级26例、B级19例。观察组男21例,女24例,年龄45~79岁,平均(66.17±12.86)岁;肿瘤直径3~8 cm,平均(5.43±1.68)cm;肿瘤个数:多发10例、单发35例;Child-Pugh肝功能分级:A级28例、B级17例。研究方案经本院伦理委员会获批,两组一般资料比较差异无统计学意义(P>0.05)。
二、纳入与排除标准
(一) 纳入标准
(1)参考《原发性肝癌诊疗规范(2011年版)》[4]诊断,经病理穿刺证实;(2)有根治性手术禁忌;(3)入院前无TACE干预史;(4)无动静脉瘘;(5)无胆管、肝静脉、门静脉癌栓;(6)知情同意。
(二)排除标准
(1)心、脑、肾、肺等系统严重损害;(2)接受靶向药物、射频消融等其他治疗;(3)要求调整栓塞材料;(4)既往有肝部手术史。
三、治疗方法
术前行MRI、CT、血常规、尿常规、肝功能、肾功能、心电图、凝血功能等检查。介入器材主要为血管鞘、微导管、穿刺针、导丝,术前4 h禁食。肝动脉造影:选取仰卧位,常规铺巾、消毒,经利多卡因(浓度为2%)行局麻,利用Seldinger技术对股动脉进行穿刺,取5F血管鞘置入,行肝总动脉造影,观察肿瘤血供、数目、位置、大小等情况。若肝区存在造影剂空白处,则需对膈下动脉、肠系膜上动脉等造影,分析血供是否处于异常状态。对照组采用传统TACE治疗(cTACE),即30 mL碘油混悬液+40 mg表阿霉素(浙江海正药业 国药准字X19990280)行化疗栓塞。观察组采用载药微球TACE(DEB-TACE)治疗,即CalliSpheres载药微球(江苏恒瑞)+表阿霉素行化疗栓塞。经注射液将CalliSpheres载药微球(7 mL)吸出,使注射器处于竖立状态,等待微球沉降(约2~3 min),推出上部清液。抽取葡萄糖水,使表柔比星(40 mg)完全溶解。经注射器抽出化疗药物,使化疗药、微球混合,每隔5 min轻轻摇晃1次,载药30 min。待化疗药完全被微球吸附后,根据1∶1比例取非离子型对比剂加入,轻摇,使其混合,等待5 min便可使用。经脉冲式注射(1 mL/min),待对比剂流速停滞,或者速度非常缓慢,则停止给药。术后通过造影观察是否栓塞完全,待栓塞满意,可将血管鞘、导管撤出,针对穿刺点给予加压包扎止血。穿刺侧制动6 h,于24 h后才可活动。
四、观察指标
(1)临床疗效[4]:于治疗后3个月评估短期疗效。完全缓解:经MRI、CT检查提示肿瘤显影彻底消失;部分缓解:肿瘤显影较治疗前减少≥30%;稳定:肿瘤较治疗前无明显缩小,也未见明显增加;进展:有新病灶形成,或与治疗前比较,肿瘤增加≥20%。总缓解率=(完全缓解+部分缓解)/总例数×100%。(2)血清指标:分别在治疗前、治疗1周、治疗4周采集3 mL静脉血,离心25 min(3 000 r/min),分离血清,经酶法测定AST、ALT、Alb水平,试剂盒由北京奥维亚生物提供。(3)随访24个月,分析不良反应发生率与预后情况。
五、统计学方法
结 果
一、两组短期疗效比较
观察组、对照组总缓解率分别为80.00%、75.56%,组间比较差异无统计学意义(P>0.05),见表1。
二、两组肝功能比较
在治疗1周,两组血清AST、ALT较治疗前明显增高,但在治疗4周,两组血清AST、ALT下调,其中观察组低于对照组(P<0.05),见表2。
三、两组不良反应分析
两组体温增高、胆道损伤、恶心、腹痛、呕吐发生率比较差异无统计学意义(P>0.05),见表3。所有患者均为轻度反应,未见严重反应病例。
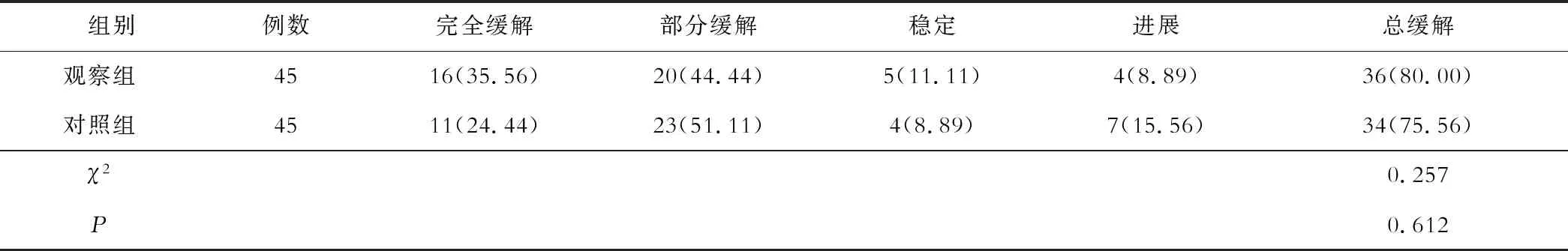
表1 两组短期疗效比较(例数,%)

表2 两组肝功能比较(±s)
注:与治疗前比较,#P<0.05

表3 两组不良反应分析(例数,%)
注:△为连续性校正卡方检验
四、两组24个月的生存、死亡、复发情况分析
观察组有22例(48.89%)生存,23例(51.11%)死亡,6例(13.33%)复发。对照组有12例(26.67%)生存,33例(73.33%)死亡,8例(17.78%)复发。观察组生存率高于对照组,死亡率低于对照组,差异有统计学意义(χ2=4.727,P=0.030)。两组复发率比较差异无统计学意义(χ2=0.338,P=0.561)。
讨 论
本研究通过观察患者的短期疗效,发现cTACE、DEB-TACE的短期效果无明显差异,表明两种栓塞方案的短期疗效均比较理想。然而,通过观察两组肝功能,提示两组治疗1周后均出现肝功能紊乱,具体表现为血清AST、ALT上调,主要因栓塞治疗可造成非肿瘤组织缺氧、缺血所致。不过在治疗4周时,两组血清AST、ALT均有所恢复,其中观察组恢复更明显。提示载药微球的应用能进一步保护肝功能。在本研究中,两组治疗前后Alb未见明显变化,这可能与观察时间短,纳入病例数少等因素有关。DEB-TACE是一种新的化疗栓塞方案,DEB能对所需化疗药物进行加载,并对药物释放有持续调控作用[5]。研究表明化疗药物经载药微球加载后,能提高药物在肿瘤组织内的浓度,使其作用癌细胞的时间延长,保护肝功能,增强疗效[6]。这为本研究结论提供了理论依据,笔者推测载药微球可能通过延长癌细胞作用时间,从而对肝功能进行保护,纠正肝功能紊乱。
本研究提示两种方案均未引起严重不良反应,且组间不良反应发生率比较未见显著差异。有研究提示DEB-TACE能减少不良反应发生[7],与本研究结论相悖。笔者分析这可能与本研究纳入病例数少有关,未来需扩大样本量进一步论证。通过观察两组中期预后,表明DEB-TACE方案能降低24个月的死亡率,提高生存率。既往有研究发现cTACE方案短期疗效良好,但该方案存在两面性,它既能促进肿瘤组织死亡,也可增强其恶化程度[8]。而DEB-TACE则对局部癌组织控制较好,化疗药释放时间明显延长,药物浓度增高,有利于提高疗效,延长生存时间。在本研究中,两组中期复发率比较未见显著差异,提示两种方案的中期复发风险相当。有研究提示虽然DEB-TACE短期效果较理想,但也存在缺陷,如残余癌组织在缺氧状态下,可能上调肿瘤生长因子水平,引起局部复发[9]。另有研究发现,即便DEB-TACE能抑制瘤体局部生长,但患者可能已有新病灶形成[10]。因此,患者在治疗期间必须定期复查,观察肿瘤生长情况,便于尽早采取措施处理,降低复发率和死亡率。
