肝硬化门静脉血栓形成高危因素的Logistic回归分析
2019-08-19舒丹黄湘荣蒋育进黄婷刘映霞许诚
舒丹 黄湘荣 蒋育进 黄婷 刘映霞 许诚
门静脉血栓( portal vein thrombosis,PVT) 是肝硬化患者的常见并发症,发生率为0.6%~26%[1]。PVT 形成可加重门静脉高压症,并最终影响患者的预后及生存[2]。本研究从临床资料、实验室检测结果及影像学等多因素分析肝硬化合并PVT的危险因素,以期为PVT的早期干预提供科学指导。
资料与方法
一、 研究对象
2016年1月至2017年12月深圳市第三人民医院就医的有完整资料的肝硬化患者314例,其中合并PVT者33例。合并PVT患者中,男28例,女5例,年龄(49.7±11.3)岁,未合并PVT的281例患者中,男232例,女49例,年龄(48.4±17.2)岁。两组性别、年龄比较,差异均无统计学意义(χ2=0.108,t=1.206,均P>0.05)。
肝硬化的诊断依据病史、临床表现、实验室检查、影像学改变或组织学检查,病因学诊断根据中国和欧洲肝脏病学会相关指南[3-6]。门静脉血栓依据超声、CT、MRI检查显示典型影像学改变确诊。排除经颈静脉肝内门体分流术后、肝或脾手术后、内镜下食道胃底静脉曲张治疗后、恶性肿瘤、非肝硬化性门脉高压、骨髓增殖性疾病等非肝病相关血栓形成、正在服用抗凝药或抗血小板药物、检查前1周内曾接受血制品输注的患者。
二、 研究方法
回顾性调查患者的病历,登记一般情况(性别、年龄、病因、并存病)及入院第二天的血常规、总胆红素(TBil)、白蛋白、凝血酶原时间(PT)、纤维蛋白原(Fib)、抗凝血酶-Ⅲ(AT-Ⅲ)、D-二聚体和Child-Pugh评分等。影像学检查:患者取平卧位,于门静脉出肝2 cm处测量门静脉主干(MPV)内径宽度。第一肝门处测量门静脉流速(portal vein velocity,PVV)。
三、 统计方法
结 果
一、肝硬化病因
PVT组HBV感染28例,HCV感染1例,酒精性肝硬化3例,其他病因1例。无PVT组HBV感染237例,HCV感染14例,酒精性肝硬化19例,AIH 7例,其他病因4例。两组比较差异无统计学意义(χ2=1.766,P=0.779)。
二、单因素分析肝硬化PVT的危险因素
两组的WBC、RBC、TBil、Alb、PT、Fib及MPV内径宽度无显著差异。PVT组的PLT、AT-Ⅲ较对照组低,PVV较慢,D-二聚体较高,Child-Pugh评分较高。见表1。
三、肝硬化PVT危险因素的logistic回归分析
将单因素分析得出差异有统计学意义的5个指标进行非条件logistic回归模型分析(后退法),结果显示AT-Ⅲ、D-二聚体、PVV及Child-Pugh评分是肝硬化患者合并PVT的独立危险因素。见表2。

表1 单因素分析肝硬化患者PVT的危险因素(±s)
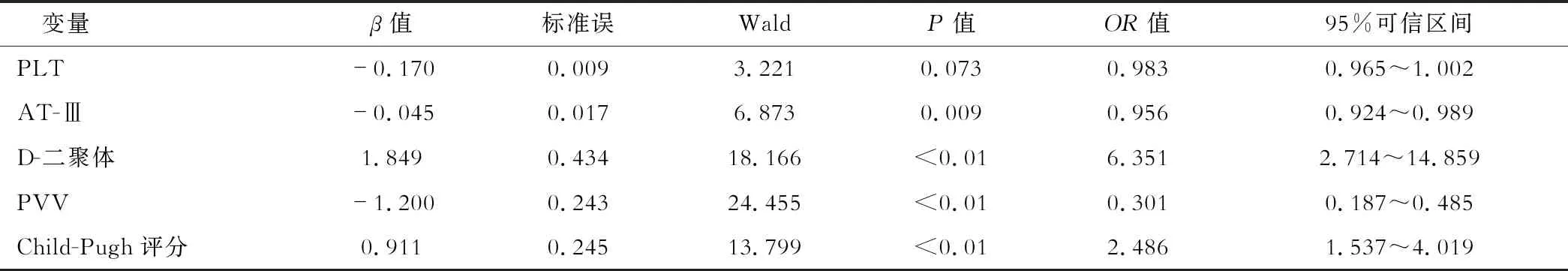
表2 肝硬化患者PVT危险因素的logistic回归分析
根据AT-Ⅲ、D-二聚体、PVV、Child-Pugh评分绘制ROC曲线,结果显示AT-Ⅲ的AUC为0.629(95%CI:0.534~0.725),D-二聚体的AUC为0.786(95%CI:0.692~0.881),PVV的AUC为0.842(95%CI:0.776~0.908),Child-Pugh评分的AUC为0.722(95%CI:0.629~0.815)。
讨 论
既往的研究显示,Child Pugh评分与PVT风险相关[7,8]。本研究中,肝硬化患者的Child-Pugh评分与PVT的发生独立相关,患者Child-Pugh评分每增加一分,PVT风险增加2.486倍,其预测PVT的AUC为0.722。但肝硬化进展本身也许并非PVT的直接原因,随着肝硬化的进展,随之而来的多种因素导致PVT的风险增高。
PVV减慢、MPV增宽、食管静脉曲张均是门脉高压的标志。本研究中,PVV是PVT的独立危险因素,AUC为0.842,预测价值最高。这一结果与文献报道[9,10]相符,提示可以根据这一特征来识别PVT高危患者。为什么是PVV而非MPV宽度?可能是血流减慢导致大量活化的凝血酶在门静脉系统沉积,从而增加了PVT风险。
肝硬化患者的深部静脉血栓(而不单是PVT)发生率较一般人群更高,并且该风险随着肝硬化的进展而进一步增加[11-13],提示全身性因素在血栓形成中发挥了一定作用,其中重要的一点就是抗凝与促凝因子的失衡。本研究显示,AT-Ⅲ是PVT的独立危险因子,与既往的研究相符[14],但其预测PVT的AUC仅0.629,诊断价值偏低。肝硬化患者D-二聚体水平通常较健康人高,并随着肝功能恶化而明显升高,提示肝硬化患者体内存在原发性凝血活化,可能与肝功能恶化后清除组织纤溶酶原激活物能力下降和纤溶蛋白抑制物合成减少有关。本研究中,患者的D-二聚体水平升高是PVT的独立危险因素,其AUC为0.791,诊断价值较高。随着对肝硬化患者凝血功能失调这一认识的日益深入,越来越多的证据提示血栓前状态与肝纤维化进展存在相关性[15]。有研究显示抗凝治疗能显著减少肝脏失代偿事件,这不能单用降低了PVT发生率来解释,可能是通过抗凝治疗打断了凝血级联与肝纤维化进展之间的链条[16]。因此,肝硬化的进展与PVT形成之间的因果关系,目前还存在争议,但及时进行抗凝干预,可能对二者都产生正面作用,值得进一步研究。
Qi等[7]的meta分析显示,肝硬化合并PVT患者中凝血酶原基因 G20210A和FVL突变的比例较无PVT者的高,但鉴于此类患者的比例非常低(5%对3%),可以推断并非关键因素。Nery等[17]的研究中, FVL和凝血酶原基因G20210A突变与PVT并无相关性。本研究未对患者的凝血酶原基因 G20210A和FVL突变进行检测,可能对研究结果产生一定的影响。
总之,本研究显示PVV减慢、高Child-Pugh评分、高D-二聚体水平及低AT-Ⅲ水平是肝硬化患者PVT的独立危险因素,提示PVT的形成与血流缓慢、高凝状态有关,且风险随着肝功能的恶化而增高。今后应将这些因素纳入预警机制,对患者进行早期干预,以期改善肝硬化患者的远期转归。
