体外受精-胚胎移植后宫内妊娠合并子宫瘢痕妊娠一例
2019-08-19李慧苓范丽梅
李慧苓,范丽梅
近年来,随着剖宫产率的逐渐升高和二胎政策的放开,子宫瘢痕妊娠(cesarean scar pregnancy,CSP)的发生率随之增加。体外受精-胚胎移植(in vitro fertilization-embryo transfer,IVF-ET) 时为提高成功率,胚胎移植的数量通常在2枚及以上,因此IVF-ET后宫内妊娠合并CSP的几率有所增加。对CSP的早期发现、早期治疗,有助于宫内正常位置妊娠囊的发育生长,减少患者的经济与心理负担。现对CSP的超声和磁共振成像(MRI)诊断技术的优缺点进行比较,并对CSP的治疗和预防提出一些思考。
1 病例报告
患者 女,37岁,患者因检查发现剖宫产术后CSP 36 d,减胎术后阴道持续不规则出血,于2018年5月15日入院。患者已婚,孕2产1,剖宫产1次,患者平素月经规律,经期7 d,周期30 d,末次月经2018年3月5日,2018年3月22日在吉林大学第二医院(我院)行胚胎移植术,共移植3枚胚胎,成功着床2枚。患者妊娠期妇科超声检查发现:宫内早孕,双胎,其中一胎为CSP,另一胎为宫腔内正常位置妊娠。随后于门诊行宫内减胎术,在阴道超声下经阴道刺入瘢痕妊娠处抽吸囊胚。此次入院时的妇科超声检查提示:子宫前位,如孕65~70 d,宫内可见2个胎囊,其一5.4 cm×3.6 cm,其内可见卵黄囊,可见胎芽,胎芽长3.4 cm,胎心(+),子宫壁回声欠均匀(见图1);其二(前壁相当于剖宫产切口处见胎囊)6.0 cm×2.4 cm,其内未见卵黄囊及胎芽,形态不规则;前壁相当于剖宫产切口处子宫肌层最薄处厚约0.1 cm,双卵巢未显示,双附件区未见明显包块(见图2)。超声印象诊断:1.宫内早孕,活胎(其一);2.CSP?(其二)请结合临床。
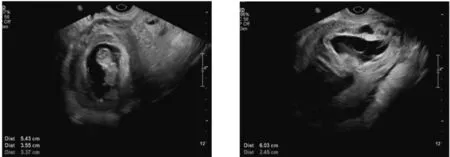
图1 宫腔内胎囊

图2 剖宫产切口处胎囊
入院查血人绒毛膜促性腺激素(hCG)98 584.3 IU/L。完善术前准备,查无手术禁忌证,全身麻醉下开腹探查,子宫下段剖宫产切口瘢痕组织处菲薄,表面呈紫蓝色,双侧输卵管及卵巢未见异常,术中诊断:CSP,宫内早孕,双胎妊娠。术中行经腹宫腔内胎盘胎儿清除术+CSP病灶切除术+剖宫产瘢痕憩室修补术,将子宫娩出盆腔,剪开膀胱返折处腹膜,充分暴露子宫下段,见胚物种植,在下段瘢痕处做一切口,见坏死胚物组织涌出,徒手清除宫腔内所有残余胚物及其附属组织,探查宫腔内无胚物组织残留,切除子宫瘢痕憩室组织。术后病理回报示:(胎盘及胚物组织)送检组织内见绒毛及滋养层细胞,部分绒毛有退化变性,局部见较多急慢性炎性细胞浸润,(剖宫产子宫切口瘢痕肌壁)子宫肌层内见多量坏死,其内可见绒毛及滋养层细胞,部分滋养层细胞侵犯血管,部分侵透肌壁达浆膜层。术后患者恢复良好。
2 讨论
CSP是受精卵着床于子宫瘢痕处的一种异位妊娠,有研究报道其发生率在 1∶2 216~1∶1 800[1]。宫内妊娠合并异位妊娠称为复合妊娠,复合妊娠很少见,有关宫内妊娠合并CSP的临床资料更为少见。
2.1 诊断 CSP可导致妊娠、刮宫或药物流产期间出现致命性的大出血和子宫破裂,严重情况下患者还有子宫切除、弥散性血管内凝血(DIC)及死亡的风险[2]。近年来,随着超声及MRI的普及,CSP可以在妊娠早期诊断[3]。Godin等[4]在1997年首次提出CSP的超声诊断标准:①宫腔内及宫颈管内无妊娠囊;②妊娠囊位于子宫峡部前壁;③膀胱和妊娠囊之间肌壁薄弱。超声操作方便,诊断准确率高,已成为CSP诊断的首选方法[5]。对CSP的超声检查可分为经腹超声和经阴道超声。与经腹超声相比,经阴道超声不需要患者的膀胱处于充盈状态,也不会因患者的腹壁较厚,造成近场回声不明显,导致信号清晰度差,影响超声诊断结果[6]。但经阴道超声存在一定的假阴性率,且与操作者的经验及检查切面有关,因此对于超声难以确诊的疑似CSP病例,可以进行MRI明确诊断[3]。MRI软组织分辨率好,且可通过多断面成像显示子宫切口处瘢痕、胎囊以及宫腔之间的位置关系,明确胎囊是否着床于瘢痕处、子宫肌层厚度以及绒毛是否植入[7]。同时MRI能观察到出血块内部的树状结构,还可观察病灶及周边血液运行情况,为CSP风险程度的预测及治疗方法提供指导[8]。
2.2 治疗 CSP的治疗方式分为保守治疗、手术治疗和联合治疗[9]。保守治疗一般选用的药物为甲氨蝶呤(MTX)。手术治疗包括B型超声(B超)监视下清宫术、子宫动脉栓塞后清宫术(在注入栓塞剂前可以在双侧子宫动脉注入适量MTX)、腹腔镜或开腹子宫局部切开取囊及缝合术、子宫次全切除或全切除术等[10]。有研究报道对CSP患者行子宫动脉栓塞介入术时向子宫动脉内注入MTX,然后再行清宫术获得了确切的临床疗效[11]。MTX作为叶酸还原酶抑制剂,对细胞内的DNA复制、RNA转录和蛋白质合成均有抑制作用,同时MTX还可特异性抑制G1和G1/S转换期细胞,有效阻止细胞的分裂与生长;最终MTX会抑制滋养细胞增生,破坏绒毛,使胚胎组织坏死、脱落[12]。近年来经阴道CSP病灶切除术成为了新兴的手术方式,其特点为直视下手术,止血较迅速,病灶切除完整,术中出血量少[13]。
该患者IVF-ET后宫内妊娠合并CSP,但考虑到患者的生育要求,需要尽可能保证宫内妊娠的正常进行,所以手术治疗以及MTX等药物治疗都不是首选方案,在阴道超声下经阴道穿刺入子宫下段切口瘢痕妊娠处抽吸囊胚进行减胎,是一个比较优选的方案。结合患者病史及超声提示,患者妊娠晚期可能会出现胎膜早破、感染、子宫破裂、大量失血的风险,患者知情同意后,要求手术。术后病理回报:瘢痕处妊娠囊内部分滋养层细胞已侵犯血管,部分已侵透肌壁到达浆膜层。有学者认为孕5周时绒毛出现并完全包绕着孕体,之后除了包蜕膜上面最表层的2/3绒毛退化成光滑的绒毛外,剩下的绒毛与底蜕膜紧密相贴,其数目快速增加,分支增多增大,最终形成丛密绒毛膜[14]。Timor-Tritsch等[15]认为,剖宫产瘢痕愈合处肌层及蜕膜不完整,存在缝隙,囊胚若在此处着床,绒毛会植入缝隙中。因此,对于CSP做到早发现,尤其是在绒毛转变成丛密绒毛膜之前发现,并行阴道超声下减胎,或许可以减少瘢痕妊娠部位绒毛植入的几率,降低减胎后因绒毛植入而持续阴道出血几率,进而使宫内正常位置的胚胎更安全的发育。另外,相比于自然妊娠,辅助生殖技术下的双胎妊娠也进一步增加了瘢痕子宫孕妇凶险性前置胎盘、产后出血、妊娠期糖尿病等的风险[16]。
鉴于瘢痕子宫的以上风险及IVF-ET治疗的特殊性,瘢痕子宫的孕妇再次妊娠前,需要进行详细的孕前咨询与评估,并用常规超声评估子宫瘢痕形态(包括宽度、长度和深度)[17]。胚胎移植时尽量减少移植胚胎的数量,尽可能降低孕妇和胎儿的不良结局。
