一站式介入治疗重度主动脉瓣狭窄合并胸主动脉溃疡1例
2019-08-13罗建方范瑞新李光李捷丁焕宇孙英皓付明郭晓纲郑胜能徐衡
罗建方 范瑞新 李光 李捷 丁焕宇 孙英皓 付明 郭晓纲 郑胜能 徐衡
1 临床资料
患者 女,77岁。因“活动后胸闷气促2年,加重2个月”于2019年2月20日至广东省人民医院就诊。患者2年前出现活动后胸闷、气促,无胸背痛,休息后可缓解。近2个月上述症状加重,至本院进一步治疗。既往有冠心病、高血压病和2型糖尿病病史,否认吸烟史。入院查体:心率66次/分,血压138/53 mmHg(1 mmHg=0.133 kPa),主动脉瓣第一听诊区可闻及3/6级收缩期喷射性杂音。美国纽约心脏病学会(New York Heart Association, NYHA)心功能分级为Ⅲ级,美国胸外科医师学会(Society of thoracic surgeons,STS)评分为2.9%。入院心电图示:一度房室传导阻滞。超声心动图示:重度主动脉瓣狭窄(aortic stenosis, AS)合并中度反流,主动脉瓣口血流速度4.0 m/s,主动脉瓣峰值压差64 mmHg,平均压差40 mmHg(图1 A),左心室射血分数46%。主动脉和冠状动脉计算机断层扫描血管造影提示主动脉瓣瓣环直径29.7 mm×23.7 mm,周长84.6 mm,面积557.5 mm2,主动脉窦部直径32.1 mm×30.6 mm×35.2 mm,左心室流出道周长89.6 mm,面积584.5 mm2(图2 A~C);左冠状动脉开口高度9.0 mm,右冠状动脉开口高度14.5 mm(图2 D~E),主动脉瓣呈Type Ⅰ型二叶主动脉瓣并重度钙化(图2 F);横位心,主动脉与左心室夹角67°(图2 G),升主动脉直径42.8 mm(图2 H),胸降主动脉穿透性溃疡(图2 I);外周血管入径条件良好。由心血管内外科、血管外科、麻醉科、心脏超声科、影像科等多学科团队对患者进行评估并签署手术知情同意书后,于2019年2月22日在广东省人民医院杂交手术室经股动脉入径行经导管主动脉瓣置换术(transcatheter aortic valve replacement, TAVR)联合胸主动脉腔内修复术(thoracic endovascular aortic repair,TEVAR)一站式治疗。
患者全身麻醉气管插管后,经右颈静脉置入临时起搏器于右心室,以右股动脉作主入径,经皮穿刺预置2把Proglide缝合器。主动脉根部造影提示主动脉瓣严重钙化,主动脉瓣中重度反流(图3 A);胸降主动脉造影可见穿透性溃疡(图3 B)。送猪尾导管至左心室,测左心室压力为150/12 mmHg,升主动脉压力为110/35 mmHg,跨瓣压差为40 mmHg。交换超硬导丝至左心室,撤出猪尾导管,送入23 mm球囊行主动脉瓣预扩张,行主动脉根部造影提示球囊无腰征,并有部分对比剂反流(图3 C)。通过22 Fr血管鞘置入VenusA-Plus瓣膜,顺利通过主动脉弓及跨越主动脉瓣,造影下调整瓣膜位置,在瓣膜标记点与主动脉瓣瓣环平行时逐步释放瓣膜,待裙边完全展开后以130次/分心室率起搏,快速完全释放瓣膜(图3 D)。退出输送系统,造影提示存在中度瓣周漏,故使用23 mm球囊后扩张,经食管超声心动图提示支架瓣膜展开完全,轻度瓣周漏,复测左心室压力为136/2 mmHg,升主动脉压力为134/55 mmHg。经右股动脉入径送入Ankura 28 mm×160 mm(先健科技)主动脉覆膜支架,支架远端定位于腹腔干动脉开口上缘,精确定位后释放主动脉支架(图3 E)。复查造影提示主动脉支架贴壁良好,穿透性溃疡被完全隔绝,未见内漏,内脏血管均正常显影(图3 F)。手术顺利完成后至重症监护室观察,术后3 d转至普通病房,术后10 d康复出院。术后1个月复查超声心动图提示主动脉瓣人工生物瓣膜功能良好,轻度瓣周漏,瓣口血流速度为1.32 m/s,跨瓣峰值压差7 mmHg(图1 B)。
2 讨论
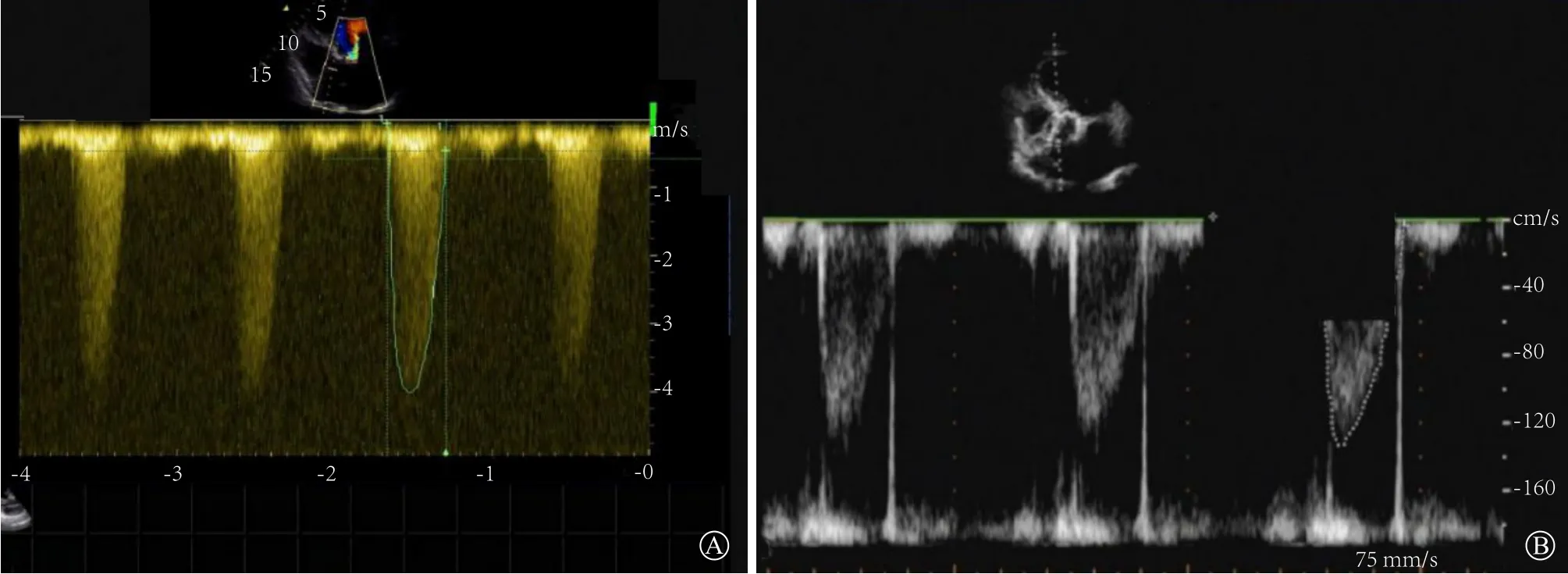
图1 超声心动图 A.术前主动脉瓣口血流速度4.0 m/s,主动脉瓣峰值压差64 mmHg(1 mmHg=0.133 kPa),平均压差40 mmHg;B.术后1个月主动脉瓣口血流速度1.32 m/s,跨瓣峰值压差7 mmHg
图2 术前主动脉CT血管造影 A~C.主动脉瓣瓣环、窦部及左心室流出道的径线测量;D~E.左、右冠状动脉开口高度;F.主动脉瓣钙化及分型;G.主动脉与左心室夹角;H.升主动脉直径;I.胸降主动脉见穿透性溃疡

图3 手术过程造影资料 A.主动脉根部造影;B.胸降主动脉造影可见穿透性溃疡;C.球囊预扩张;D.主动脉瓣瓣膜置入后;E.主动脉覆膜支架置入后;F.同期经导管主动脉瓣置换术与胸主动脉腔内修复术术后
目前TAVR已成为外科手术禁忌或外科手术高危的重度AS患者的首选治疗策略[1-3]。近年开展的PARTNER 2A研究[4]和SURTAVI研究[5]结果显示,在外科手术中危的重度AS患者中,TAVR不劣于传统外科瓣膜置换术。2019年,PARTNER 3研究[6]和EVOLUT研究[7]结果表明,在外科手术低危的重度AS患者中,TAVR优于或不劣于传统外科瓣膜置换术。主动脉穿透性溃疡是指主动脉粥样硬化斑块穿透内弹力板,破入中膜,多见于老年患者,其自然病程可进展为主动脉夹层、壁间血肿、假性动脉瘤甚至主动脉破裂。TEVAR是一种微创的介入治疗手段,对于病变位于降主动脉的患者,可通过置入主动脉覆膜支架从而达到封堵溃疡预防病情进展的目的。随着TEVAR在主动脉疾病中的广泛应用,相关指南与共识均推荐TEVAR作为胸降主动脉疾病的首选治疗方式[8-9]。目前,同时应用TAVR和TEVAR一站式处理重度AS和胸主动脉疾病的相关报道较少。Drury-Smith等[10]在2012年报道了经股动脉入径行TAVR和腹主动脉腔内修复术一站式处理重度AS和腹主动脉瘤,开启了同期介入治疗重度AS和主动脉疾病的先例。Allen等[11]在2015年报道了经心尖入径同期进行TAVR与TEVAR。本文报道的经股动脉入径TAVR联合TEVAR一站式治疗重度AS合并胸主动脉穿透性溃疡在国内外尚未见相关报道。
对于重度AS合并主动脉疾病的管理,同期手术和分期手术各有利弊。同期手术会增加辐射剂量和对比剂用量,延长手术时间和麻醉时间,增加手术风险和难度;但可减少入径的反复穿刺,缩短住院时间,减少手术费用。因此,在进行同期手术前,需要全面评估患者的手术风险和难度,制定严密周全的手术策略。同期进行TAVR和TEVAR时,手术的先后顺序目前无统一方案。笔者认为需要根据TAVR和TEVAR的手术难度、AS和降主动脉疾病的严重程度、进行TAVR或TEVAR后是否增加后续手术的难度等进行综合考量。针对本例患者,若先行TAVR,人工瓣膜释放后主动脉压力升高,提高脊髓动脉灌注压,有助于降低TEVAR术后脊髓缺血的风险;但血管壁剪切力的升高有使主动脉溃疡进展为夹层甚至破裂的潜在风险。若先行TEVAR,可能会对瓣膜置入的入径造成影响,特别是VenusA-Plus可回收系统硬度较大,跨越主动脉弓部及瓣膜调整过程中可能会导致大动脉支架发生移位。本病例中,胸降主动脉病变为局限性的穿透性溃疡,破裂风险较低,另外病变未累及主动脉弓上分支血管,降主动脉无明显弯曲,TEVAR的操作过程相对简单,可快速完成。先进行TAVR不会妨碍主动脉支架的置入,并未对TEVAR的操作带来困难,因此,本病例最终采用TAVR后同期行TEVAR的一站式治疗策略。
