氰化渣的无害化处置试验研究
2019-08-08于艳杰方登志肖淑君
于艳杰,方登志,肖淑君,吴 莹,徐 冬
(中国人民解放军61699部队,湖北 枝江 443200)
用氰化法从银矿石中浸出银,浸出液经锌粉置换后得到银泥和氰化贫液,氰化贫液经循环回收氢化氰后会产生一定量氰化渣[1-5]。氰化渣中含有重金属、少量氰化物、重金属氰配合物和硫氰酸盐等[6-8],属剧毒物质,对人和环境都有极大危害,须谨慎处理[9]。
目前,国内大多含银氰化贫渣只是简单堆存,自然降解,未做进一步处理[10-12]。试验采用二氧化氯氧化—硫酸亚铁配合沉淀工艺处置氰化渣,回收其中的重金属,并使废水达标排放。
1 试验部分
1.1 试验原料与仪器
试验仪器:Starter300型便携式pH计,美国奥豪斯;ICAP7000型等离子发射光谱仪,美国赛默飞;CP224C型电子天平,美国奥豪斯。
试验试剂:次氯酸钠溶液(100 g/L),七水合硫酸亚铁,分析纯,西陇化工股份有限公司;双氧水溶液(300 g/L),武汉旺森化试公司;漂白粉,氯酸钠,分析纯,国药集团化学试剂有限公司;二氧化氯(新鲜自制,8 g/L);浓磷酸,分析纯,太仓沪试试剂有限公司;乙二胺四乙酸二钠,分析纯,汕头市化学试剂厂;浓硫酸,分析纯,宜昌日兴化工有限责任公司;浓硝酸,分析纯,成都市科龙化工试剂厂;浓盐酸,分析纯,昆山晶科微电子材料有限公司;氢氧化钠,分析纯,天津市博迪化工有限公司;硝酸银,分析纯;南京化学试剂股份有限公司;试银灵,分析纯,北京化工厂。
试验所用氰化渣取自湖北某矿业公司,为处理氰化物浸出银生产过程中产生的含氰废水的产物,pH=2.18,含水率67.2%,金属及总氰分析结果见表1。氰化渣中重金属含量较高。

表1 氰化渣中金属及总氰分析结果 %
总氰的测定:采用硝酸银滴定法,向水样中加入磷酸和EDTA-2Na,在pH<2条件下加热蒸馏,利用金属离子与EDTA配合能力比氰根离子配合能力强的特点,使配合氰化物解离出氰离子,并以氰化氢形式蒸馏出来,用氢氧化钠溶液吸收[13]。
重金属含量采用等离子体发射光谱法测定。
1.2 试验原理与方法
氰化物的处理可以采用破坏法。破坏法是用氧化剂将氰化物分解为无毒物质,主要有氯碱法、过氧化氢氧化法、SO2/Air法、臭氧氧化法等[14-15]。氯碱法是在pH=10~11条件下,利用活性氯的氧化作用对氰化物进行分解。活性氯包括漂白粉、次氯酸钠、二氧化氯、液氯等[16-18]。过氧化氢氧化法是在pH=9.5~11、Cu2+作催化剂条件下,利用H2O2将游离氰化物及其金属配合物氧化成氰酸盐及金属离子,金属离子以氢氧化物形式沉淀[19]。重金属氰化物氧化反应如下:

氯碱法和过氧化氢氧化法均不能完全破坏铁氰配合物,所以,滤液中仍含有少量铁氰化物。向滤液中加入硫酸亚铁,铁氰化物被转化成亚铁蓝,亚铁蓝可在酸性条件下被氧气氧化成普鲁士蓝沉淀[20]。主要反应如下:
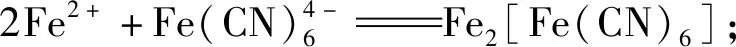
氰化浸出渣和水按一定比例混合成悬浊液,加入400 g/L氢氧化钠溶液调节pH,先采用氯碱法和过氧化氢氧化法破氰,通过单因素条件试验考察氧化剂种类、氧化剂用量、固液质量体积比及反应时间对氰化物的破坏效果,然后向滤液中加入一定量七水合硫酸亚铁,曝气搅拌,将氰化物转变成普鲁士蓝沉淀,最后过滤,得滤渣,滤液达标排放。
2 试验结果与讨论
2.1 氰化渣的氧化
2.1.1 氧化剂种类对破氰的影响
氰化渣质量100 g,水400 mL,加入400 g/L氢氧化钠溶液调节pH=10左右,慢慢加入200 mL氧化剂,搅拌反应3 h,过滤。氧化剂种类对破氰的影响试验结果见表2。可以看出:相同条件下,二氧化氯对CN-的破坏效果最好,滤液和滤渣中氰含量都最低;双氧水的氧化效果次之。考虑到生产成本,试验选择二氧化氯作为氧化剂进行破氰。

表2 氧化剂种类对破氰的影响
2.1.2 固液体积质量比对破氰的影响
氰化渣质量100 g,加400g/L氢氧化钠溶液调pH=10左右,逐渐加入8 g/L二氧化氯水溶液200 mL,搅拌反应3 h,过滤。固液质量体积比对破氰的影响试验结果见表3。
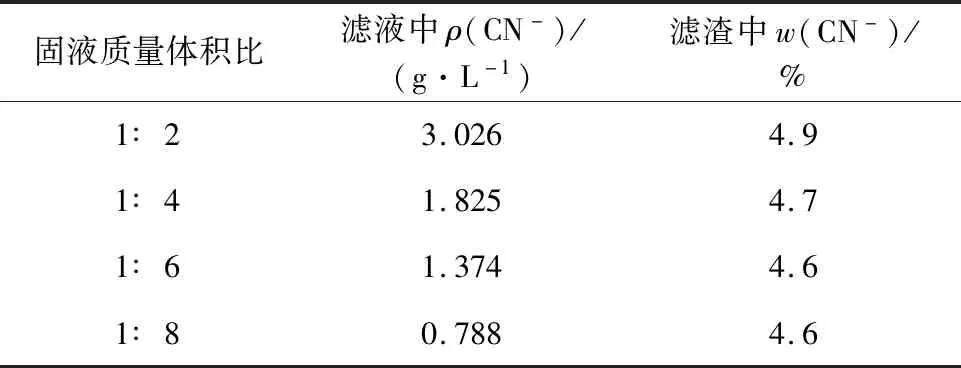
表3 固液质量体积比对破氰的影响
由表3看出:随固液质量体积比减小,滤液和滤渣中总氰含量都逐渐降低。综合考虑,确定固液体积质量比以1∶6较为宜。
2.1.3 氧化剂用量对破氰的影响
渣质量100 g,加水400 mL,用400 g/L氢氧化钠溶液调pH=10左右,慢慢加入质量浓度8 g/L的二氧化氯水溶液,搅拌反应3 h,过滤。氧化剂二氧化氯用量对破氰的影响试验结果见表4。

表4 氧化剂用量对破氰的影响
由表4看出:随ClO2用量增加,滤渣中总氰质量分数明显降低,滤液中总氰质量浓度变化不大。表明滤液中仍存在不能被ClO2氧化的铁氰配合物。综合考虑,二氧化氯水溶液用量以250 mL为宜。
2.1.4 反应时间对破氰的影响
氰化渣质量100 g,加水400 mL,用400 g/L氢氧化钠溶液调pH=10左右,逐渐加入250 mL二氧化氯水溶液(8 g/L),搅拌反应一定时间后过滤。反应时间对破氰的影响试验结果见表5。

表5 反应时间对破氰的影响
由表5看出:随反应时间延长,滤渣和滤液中总氰含量都明显减少;反应时间超过5 h后,总氰含量趋于稳定。综合考虑,确定反应时间以5 h为宜。
2.1.5 综合验证试验
氰化渣质量100 g,加水600 mL,搅拌,用400 g/L氢氧化钠溶液调pH=10左右,慢慢加入250 mL二氧化氯水溶液(8 g/L),搅拌5 h后过滤,测定滤渣和滤液中铜、锌、铁及总氰含量,结果见表6。

表6 氰化渣的二氧化氯氧化结果
由表6看出:氧化处理后,滤渣中的氰化物含量已检测不出;滤液中铜、锌质量浓度达到《污水综合排放标准》(GB 8978—1996)一级排放标准[21],总氰质量浓度为1 369 mg/L,远远超标,还需进一步处理。
2.2 废水中氰化物的配合沉淀
过滤后的滤液200 mL,用硫酸溶液调pH至6左右,加入FeSO4·7H2O,曝气搅拌1 h,充分反应后过滤,测定滤液中总氰质量浓度,试验结果如图1所示。
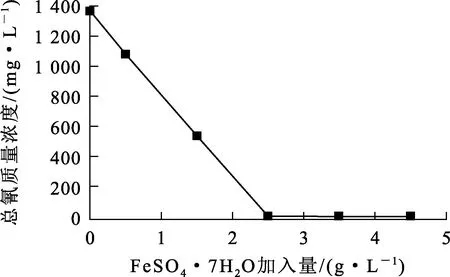
图1 FeSO4·7H2O加入量对总氰去除的影响
由图1看出:随FeSO4·7H2O加入量增加,滤液中总氰质量浓度逐渐降低;FeSO4·7H2O加入量为2.5 g/L时,滤液中总氰质量浓度达0.4 mg/L,而后变化不大。为避免过多的Fe2+进入滤液,选择FeSO4·7H2O用量为2.5 g/L。经测定,滤液pH=6.5,铜、锌、铁质量浓度分别为0.5、0.5、2.8 mg/L,均满足《污水综合排放标准》GB 8978—1996一级排放标准[21]。过滤后的滤渣为蓝色沉淀,为纯度较高的普鲁士蓝,可以作为产品销售。
3 结论
采用二氧化氯氧化—硫酸亚铁配合沉淀法处理氰化浸出渣可实现氰化浸出渣的无害化,使其中的重金属得到回收,处置后的出水可达标排放。该工艺可操作性强,可供同类废渣处置参考。
